前列腺癌生化复发危险因素报告
——单中心11年回顾分析
2022-09-02严于昊胡广漠谢超耿振翔薛波新
严于昊 胡广漠 谢超 耿振翔 薛波新
前列腺癌是男性泌尿生殖系统中最常见的恶性肿瘤,据2018年世界卫生组织GLOBOCAN统计,在世界范围内,其发病率在男性所有恶性肿瘤中位居第2位,仅次于肺癌[1]。与欧美国家相比,中国是前列腺癌发病率及死亡率较低的国家之一,但近年来其发病率呈持续快速增长的趋势[2]。我院建立的前列腺癌数据库包含了2010年1月至2020年12月确诊为前列腺癌患者的基本临床数据及相关随访数据。经统计,接受前列腺根治性切除术(radical prostatectomy, RP)的患者共有559例,我们分析了接受腹腔镜前列腺根治性切除术(laparoscopic radical prostatectomy, LRP)且随访资料完整的384例患者的临床资料,以探究术后生化复发的独立危险因素。
对象与方法
一、一般资料
回顾性分析2010年1月至2020年12月我院接受RP的患者共559例。排除临床资料不完整及失访的患者、术前接受新辅助内分泌治疗以及术后病理为非腺泡腺癌的患者,总共纳入接受LRP的患者384例。
二、研究设计及随访方法
根据术后随访时生化复发的情况将患者分为生化复发组与未生化复发组,纳入的指标包括年龄、BMI、术前PSA、游离PSA(free PSA, fPSA)、PSA比值、前列腺体积(prostate volume, PV)、穿刺Gleason评分、有无术后病理Gleason评分升级、临床分期、中性粒细胞淋巴细胞百分比(neutrophil to lymphocyte ratio, NLR)、血小板淋巴细胞百分比(platelet to lymphocyte ratio, PLR)、前列腺特异抗原密度(prostate specific antigen density, PSAD)、病理淋巴结阳性情况、切缘情况、精囊侵犯、神经侵犯、有无被膜侵犯及是否合并高血压、糖尿病、高血脂。
患者术前均完善胸部X线/CT、腹盆部CT/MRI及骨扫描除外远处转移。对PSA>20 ng/ml、Gleason评分≥8分、临床分期≥T2c期的高危患者及术前影像学检查怀疑淋巴结阳性的患者行盆腔淋巴结清扫。术后于门诊规律随访并复查PSA及睾酮水平。术后6个月每月复查1次,6个月至2年每3个月复查1次,2年以上每6个月复查1次。
根据术后病理情况,结合患者意愿,对术后病理淋巴结阳性或术后6周PSA仍未降至0 ng/ml的患者进行辅助放疗或12~18个月的辅助内分泌治疗。
生化复发定义为术后随访过程中连续2次PSA>0.2 ng/ml,并将生化复发作为随访的终点事件。
三、统计学方法
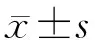
结 果
一、患者临床病理特征及单因素分析
所有患者随访3~135个月,中位随访时间41(26,62)个月。共有115例患者术后出现生化复发,总体生化复发率29.95%(115/384),见图1。术后3年和5年无生化复发生存率分别为74.0%和69.2%。生化复发组与未生化复发组的临床病理特征见表1。单因素分析比较显示,两组在PSA、fPSA、穿刺Gleason评分、T分期、PSAD、术后病理Gleason评分升级、精囊侵犯、神经侵犯、淋巴结阳性和标本切缘阳性上存在差异,差异有统计学意义(P<0.05)。而在年龄、BMI、PSA比值、NLR、PLR及患者是否合并高血压、糖尿病、高血脂等方面差异无统计学意义(P>0.05)。
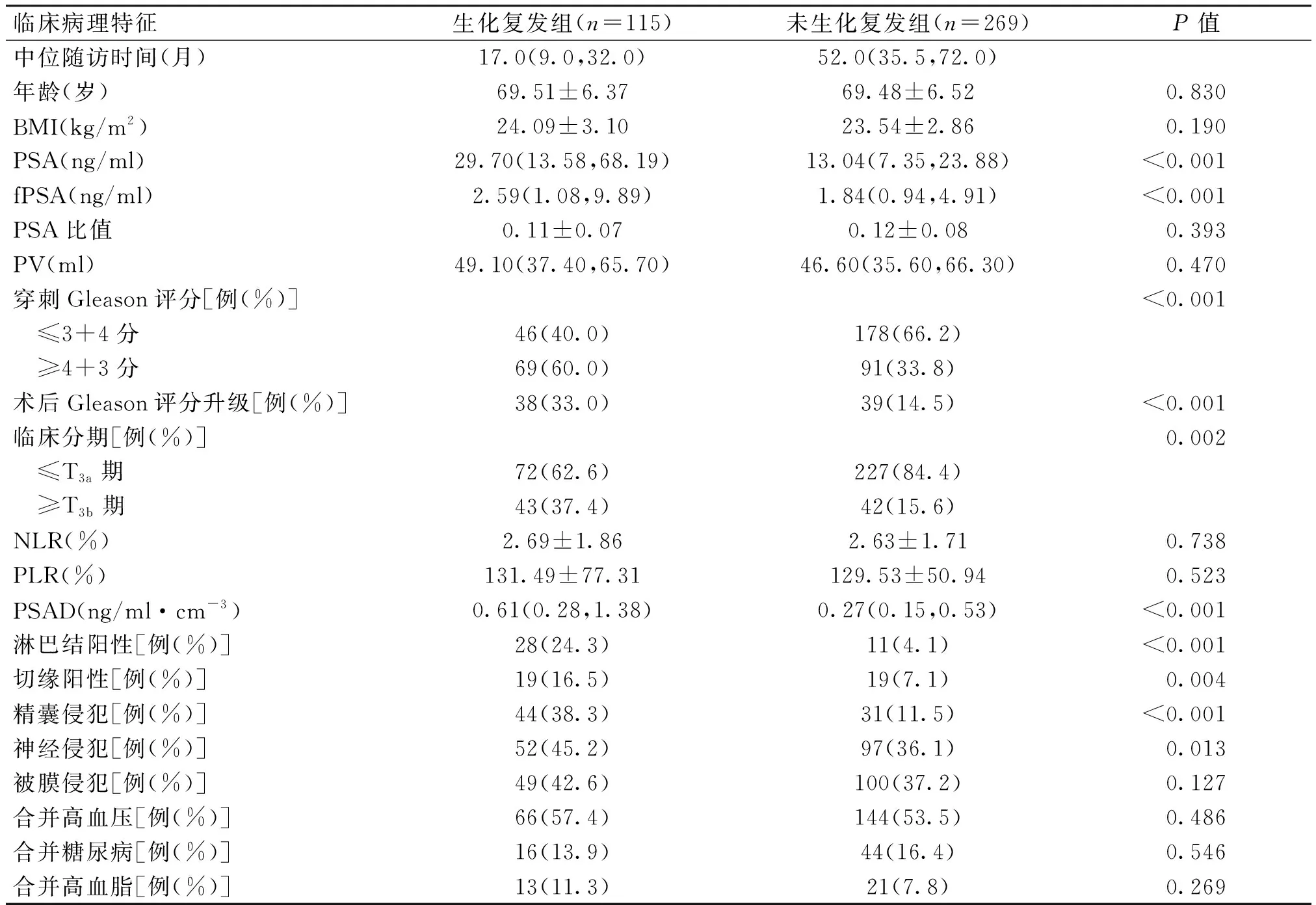
表1 两组患者临床病理特征及单因素分析
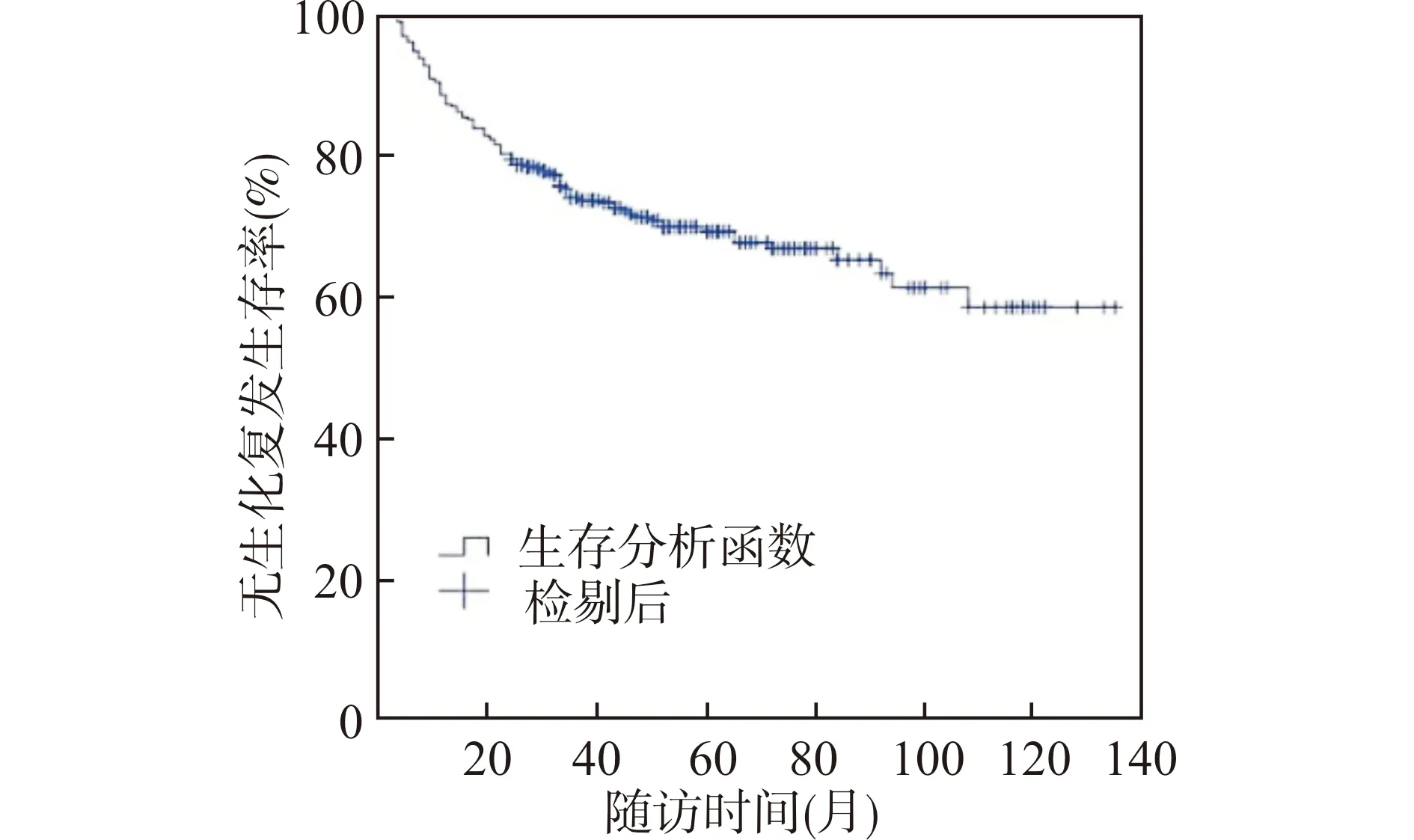
图1 384例患者无生化复发生存曲线
二、单因素最佳截断值选定
绘制有统计学意义连续性变量(PSA、fPSA、PSAD)的受试者工作特征曲线(receiver operating characteristic curve, ROC),见图2。当PSA、fPSA、PSAD分别为23.25、2.44、0.52时约登指数最大,分别为0.36、0.279、0.321。此时曲线下面积(area under the curve, AUC)最大,特异度分别为0.617、0.532、0.722。因此选定PSA、fPSA、PSAD的最佳截断值分别为23.25、2.44、0.52,将PSA、fPSA、PSAD进行进一步分层。
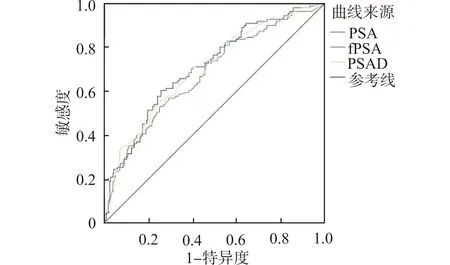
图2 生化复发单因素有意义连续性变量ROC曲线
三、Cox多因素回归分析
将单因素分析中有意义的指标进一步进行Cox多因素回归分析。Cox多因素分析显示,患者首诊时PSA≥23.25 ng/ml、穿刺活检病理Gleason评分≥4+3分、术后病理Gleason评分出现升级、术后病理淋巴结阳性和精囊侵犯是患者接受根治手术后出现生化复发的独立危险因素(表2)。
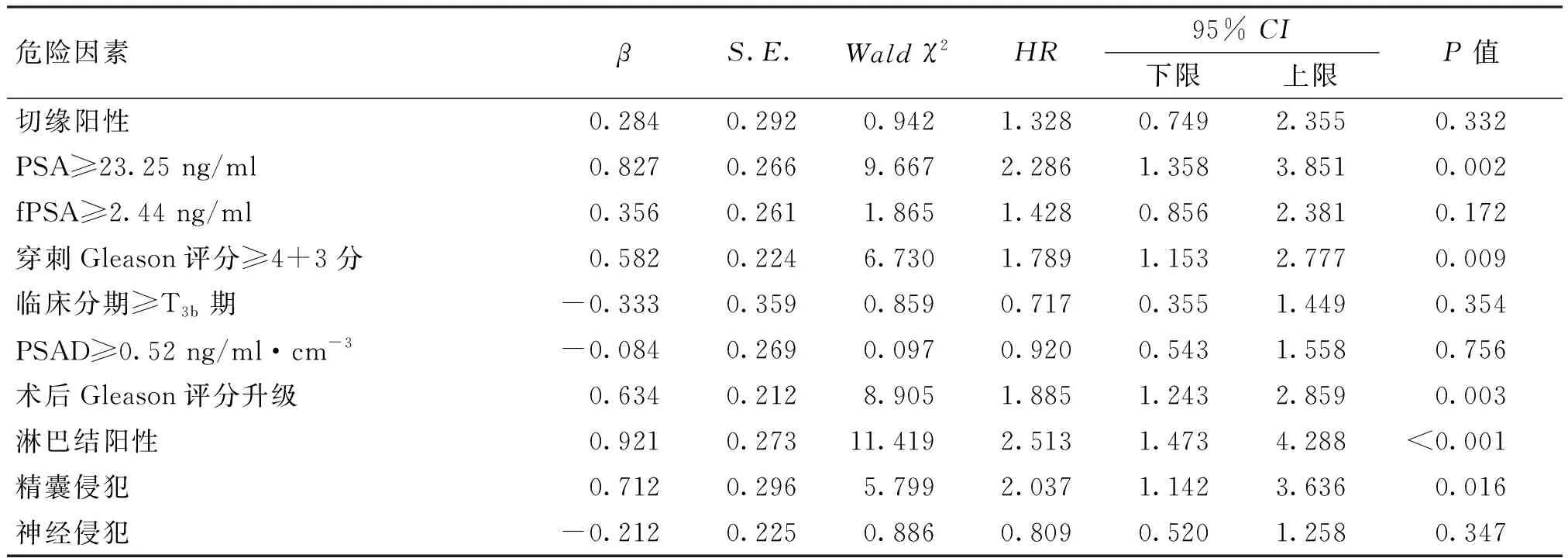
表2 前列腺癌患者术后生发复发的Cox回归分析
四、构建预测模型
对多因素分析中有统计学意义的独立危险因素分别单独赋值,并构建生化复发预测模型,即PSA<23.25 ng/ml为0分,PSA≥23.25 ng/ml为1分;穿刺Gleason评分≤3+4为0分,穿刺Gleason评分≥4+3为1分;淋巴结阴性为0分,淋巴结阳性为1分;术后Gleason评分无升级为0分,术后Gleason评分升级为1分;无精囊侵犯为0分,有精囊侵犯为1分。根据赋值计算患者的总得分,并根据赋值后的加权得分将患者重新分为3组:0~1分为低风险组,2~3分为中风险组,4~5分为高风险组。低风险组244例,中风险组111例,高风险组29例。Cox回归分析结果显示,以低风险组为参照,中风险组(HR:3.389;95%CI:2.233~5.143;P<0.001)和高风险组(HR:12.466;95%CI:7.427~20.922;P<0.001)均为根治术后生化复发的危险因素。不同风险组生存结果如图3所示。3组患者5年累积无生化复发生存率分别为83.1%、54.9%、9.5%。
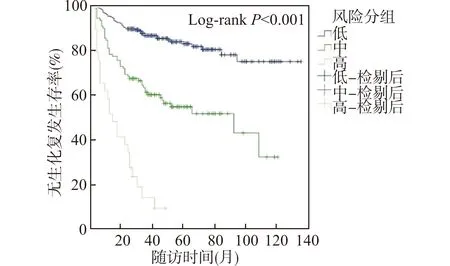
图3 不同风险组患者无生化复发生存曲线
讨 论
LRP和机器人辅助腹腔镜前列腺根治性切除术是在具备相应条件的地区被用作治疗局限性前列腺癌的常规手段。部分接受了根治术的患者,在术后出现生化复发时如不进行及时干预,则会进一步进展至临床复发。临床上也一直在进行对前列腺癌生化复发危险因素的相关研究。本研究统计RP术后患者累积5年无生化复发生存率为69.2%,与戴波等[3]研究结果中的70.89%相近,但仍远低于欧美国家80%的5年无生化复发生存率[4]。究其原因可能是本研究中的患者与欧美国家患者相比,在接受手术时的肿瘤T分期相对较晚,且Gleason评分等级相对偏高。另外部分患者术后对定期随访重视程度不够,从而错过了最佳治疗时机。
既往研究结果显示,PSA>20 ng/ml、穿刺病理Gleason评分及术后病理Gleason评分、术后病理分期等是影响患者生化复发的重要危险因素[5-6]。近年来研究者也对其他指标如PSAD、NLR、PLR、代谢综合征、前列腺慢性炎症等因素进行了探究,但仍未达成更广泛的共识。本研究发现PSA≥23.25 ng/ml、穿刺病理Gleason评分≥4+3分、术后病理Gleason评分升级、病理淋巴结阳性和精囊侵犯是患者接受根治手术后出现生化复发的独立危险因素。
Tilki等[7]的研究结果表明术前PSA在肿瘤局部复发或远处转移前开始上升,生化复发通常是肿瘤局部复发或远处转移的前兆,往往提示预后不良。因此在本研究中,我们运用ROC曲线取最佳截断值对PSA进行了分层,当PSA≥23.25 ng/ml时,术后生化复发可能性较高(P=0.002)。而Gleason评分作为目前应用最广泛的前列腺恶性肿瘤分级系统,直接反映了肿瘤的侵袭性,有助于选择合适的治疗方案和判断患者的预后[8]。Gleason评分标准中,评分为3+4与4+3之间主要区别在于分化不良腺体的占比程度。在4+3中完好的腺体只占有少量的比例,而在3+4中则正好相反。2014年国际泌尿病理协会(International Society of Urological Pathology, ISUP)专家共识会议提出了一项前列腺癌分级分组标准:建议将两者区别对待。Offermann等[9]也证实了ISUP 2014分级分组系统较以往单纯的Gleason分级在生化复发上具有更高的预测准确性。本研究中当Gleason评分临界值选为3+4和4+3时,两组间无生化复发生存率差距最为明显,考虑未来早中期、低Gleason评分的前列腺癌患者将逐渐占到主体,对早中期和低Gleason评分患者的长期随访和治疗是必要的,对Gleason评分3+4、4+3患者的区别研究也将有助于患者个体化的精准治疗。文献报道约28%~68%的RP患者病理标本的Gleason评分与术前穿刺病理评分会出现不一致的情况[10]。并且在穿刺病理Gleason评分≤6分的低危型前列腺癌患者中这一现象更为显著。程万里等[11]研究指出,在术前穿刺病理Gleason评分≤6分的患者中,有高达53.8%的患者术后病理Gleason评分升高,且比例明显高于穿刺评分更高的患者。Gleason评分升级通常意味着生化复发率及局部进展率升高,肿瘤特异性生存率降低[12]。本研究显示术后病理Gleason评分升级是生化复发的独立危险因素,在后续的研究中,我们将进一步研究Gleason评分升级的危险因素以及不同升级程度对预后的影响。此外,本研究中淋巴结阳性在术后生化复发研究中被证实有统计学意义(P=0.001)。既往认为盆腔淋巴结清扫主要意义在于临床诊断,有助于明确临床分期。然而越来越多的研究发现,盆腔淋巴结清扫的病理标本结果有助于预测疾病进展和复发的风险[13]。但本研究术后病理显示淋巴结阳性患者的数量较少,可能存在数据偏倚,因此在今后的工作中需要纳入更多的病例来验证结果的可靠性。
本组临床分期在单因素分析上显示出了明显的差异(P=0.002),但进一步多因素分析中临床分期的差异却并不显著(P=0.354),这与高旭等[14]的研究结论不同。分析原因可能与入组患者的数量、临床分期亚分组不同有关。Peng等[15]发现PSAD>0.5 ng/mL/cm3时,中危组和高危组前列腺癌患者的无生化复发生存率相当(P=0.735)。Yashi等[16]对行机器人辅助腹腔镜前列腺癌根治性切除术的高危患者回顾性研究发现,PSAD在高危组中对生化复发有独立的预测价值。本研究中,当PSAD以0.52 ng/ml·cm-3分组时,在多因素分析中却并不显著(P=0.756)。造成这些现象主要的原因在于各研究之间样本量与计算PV的方法不同。本研究参考了经直肠彩超测定PV的方法,也有学者参考了术前磁共振或使用术后标本直接计算PV,可能导致不同研究在结论上的差异。
本研究发现精囊侵犯在多因素分析中是生化复发的独立危险因素(P=0.016)。肿瘤精囊侵犯提示较晚的术后病理分期,可能与较高的术后生化复发率相关[17-18]。Kang等[19]的研究提出神经侵犯与生化复发风险增加有关,本研究中病理切缘阳性、神经侵犯也表现出了一定预测意义,但并不是独立危险因素。以往的研究多认为切缘阳性与生化复发和疾病进展存在相关性[20-22],但也有学者提出切缘阳性并不是生化复发的独立危险因素[6,23],尚需要更大规模的前瞻性研究进一步验证这些结论。
本研究中,我们构建了一个模型用以预测术后累计无生化复发生存率。将独立危险因素分别赋值,通过计算总分,将患者分为低、中、高风险组。3组患者的5年累积无生化复发生存率有着较明显的差异,可以为临床工作提供一定的参考。本研究存在以下不足:①本研究属回顾性分析,存在一定的局限性,且样本量有限,需要进一步行前瞻性研究以及更多的临床数据来支撑本研究的结论;②本中心是苏州泌尿男生殖系肿瘤诊疗中心之一,研究数据具有代表性,但尚不能完全代表全国前列腺癌患者的情况,有待今后多中心进一步研究。
综上所述,本组患者总体生化复发率为29.95%。术后3年和5年无生化复发生存率分别为74.0%和69.2%。其中PSA≥23.25 ng/ml、穿刺病理Gleason评分≥4+3分、术后病理Gleason评分升级、病理淋巴结阳性和精囊侵犯是患者接受根治术后出现生化复发的独立危险因素,需要对符合预测模型中风险和高风险的患者进行密切的术后随访,以免贻误治疗时机。
