TiFexCeyOz催化剂SCR脱硝及气体吸附特性研究
2022-08-25李帅飞牛艳青温丽萍惠世恩
李帅飞,吕 媛,牛艳青,温丽萍,惠世恩
TiFeCeO催化剂SCR脱硝及气体吸附特性研究
李帅飞,吕 媛,牛艳青,温丽萍,惠世恩
(西安交通大学能源与动力工程学院,西安 710049)
采用溶胶-凝胶法进行Ti-Fe-Ce混合金属氧化物(TiFeCeO)的制备并对催化剂的脱硝效率进行研究;同时,利用第一性原理模拟研究反应气体(NO、NH3)在催化剂表面的吸附特性.结果表明:随着Fe、Ce元素的加入,催化剂脱硝效率增大,低温区(100~250℃)脱硝效率最高达到90%以上.当掺杂Fe、Ce元素后,反应气体在催化剂表面的吸附难度下降,同时由于金属掺杂导致锐钛矿晶胞对称性下降,表面氧空位数量增加,促进反应气体的吸附.
混合金属氧化物;选择性催化还原;脱硝效率;气体吸附
选择性催化还原(SCR)脱硝技术是一种常用的高效NO脱除技术,能够大幅度降低燃煤锅炉排放烟气中NO的含量.目前,典型的商用催化剂如V2O5-WO3(MoO3)/TiO2在燃煤电站锅炉上已取得较好的脱硝效果并已广泛应用[1],但其仍然存在一些严重的问题,如工作温度窗口(不低于290℃)较低、重金属元素V毒性较大难以处理以及成本昂贵等.更为重要的是,工业锅炉SCR催化剂工作温度在200℃左右,开发中低温催化剂是目前亟待解决的难点.为解决目前商用催化剂所面临的问题,许多学者开发了一系列新型过渡金属元素氧化物负载型催化剂以及特殊结构的催化剂,如Fe2O3/TiO2[2]、CuO/Cu2O[3]、MnO-CeO2/Al2O3[4]以及中空MnO-CeO2[5]等.
Fe2O3因其来源广泛、价格低廉且具有较好的耐酸性、环境友好、易于处理等优点而受到广泛关注[6-8].目前对于铁基新型催化剂研究大多以负载型催化剂为主,以Fe2O3为活性组分或改性物质负载于TiO2颗粒、碳纳米材料表面等.Shu等[9]采用浸渍法将Fe负载于蜂窝状载体表面制备得到Fe/TiO2,结果表明Fe元素的加入能够显著提高催化剂抗硫性.核壳结构以及纳米尺寸的负载型铁基催化剂也受到广泛关注,Chang等[10]制备出核心为Fe2O3、外部壳层为SiTiO的核壳型Fe2O3@SiTi催化剂,SiTiO外壳的存在导致催化剂表面存在较高浓度的Fe2+以及吸附氧,使得催化剂表现出优异的SCR活性.将活性组分MnO以及Fe2O3分步负载于碳纳米管(CNT)表面,得到多壳层的Fe2O3@MnO@CNTs催化剂[11].但上述负载型铁基催化剂存在脱硝效率较低或制备困难、载体成本昂贵等问题,若能够利用Fe2O3与其他金属元素的协同作用提高催化剂脱硝效率,对大幅度降低脱硝成本具有重要意义.Ce元素作为一种稀有金属元素在提高催化剂低温活性方面的优异表现逐渐得到认可[12-13],Ce-Ti混合金属氧化物催化剂不但表现出优异的SCR脱硝性能,并具有较好的抗水抗硫性[14].
气体在催化剂表面的吸附是催化反应过程进行的前提,反应气体在催化剂表面的吸附特性是影响催化剂的脱硝效率的重要因素.Peng等[15]研究了NH3在Fe、Mn等元素改性的CeO2表面的吸附特性,结果表面Fe和Mn原子的掺杂显著改变催化表面,并产生更多的氧空位,促进NH3的吸附.Yang等[16]应用GGA-PAW方法研究了NO在CeO2(110)表面的几个吸附位点,结果表明,分子在吸附位点的吸附均表现为分子与表面之间的弱相互作用,NO在该表面难以稳定吸附.
因此,本研究通过溶胶-凝胶法制备多元(Ti-Fe-Ce)混合金属氧化物催化剂,利用3种金属氧化物之间的协同作用提升催化剂的脱硝性能,优化各组分掺杂比例以获得脱硝活性最好的催化剂.同时,建立相应的表面吸附模型,利用第一性原理探究不同元素掺杂对反应气体(NO、NH3)在催化剂表面吸附特性的影响,进一步指导催化剂的性能优化.
1 实验及模拟
1.1 催化剂的制备
利用溶胶-凝胶法制备Ti-Fe-Ce混合金属氧化物催化剂,根据各元素摩尔比例将催化剂标记为TiFeCeO,其中Ti为0.1mol.首先,称取一定量的硝酸铁(Fe(NO3)3·9H2O,分析纯)和硝酸铈(Ce(NO3)3·6H2O,分析纯)溶于30mL去离子水中,搅拌0.5h直至全部溶解得到溶液A,并调节溶液pH=1.同时,称取34mL钛酸四丁酯(Ti(OC4H9)4,分析纯)溶于100mL无水乙醇,搅拌0.5h得到溶液B.随后,将溶液B添加至溶液A中得到混合溶液C,将C溶液置于恒温油浴磁力搅拌器中,在室温(25℃)下搅拌1h得到透明溶胶.最后,将得到的透明溶胶在60℃下回流、老化4h得到湿凝胶.将湿凝胶放置105℃干燥箱内干燥24h后在马弗炉内400℃下煅烧5h,研磨、筛分取粒径为0.30~0.45mm的颗粒备用.
1.2 催化剂活性测试
NH3-SCR催化剂活性测试系统如图1所示.实验模拟烟气组分以N2为平衡气,NO与NH3体积分数为700×10-6,O2体积分数为4%,总气量为1L/min.称取1g催化剂放置于石英管底部孔板上方,各组分气体经预混器充分混合后首先经过烟气旁路进入烟气分析仪(Gasmet,Dx4000)进行NO入口基准浓度标定.随后关闭烟气旁路阀门,模拟烟气进入竖直管式炉内的石英管中,经过催化剂后进入烟气分析仪测得NO出口浓度,活性测试温度为150~350℃,温度间隔50℃.实验空速为50000h-1,各个活性测试温度停留时间为60min.催化剂活性评价指标NO脱除效率定义为式(1)

式中:Cin为反应装置NO入口体积分数,10-6;Cout为反应装置NO出口体积分数,10-6.
1.3 催化剂表征手段
通过一定的表征手段对催化剂的理化性质(如晶型、气体吸附强度等)进行进一步的了解,为后续探究反应气体在催化剂表面的吸附提供事实依据.
1.3.1 XRD分析
本实验所使用的D8 ADVANCE X射线衍射仪产自荷兰的帕纳克公司,其角度精度0.0025°,分辨率0.037°;正比探测器X’Celerator,测量角度范围,步长为0.033°,扫描方式为/.管电压40kV,电流30mA.
1.3.2 TPD分析
本实验所用的全自动化学吸附仪产自中国教学仪器设备有限公司,型号为Auto ChemTMⅡ 2920,其最高工作温度为1100℃,可进行TPR、TPO、TPD (程序升温脱附)等测试.首先,将0.2g催化剂放置于仪器吸附室内,以10℃/min升温至50℃后利用He气吹扫30min.通入体积分数为5%的NO(NH3),在50℃下恒温吸附NO(NH3)至饱和状态.随后关闭吸附气体并用He气吹扫10min,最后以10℃/min升温至400℃,采集脱附数据.
1.4 表面吸附模型建立及计算方法
本文利用Material Studio模拟软件探究NO和NH3在催化剂表面的吸附特性.催化剂XRD表征显示TiO2主要以锐钛矿晶体结构存在,因此采用晶格常数为==0.3776nm、=0.9486nm的锐钛矿晶胞模型.沿晶胞(101)面切割并建立2×3超胞得到表面吸附模型S1(TiO2催化剂吸附模型).随后将S1中两个Ti5c原子分别替换为Fe原子和Ce原子得到Fe、Ce共掺杂的表面吸附模型S2(TiFe0.5Ce0.1O催化剂吸附模型),将S2表面与Fe原子相连的O2c原子删除后得到含有氧空位的表面吸附模型S3(TiFe0.5Ce0.1O催化剂吸附模型).表面吸附模型S1、S2、S3如图2所示,模型中红色小球代表O原子,灰色小球代表Ti原子,绿色小球代表Fe原子,黑色小球代表Ce原子,黄色区域代表O空位.吸附表面按照配位数分为O2c、O3c、Ti5c、Ti6c共4种吸附位点,Ti5c是吸附能力较强的一个位点[17],因此本文以Ti5c吸附位点为研究对象.
利用模拟软件对NO和NH3在不同催化剂表面的吸附能力进行研究,气体分子在模型表面的吸附能定义为
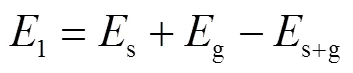
式中:1为吸附能;s为吸附模型能量;g为吸附气体的能量;s+g为气体吸附于模型表面后的总能量.当吸附能为正值时,气体吸附为放热反应,气体能够稳定地吸附于催化剂表面,吸附能越大气体越容易吸附.当吸附能为负值时,气体在表面吸附需要吸热,气体不易吸附且吸附状态不稳定.
TiO2锐钛矿晶体内部掺杂Fe、Ce原子后,部分Ti原子分别被Fe、Ce原子替代,导致晶体结构发生畸变,产生更多的氧空位[18].氧空位形成能定义为
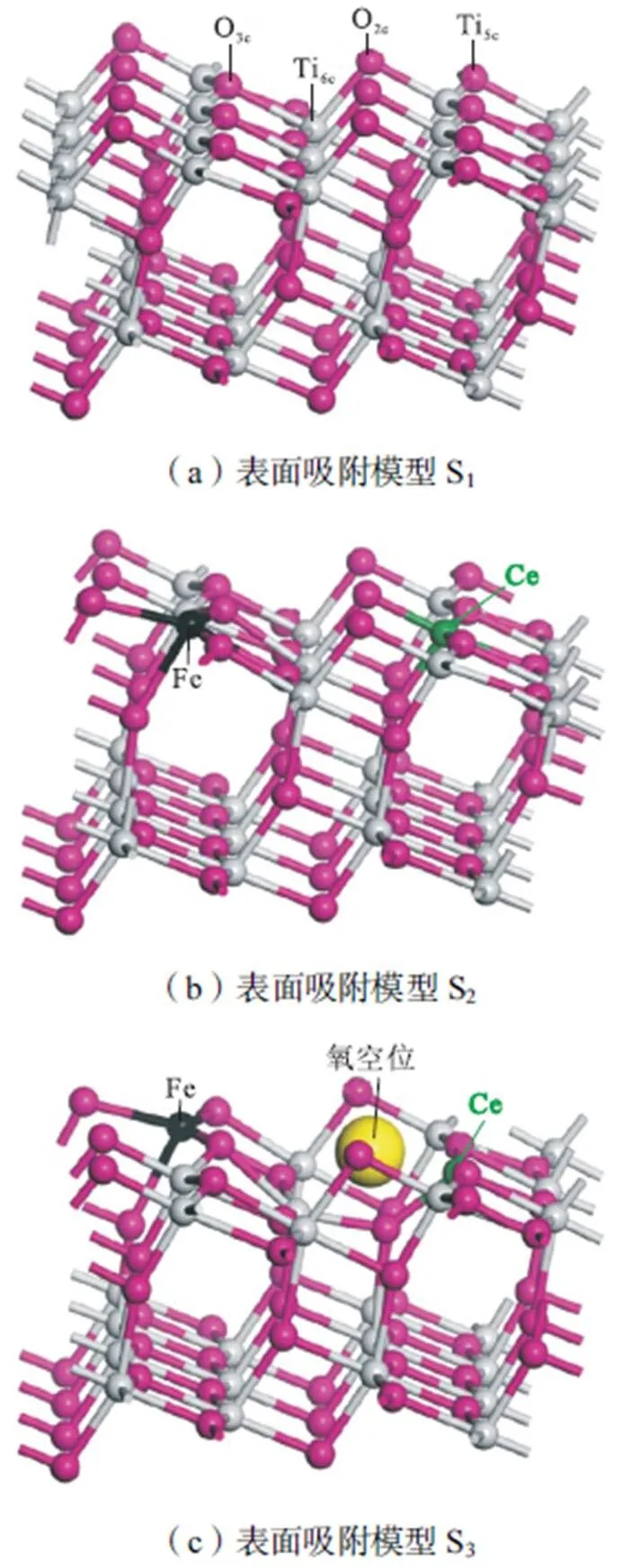
图2 表面吸附模型S1(TiO2)、S2(Fe、Ce掺杂TiO2)、S3(含O空位的Fe、Ce掺杂TiO2)

式中:v为删掉O原子后晶胞总能;O为O原子能量;c为完整晶胞总能.
2 结果与讨论
2.1 催化剂脱硝活性
混合金属氧化物催化剂TiO2、TiFeO和TiFeCeO的NO脱除效率如图3所示.从图3(a)中可以看出,TiO2在整个温度区间内脱硝活性较差,350℃时NO脱除效率最大值仅为22%.当Fe元素掺杂进入TiO2后,催化剂活性显著增加,300℃时TiFe0.5O的NO脱除效率达到85%左右,且随着温度的增加(300~350℃)催化活性仍保持在较高水平.但在低温区(100~250℃)催化剂的脱硝效率较差,其NO脱除效率最高只有75%. Fe2O3仅对催化剂在高温区的脱硝活性存在明显的提升作用,在中低温区,特别是在低温区,催化剂的脱硝活性仍难以满足实际工程要求.

图3 TiFexCeyOz催化剂NO脱除效率
Ce元素在提升催化剂低温性能方面效果显著[5,13],因此考虑在TiFe0.5O的基础上进一步掺杂CeO2对催化剂改性.图3(b)为TiFe0.5CeO(=0,0.1,0.2,0.3)催化剂在150~350℃区间内NO脱除效率.随着Ce元素的掺杂,催化剂在150~250℃内的脱硝活性进一步提高,TiFe0.5Ce0.1O在250℃时脱硝效率达到90%.当反应温度超过250℃后,催化剂的脱硝效率出现了轻微下降,说明CeO2导致催化剂热稳定性下降,但其在高温区内的NO脱除效率仍然保持在80%~90%.综合比较,TiFe0.5Ce0.1O催化剂中Ti、Fe、Ce 3种金属元素表现出较好的协同作用,使催化剂在低温区以及高温区均获得优秀的脱硝 活性.
2.2 XRD表征
催化剂晶型对其脱硝效率存在较大的影响,为探究催化剂中金属氧化物的结晶程度以及晶体结构,对TiO2、TiFe0.5O、TiFe0.5Ce0.1O进行XRD测试,测试结果如图4所示.从图谱可以看出,TiO2催化剂在25°、38°、48°、62°处出现特征衍射峰,表现出典型的锐钛矿晶体结构.Fe元素加入后,TiFe0.5O催化剂的结晶程度大幅度增加,除锐钛矿晶型外还出现大量的Fe、Ti混合氧化物Fe2TiO5晶型.催化剂中的活性组分以无定型状态存在时的脱硝活性是远远强于活性组分以晶体结构存在时的脱硝活性[19],而Fe元素的加入促进了金属氧化物从无定型状态向晶体结构转变,不利于催化反应的进行.当Ce元素加入后,TiO2结晶程度大幅度下降,Fe、Ce氧化物以无定型高度分散于TiO2锐钛矿晶胞内部.25°处锐钛矿峰值右移,说明Fe、Ce的加入使得部分Ti原子被取代,晶格缺陷严重甚至出现部分晶型改变.催化剂表面产生更多的氧空位以及活性位点,促进反应气体吸附,大幅度提升催化剂的脱硝活性.
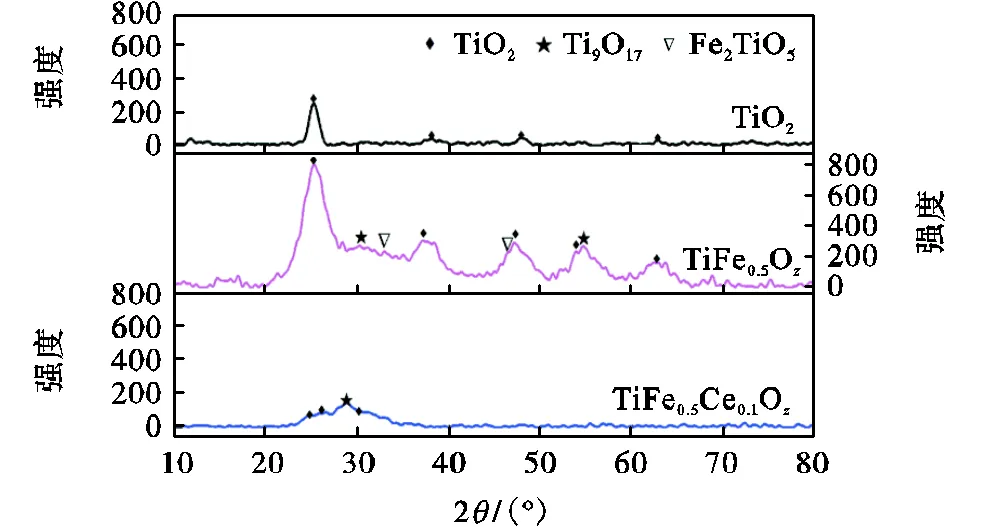
图4 TiO2、TiFe0.5Oz、TiFe0.5Ce0.1Oz催化剂的 XRD图谱
2.3 NO、NH3-TPD表征
低温脱硝过程中NO和NH3首先吸附于催化剂表面,NO吸附后转变为—NO2并与表面吸附的NH4+结合生成NH4NO2中间体,最后分解为N2和H2O.该反应过程中气体吸附是决定反应速率的重要因 素[20].因此,研究NO、NH3在催化剂表面吸附特性对催化剂开发研究至关重要.TiO2和TiFe0.5Ce0.1O催化剂在50~400℃温度区间内的NO-TPD和NH3-TPD曲线如图5所示.
从图中可以看出NH3在TiO2催化剂表面的脱附量远远大于NO,125℃时达到脱附最大值并在随后的升温过程中基本保持不变.而TiO2催化剂表面的NO脱附强度较弱,在100℃附近NO脱附出现一个微小的峰值之后便快速下降.TiO2掺杂Fe、Ce元素后,TiFe0.5Ce0.1O催化剂表面的NH3脱附峰提前至100℃,且峰值出现一定程度的上升,但整体上NH3的脱附强度变化不大.NO在TiFe0.5Ce0.1O催化剂表面的脱附强度出现明显的提升,100℃附近出现NO脱附峰,且NO的脱附强度在100~400℃温度区间内保持在0.005以上.气体脱附量越大、脱附强度越大说明气体在催化剂表面的吸附也就越多.从气体脱附曲线可以看出,NO在催化剂TiFe0.5Ce0.1O表面的吸附明显增强,该催化剂的脱硝效率也出现明显提升,250℃时NO脱除效率由TiO2催化剂的20%上升至TiFe0.5Ce0.1O催化剂的90%.由此可以推测出NO在TiO2催化剂表面的弱吸附是影响其脱硝效率的重要因素.对比NO和NH3在催化剂TiFe0.5Ce0.1O的吸附量,NO的弱吸附仍然是限制TiFe0.5Ce0.1O催化剂脱硝活性的主要原因.

图5 NO、NH3在TiO2和TiFe0.5Ce0.1Oz催化剂表面脱附曲线
2.4 NO、NH3在催化剂表面吸附特性
NO和NH3均以N原子为吸附端垂直放置于S1表面Ti5c上方、S2表面Fe5c、S3表面Fe4c上方,N原子与吸附位点初始距离为0.2nm.随后对该模型进行结构优化得到气体分子吸附结构,NO、NH3在表面吸附模型S1、S2、S3的吸附结构、吸附距离及其吸附能如表1所示.
表1 NO、NH3在S1、S2、S3的吸附结构、吸附能及吸附距离

Tab.1 Adsorption structure,adsorption energy and adsorption distance of NO and NH3 in models S1,S2 and S3
NO和NH3在表面吸附模型S1吸附能分别为62.4kJ/mol和109.4kJ/mol,吸附过程放出热量,模型总能量下降,气体吸附结构稳定,NO和NH3在模型表面均为化学吸附,能够稳定地吸附于催化剂表面.相比于NH3的吸附,NO在表面吸附模型S1的吸附能力较弱,结果显示NO在表面吸附模型S1的吸附距离为0.2468nm,且吸附能仅约为NH3吸附能的一半,吸附能力较弱.掺杂Fe、Ce原子后,NH3在表面吸附模型S2的吸附性更强,气体向模型表面靠近,吸附距离减小至0.1982nm.吸附能也由109.4kJ/mol增加至149.8kJ/mol,气体更容易吸附于模型表面,吸附结构也更加稳定.表面吸附模型S2对NO表现出极强的吸附能力,NO在表面吸附模型S2的吸附距离减小至0.1682nm,吸附能由62.4kJ/mol增加至214.8kJ/mol,吸附难度下降.从实验结果也可以看出,由于NO吸附量的增加,TiFe0.5Ce0.1O催化剂在整个温度区间的脱硝效率都出现了明显的提升.
表面吸附模型S3氧空位形成能为240.21kJ/mol,O原子脱离时模型表面放热,O空位形成难度较低.NO表面吸附模型S3稳定吸附时,吸附距离分别为0.1651nm,吸附能为313.49kJ/mol.O空位促进NO在催化剂表面吸附,吸附难度进一步下降.但NH3在表面吸附模型S3的吸附却受到抑制,吸附能下降为92.75kJ/mol,气体分子与催化剂表面吸附距离增大至0.2003nm.
3 结 论
采用溶胶-凝胶法制备了一系列Ti-Fe-Ce混合金属氧化物催化剂,探究不同金属元素对催化剂脱硝性能的影响以及不同金属氧化物间的协同作用,并利用Material Studio软件对NO和NH3在催化剂表面的吸附特性进行研究.实验结果表明:
(1) TiO2的凝胶作用与Fe3+、Ce3+在溶液中的分散作用相互协同可以获得均匀度较高的混合金属氧化物,Ce元素能够促进Ti、Fe、Ce 3类金属元素互相掺杂,Fe和Ce均以无定型高度分散在锐钛矿晶胞内部.TiFe0.5Ce0.1O催化剂中Ti、Fe、Ce 3种金属元素表现出较好的协同作用,使得催化剂在低温区以及高温区均获得优秀的脱硝活性,当反应温度为250℃时脱硝效率达到90%左右.
(2) NO在催化剂表面吸附较弱,在TiO2表面只有微量的吸附,Fe、Ce元素的掺杂能明显提升NO在TiFe0.5Ce0.1O催化剂表面的吸附能力,但NO吸附量仍远远小于NH3的吸附量,NO的弱吸附性是影响催化剂脱硝效率的重要因素.
(3) 通过模拟计算结果发现,随着Fe、Ce的掺杂,NO和NH3在催化剂表面的吸附能由62.4kJ/mol和109.4kJ/mol增大至214.8kJ/mol和149.8kJ/mol,吸附距离由0.2468nm和0.2288nm减小至0.1628nm和0.1982nm,吸附难度下降,吸附状态更加稳定.同时,由于锐钛矿中部分Ti原子被Fe、Ce原子代替,晶胞畸变并产生更多的氧空位,进一步促进NO的吸附,但对NH3的吸附却产生一定的抑制作用.
[1] 朱崇兵,金保升,李 锋,等. 蜂窝状V2O5-WO3/TiO2催化剂脱硝性能研究[J]. 中国电机工程学报,2007,27(29):45-50.
Zhu Chongbing,Jin Baosheng,Li Feng,et al. Study on de NOperformance of honeycomb V2O5-WO3/TiO2catalysts[J].,2007,27(29):45-50(in Chinese).
[2] Liu Fudong,He Hong,Zhang Changbin. Novel iron titanate catalyst for the selective catalytic reduction of NO with NH3in the medium temperature range[J].,2008,204(17):2043-2045.
[3] Wang Qiaoyun,Xu Hailong,Huang Wentao,et al. Metal organic frameworks-assisted fabrication of CuO/Cu2O for enhanced selective catalytic reduction of NOby NH3at low temperatures[J].,2019,364:499-508.
[4] Wang Chao,Yu Feng,Zhu Mingyan,et al. Highly selective catalytic reduction of NOby MnO-CeO2-Al2O3catalysts prepared by self-propagating high-temperature synthesis[J].,2019,75:124-135.
[5] Shen Qun,Zhang Lingyun,Sun Nannan,et al. Hollow MnO-CeO2mixed oxides as highly efficient catalysts in NO oxidation [J].,2017,322:46-55.
[6] Liu Zhiming,Su Hang,Chen Biaohua,et al. Activity enhancement of WO3modified Fe2O3catalyst for the selective catalytic reduction of NOby NH3[J].,2016,299:255-262.
[7] Chen Zhihang,Wang Furong,Li Hua,et al. Low-temperature selective catalytic reduction of NOwith NH3over Fe-Mn mixed-oxide catalysts containing Fe3Mn3O8phase[J].,2011,51(1):202-212.
[8] Cui Xiaojing,Xu Jian,Zhang Chenghua,et al. Effect of pretreatment on precipitated Fe-Mo Fischer-Tropsch catalysts:Morphology,carburization,and catalytic performance[J].,2011,282:35-46.
[9] Shu Yun,Aikebaier Tanana,Quan Xie,et al. Selective catalytic reaction of NOwith NH3over Ce-Fe/TiO2-loaded wire-mesh honeycomb:Resistance to SO2poisoning[J].,2014,150-151:630-635.
[10] Chang Huazhen,Zhang Tao,Dang Hao,et al. Fe2O3@SiTi core-shell catalyst for the selective catalytic reduction of NOwith NH3:Activity improvement and HCl tolerance[J].,2018,8(13):3313-3320.
[11] Cai Sixiang,Hu Hang,Li Hongrui,et al. Design of multi-shell Fe2O3@MnO@CNTs for the selective catalytic reduction of NO with NH3:Improvement of catalytic activity and SO2tolerance[J].,2016,8(6):3588-3598.
[12] Yan J F,Qiu W G,Song L Y,et al. Ligand-assisted mechanochemical synthesis of ceria-based catalysts for the selective catalytic reduction of NO by NH3[J].,2017,53(7):1321-1324.
[13] Peng Yue,Liu Caixia,Zhang Xueying,et al. The effect of SiO2on a novel CeO2-WO3/TiO2catalyst for the selective catalytic reduction of NO with NH3[J].,2013,140-141:276-282.
[14] Fei Zhaoyang,Yang Yanran,Wang Minghong,et al. Precisely fabricating Ce-O-Ti structure to enhance performance of Ce-Ti based catalysts for selective catalytic reduction of NO with NH3[J].,2018,353:930-939.
[15] Peng Yue,Yu Weiwei,Su Wenkang,et al. An experimental and DFT study of the adsorption and oxidation of NH3on a CeO2catalyst modified by Fe,Mn,La and Y[J].,2015,242:300-307.
[16] Yang Zongxian,Woo Tom K,Hermansson Kersti. Adsorption of NO on unreduced and reduced CeO2surfaces:A plane-wave DFT study[J].,2006,600(22):4953-4960.
[17] Wanbayor Raina,Ruangpornvisuti Vithaya. Adsorption of CO,H2,N2O,NH3and CH4on the anatase TiO2(001) and(101)surfaces and their competitive adsorption predicted by periodic DFT calculations[J].,2010,124(1):720-725.
[18] Rafique Muhammad,Shuai Yong,Hassan Muhammad. Structural electronic and optical properties of CO adsorbed on the defective anatase TiO2(101)surface;A DFT study[J].,2017,1142:11-17.
[19] 王 栋,吴惊坤,牛胜利,等. Sn、Ti掺杂改性γ-Fe2O3催化剂结构及NH3-SCR脱硝活性研究[J]. 燃料化学学报,2015,43(7):876-883.
Wang Dong,Wu Jingkun,Niu Shengli,et al. Structural property of γ-Fe2O3catalysts doped with Sn and Ti and their activity in the selective catalytic reduction of NO[J].,2015,43(7):876-883(in Chinese).
[20] Chen Liqiang,Yuan Fulong,Li Zhibin,et al. Synergistic effect between the redox property and acidity on enhancing the low temperature NH3-SCR activity for NOremoval over the Co0.2CeMn0.8-xTi10(=0—0.40) oxides catalysts[J].,2018,354:393-406.
SCR de NOand Gas Adsorption Characteristics of TiFeCeOCatalyst
Li Shuaifei,Lü Yuan,Niu Yanqing,Wen Liping,Hui Shi’en
(School of Energy and Power Engineering,Xi’an Jiaotong University,Xi’an 710049,China)
In this paper,mixed metal oxides(TiFeCeO)were prepared by the sol-gel method,and the de NOefficiency of catalysts was investigated. At the same time,the adsorption characteristics of the reaction gas(NO and NH3)on the catalyst surface were studied on the basis of the first principle. The results showed that the de NOefficiency increased with the addition of Fe and Ce to the catalyst. The highest NO conversion efficiency was above 90% within the low temperature range(100—250℃). After the doping of Fe and Ce,the adsorption difficulty of the reaction gas on the catalyst surface decreased. Meanwhile,the symmetry of anatase cell decreased due to the blend of metal oxide,and the number of oxygen vacancies increased,which promoted the adsorption of reaction gas.
mixed metal oxides;selective catalytic reduction;de NOefficiency;gas adsorption
TQ426
A
1006-8740(2022)04-0457-07
10.11715/rskxjs.R202112016
2021-03-22.
国家自然科学基金资助项目(51776161).
李帅飞(1994— ),男,硕士研究生,lishuaifei@stu.xjtu.edu.cn.
牛艳青,男,博士,副教授,yqniu85@mail.xjtu.edu.cn.
(责任编辑:隋韶颖)
