非小细胞肺癌KRAS 基因突变的临床治疗研究进展
2022-08-23庞雅琪刘思琪李代龙许新华通信作者
庞雅琪,刘思琪,李代龙,许新华通信作者)
(三峡大学 第一临床医学院[宜昌市中心人民医院] 肿瘤科 & 三峡大学肿瘤防治中心 & 三峡大学肿瘤研究所,湖北宜昌 443000)
0 引言
非小细胞肺癌(NSCLC)病死率呈连年上升趋势,据WHO 全新数据显示,2020 年全球恶性肿瘤病死数为996 万例,其中肺癌死亡数达180 万例,远超其他类型癌症[1]。过去针对NSCLC 的治疗策略多以手术、化放疗为主。表皮生长因子受体(EGFR)突变基因做为 NSCLC 中最典型的驱动基因,与其相应的靶向药物(EGFR-TKI)的诞生及临床应用,推动着NSCLC 的治疗途径向靶向治疗时期迈进,携带敏感基因突变的末期NSCLC 患者5 年总生存期在临床明显改善[2]。鉴于现代基因检测水平及有关肿瘤讯号传导通路的发展,NSCLC相关驱动基因被先后发现,NSCLC 的分子基因谱也不断更新,除EGFR 外,还包括 KRAS 基因等,本文对KRAS 基因突变NSCLC 治疗研究进展作一简述,以提供更多的诊治策略。
1 KRAS 突变肺癌患者的流行病学特点
KRAS 充当RAS 基因家族的一员,是位于12号染色体上长约35kb 的一种原癌基因,该基因出现突变而被过度活化时,突变的KRAS 基因则连续不断触发下游MAPK 信号通路造成级联反应,导致细胞的增殖不易受限,继而形成肿瘤细胞[3]。RAS 基因家族有三种——K-ras、N-ras 和H-ras,其中K-ras 对机体患癌概率影响最大,早在1984年发觉KRAS 基因突变存在NSCLC 患者中,而后该基因逐渐成为针对NSCLC 治疗研究的突出靶点,KRAS 突变类型有G12C,G12V 和G12D,而在NSCLC 中主要为KRAS-G12C 突变[4]。有相关研究证明KRAS 基因在不同的种族中突变率表现具有差异性,在西方国家中突变率为25%~30%,而在亚洲国家中KRAS 突变发生率为5%~15%[5],相比从不吸烟者,KRAS G12C 突变机率在有吸烟史的NSCLC 患者中更高,且多见于腺癌患者,通常这部分患者肿瘤突变负荷占比也更高[6,7]。
2 NSCLC 患者针对RAS 信号通路的治疗
RAS 突变可恒久触发其下游通路的激活,常见的RAS 下游途径有MAPK 通路(RAS-RAF-MEKERK) 和PI3K 通路,其他依赖于RAS 激活的传导通路还包括TIAM1/ RAC/PAK[8-10],以下则针对KRAS 抑制剂及上述信号通路抑制剂进行阐述。
2.1 KRAS 抑制剂
RAS 蛋白翻译后成功进行法尼基化是将RAS蛋白设于胞膜内侧的必需修饰过程,故而遏制此途径可作为开拓新药剂的靶点之一[11]。研究人员基于法尼基化过程中的转移酶研制了相应药物,如lonafarnib、tiparfinib 等法尼基转移酶抑制剂(farnesyl transferase inhibitor,FTIs),但FTIs 对KRAS 突变肿瘤患者而言其疗效均已失败而告终,然而近年来发现 KRAS 基因中最常见的G12C 点突变为“不可成药”的靶点带来了新希望。一项Ⅰ期临床研究针对口服的KRAS G12C 突变小分子抑制剂——MRTX849,分析表明在NSCLC 患者中客观缓解率(Overall Response Rate,ORR)为50%,疾病控制率(Disease Control Rate,DCR)达到100%,这一研究结果颇受满意[12]。Mirati Therapeutics 等人共同研发了一种针对KRAS G12C 的共价拮抗剂——Adagrasib,关于Adagrasib 的临床Ⅱ期及Ⅲ期研究目前正在探索与免疫抑制剂联合使用以及单一疗法的疗效及耐药性[13,14]。虽然上述药物在相关研究中获得了显著益处,但国内外仍然没有批准合适KRAS G12C 突变患者的靶向药物,及至2021 年5 月28 日,美国FDA 宣告准许KRAS 抑制 剂Lumakras( 活 性 成 分sotorasib,AMG510) 上市,为首款治疗KRAS G12C 突变NSCLC 患者的靶向药物,此前在2019 年Ⅰ期临床试验研究10 例接受Lumakras 治疗NSCLC 患者,记录显示50%病人取得部分缓解,有40%达到病情稳定,疾病控制率(Disease Control Rate DCR) 达到90%,且药物安全性好[15]。而随即在CodeBreaK 100 临床试验中涵盖124 例KRAS G12C 突变接受免疫治疗和(或)化疗后发生疾病进展的NSCLC 患者,事实证明使用Lumakras 治疗的患者总缓解率为36%,DCR 达到81%,中位缓解持续时间为10 个月[16],Lumakras 也是首款证明可使患者实现无进展生存的靶向药物,FDA 对 Lumakras 的特批恰是基于CodeBreaK 100 临床实验结论。
2.2 RAF 抑制剂
RAF 拮抗剂被指出是治疗NSCLC 患者KRAS突变的潜在性药物,有相关研究显示索拉非尼可作为潜在靶向药物之一,但与其他药物相比疗效仍较差,临床试验结果尚无定论[11]。另有研究结果示在某些NSCLC 患者中过表达的Weel 可不同程度的影响索拉菲尼的疗效,利用Weel 拮抗剂MK1775联合索拉非尼治疗,可提高患者对索拉菲尼的反应性,但该结论还需进一步临床研究证实[17]。
2.3 MEK 抑制剂
丝裂原激活的细胞外信号调节激酶(mitogenactivated extracellular signal-regulated kinase MEK)是KRAS 下游信号的转导蛋白, 针对末期KRAS基因突变NSCLC 患者来说,MEK 抑制剂单药治疗临床疗效一直差强人意[18],MEK 抑制剂联合治疗研究结果也不径相同,司美替尼(selumetinib)作为MEK 拮抗剂的一种,尚有数项临床研究证明其药物疗效。一项Ⅱ期临床试验,将患者划分为RAS G12C 突变及其他KRAS 突变,患者均给予selumetinib 联合多西他赛治疗,前者无进展生存期(Progression Free Survival PFS)、总生存期(Overall Survival OS)、ORR 均有明显改善的势态[19], 而在另一项Ⅲ期研究中,比较多西他赛联合selumetinib 较多西他赛单药相比,联合治疗对KRAS 突变患者而言未显著改善PFS、OS 及ORR,并且联合治疗带来的副作用更大[20]。比尼替尼(MEK162) 做为另一种MEK 拮抗剂,一项关于MEK162 在特定实体瘤或血液系统恶性肿瘤患者中疗效和安全性的Ⅱ期临床研究仍在进行中[21]。
2.4 PI3K 通路抑制
PI3K 作为KRAS 下游通路的效应激酶,与细胞癌变密切相关[22]。临床前证据显示,KRAS突变型肺癌依赖PI3K 通路途径的激活[11],故而PI3K 通路也是NSCLC 治疗的另一个关键靶点。当前针对NSCLC 患者PI3K 拮抗剂主要包含Pictilisib(GDC-0941)、Buparlisib(BKM120),在BASALT-1 研究列入了60 例治疗后病情复发的鳞癌与非鳞肺癌病人,经Buparlisib 治疗后12 周PFS 率在前者为23.3%、后者为20.0%,该分析表明PI3K 抑制剂与其它药剂联合治疗可能比单药治疗更合理,BASALT-1 在第1 阶段没有达标,故两组均未启动第2 阶段[23]。关于GDC-0941 的I期临床研究显示出良好的耐受性和安全性,其在NSCLC 的临床疗效需待进一步验证[22]。
3 KRAS 突变肺癌患者的免疫治疗
近些年来,免疫检查点抑制剂(ICIs)的发展中热火朝天,免疫治疗在各类实体瘤研究中接连获取好评,免疫检查点在机体免疫系统中起保障作用,遏止T 细胞极度活化而导至炎症损伤等[24],肿瘤细胞借由机体免疫系统此种特点,依此过度表达出免疫检查点分子,进而逃离人体免疫监视与杀伤,扼制T 细胞诱导的免疫反应,加剧肿瘤细胞胞的繁殖生长[25]。ICIs 主要包括PD-1/PD-L1 抑制剂和CTLA4/B7 抑制剂,ICIs 通过阻遏不同通路,再次诱发T 细胞对肿瘤细胞的杀伤活性,皆以发挥抗肿瘤作用,其中以PD-1/PD-L1 为典型的ICIs 发展尤为迅速,在肺癌患者中也显示出了良好的治疗趋势,单药ICIs 及免疫联合策略已在晚期NSCLC 中火热开展。
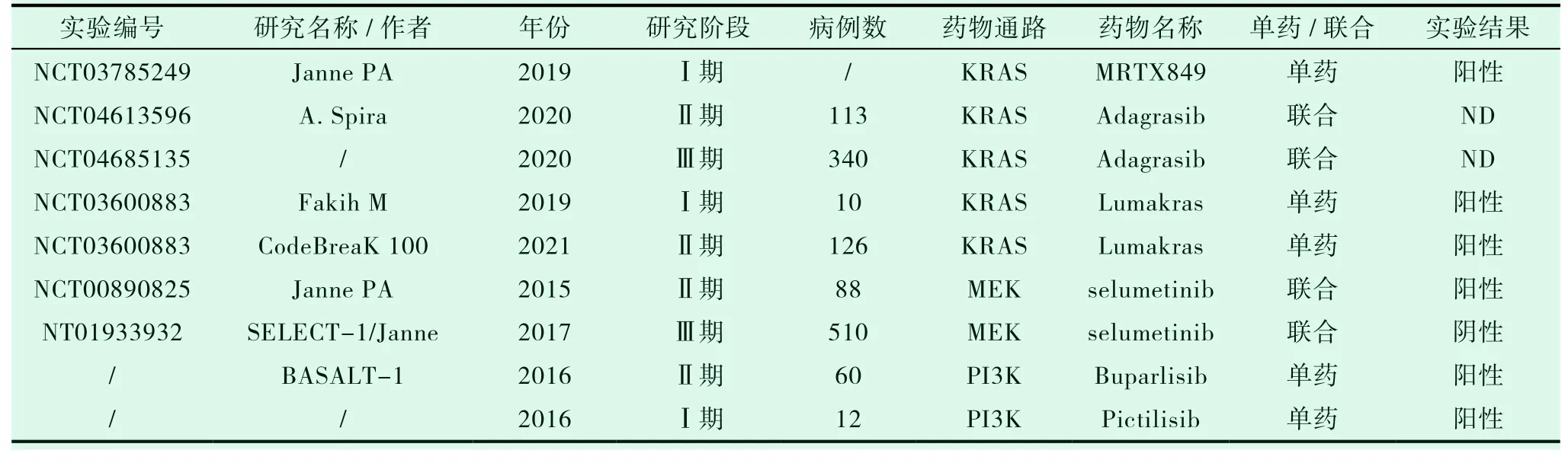
表1 不同靶向药物治疗KRAS 突变晚期NSCLC
3.1 单药ICIs
在BIRCH 二期试验中,研究人员使用免疫单药阿特丽珠单抗(Pembrolizumab) 对KRAS突变患者疗效明显优于KRAS 野生型患者[26],KEYNOTE-042 是一项随机、开放的大型Ⅲ期临床研究,该研究包含KRAS 突变的患者,KRAS 突变患者接受Pembrolizumab 的中位PFS 为12 个月,客观缓解率为56.7%,特别在KRAS G12C 突变的病人中,客观缓解率为66.7%,中位无进展生存期为15 个月,其结果显示较阴性患者而言客观缓解率、PFS 及OS 明显获益[27],同样在KEYNOTE-189研究[28]中包含有KRAS 突变、KRAS G12C 突变非鳞NSCLC 患者,与联合用药相比从Pembrolizumab单药治疗中取得OS 获益显著(HR=0.28)。CheckMate 057 研究[29]是一项Ⅲ期随机对照、双盲的临床研究,主要分析了纳武利尤单抗(Nivolumab)对比多西他赛单药治疗末期非鳞NSCLC 患者的药效差异,其中内含62 例KRAS 突变患者,此类病患经Nivolumab 治疗后总生存期(OS) 获益(HR=0.52,95%CI 0.29~0.95),而突变阴性病患OS 获 益 有 限(HR=0.98,95%CI 0.29~0.95)。OAK研究[30]是一项随机双盲Ⅲ期临床研究,将多西他赛及阿替利珠单抗的药效进行差异对比,亚组分析记录显示59 例KRAS 突变病患的OS 可从阿替利珠单抗治疗中获益(HR=0.71,95%CI 0.38~1.35)。
3.2 ICIs 联合治疗
除上述免疫单药治疗之外,另有研究者正积极探讨ICIs 与其他药物联合使用疗效,如Amgen等人研究Lumakras 与PD-1 抗体帕博丽珠单抗(pembrolizumab)的联用疗效[31],该研究在10 只接受联合治疗的小鼠身上进行,治疗后观察到其中9 只小鼠肿瘤成分被完全清除,且联合治疗治愈的小鼠,之后还具备排斥KRAS G12D 肿瘤的能力,表明联合治疗可能长期建立肿瘤T 细胞免疫应答,该研究还表明Lumakras 能增加CD8+T 细胞上的PD-1 表达,这在Lumakras 联合抗PD-1/PD-L1 治疗方面提供了机会,近期一项使用PI3K/PLK 抑制剂Rigosertib 联合免疫治疗药物PD-1 抑制剂纳武单抗,共同治疗KRAS 突变阳性非小细胞肺癌患者的临床试验正式开启(NCT04263090)。
综上所述,无论是单药ICIs 或是联合治疗都可能是晚期KRAS 突变NSCLC 最有前景的研究方向之一,今后需更多大型前瞻性临床研究来分析KRAS 突变NSCLC 病患,尤其是KRAS G12C 突变患者的免疫治疗疗效,且需探索最佳的用药剂量及联合方案,并重视不良反应的预防与管理。
4 总结与展望
经过几十载,曾一直作为“最难攻克靶点”的KRAS 突 变,自2021 年5 月FDA 首 次 获 批 的Lumakras (Sotorasib,AMG510)对其已有重大突破,这为全球肺癌患者带来福音,但Sotorasib 的上市并非最后终点,多款靶向药物不断涌现,并已有多个药物在临床研究阶段取得了早期成功,且通过基因检测技术的不断进步,同时可以使越来越多的晚期KRAS 突变NSCLC 患者获益,而单药治疗无论响应率还是持续时间都是有限的,越来越多的联合用药方案正在以更好的疗效占据着推荐治疗方案中更多的席位,在未来针对晚期KRAS 突变NSCLC患者而言联合治疗可能成为另一条有效途径。
