基于气相色谱的7种食品添加剂并行检测技术
2022-08-23徐大玮毕玉琦解恒杰
徐大玮,毕玉琦,解恒杰,刘 睿
(1.山东省食品药品检验研究院//山东省食品药品安全检测工程技术研究中心,山东 济南 250103;2.山东省质量技术审查评价中心有限公司,山东 济南 250014)
食品添加剂对于食品技术的发展有着重要的意义,目前来说我国法律明确的具体食品添加剂的种类超过2 000种[1]。食品添加剂的使用和消费情况。是食品工业和人们生活质量的一个有效反馈[2]。世界各地均存在大量的食品添加剂消费,从而使得食品添加剂的检测技术。成为一项关乎国民安全的重要技术[3]。
香料、甜味素等食品添加剂的使用可以有效提高食物的口感,并能在相当的范围内。提高食物的营养价值,提高其存储时间[4]。在法律规范内使用食品添加剂,可以有效地提高食品技术和食品行业的发展程度,也能使得人们的生活质量有所提高[5]。但是,违规使用食品添加剂,也对于人们造成严重的身体伤害和社会恐慌。“三鹿奶粉”的影响,依然多年不能消除。因此,对于食品添加剂的检测技术,受到业内的广泛重视[6]。
如何快速有效地完成食品添加剂的检测,规范检测单位的检测质量,提高食品加工企业的质量监管效果,受到各界的重视[6]。我们利用气相色谱技术,充分发挥其灵敏度高、选择性好的优点,建立一种并行的食品添加剂检测方法,该方法可以同时完成甜蜜素、丙酸、苯甲酸和山梨酸等多种食品添加剂的高效检测。优化后的检测工艺,可以有效节省检测过程中的资源,对于食品安全的监管和食品加工的检测方面,具有重要的意义。
1 基于气相色谱的检测技术
对于食品行业的监管,由于受到设备、资金、技术等方面的限制,使得其检测质量不能得到有效地保障[7]。标准检测方法由于效率低下,也会对食品行业的发展,造成一定的影响[8]。
对于食品添加剂的检测,可以采用分光光度法、色谱法等[9]。色谱法主要包括气相色谱、液相色谱和离子色谱等[10]。这些方法均能有效完成食品添加剂的检测,但是分光光度计法的检测精度较低,不能满足检测要求[11]。气相色谱由于检测效率高,检测成本较低,发展迅速[12]。
利用色谱技术,可以对多种食品添加剂进行并行检测,整个实验过程的工作流程见图1。

图1 气相色谱并行检测技术流程
通过在提取后的样品中添加沉淀剂,从而将检测样品进行分离[13]。提取滤液后分别通过添加不同的试剂进行样品处理,使得处理后的提取液。能够满足气相色谱的检测要求,进而可以完成不同添加剂的检测。通过对于工艺参数的调整和优化,利用该方法,可以同时完成甜蜜素、丙酸、苯甲酸和山梨酸等多种食品添加剂的高效检测[14]。
2 实验材料与方法
2.1 实验材料
实验中使用的各种待检测食品均购自某正规超市,采购的食品主要包括桃酥、蛋糕、果酱、糯米糕、饼干等。
实验采用的色谱级试剂主要包括有正己烷、乙酸乙酯、甲醇、无水乙醇等。
实验用的其他试剂均为分析纯,包括盐酸、硫酸、亚铁氰化钾、乙酸锌、亚硝酸钠、氯化钠等。
实验采用的食品添加剂物质信息见表1,实验采用的添加剂均购自于天津科密欧。

表1 食品添加剂物质信息
2.2 实验设备
实验中使用的仪器主要如表2所示。

表2 仪器设备
2.3 实验条件与试验步骤
2.3.1实验样品处理
称取定量样品置于离心管中,样品质量选择为15 mg。对离心管中的样品加纯水进行稀释至30 ml,并进行超声处理,促进其融合,超声时间为18 min。对样品中添加沉淀剂,分别加入亚铁氰化钾和乙酸锌各3 ml,加盖后通过混合仪进行2 min振荡和6 min 5 000 r/min离心处理。过滤后超声脱气处理10 min后静置,获取其分层后上部清液。
分别取出10 ml置于2支不同的比色管中。一支利用酸溶液进行酸化,实验采用1 ml的盐酸作为处理溶液,酸化后加入正己烷,体积为5 ml。混合后的溶液进行涡旋振荡后静置分层,提取上清液待处理。另一支比色管中加入硫酸和亚硝酸钠溶液,体积均为5 ml。冰浴30 min后加入正己烷,体积为5 ml,加入氯化钠晶体5 g。充分混合后置于室温,取其上清液备用。
将两支比色管中提取出的上清液进行混合,提取上层液体并通过滤膜过滤,得到待检测液体。
2.3.2标准溶液的配制
根据标准品的配制浓度要求来称量实验中需要的标准品质量,配置后的溶液浓度为10 mg/ml,由于不同的标准品对于溶剂的要求不同,因此需要根据实际情况来选择水、甲醇、无水乙醇等溶剂。配制好的溶液需要低温存储,通常情况下保存完好的溶液有效期长达1年[15]。
将本实验中所需要的多种防腐剂进行配制成10 ml,浓度为1.0 mg/ml的标准溶液,用乙酸乙酯为溶剂,对其进行定容。
2.4 试验方法
市面上的面包、糕点、食醋、果酱等商品几乎都含有甜蜜素和不同的防腐剂,以提高其口感和保质期。在本实验样品中添加不同的检测标准溶液,浓度为100 μg/ml。
对混合后的溶液进行多次检测,取平均值,从而计算该被检测物的回收率情况。选取不同的浓度点,对实验样品进行测试,从而得到其线性方程和相关系数等。
2.5 实验数据处理
每个实验均采用5组平行数据取平均值的方式,进行数据处理,用SPSS16.0软件进行统计分析。
3 实验结果与数据分析
3.1 前处理条件优化
3.1.1沉淀剂的影响
对于实验样品的处理,需要添加不同的沉淀剂,以使样品中的蛋白质变成固体沉淀,从而与样品进行分离。实验中常用的沉淀剂有多种,主要包括金属的化合物溶液,乙醇等有机溶剂或者一些碱性混合溶液等。通过不同的沉淀剂进行对比,可以发现不同的沉淀剂效果相差明显。亚铁氰化钾和乙酸锌的混合溶液,对于样品的沉淀速率较慢,且色谱分离效果较差。利用乙醇作为沉淀剂的样品虽然可以具有很好的沉淀效果,但是在色谱分析中出现若干杂质吸收峰,不利于本实验。而采用亚铁氰化钾和硫酸锌的混合溶液,不仅沉淀效果好,沉淀速率快,且无杂质吸收峰,从而可以用于本研究的实验沉淀剂。最终通过不同配比的对比,实验选择的沉淀剂为20%比例亚铁氰化钾和25%比例硫酸锌的混合溶液。沉淀剂使用量的不同也会对于其沉淀效果造成影响。选取5 g样品,对其添加不同质量的沉淀剂,比较其沉淀情况,沉淀结果见图2。

图2 沉淀剂与沉淀时间的关系
由图2可见,对于不同用量的沉淀剂使用情况,其沉淀时间具有明显的区别。在沉淀剂用量低于2.5 ml的情况下,其沉淀时间均超过5 min,在沉淀剂更低的情况,其沉淀时间甚至超过了15 min。当沉淀剂超过2.5 ml时,沉淀时间大幅下降,在对其进行8 000 r/min 离心处理,离心时间5 min后,可以获得高质量的上清液。为了有效节省实验的耗材成本,沉淀剂的剂量选择为2.5 ml。
3.1.2试剂环境的影响
实验过程中的衍生反应发生在酸性环境中,通过改变实验酸性试剂浓度,室温下可以得到其与甜蜜素吸收峰面积的关系情况,见图3。

图3 硫酸与峰面积的关系
由图3中可见,随着反应剂中硫酸从25 g/L提高至250 g/L,甜蜜素的吸收峰逐渐增加。当超过250 g/L 之后,吸收峰的面积开始下降。
酸性环境的维持可以确保衍生反应的顺利进行,同时硫酸可以与亚硝酸钠发生反应,从而生成该气相色谱检测中需要的亚硝酸,并为化合物反应提供羟基。对于通常食品中约为0.20 mg/ml甜蜜素含量,采用250 g/L的硫酸可以满足实验要求。
3.1.3气相色谱优化
对于食品的并行检测技术来说,色谱的效果决定了整个检测的成败,因此色谱柱的选择至关重要。只有选择了合适的色谱柱,才能保证样品检测的灵敏度、检测分离度。
本实验检测内容主要针对糕点、食物佐料等的食品添加剂情况,尤其是关于甜蜜素和防腐剂类的检测,因此我们所比较和使用的色谱柱主要有三种,分别为HP-5、DB-wax和DB-17。在相同的溶液测试环境中,比较不同的色谱柱的检测结果。
最终,HP-5色谱相比其他两种色谱柱,其分离度更好,对于不同样品的检测结果也更合适,被选择为本实验的检测色谱柱,填料部分为5%含量的苯基和95%含量的聚甲基硅氧烷。
同样,对色谱柱中涉及到的温度因素进行比较,尤其是色谱柱的温度可以影响待检测物质的出峰情况,因此需要密切关注。柱温的升高有利于提高检测效率,但是也会降低色谱的分离。
经过多次实验比较,最终确定色谱柱温度为折线升温形式,温度曲线变化为75℃恒温5 min,后升温5 min,升温至200℃恒温3 min,继续升温2 min,升温至250℃保持5 min。
3.1.4进样的优化
对于进样的量来说,不能选择太大,否则容易造成色谱柱检测超载,形成峰形差或者色谱分离度差的情况。若进样量太小,则容易造成检测灵敏度下降,部分待检测组分出峰困难,从而影响检测效果。最终实验选择分流进样方式,进样分流比为8∶1,从而使得杂质峰较小,各检测峰的分离效果较好。
对于进样口来说,其温度要求要高于被分析组分的沸点,从而使得样品进入后能迅速气化。然而过高的温度会破坏样品的结果,造成降解。根据经验,需要使得进样口温度高于柱温20~80℃。
样品气化的效果会严重影响色谱的检测,气化不彻底容易形成峰形变化、峰距加剧等情况,影响分离消耗。最终根据本实验条件,选定进样口温度为 220℃,该条件下分离效果良好。
3.1.5气体流速的选择
气相色谱的检测实验主要涉及三种气体:空气、氮气和氢气。空气的作用为助燃气体,因此其流速流量会影响到样品检测的灵敏度。氮气作为载气,其流速的不同会严重影响分离的效果。氢气的流速会影响到整个样品检测的灵敏度。
根据实验比较和气相色谱的性能参数要求。最终确定氢气流速为45 ml/min,空气流速设置为450 ml/min,恒流模式下氮气的最佳流速为2 ml/min。
3.1.6气相色谱条件
本实验的气相色谱条件设定为:色谱柱选择为HP-5(30 m×0.25 mm×0.25 μm),利用氢火焰光度检测器进行实验检测。实验中的载气为氮气,流速选择为2 ml/min,其他实验中用到的气体如空气流速为450 ml/min,氢气流速为45 ml/min。采取分流进样方式,进样分流比为8∶1。
3.2 回收率和RSD
选择本实验采购的不同实验样品,并分别添加100 μg/ml的标准混合溶液,相同实验条件下,测定多次结果,取平均值,作为实验测试数据。加标回收率和相对标准偏差的实验结果见表3。
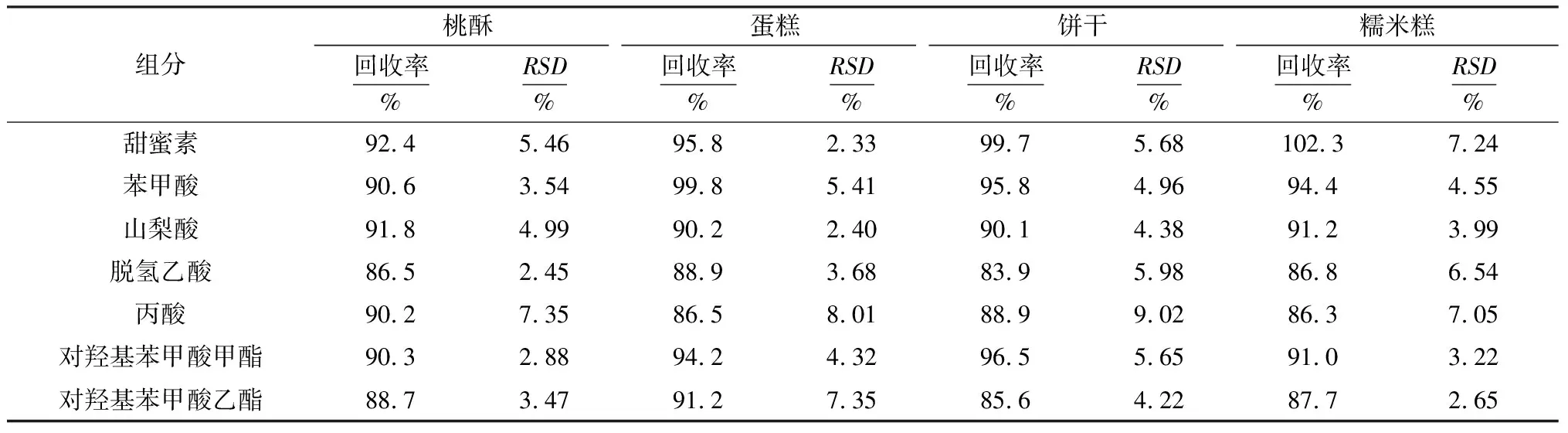
表3 加标回收率和相对标准偏差的实验结果
表3的实验结果表明,利用本实验方法,其加标回收率均超过83.9%,数值一般在83.9%~110%,相对标准偏差(RSD)最小值为2.33%,最大值为9.02%。从而可以在数据上证明本并行检测方法的有效性和精密度。
被测组分的回归方程以及相关系数等见表4。

表4 被测组分的回归方程以及相关系数
3.3 样品的检测
横向比较了不同检测样品的测试结果,利用购自超市的桃酥等糕点和果酱等佐料情况,作出相应的色谱检测,从而获得其添加剂的使用情况,实验结果见表5。
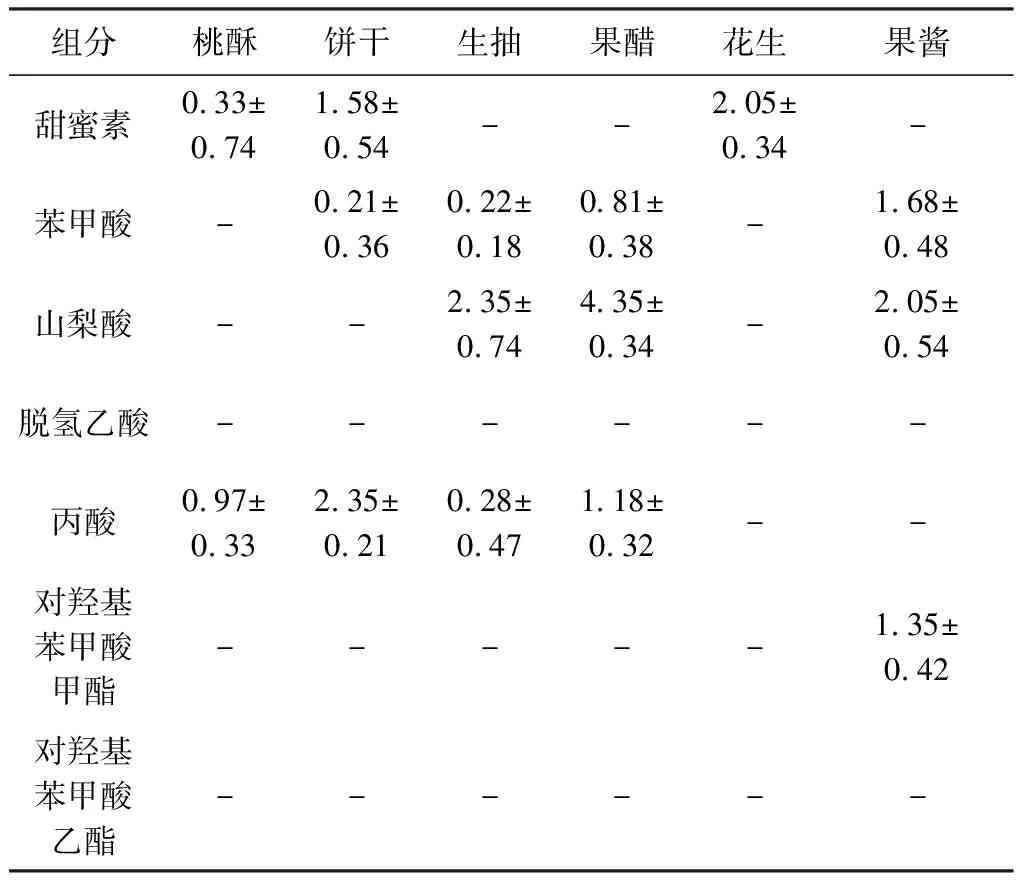
表5 商品中添加剂测试结果 mg/kg
从实验测试的数据结果,可以看到,对于桃酥中,存在有丙酸0.97 mg/kg和甜蜜素0.33 mg/kg的添加剂使用。而饼干中除了含有丙酸2.35 mg/kg和甜蜜素1.58 mg/kg以外,还被检测出使用了苯甲酸0.21 mg/kg。根据食品安全的规定,糕点类食品中,不应存在苯甲酸,因此该添加剂属于超范围使用情况。其他检测样品中,生抽和果醋均含有丙酸、山梨酸和苯甲酸,生抽总添加剂的含量分别为0.28、2.35、0.22 mg/kg。而果醋中的含量为1.18、4.35、0.81 mg/kg,而花生则使用了甜蜜素2.05 mg/kg,果酱中含有山梨酸2.05 mg/kg和苯甲酸1.68 mg/kg,且还有对羟基苯甲酸甲酯1.35 mg/kg。
其中饼干和桃酥的色谱图见图4、图5。
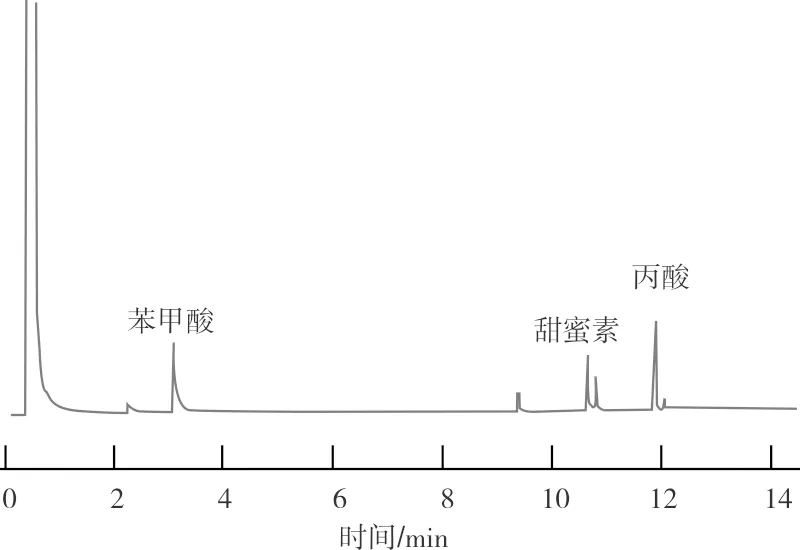
图4 饼干的色谱图
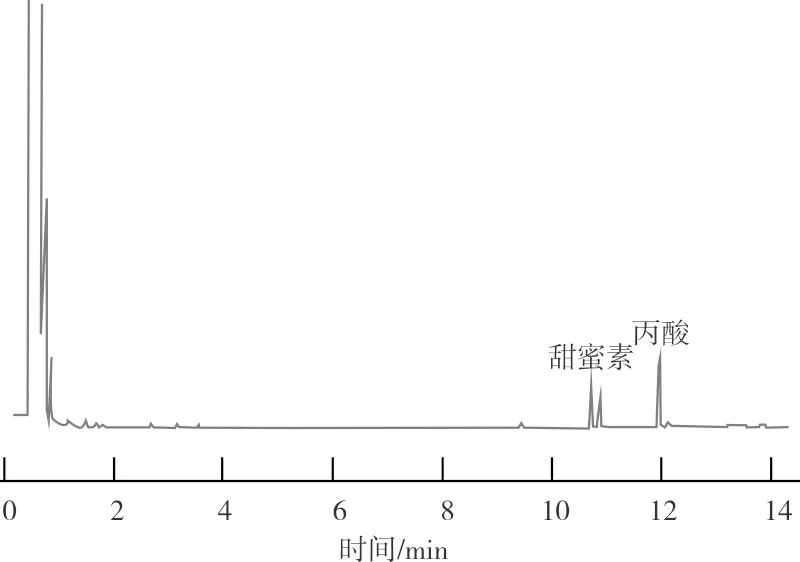
图5 桃酥的色谱图
3.4 与国标的比较
取其中一份样品利用本实验方法与国标方法进行直接对比。以含有丙酸与苯甲酸、甜蜜素的饼干样品为例,结果见表6。

表6 样本测试结果对比 mg/kg
表6可知,本实验方法与国标方法尽管结果稍有不同,但是也与其相差不大,属合理范围之内,证明本实验方法有效。
4 结论
本实验针对食品添加剂的并行检测,利用气相色谱技术,对于整个检测过程进行了优化和处理。最终通过调整沉淀剂的使用、前处理参数的细化、色谱柱的选择等条件优化,得到满足食品检测的多种添加剂并行检测气相色谱方案,实验结果证明本实验方法的回收率高和相对偏差较低,对于待检测添加剂具有很好的分离度和检测精度。
通过食品样品的测试验证,证明不同食品均可通过气相色谱的方法,同时检测出多种添加剂。并在饼干样品中检测出不符合规定的苯甲酸,证明本实验方法的有效性。本实验方法可以大量节省资源,提高检测效率,可以作为食品检测领域的一种重要检测手段。
