外加磁场对乙炔气体爆炸反应影响研究*
2022-08-18高建村杨喜港胡守涛洪子金李如霞夏艺萌
高建村,杨喜港,胡守涛,洪子金,王 乐,李如霞,夏艺萌,孙 谞
(1. 北京石油化工学院安全工程学院,北京 102617;2. 北京市安全生产工程技术研究院,北京 102617;3. 北京旭阳科技有限公司,北京 100067)
燃烧和爆炸基元的化学反应过程主要是自由基反应过程,自由基是磁性物质,磁场能对自由基产生作用,从而对燃烧产生一定的影响。很多学者认为磁场能促进甲烷、丙烷、LPG 的燃烧。Kumar 等和Agarwal 等使用圆光栅 Talbot 干涉仪发现梯度向上减小的磁场能促进燃烧,梯度向上增加的磁场则抑制燃烧,均匀磁场对火焰的影响可忽略不计。针对磁场影响燃烧的理论和动力学研究,Itoh 等、Kajimoto 等、Shinoda 等和Yamada 等通过PLIF 测量和数值模拟,研究了磁场对甲烷燃烧火焰中·OH 自由基的分布,发现磁场对·OH 自由基的作用力最大并使·OH 自由基聚集。高建村等研究发现,磁性金属阻隔防爆材料比非磁性金属阻隔防爆材料对丙烷爆炸具有更明显的抑制效果,还发现在相同填充密度下,非磁性金属阻隔防爆材料对乙炔爆炸具有促进作用,与对烷烃气体爆炸的影响效果相反。
乙炔作为最简单的炔烃分子,含有 C ≡C 叁键,有很高的化学反应活性,在当量浓度下最小点火能量可低至0.02 mJ,安全间隙也比烷烃气体小。乙炔爆炸是自由基反应,·O+CH是乙炔氧化的第一步,会生成H、HCCO、CH和CO 等。Bastin 等用分子束质谱仪测量了乙炔爆炸产物,也会生成CH、CH、CH、CH、CH、CH、CHO 和CHO。CH、CH、CH、CH等物质产生自由基的第一步都是脱去一个·H,生成·CH、·CH、·CH、·CH。CH产生自由基的第一步也是脱去一个·H,生成CH,CH+e=·CH+·H 是剧烈反应,这已被Winter 等用实验和理论证实。·CH 是乙炔爆炸反应的重要中间体,发生光解时会产生大量的·CH。McKee 等和Smith 等实验研究了OH + CH的反应速率并理论计算了此基元反应的压力、温度、焓变等热力学和动力学数据,证明此基元反应很容易被激发。Hiraoka 等用热解质谱和红外光谱研究低温下H 原子和固态C碳氢化合物的反应,发现固态C碳氢化合物与H 原子反应速率由高到低的顺序为:CH、CH、CH。
Yang 等发现磁场对丙烷爆炸具有一定的抑制效应。为了进一步研究磁场影响气体爆炸的特征,本文中将实验测量当量浓度乙炔爆炸火焰的传播速度和爆炸瞬态压力,并通过数值模拟研究磁场对乙炔爆炸反应自由基链式反应过程的影响,探究磁场影响乙炔爆炸的机理。
1 实验系统
实验系统由实验管道、磁场装置、爆速测量系统、瞬态压力采集装置、气体分配系统和点火装置组成,系统的示意图如图1 所示。
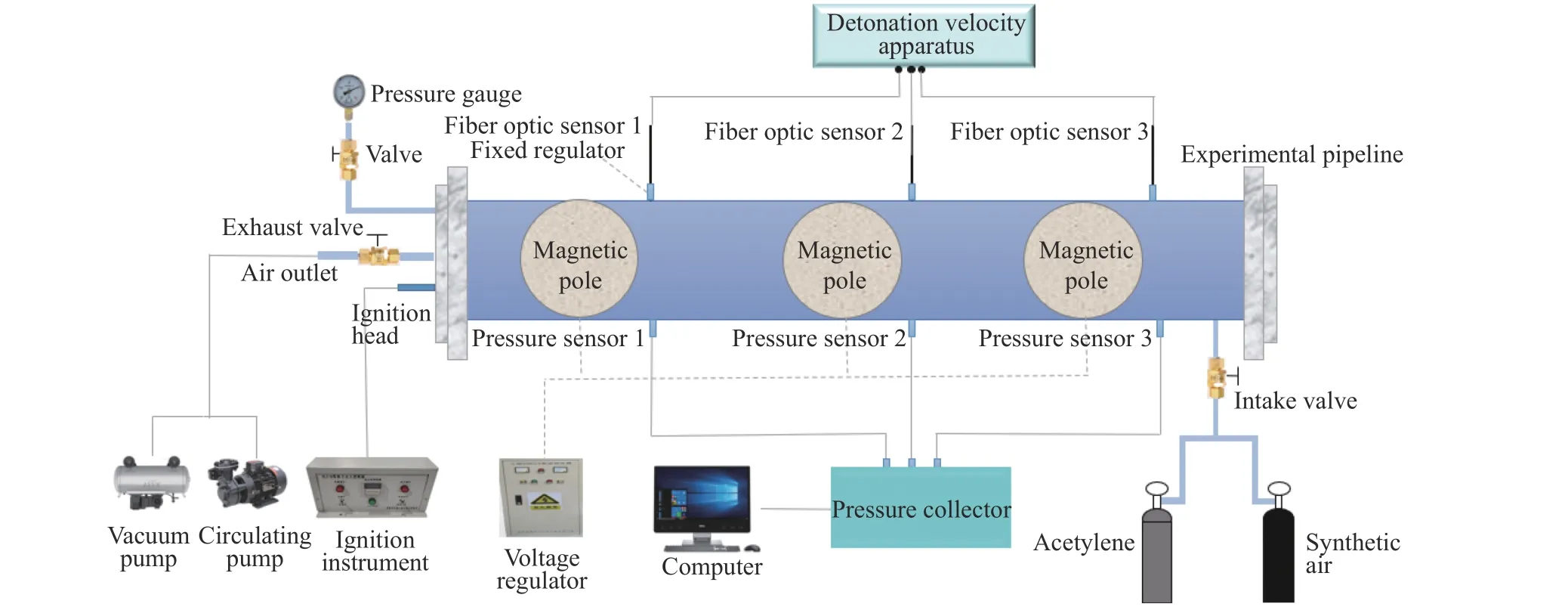
图1 电磁场下预混气体爆炸实验装置示意图Fig. 1 Schematic of gas explosion experiment device under electromagnetic field
该实验管道由自主设计加工,管道长1 000 mm、内径100 mm、厚6 mm,由非金属耐压材料制成,配有爆破片等安全附件。磁场装置由3 对并联磁极和电压调节器组成,可通过调节电压控制磁场强度。磁场为直流电磁场,低电压下形成的较低磁场强度为0.03 T,高电压下形成的较高磁场强度为0.33 T。
爆速测量系统由高精度爆速仪、光纤传感器和固定调节器组成。光纤传感器为感光全反射元件。固定调节器为固定和调节光纤传感器位置的元件。实验管道上有3 个光纤传感器,爆速仪通过2 个光纤传感器接受光信号的时间差得到爆炸火焰传播速度,可以测量两段距离的爆炸火焰传播速度。瞬态压力采集装置由Kistler-211B3 传感器、采集装置和电脑组成。管道上有3 个压力传感器,位置和光纤传感器上下相对。第1 个传感器距离管道左端水平距离为300 mm,相邻传感器距离均为300 mm。气体分配系统包括气瓶、阀门、真空泵和循环泵。点火装置包括点火头和点火仪,点火能量为500 mJ。
具体步骤如下:利用真空泵使管道呈负压状态,压力表显示压力在5 min 内没有变化,表明管道气密性完好;利用负压注入计算当量体积的乙炔,补足空气至常压;利用循环泵循环管道内的气体,再静置使其充分混合均匀;设置爆速仪和压力采集器至待测量状态;打开电压调节器,添加磁场;打开点火器待爆炸结束后,收集爆炸火焰传播速度和压力数据,将尾气进行无害化处理。
2 结果分析
2.1 实验结果与分析
2.1.1 压力分析
为了保证实验的可重复性,每组爆炸实验重复3 次,实验误差不超过1%。不同条件下乙炔/空气爆炸压力曲线如图2 所示,爆炸压力上升速率和最大压力峰值如图3 所示。
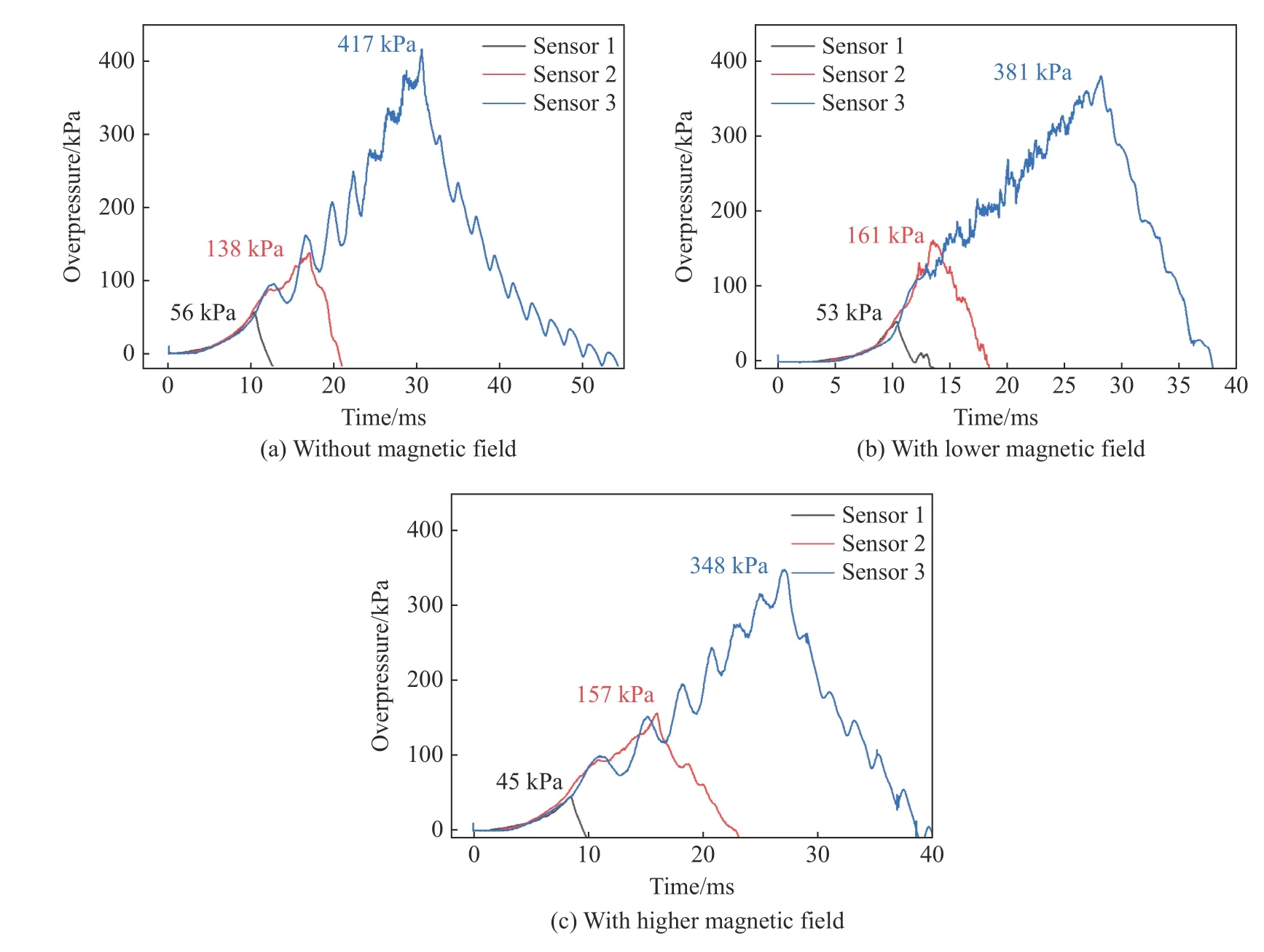
图2 不同磁场强度下乙炔/空气的爆炸压力Fig. 2 Explosion pressures of C2H2/air under different magnetic fields strengths
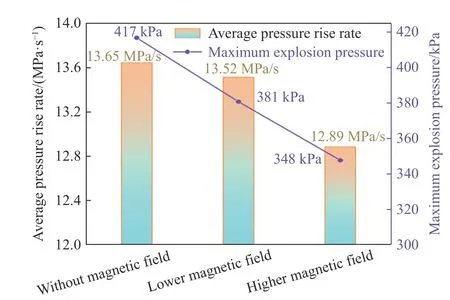
图3 平均压力上升速率和最大压力对比图Fig. 3 Average pressure rise rate and maximum explosion pressure
由图2 可知,最大爆炸压力是评价爆炸强度的重要参数,压力传感器1~2 所测得的压力峰值比压力传感器3 测得的要小得多,因此,选择压力传感器3 的压力数据进行分析。与无磁场相比,磁场强度为0.03 T 时,最大爆炸压力降低了8.63%,磁场强度为0.33 T 时,最大爆炸压力降低了16.55%。由图3 可知,磁场强度能减缓乙炔爆炸压力上升速率,在0.03 T 磁场强度下,爆炸压力上升速率降低了0.13 MPa/s,在磁场强度为0.33 T 时,爆炸压力上升速率降低了0.76 MPa/s。不同磁场强度对乙炔爆炸抑制效果不同,随着磁场强度从0.03 T 增加到0.33 T,对爆炸压力和爆炸压力上升速率的抑制作用也逐渐增大。
2.1.2 爆炸火焰传播速度分析
把光纤传感器1~2 之间的管段定义为第1 段,光纤传感器2~3 之间的管段定义为第2 段。瞬态压力和爆炸火焰传播速度是同时测量的,实验重复3 次,爆速仪测得不同条件下乙炔/空气爆炸火焰传播速度和火焰平均传播速度如表1~3 所示。
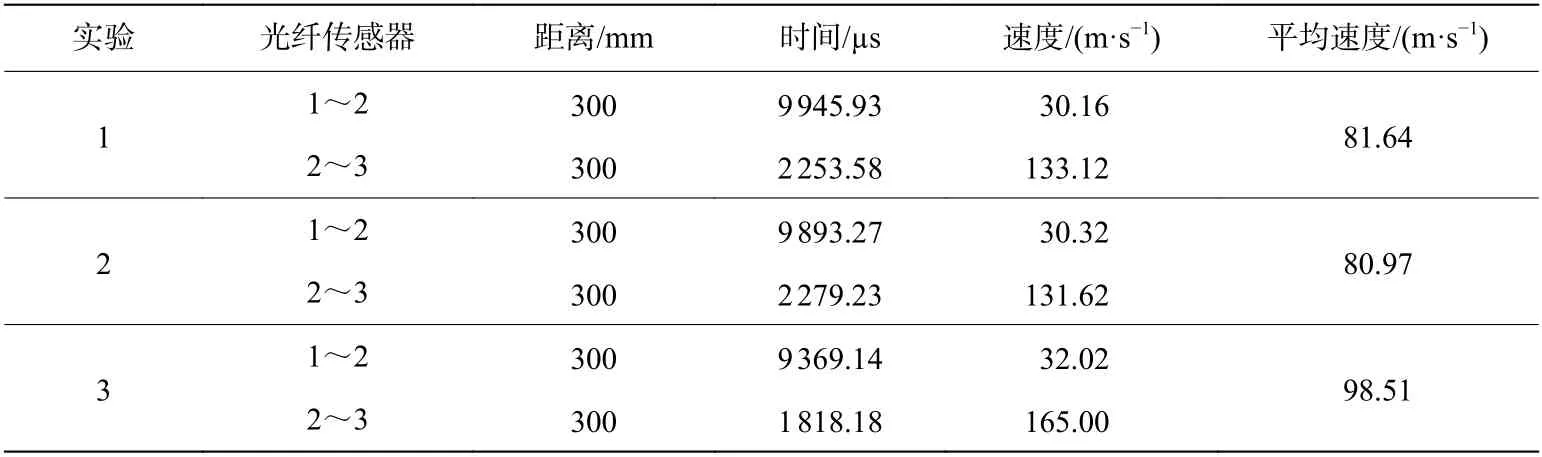
表1 无磁场时乙炔/空气的爆炸火焰传播速度Table 1 Flame propagation velocity of C2H2/air explosion without a magnetic field
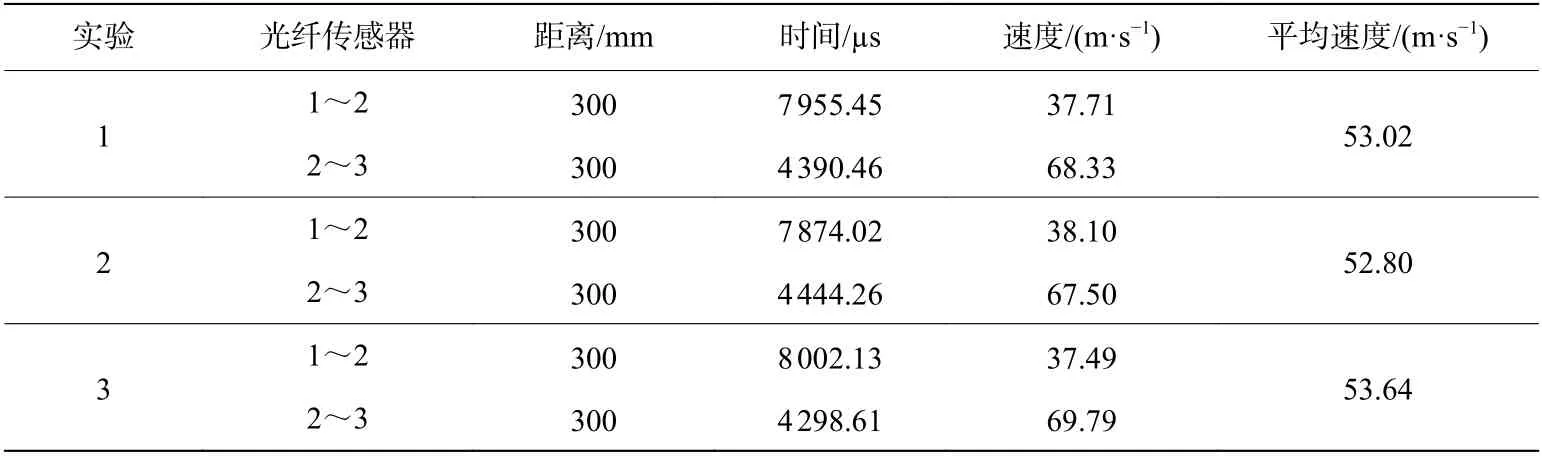
表2 较低磁场强度下乙炔/空气的爆炸火焰传播速度Table 2 Flame propagation velocity of C2H2/air explosion under lower magnetic field strength
取爆速仪测得的3 组实验数据的平均值分析,如图4 所示。
从图4 可知,加入磁场后,第1 段火焰传播速度提高,第2 段火焰传播速度降低,随着磁场强度的增大,第1 段火焰传播速度不断提高,第2 段火焰传播速度不断降低。与无磁场情况相比,在0.03 T 磁场强度下,第1 段火焰传播速度提高了6.94 m/s,第2 段火焰传播速度降低了74.71 m/s。在0.33 T 磁场强度下,第1 段火焰传播速度提高了32.42 m/s,第2 段火焰传播速度降低了119.07 m/s。随着磁场强度的增加,整体火焰平均传播速度逐渐降低。在0.03 T 磁场强度下,火焰平均传播速度降低了38.94%,在0.33 T磁场强度下,火焰平均传播速度降低了49.62%。沿着火焰传播方向,磁场对乙炔/空气爆炸火焰传播速度先促进后抑制,抑制效果远大于促进效果,磁场对爆炸火焰整体呈现抑制作用。
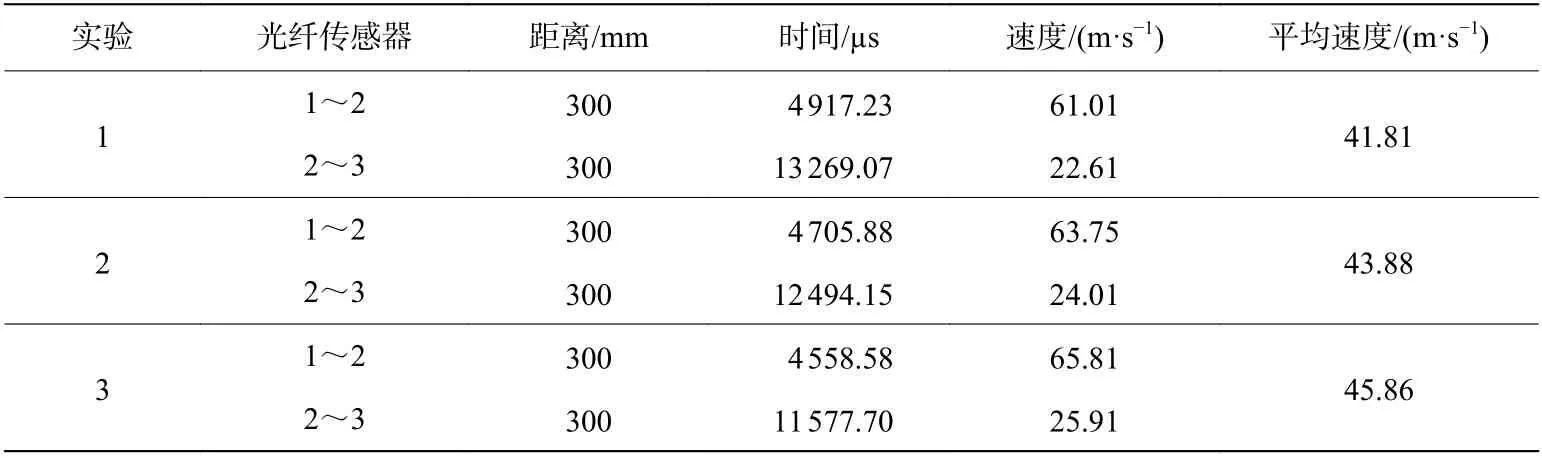
表3 较高磁场强度下乙炔/空气的爆炸火焰传播速度Table 3 Flame propagation velocity of C2H2/air explosion under higher magnetic field strength
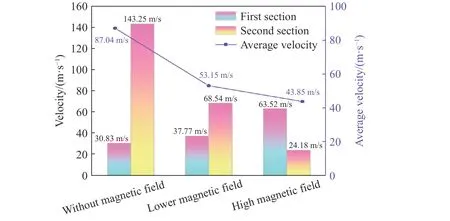
图4 乙炔/空气爆炸火焰传播速度和平均传播速度Fig. 4 Flame propagation velocity and average propagation velocityof C2H2/air explosion
2.2 数值模拟研究与分析
为了开展更深入的研究,通过数值模拟研究乙炔爆炸自由基基元反应过程,解释磁场影响乙炔爆炸更深层的原因。模拟采用Chemkin-Pro 软件中的封闭式0-D 均质间歇反应模型,并设置恒定体积反应器。
模拟参数设置见表4。

表4 起始参数Table 4 Initial parameters


基元反应的正负值表示CH的生成或消耗。基元反应前面的数字代表Chemkin-Pro 中每一个基元反应的代号,反应速率最快的5 个基元反应如图5 所示。
从图5 中可以看出,CH与·O 的主要反应为R155 反应,同时也是消耗乙炔最快的基元反应,生成·HCCO 和·H;CH与·O 的次要反应为R156 反应,生成·CH和CO。O和CH可以快速生成·O、·H、·OH、·HCCO、·HCO、·CH、·CH等自由基。R156 消耗乙炔的速率仅次于R155,CH和·OH 反应生成·CH 和HO。R165 在刚开始反应阶段消耗乙炔生成·CH和·H,随着反应的进行,温度不断升高,逆向反应速率远大于正向反应。R259 是生成乙炔最快的基元反应,·CH和·OH 反应生成·HCO 和CH。R159 反应消耗乙炔生成·CH,R165 消耗·CH,且乙炔都是直接参与反应,两者可以构成一个链式反应,更快地消耗乙炔。乙炔的消耗速率与生成速率之比为98∶2。

图5 C2H2 的生成速率分析Fig. 5 Rate of product analysis of C2H2
2.2.3 敏感性分析
敏感性分析方程为:

通过敏感性分析,选出对CH敏感性影响最大的6 个基元反应,敏感性系数的绝对值越大代表此基元反应对CH敏感性影响越大,敏感性系数为正代表利于CH生成,敏感性系数为负代表利于消耗CH,如图6 所示。

图6 C2H2 的敏感性分析Fig. 6 Sensitivity analysis of C2H2
由图6 可以看出,对CH敏感性影响最大的基元反应有R1、R50、R51、R145、R147 和R155。某些基元反应并不能直接影响CH的敏感性,而是通过链式反应间接影响。R1、R50、R147、R155 都是促进CH的消耗,R51、R145 是促进CH的生成。R1 敏感性系数的绝对值最大,表明基元反应中的·O、·OH 可以快速消耗CH,此基元反应对CH浓度变化的影响最大。R50、R51、R145、R147 都是生成CO 的基元反应,说明CO 对CH的浓度影响很大。
3 讨 论

由式(6)可知,不同的自由基孤对电子数不同,磁矩也不同。存在外加磁场时,磁矩方向沿磁场方向排列,受到磁场的作用力。由式(7)可知,自由基孤对电子数和摩尔质量不同,磁化率和磁化强度也不同,摩尔质量越大,磁化率越小。由式(8)可知,磁化强度与磁化率和磁场强度呈正相关。磁场强度越大,磁化强度也越大。在相同磁场强度下,梯度磁场力和洛伦兹力对这些·H、·O、·OH、·CH小分子量自由基比对·HCCO、·HCO、·CH 大分子量自由基作用更显著。磁场改变了这些自由基的运动轨迹,这些自由基参与的基元反应速率也会改变。磁场使·OH 发生聚集,运动轨迹和速度发生改变,这一现象被实验测量和理论计算所证实。磁场可能使其他同种小分子量自由基聚集,自由基碰撞面积减少,减少了不同种关键自由基之间的碰撞,参与的基元反应速率降低。小分子量的自由基也可能更容易被吸引到管壁,产生器壁效应。CH爆炸生成很多产物,CO和HO 是最主要的产物,根据敏感性分析,CH对CO 生成影响很大,根据反应机理分析,CO主要是由CO+·OH→·H+ CO、CO+·O→CO生成。因此,分析CO 产物更具有代表性。磁场下CH生成CO 和HO 反应路径变化如图7~8 所示,线段的粗细代表基元反应速率快慢,线段越粗,基元反应速率越快。
从图7~8 可以看出,·H、·O、·OH、·CH、·CH等这些小分子量自由基受到磁场力作用,所参与的基元反应速率降低。·CH→·CH、·CH→·CH、·HCCO→·CH 这些不需要·H、·O、·OH 参与的自分解反应不受磁场影响,·CH→CO、·CH→HCO、HCO→CO 和 HO、·CH→CO 和HO、·CH→CO 和 HO、·HCCO→CO 和HO 的基元反应中有·H、·O、·OH 参与,基元反应速率降低。·CH 的数量没有·H、·O、·OH 等自由基的数量多,一部分·CH 在磁场中发生聚集,一部分·CH 产生器壁效应,·CH 参与的基元反应速率降低,且·CH 数量减少,甚至不能继续参与链式反应。对于整个爆炸反应,磁场使整体的链反应速率降低,导致压力和爆炸火焰传播速度降低。
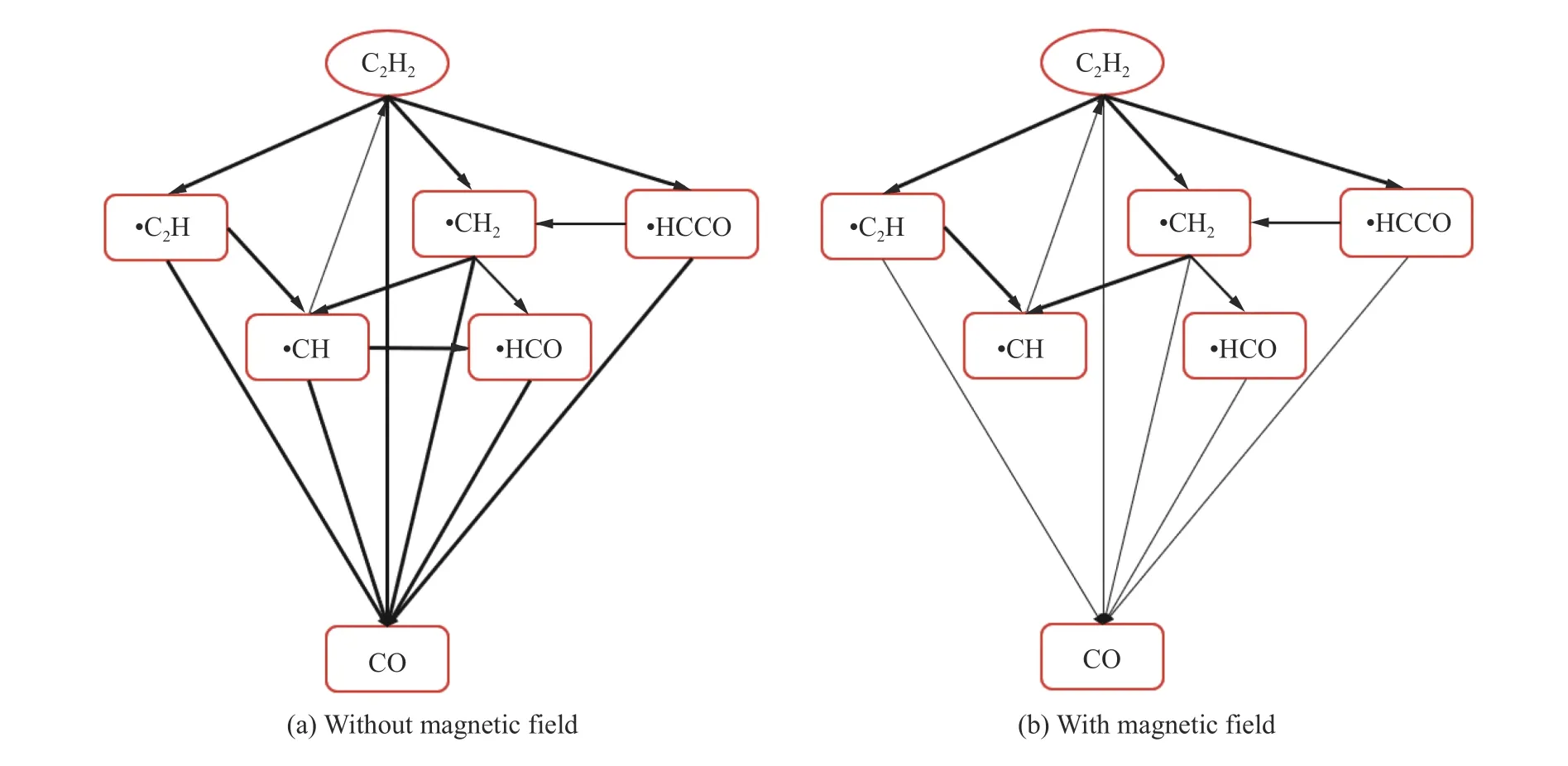
图7 有无磁场时C2H2 生成CO 的反应路径变化Fig. 7 Changes in reaction pathto produce CO from C2H2 due to magnetic field
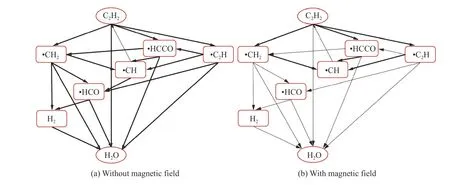
图8 有无磁场时C2H2 生成H2O 的反应路径变化Fig. 8 Changes inreaction path to produce H2O from C2H2 due to magnetic field
4 结 论
(1)外加磁场对气体爆炸自由基反应具有明显的影响,磁场能降低乙炔气体爆炸压力和爆炸压力上升速率,对乙炔气体爆炸呈现抑制作用。在较低磁场强度下,最大爆炸压力降低了8.63%,爆炸压力上升速率减小了0.13 MPa/s;在较高磁场强度下,最大爆炸压力降低了16.55%,爆炸压力上升速率减小了0.76 MPa/s,实验证明,磁场强度越大,抑制效果越明显。
(2)沿火焰传播方向,磁场对气体爆炸火焰传播速度是先促进后抑制的效果,抑制效果大于促进效果。在较低磁场强度下,火焰平均传播速度降低了38.94%;在较高磁场强度下,火焰平均传播速度降低了49.62%。
(3)磁场会改变乙炔爆炸反应的路径。不同自由基受到的磁场作用力因磁化强度不同而不同,磁化强度与分子量成反比,分子量越大,受到的磁场作用力越小;不同分子量的自由基在磁场作用力的影响下,运动轨迹会发生变化,同种自由基相互聚集,不同种类自由基相互脱离,自由基碰撞几率减小,关键自由基参与的基元反应速率降低,最终影响气体爆炸特征。这种效应还需要进一步实验验证。
