深圳医疗器械唯一标识追溯平台助力精准监管 保障患者安全
2022-08-17深圳市标准技术研究院孙勇陈利平郭静文
深圳市标准技术研究院 孙勇 陈利平 郭静文
为进一步推动医疗器械唯一标识(UDI)的实施应用,将UDI扩展到所有第三类医疗器械产品(含体外诊断试剂),并鼓励其他品种医疗器械实施UDI,深圳市先行先试,以标准先行、行业宣贯、企业培训、平台应用全方位建设医疗器械追溯体系,搭建出广东省首个医疗器械唯一标识追溯平台。
创新工作模式
形成“一个平台支撑,两个端口发力,三个部门联动”的工作模式。“一个平台支撑”即搭建“深圳市医疗器械唯一标识(UDI)追溯平台”,提供技术支撑,实现精准监管、智慧监管;“两个端口发力”即抓住生产和使用两个端口,选取信息化建设完善的医疗器械生产企业和医院作为试点,打造生产端到使用端的数据闭环;“三个部门联动”即深圳市市场监管局、深圳市卫健委和深圳市医保局联合,共同推进深圳市医疗器械唯一标识工作向纵深开展。
对标国际国内标准
依托深圳市标准技术研究院物品编码管理中心力量,采用在全球广泛实施的基于GS1 标准的UDI 编码体系,通过系统宣贯、上门服务、在线培训等多种方式提供技术咨询和支持服务,满足国内外医疗器械合规要求,有效应对欧美技术性贸易壁垒,降低产品出口风险。同步完成三项深圳市地方标准的制定发布,进一步指导企业落地实施医疗器械编码标识。
全生命周期精准追溯
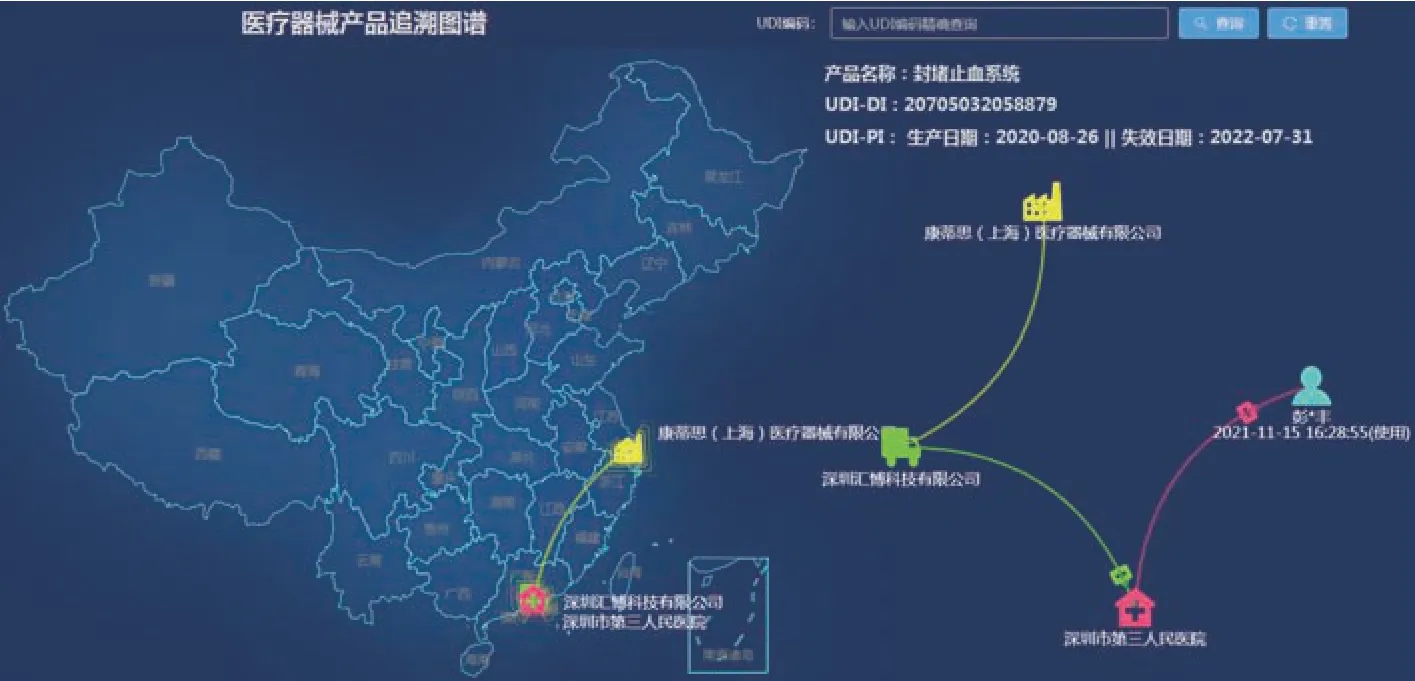
初步建立起医疗器械全生命周期监管体系框架,通过UDI 编码串联各环节信息,从生产厂家到产品供应商,直至患者,直观地展示了生产、经营、流通和使用环节中的医疗器械产品的追溯链条,动态展现医疗器械全生命周期流向,助力精准监管、保障患者安全。
扩大应用试点
持续完善该追溯平台,有序扩大UDI 实施企业范围,增加医疗机构试点,丰富数据对接方式,把平台打造成推动UDI 工作的实际“抓手”,全面实现深圳市医疗器械全生命周期精准追溯,促深圳医疗器械产业高质量发展。