川芎嗪-哒嗪酮耦联化合物的合成及其抗血小板聚集活性*
2022-08-16贾学敏罗忠福李毅汤磊杨元勇
贾学敏,罗忠福,李毅,汤磊,2,杨元勇*
(1.贵州医科大学 药学院,贵州 贵阳 550025;2.贵州省化学合成药物研发利用工程技术研究中心,贵州 贵阳 550004)
血栓可引起动脉粥样硬化、冠心病以及缺血性脑卒中等心脑血管疾病,严重危害着人类健康[1-2]。血小板是血液中的重要组成成分,不仅在生理性止血中发挥重要作用,而且在动脉粥样硬化斑块破裂、血管内皮细胞损伤或外源性物质(如心脏内支架或手术过程中的异物)刺激时,都会由静息转为活化,再通过粘附、聚集形成血栓[3]。因此,通过抗血小板聚集能够有效预防和治疗血栓。川芎嗪的化学名称为2,3,5,6-四甲基吡嗪(2,3,5,6-tetramethylpyrazine,TMP),是从传统中草药川芎中提取分离得到的有效活性单体,具有抗血小板聚集、抗阿尔茨海默病及抗缺血再灌注损伤等作用[4-6],已被开发应用于临床,如TMP注射液、丹参TMP注射液等[7-8]。有研究表明,由于TMP具有药代动力学不佳、半衰期短、代谢较快及药理活性不强等缺点,研究者对其进行了结构改造,以期发现活性更好的TMP衍生物[9-16]。研究表明,6-苯基-4,5-二氢哒嗪-3(2H)-酮类化合物在体外具有强效的抗血小板作用,如CI-914、CI-930等,通过对6-苯-4,5-二氢哒嗪-3(2H)-酮化合物构效关系分析不难发现,该类小分子的药效基团为6-苯基-4,5-二氢哒嗪-3(2H)-酮,同时苯环上对位取代活性最好,但是这些化合物在体内的活性较弱,选择性较差,限制了其应用[17-18]。因此,丰富该类化合物的结构类型,寻找活性更佳、选择性更好及副作用更低的抗血小板聚集化合物具有重要意义。本研究根据药物化学中经典的药效团拼合原理以及生物电子等排原理,将TMP与6-苯基-4,5-二氢哒嗪-3(2H)-酮进行耦联,设计、合成3个TMP-哒嗪酮衍生物,并进行体外抗血小板聚集活性研究,以期获得活性更佳、副作用更低的抗血小板聚集候选化合物。
1 材料与方法
1.1 实验材料
1.1.1动物来源 雄性新西兰兔6只,体质量1.5~2.5 kg,年龄90~120 d,购自贵州医科大学动物中心[合格证号SYXK(黔)2018-0001],动物于室温(23±3)℃、相对湿度60%~80%条件下饲养1周后实验。
1.1.2主要药物、试剂及仪器 TMP和阿司匹林(aacetylsalicylic acid,ASA;上海皓鸿),二磷酸腺苷(adenosine diphosphate,ADP;南京建成),花生四烯酸(arachidonic acid,AA;北京索莱宝),柱层析硅胶(青岛海洋),三甲基吡嗪、α-酮戊二酸、乙酰苯胺、丁二酸酐及3-(4-甲氧基苯甲酰基)丙酸(上海皓鸿);98-Ⅱ-B磁力搅拌电热套和冷冻机(长城科工),EYELA N-2100旋转蒸发仪和SHE-Ⅲ循环真空水泵(上海亚荣),Avance NEO-600或400型核磁共振光谱仪(瑞士Bruker),UPLC-QTOF型高分辨质谱分析仪(美国Waters),半自动凝血分析仪(北京中勤世帝)。
1.2 合成方法
1.2.12-(溴甲基)-3,5,6-三甲基吡嗪的合成 取TMP 5 g溶于20 mL四氯化碳,加入N-溴代琥珀酰亚胺(N-Bromosuccinimide,NBS)6.54 g,催化量的过氧化二苯甲酰(benzoyl peroxide,BPO),回流反应12 h、抽滤、滤液减压蒸除溶剂,硅胶层析柱分离纯化(V石油醚∶V二氯甲烷=2∶1),得黄色油状物4.17 g,产率为53%,放置备用[19]。
1.2.24-(4-乙酰氨基苯基)-4-氧代丁酸(中间体2)的合成 取无水三氯化铝27.37 g置于100 mL反应瓶,室温滴加N,N-二甲基乙酰胺(N,N-Dimethylacetamide,DMF)4.4 mL、待反应,降至室温时移入70 ℃油浴,滴加碾碎的乙酰苯胺2.70 g和丁二酸酐2.03 g的混合物,反应2 h,加冰水180 mL,抽滤不溶性杂质,收集滤液加浓盐酸12 mL,4 ℃放置过夜,抽滤,收集滤饼,无水乙醇重结晶,获得浅黄色固体(中间体2)1.70 g,产率为36%。
1.2.34-(4-氨基苯基)-4-氧代丁酸(中间体3)的合成 取中间体2500 mg,加6 mol/L盐酸溶液5 mL,110 ℃反应2 h,置于冰浴,无水碳酸钠pH调节至4,米白色固体析出,抽滤收集滤饼,用蒸馏水反复冲洗滤饼,干燥,得米白色固体(中间体3)381 mg,产率为93%。
1.2.44-(4-氨基苯基)-4-氧代丁酸甲酯(中间体4)的合成 取中间体375 mg置于10 mL反应瓶,加甲醇2 mL、浓硫酸1滴,回流反应6 h,加饱和碳酸氢钠至无气泡产生后,使用乙酸乙酯萃取3次,无水Na2SO4干燥,减压蒸除溶剂,用乙酸乙酯和石油醚进行重结晶,得浅黄色固体(中间体4)69 mg,产率为85%。
1.2.54-氧代-4-{4-[(3,5,6-三甲基吡嗪-2-基甲基)氨基]苯基}丁酸甲酯(中间体5)的合成 取中间体4208 mg、1.2.1项下黄色油状物200 mg、K2CO3276 mg置于25 mL反应瓶中,加丙酮10 mL,氮气环境下回流反应8 h,放冷,抽滤除去过量K2CO3,减压蒸除溶剂,经硅胶柱分离纯化(V石油醚∶V乙酸乙酯=2∶1),得黄色固体(中间体5)209 mg,产率为61%。
1.2.66-{4-[(3,5,6-三甲基吡嗪-2-基甲基)氨基]苯基}-4,5-二氢哒嗪-3(2H)-酮的合成 取中间体5188 mg,溶于乙醇5 mL,加85%水合肼41 mg,回流反应5 h,放冷,抽滤,滤饼充分干燥,乙醇重结晶,得白色固体(目标化合物a)166 mg,产率为93%。
1.2.74-(4-羟基苯基)-4-氧代丁酸(中间体7)的合成 取3-(4-甲氧基苯甲酰基)丙酸2 g置于50 mL反应瓶,加冰醋酸18 mL、40%氢溴酸溶液8 mL,130 ℃反应24 h,加适量水,乙酸乙酯萃取,无水Na2SO4干燥,减压蒸除溶剂,乙酸乙酯和石油醚重结晶,得灰色固体(中间体7)1.40 g,产率为75%。
1.2.84-(4-羟基基苯基)-4-氧代丁酸甲酯(中间体8)的合成 取中间体71.00 g,溶于甲醇20 mL,滴浓硫酸3滴,回流反应5 h,加饱和碳酸氢钠至无气泡产生,乙酸乙酯萃取,无水Na2SO4干燥,减压除去溶剂乙酸乙酯和石油醚重结晶,得到白色固体(中间体8)0.92 g,产率为88%。
1.2.94-氧代-4-[4-(3,5,6-三甲基吡嗪-2-甲氧基)苯基]丁酸甲酯(中间体9)的合成 取中间体8486 mg、2-溴甲基-3,5,6-三甲基吡嗪(1.2.1项下黄色油状物)500 mg及K2CO3645 mg置于50 mL反应瓶,加丙酮25 mL,氮气环境下回流反应5 h,放冷,抽滤除去不溶物,减压蒸溶剂,经硅胶柱纯化(V石油醚∶V乙酸乙酯=2∶1),得白色固体(中间体9)480 mg,产率为59.9%。
1.2.106-[4-(3,5,6-三甲基吡嗪-2-甲氧基)苯基]-4,5-二氢哒嗪-3(2H)-酮的合成 取中间体9191 mg,溶于乙醇10 mL,加85%水合肼48 mg,回流反应5 h,反应完成后,放冷,抽滤,滤饼充分干燥,使用乙醇进行重结晶,得白色固体(目标化合物b)178 mg,产率为94.7%。
1.2.114-氧代-4-(3,5,6-三甲基吡嗪-2-基)丁酸(中间体12)的合成 取三甲基吡嗪1 g,溶于乙腈50 mL,加过硫酸铵9 g和AgNO30.2 g,氮气下加乙腈12 mL、水60 mL及α-酮戊二酸 3.6 g,65 ℃搅拌5 h,放冷,加水50 mL,乙酸乙酯萃取,无水Na2SO4干燥,减压蒸除溶剂,层析柱纯化后(V二氯甲烷∶V甲醇=20∶1),得淡黄色固体(中间体12)1.6 g,产率为87.9%。
1.2.126-(3,5,6-三甲基吡嗪-2-基)-4,5-二氢哒嗪-3(2H)-酮的合成 取中间体12200 mg,溶于乙醇10 mL,加85%水合肼64 mg,回流反应4 h,放冷,抽滤收集滤饼,滤饼充分干燥,乙醇打浆,得白色固体(目标化合物c)180 mg,产率为91.7%。
1.2.13体外抗血小板聚集活性检测 体外的抗血小板聚集活性评价采用born比浊法进行测试[20]。家兔心脏取血,3.8%枸橼酸钠抗凝(V血液∶V抗凝剂=9∶1),1 200 r/min离心15 min,取上清得富血小板血浆(platelet-rich plasma,PRP);剩余血浆3 000 r/min离心10 min,取上清得贫血小板血浆(platelet-poor plasma,PPP)。采用半自动凝血分析仪进行测试,取PRP 189 μL于测试杯,分别加目标化合物或阳性药ASA 1 μL于37 ℃下孵育3 min,使用10 μmol/L ADP 10 μL或0.5 mmol/L AA 10 μL为诱导剂诱导PRP中血小板聚集,记录5 min以内的最大聚集率,重复7次取均值,根据公式计算出目标化合物的抗血小板聚集率(aggregation inhibition rate,AIR)[20],并计算半数抑制浓度(50% inhibitory concentration,IC50)。
2 结果
2.1 化合物结构表征
2.1.1中间体2系4-(4-乙酰氨基苯基)-4-氧代丁酸,熔点为202~204 ℃;1H NMR(600 MHz,DMSO-d6)δ: 12.11(s,1H),10.27(s,1H),7.94(d,J=8.8 Hz,2H),7.72(d,J=8.7 Hz,2H),3.21~3.16(m,2H),2.58~2.54(m,2H),2.09(s,3H);HRMS(ESI)C12H14N3O4[M-H]-的理论值和实际值分别为234.076 6和234.076 4。
2.1.2中间体3系4-(4-氨基苯基)-4-氧代丁酸,熔点为180~182 ℃;1H NMR(600 MHz,DMSO-d6)δ: 12.03(s,1H),7.69(d,J=8.7 Hz,2H),6.57(d,J=8.7 Hz,2H),6.03(s,2H),3.06(t,J=6.4 Hz,2H),2.51(t,J=4.3 Hz,2H);HRMS(ESI)C10H10NO3[M-H]-的理论值和实际值分别为192.066 1和192.066 0。
2.1.3中间体4系4-(4-氨基苯基)-4-氧代丁酸甲酯,熔点为163~165 ℃;1H NMR(400 MHz,DMSO-d6)δ: 7.69(d,J=8.7 Hz,2H),6.56(d,J=8.7 Hz,2H),6.08(s,2H),3.58(s,3H),3.18~2.99(m,2H),2.64~2.53(m,2H);HRMS(ESI)C11H14NO3[M+H]+的理论值和实际分别为208.097 4和208.096 7。
2.1.4中间体5系4-氧代-4-{4-[(3,5,6-三甲基吡嗪-2-基甲基)氨基]苯基}丁酸甲酯,熔点为93~95 ℃;1H NMR(600 MHz,DMSO-d6)δ: 7.73(d,J=8.7 Hz,2H),7.00(t,J=5.2 Hz,1H),6.73(d,J=8.8 Hz,2H),4.40(d,J=5.2 Hz,2H),3.57(s,3H),3.12(t,J=6.3 Hz,2H),2.58(t,J=6.3 Hz,2H),2.47(s,3H),2.44(s,3H),2.42(s,3H);HRMS(ESI)C19H24N3O3[M+H]+的理论值和实际值分别为342.181 8和342.181 9。
2.1.5目标化合物a系6-{4-[(3,5,6-三甲基吡嗪-2-基甲基)氨基]苯基}-4,5-二氢哒嗪-3(2H)-酮;熔点为199~200 ℃;1H NMR(600 MHz,DMSO-d6)δ: 10.65(s,1H),7.51(d,J=8.8 Hz,2H),6.72(d,J=8.8 Hz,2H),6.46(s,1H),4.35(s,2H),2.83(t,J=8.2 Hz,2H),2.48(s,3H),2.45(s,3H),2.42(s,3H),2.39~2.34(m,2H);13C NMR(150 MHz,DMSO-d6)δ: 167.43,150.33,150.00,149.68,148.67,148.06,147.84,127.27,123.95,112.31,46.37,26.70,22.09,21.50,20.65;HRMS(ESI)C18H22N5O[M+H]+的理论值和实际值分别为324.183 1和324.182 4。
2.1.6中间体7系4-(4-羟基苯基)-4-氧代丁酸,熔点为157~159 ℃;1H NMR(600 MHz,DMSO-d6)δ: 12.00(s,1H),10.37(s,1H),7.85(d,J=8.8 Hz,2H),6.85(d,J=8.7 Hz,2H),3.17~3.12(m,2H),2.56~2.51(m,2H);HRMS(ESI)C10H9O4[M-H]-的理论值和实际值分别为193.050 1和193.050 5。
2.1.7中间体8系4-(4-羟基苯基)-4-氧代丁酸甲酯,熔点为169~170 ℃;1H NMR(600 MHz,DMSO-d6)δ: 10.36(s,1H),7.85(d,J=8.8 Hz,2H),6.85(d,J=8.7 Hz,2H),3.58(s,3H),3.25~3.13(m,2H),2.67~2.56(m,2H);HRMS(ESI)C11H13O4[M+H]+的理论值和实际值分别为209.081 4和209.081 3。
2.1.8中间体9系4-氧代-4-[4-(3,5,6-三甲基吡嗪-2-甲氧基)苯基]丁酸甲酯,熔点为104~106 ℃;1H NMR(600 MHz,DMSO-d6)δ: 7.96(d,J=8.9 Hz,2H),7.14(d,J=8.9 Hz,2H),5.26(s,2H),3.59(s,3H),3.27~3.22(m,2H),2.65~2.61(m,2H),2.49(s,3H),2.45(s,3H),2.44(s,3H);HRMS(ESI)C19H23N2O4[M+H]+的理论值和实际值分别为343.165 8和343.165 9。
2.1.9目标化合物b系6-[4-(3,5,6-三甲基吡嗪-2-甲氧基)苯基]-4,5-二氢哒嗪-3(2H)-酮,熔点为209~211 ℃;1H NMR(600 MHz,DMSO-d6)δ: 10.82(s,1H),7.69(d,J=8.8 Hz,2H),7.07(d,J=8.9 Hz,2H),5.19(s,2H),2.90(t,J=8.2 Hz,2H),2.48(s,3H),2.45(s,3H),2.44(s,3H),2.41(t,J=8.2 Hz,2H);13C NMR(150 MHz,DMSO-d6)δ: 167.39,159.70,151.50,149.77,149.58,148.76,145.67,129.34,127.64,115.15,69.84,26.51,22.29,21.72,21.43,20.62;HRMS(ESI)C18H21N2O4[M+H]+的理论值和实际值分别为325.166 5和325.166 6。
2.1.10中间体12系4-氧代-4-(3,5,6-三甲基吡嗪-2-基)丁酸,熔点为159~161 ℃;1H NMR(600 MHz,DMSO-d6)δ: 12.14(s,1H),3.33(t,J=6.5 Hz,2H),2.60(s,3H),2.57(t,J=6.5 Hz,2H),2.52(s,6H);HRMS(ESI)C11H13N2O3[M-H]-的理论值和实际值分别为221.092 6和221.093 1。
2.1.11目标化合物c系6-(3,5,6-三甲基吡嗪-2-基)-4,5-二氢哒嗪-3(2H)-酮,熔点为240~243 ℃;1H NMR(400 MHz,CD3OD)δ: 3.15~3.09(m,2H),2.66(s,3H),2.58~2.52(m,2H),2.50(s,6H);13C NMR(100 MHz,CD3OD)δ: 168.92,150.46,148.74,148.55,144.59,140.86,25.88,22.40,22.25,20.09,19.98;HRMS(ESI)C11H15N4O2[M+H]+的理论值和实际值分别为219.124 6和219.124 7。
2.2 抗血小板聚集活性
目标化合物a、b及c对ADP和AA所诱导的血小板聚集均有较好的抑制作用,其中化合物c的活性最佳,在ADP和AA诱导下的抗血小板聚集IC50分别为132.2 μmol/L和118.8 μmol/L,在2种诱导剂作用下,目标化合物的抗血小板聚集活性顺序一致:c>a>b,优于先导化合物TMP和临床常用药物ASA。见表1。
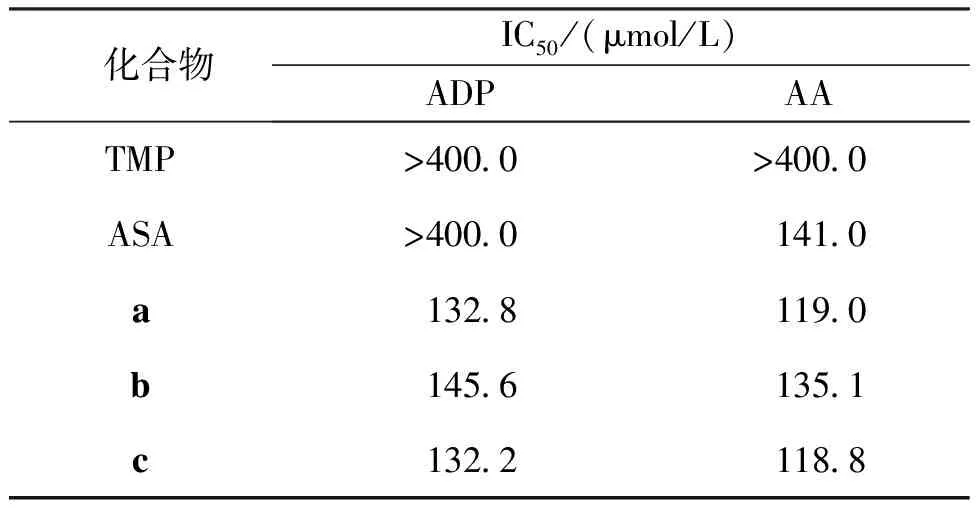
表1 化合物a、b及c的体外抗血小板聚集活性
3 讨论
由于血小板不仅在血栓形成中扮演重要角色,在生理性止血中同样具有重要作用,因此血小板作为血栓交联的中心,常常成为抗血栓药物的“明星靶点”。但遗憾的是目前临床所应用的抗血小板聚集药物或多或少的存在出血时间延长的副作用[21]。因此,如何平衡出血和凝血之间的平衡或寻找出血副作用小的抗血小板聚集药物一直都是研究的热点,迫切需要发现新型的抗血小板聚集的化合物。
药物化学中的药效团拼合原理和生物电子等排原理是药物开发的经典策略之一,常常可得到药效协同或药效增加的目标化合物[22-25]。TMP作为传统中药提取出的有效单体,以各种形式的制剂或复方应用于临床,TMP具有一定的抗血小板聚集活性,但其活性较弱[19];TMP的分子结构简单,可修饰空间较小,所以其结构修饰多与其他活性小分子化合物进行耦联[12-14]。小分子6-苯基-4,5-二氢哒嗪-3(2H)-酮已经被证明具有较好的抗血小板聚集作用,但副作用较多[17],同样有待进一步研究。因此,本研究通过3条合成路线,以TMP为原料,经溴代得到关键中间体2-(溴甲基)-3,5,6-三甲基吡嗪;然后以乙酰苯胺为原料,分别经傅-克反应、脱乙酰基、与水合肼环合,最后与2-(溴甲基)-3,5,6-三甲基吡嗪发生取代反应得到目标化合物a;以3-(4-甲氧基苯甲酰基)丙酸为原料,分别经脱甲基、与水合肼环合,再与2-(溴甲基)-3,5,6-三甲基吡嗪发生取代反应得目标化合物b;以三甲基吡嗪和α-酮戊二酸为原料,分别经Minisci反应和水合肼环合得到目标化合物c。这3条路线合成路线中的原料廉价易得,合成过程中操作简单方便,以高产率得到目标化合物a~c,目标产物结构经HRMS、1H NMR、13C NMR表征,且经Scifinder检索均为新化合物。
ADP和AA是血小板聚集的常用诱导剂,涉及到不同的机制通路,ASA通过抑制环氧化酶-1(cyclooxygenase-1,COX-1)使AA代谢为前列腺素G2受阻,使血栓烷A2(thromboxane,TXA2)的生成减少从而发挥抑制血小板聚集的作用[26]。而血小板二磷酸腺苷受体亚基12(platelet adenosine diphosphate receptor subunit 12,P2Y12)是ADP的受体,ADP与P2Y12受体结合后,可使血小板激活,从而形成血栓[27]。因此,作用于这两种通路的任一通路都可以影响血小板的聚集。Born比浊法广泛用于抗血小板聚集活性研究,其原理是在正常情况下、低转速下收集的富血小板血浆为米黄色的浑浊液体,加入诱导剂后,血浆中的血小板被激活,血小板发生聚集,血浆的透光度增加,通过透光度的变化反应血小板的聚集情况,该法具有操作简便、重复性好等优点[28-30]。因此,本研究以ADP和AA为诱导剂,采用Born比浊法进行目标化合物的抗血小板聚集活性测试,结果显示,与ASA不同,化合物a~c不仅能够发挥抗AA诱导的血小板聚集作用,对ADP诱导的血小板聚集同样具有较好的抑制效果,提示该类化合物可以通过多重作用机制发挥抗血小板聚集活性。
综上所述,在保留TMP活性母核的条件下,通过O、N桥与6-苯基-4,5-二氢哒嗪-3(2H)-酮进行耦联,得到化合物a和b;另外,根据生物电子等排原理将6-苯基-4,5-二氢哒嗪-3(2H)-酮的苯基替换为TMP环,合成了化合物c,并对目标化合物进行体外的抗家兔的血小板聚集活性测试。如预期的那样,目标化合物在AA和ADP诱导下的抗血小板聚集活性优于先导化合物TMP和ASA,具有进一步研究的价值。此研究为后续抗血小板聚集化合物的研究提供了实验依据和理论参考。
