2021欧洲心脏病学会《共识文件:心力衰竭调整药物治疗的患者特征》解读*
2022-08-15韩丽珠尹琪楠边原黄雪飞雷洋唐凌茜童荣生
韩丽珠,尹琪楠,边原,黄雪飞,雷洋,唐凌茜,童荣生
(四川省医学科学院·四川省人民医院/电子科技大学附属医院药学部·个体化药物治疗四川省重点实验室,成都 610072)
心力衰竭(heart failure,HF)和射血分数降低心力衰竭(heart failure with reduced ejection fraction,HFrEF)患者的药物治疗有大规模临床随机对照试验(randomized clinical trials,RCT)支持,并且欧洲心脏病学会/心力衰竭协会(European Society of Cardiology/Heart Failure Association,ESC/HFA)指南作出了明确推荐,但治疗效果仍然欠佳。多数患者没有接受所有改善预后的药物治疗或仅接受低于目标剂量的治疗,这可能因为用药期间出现低血压、心率减慢、肾功能受损或高钾血症等耐受性问题。另外,人为因素方面,由于专科护理的关注度有限,患者的社会经济状况不佳,缺乏社会医疗保障的支持和药物依从性差等同样可导致HF患者药物治疗不足。
近年来,HF治疗药物增加了许多新品种,同时也增加了药物治疗管理的复杂性。既往药物治疗HFrEF患者需要血管紧张肽转换酶抑制剂(angiotensin-converting enzyme inhibitor,ACEI)/血管紧张肽受体阻断剂(angiotensin receptor blocker,ARB)、β-受体阻断剂(beta-blockers,BB)、醛固酮受体拮抗剂(mineralocorticoid receptor antagonists,MRA)、地高辛、利尿剂等。近十年来增加了伊伐布雷定、沙库巴曲/缬沙坦、钠-葡萄糖共转运体2抑制剂(sodium-glucose co-transporter 2 inhibitor,SGLT2i)、羧基麦芽糖铁以及维利西呱(vericiguat)和omecamtiv mecarbil(一种新型选择性心脏肌球蛋白激活剂)等药物,这些药物均可降低HFrEF患者死亡率和(或)发病率。
在HFrEF患者中,指南指导的药物治疗(guideline-directed medical therapy,GDMT)的实施和剂量调整较为复杂,因为许多药物对血压、肾功能和血钾水平有影响。患者可能不能耐受所有目标剂量的药物治疗,治疗方案的制定者需要决定哪种药物对个体患者最有益。2021欧洲心脏病学会《共识文件:心力衰竭调整药物治疗的患者特征》(简称《共识》),分析患者治疗不足的药物因素和人为因素,结合RCT的纳入和排除标准、亚组分析和荟萃分析,最终确定与HFrEF患者治疗实施相关的患者特征,便于制定个性化治疗方案,有利于更好开展GDMT[1]。
1 药物治疗实施的障碍
HF失代偿入院的患者,出院是一个特殊挑战,所以出院后的药物治疗计划在从医院到门诊随访的过渡中起着重要作用。计划中应该体现GDMT调整和监测时间表、评估器械治疗的适应证和时机、锻炼方式或康复计划以及生活方式的调整,计划还应包括出院后第一周的就诊安排及专科随访。对于改善HF预后药物,有证据表明,血管紧张素受体-脑啡肽酶抑制剂(angiotensin receptor-neprilysin inhibitor,ARNI)和SGLT2i在住院期间即可启动,其有助于降低再住院率和死亡率。
过渡阶段,即HF失代偿住院后的前2个月,GDMT的实施和调整尚不达标。主要由于对指南建议认识不足,以及未能将指南和RCT证据与临床实践相结合。在HART试验中[2],医生不遵从指南的情况主要涉及老年患者及并发症多的患者,HF患者存在共病需要药物治疗时,潜在的不适当用药风险显著增加(使用GDMT对共病的影响见表1)。尽管如此,仍有明确的证据表明,坚持用药与慢性HF门诊患者心血管死亡率降低和HF住院率减少相关。

表1 HF常见并发症及对GDMT的影响
2 慢性肾病(chronic kidney disease,CKD)患者药物治疗的优化
CKD指eGFR<60 mL·min-1·(1.73 m2)-1的肾功能不全,在HF患者中高达50%[3]。合并CKD的HF患者具有双倍全因死亡风险,且肾功能是比左室射血分数(left ventricular ejection fraction,LVEF)更强的预后预测因子。eGFR在HF的病程中动态变化,可能导致不适当的减量甚至停用缓解充血的药物及调节神经内分泌的药物。例如急性HF持续利尿并改善HF症状时eGFR下降,以及慢性HF在GDMT调整过程中eGFR下降,这两种情况都不应突然停止用药。
CKD患者可能从神经内分泌调节药物治疗中获益最大。对RALES试验的分析表明[4],与安慰剂相比,使用螺内酯治疗时,基线eGFR较差患者死亡率的绝对风险降低更显著。使用肾素-血管紧张素-醛固酮系统抑制剂(renin-angiotensin-aldosterone system inhibitor,RAASI)出现eGFR下降并不表示预后差,事实上降低了HF患者死亡率。使用SGLT2i的最初几天,也可能出现eGFR下降,这并不表示CKD恶化,相反,SGLT2i已被证实在HF和(或)糖尿病和(或)CKD患者中具有肾脏保护作用。
3 根据患者临床症状特征进行治疗
来自EPICAL2研究的数据显示[5],长期坚持GDMT的HFrEF患者3年全因和心血管死亡率降低。然而,HF患者充血状态、血流动力学和肾功能各不相同,并且HF治疗药物会影响血压、心率、肾功能和血钾,因此,需要根据患者特征进行调整,制定个性化治疗方法,确保每位患者受益于GDMT。心衰患者临床特征见图1。
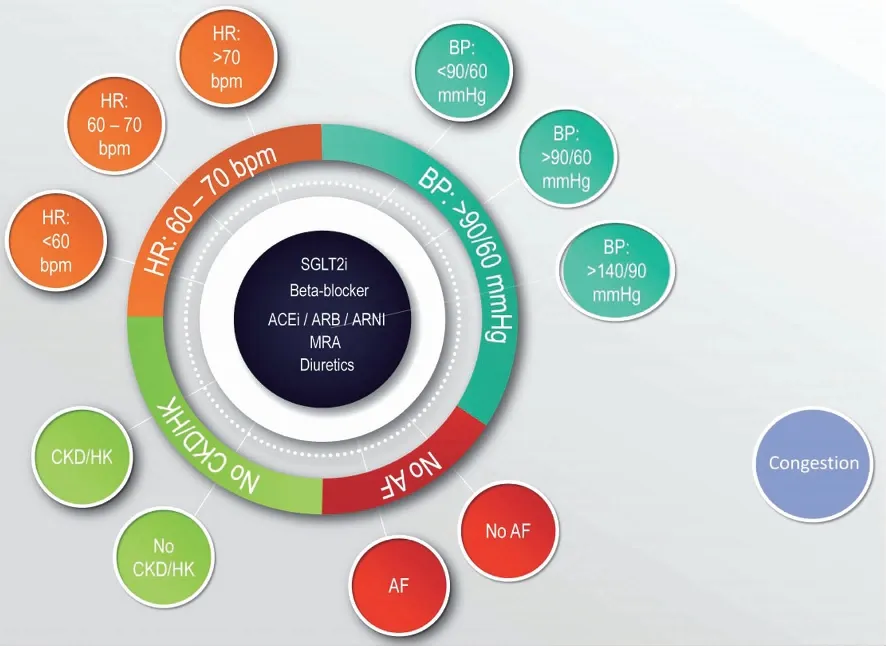
BP:血压;HR:心率;AF:心房颤动;HK:高钾血症。
HF核心治疗药物包括ACEI/ARB/ARNI、BB、MRA和SGLT2i,所有HF患者都应启动,这与2021年CCS/CHFS《心力衰竭指南更新:定义新的射血分数降低心力衰竭药理学标准》[5-6]推荐一致,并将其定义为HFrEF患者的标准治疗。HF核心药物治疗可以降低住院率和死亡率以及对器械治疗的需求。但如何实施核心治疗是一个难题,因为除SGLT2i之外,所有的核心药物治疗都会影响血压、心率或血钾,需要逐步调整剂量。因此,SGLT2i在复杂HF治疗中更容易实施,另外患者的特征识别有助于确定治疗策略(图2)。《共识》确定了9个需要个性化治疗的患者特征。
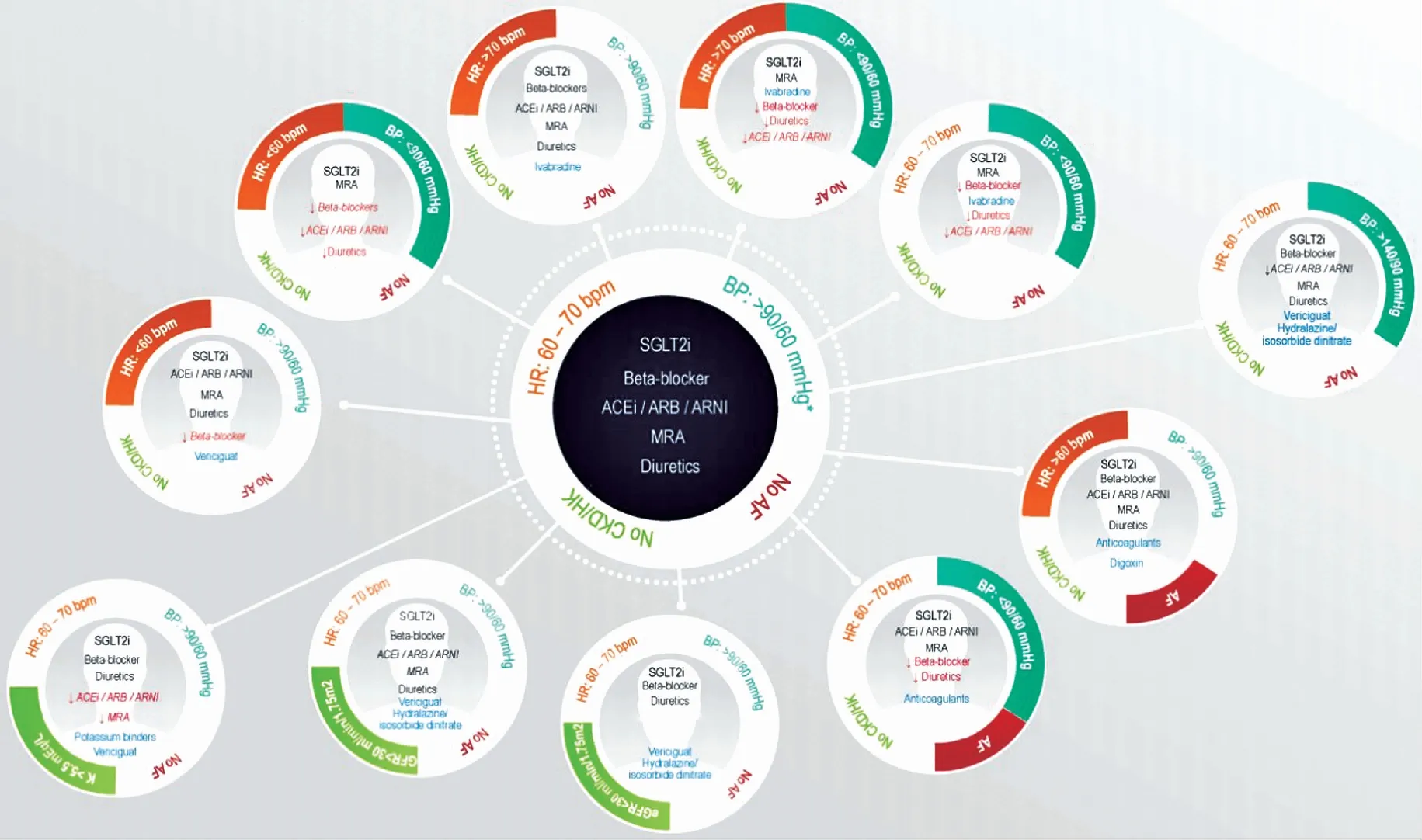
根据患者特征(血压、心率、是否存在房颤、CKD或高血压),减少、停用或添加药物。黑色:应给予患者的药物;红色:应减少或停用的药物;蓝色:应添加的药物。*慢性冠状动脉综合征患者,血压阈值为120/80 mmHg。
3.1特征1:低血压、快心率患者 HF患者的低血压通常定义为收缩压<90 mmHg(1 mmHg=0.133 kPa),合并冠状动脉疾病时,建议收缩压>120 mmHg[7]。此时应分析低血压原因,如低血容量、出血或感染。检查所有非HF治疗药物,评估硝酸酯类、钙通道阻滞剂和其他血管扩张剂的必要性,并尽可能停用。如果患者血容量正常,可尝试减停利尿剂,严密监测。只有当患者有症状性低血压时才需要调整GDMT。心率最好维持在60次·min-1,BB是HFrEF核心治疗药物的一部分,应调整到目标或最大耐受剂量。患者停用不必要的降压药物后,仍存在症状性低血压时,可能需要减少甚至停用BB。可以考虑使用伊伐布雷定,减慢心率而不影响血压。MRAs和SGLT2i对血压影响非常小,不需要或很少需要停药。收缩压<100 mmHg的患者禁止使用沙库巴曲/缬沙坦。此类症状严重的患者,omecamtiv mecarbil可能是一种治疗选择。
3.2特征2:低血压、慢心率患者 评估低血压的其他原因及其他药物,同特征1。只有当患者有症状性低血压时才需要调整GDMT。MRA和SGLT2i对血压的影响非常小,无需停药。如果患者心率<50次·min-1或症状性心动过缓,则BB可能需要减量。对于GDMT使用有限的患者,可以使用omecamtiv mecarbil。
3.3特征3:血压正常、慢心率患者 评估负性肌力作用药物,如果可能应停用,如非二氢吡啶钙通道阻滞剂(地尔硫和维拉帕米)、地高辛或抗心律失常药物。出现症状性心动过缓或心率<50次·min-1患者,伊伐布雷定应减量或停用,BB也需要减量。
3.4特征4:血压正常、快心率患者 增加BB达到目标剂量。窦性心律,心率>70次·min-1,联合使用BB和伊伐布雷定可以更好地控制心率,且在不增加不良反应的情况下更容易上调BB。ACEI/ARB/ARNI应调整至目标剂量。住院患者出院前应考虑启动维利西呱治疗。
3.5特征5:正常血压、心房颤动(房颤)患者 HF合并房颤患者的最佳静息心室率可能在60~80次·min-1[8]。与窦性心律患者相比,心率并不是HFrEF合并房颤患者死亡率的预测因子。目前BB对HF合并房颤患者获益证据不足,调整到最大耐受剂量可能不利,因为心室率<70次·min-1提示预后差。如无禁忌,房颤患者需要抗凝治疗。
3.6特征6:低血压、房颤患者 如前所述,BB获益证据不足,必要时可以减量或停用。地高辛可以替代BB控制心率,维持心率>70次·min-1。启动或调整有助于降低死亡率和发病率的药物,如ACEI或ARNI。MRAs和SGLT2i对血压的影响非常小,无需停药。HF合并房颤患者应始终进行抗凝,若无禁忌证最好使用非维生素K拮抗剂口服抗凝剂。
3.7特征7:CKD患者 大多数RCTs排除了严重CKD患者,药物安全性和有效性证据有限。如果RAASI调整期间出现肾功能恶化(称为假性肾功能恶化):血清肌酐增加>100%,或血钾水平升高>5.5 mmol·L-1,则应暂时停药;血清肌酐增加<50%且<3 mg·dL-1,eGFR>25 mL·min-1·(1.73 m2)-1,则减量即可。不良反应好转后,建议重新启动。沙库巴曲/缬沙坦可使用到eGFR<30 mL·min-1·(1.73 m2)-1。eGFR≥30 mL·min-1·(1.73 m2)-1的患者可以安全使用BB,有助于降低死亡率。eGFR≥30 mL·min-1·(1.73 m2)-1的患者,只要血钾≤5.0 mmol·L-1,高钾血症和肌酐升高的风险低,MRA也可以使用。在MRA启动或加量后的1~4周监测血钾,此后定期检测血钾。已经证明,在eGFR>20~25 mL·min-1·(1.73 m2)-1患者中,达格列净和恩格列净可以改善心血管和肾脏终点,并且在eGFR<20 mL·min-1·(1.73 m2)-1患者中,达格列净也有益。维利西呱和omecamtiv mecarbil分别可用于eGFR>15 mL·min-1·(1.73 m2)-1和eGFR>20 mL·min-1·(1.73 m2)-1的患者。禁用其他可能导致肾功能恶化的药物,如非甾体抗炎药。钾粘合剂(patiromer和环硅酸锆钠)可降低患者血钾,但并不改善预后。
3.8特征8:临近出院前患者的药物治疗管理 30% HF住院患者出院时伴有残留充血的临床症状,尤其是三尖瓣反流、糖尿病或贫血患者[9]。如果这些患者没有接受BB治疗,可暂不启动,因为充血状态患者开始BB可能导致临床恶化。已经接受足量ACEI治疗的患者,若收缩压>90 mmHg(或>100 mmHg),应启动ACEI(或ARNI治疗)。即使是充血状态和低血压患者,MRAs和SGLT2i也可以安全启动。恩格列净在这类患者中耐受性良好,并降低60 d时HF恶化、HF再住院或死亡的复合终点。在因HF住院的糖尿病患者中,SGLT1和SGLT2抑制剂索格列净降低了出院前或出院后的心血管死亡、住院和紧急就诊率。omecamtiv mecarbil和维利西呱已被证明用于出院前一些特定患者中可减少事件,并且缓解充血,为安全启动BB创造了条件。
3.9特征9:经GDMT仍有高血压的患者 对于高血压患者,首先需要确保患者没有服用任何可能升高血压的药物,如非甾体抗炎药、糖皮质激素或支气管扩张剂。确保患者对药物的依从性,并正在使用较高的推荐剂量。如果患者在GDMT最佳剂量仍有高血压,应联用硝酸异山梨酯和肼屈嗪。
4 结束语
《共识》与2021年CCS/CHFS《心力衰竭指南更新:定义新的射血分数降低心力衰竭药理学标准》一致认同GDMT对HF患者死亡率和发病率的重大益处,应尽一切努力启动并调整基础治疗。《共识》着重根据患者特征进行个性化治疗药物调整,将GDMT调整到适合患者的充血状态、血流动力学和肾功能,可以使每例患者比传统最大限度调整“一刀切”方法获得更好、更全面的治疗。
