复方二甲双胍格列吡嗪胶囊含量测定标准提升研究
2022-08-09漆欣筑何劼毅黄翰林
漆欣筑,祝 晶,何劼毅,黄翰林
(贵州省食品药品检验所,贵州 贵阳 550004)
0 引言
复方二甲双胍格列吡嗪胶囊为盐酸二甲双胍与格列吡嗪的复方制剂,临床上用于改善II型糖尿病患者的血糖控制[1-4]。目前,复方二甲双胍格列吡嗪胶囊在国内尚属独家品种,现行的标准为《国家药品标准》化学药品地方标准上升国家标准第七册,检验项目较为简单,其中含量测定部分为紫外分光光度法测定盐酸二甲双胍的含量[5],该方法灵敏度低、专属性较差,易导致测量结果不准确[6],且原标准中未对格列吡嗪的含量进行控制。
为了更好地控制药品质量,定量测定2个有效成分的准确含量,本研究拟对原标准中的含量测定部分进行提升,将盐酸二甲双胍的含量测定方法由UV法修订为高效液相色谱(HPLC)法,并增加了格列吡嗪的HPLC含量测定法,提升后的含量测定方法专属性强、准确度高,对提高产品的质量可控性有较好的帮助[7~9]。
1 仪器与试剂
1.1 仪器
高效液相色谱仪(岛津20A、Thermo Ultimate3000、Agilent1260),电子天平(METTLER TOLEDO XS205、METTLER TOLEDO AE240S),C18色谱柱(4.6 mm×250 mm,SHISEDO、Agilent、Thermo)。
1.2 药品与试剂
复方二甲双胍格列吡嗪胶囊(厂家送检),盐酸二甲双胍原料药、格列吡嗪原料药、肉桂提取物、淀粉(以上原料及原料药由厂家提供),格列吡嗪对照品(来源:中检院,批号:100281-201203),庚烷磺酸钠,磷酸二氢钠,甲醇,纯化水(实验室自制)。
2 实验部分
2.1 色谱条件与系统适应性试验
盐酸二甲双胍含量测定色谱条件:色谱柱采用C18柱;以庚烷磺酸钠与磷酸二氢钠的混合溶液(取庚烷磺酸钠1 g,加0.1 mol/L磷酸二氢钠溶液1 000 mL使溶解)-甲醇(80∶20,V∶V)为流动相;流速:1.0 mL/min;柱温:30 ℃;检测波长为233 nm。理论板数按盐酸二甲双胍计算不低于3 000,盐酸二甲双胍与相邻色谱峰的分离度应符合要求。
格列吡嗪含量测定色谱条件:色谱柱采用C18柱;以庚烷磺酸钠与磷酸二氢钠的混合溶液(取庚烷磺酸钠1 g,加0.1 mol/L磷酸二氢钠溶液1 000 mL使溶解)-甲醇(45∶55,V∶V)为流动相;流速:1.0 mL/min;柱温:30 ℃;检测波长为225 nm。理论板数按格列吡嗪计算不低于3 000,格列吡嗪与相邻色谱峰的分离度应符合要求。
2.2 测定方法
盐酸二甲双胍含量测定方法:取装量差异项下的内容物,混合均匀,精密称取适量(约相当于盐酸二甲双胍125 mg),置100 mL量瓶中,加水适量振摇使盐酸二甲双胍溶解,稀释至刻度,摇匀,滤过,精密量取续滤液1.0 mL,置50 mL量瓶中,加水稀释至刻度,摇匀,作为供试品溶液,精密量取20 μL注入液相色谱仪,记录色谱图。另取盐酸二甲双胍对照品,精密称定,加水溶解并稀释制成每1 mL中约含25 μg的溶液,同法测定,按外标法以峰面积计算,即得。
格列吡嗪含量测定方法:取装量差异项下的内容物,混合均匀,精密称取适量(约相当于格列吡嗪2.5 mg),置100 mL量瓶中,加甲醇60 mL,振摇使格列吡嗪溶解,用水稀释至刻度,摇匀,滤过,取续滤液作为供试品溶液,精密量取20 μL注入液相色谱仪,记录色谱图。另取格列吡嗪对照品约12.5 mg,置50 mL量瓶中,加甲醇30 mL,振摇使溶解,用水稀释至刻度,摇匀,精密量取5.0 mL置50 mL量瓶中,用60%甲醇溶液稀释至刻度,作为对照品溶液,同法测定。
3 盐酸二甲双胍含量测定方法学验证
3.1 专属性试验
溶液配制:精密称取盐酸二甲双胍原料药125 mg、格列吡嗪原料药2.5 mg、肉桂提取物150 mg、淀粉约70 mg,分别置100 mL量瓶中,加水适量,振摇使溶解并稀释至刻度,摇匀,精密量取1.0 mL置50 mL量瓶中,加水稀释至刻度,即得盐酸二甲双胍溶液、格列吡嗪溶液、肉桂提取物溶液及淀粉溶液。
盐酸二甲双胍阴性溶液:精密称取格列吡嗪原料药2.5 mg,置100 mL量瓶中,加水适量,振摇使溶解并稀释至刻度,摇匀,精密量取1.0 mL置50 mL量瓶中,加水稀释至刻度,摇匀,即得。
混合溶液:精密称取盐酸二甲双胍原料药125 mg、格列吡嗪原料药2.5 mg、肉桂提取物150 mg、淀粉约70 mg,置100 mL量瓶中,加水适量,振摇使溶解,并加水稀释至刻度,摇匀,精密量取1.0 mL置50 mL量瓶中,加水稀释至刻度,摇匀,即得。
分别精密量取上述溶液和配制用水各20 μL,照盐酸二甲双胍含量测定方法进样。试验结果表明,盐酸二甲双胍阴性溶液色谱图中未见盐酸二甲双胍色谱峰,色谱图显示其他各组分及配置用水均不会对盐酸二甲双胍的含量测定产生干扰,混合溶液中盐酸二甲双胍色谱峰与盐酸二甲双胍原料药色谱峰保留时间一致,分离度符合要求。该方法专属性好,能有效分离待测组分与其他组分,如图1所示。
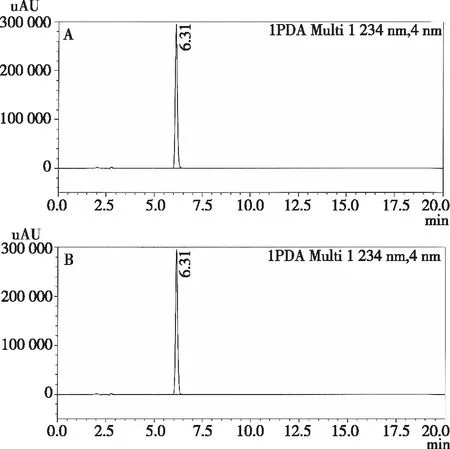
图1 混合对照品溶液(A);不含盐酸二甲双胍阴性对照溶液(B)Fig.1 Mixture reference (A); Non metformin hydrochloride negative sample (B)
3.2 线性考察
储备液制备:精密称取盐酸二甲双胍对照品25.0 mg,置100 mL量瓶中,加水振摇使溶解并稀释至刻度,摇匀,即得。
80%、90%、100%、110%、120%线性溶液:分别精密量取线性贮备液8.0 mL、9.0 mL、10.0 mL、11.0 mL、12.0 mL,置100 mL量瓶中,加水稀释至刻度,摇匀,即得。
根据含量测定方法取上述5种不同浓度的线性溶液各20 μL进样。试验结果表明,盐酸二甲双胍在20.07~30.11 μg/mL范围内呈良好的线性关系(图2)。

图2 盐酸二甲双胍线性结果Fig.2 The standard curve line of metformin hydrochloride
3.3 精密度考察
照含量测定方法,精密量取专属性试验中混合溶液20 μL进样,重复进样6次,记录色谱图,考察仪器精密度,以峰面积计算精密度,RSD为0.12%。
取盐酸二甲双胍格列吡嗪胶囊20粒,取混合均匀的内容物,平行处理6份样品,照含量测定方法进样,记录色谱图,考察方法精密度,以峰面积计算精密度,RSD为0.05%。试验表明,仪器精密度与方法精密度均良好。
3.4 稳定性考察
取样品1粒,照含量测定方法中供试品溶液配制方法处理,作为供试品溶液,放置在室温条件下,经0 h、1 h、2 h、4 h、6 h和8 h分别精密量取供试品溶液20 μL进样,记录色谱图,以峰面积计算稳定性,RSD为0.61%,试验结果表明:供试品溶液在8 h内稳定性良好。
3.5 回收率考察
精密称取盐酸二甲双胍对照品1.25 g,置200 mL量瓶中,加水适量,振摇使溶解并稀释至刻度,作为回收率贮备液。精密称取样品适量,加回收率贮备液后制成高浓度样品溶液(120%)、中浓度样品溶液(100%)、低浓度样品溶液(80%)3份,照含量测定方法进样,记录色谱图,计算回收率分别为99.09%、100.00%、99.73%、99.34%、99.11%、100.62%、101.19%、101.03%、101.03%,平均回收率为99.8%,RSD为0.95%,试验结果表明,该方法回收率良好。
3.6 耐用性考察
分别使用正常色谱条件,不同柱温(30±5)℃、不同流速(1.0±0.1)mL/min、不同流动相比例、不同色谱柱(Thermo C18、Agilent C18、SHESEIDO C18)以及不同的液相色谱仪(岛津、Agilent、Thermo)进行测试,分别计算,对盐酸二甲双胍含量进行考察。结果显示盐酸二甲双胍含量的RSD为0.45%,含量耐用性较好。
4 格列吡嗪含量测定方法学验证
4.1 专属性试验
溶液配制:精密称取盐酸二甲双胍原料药125 mg、格列吡嗪原料药2.5 mg、肉桂提取物150 mg、淀粉约70 mg,分别置100 mL量瓶中,加甲醇60 mL振摇使溶解,并加水稀释至刻度,摇匀,即得盐酸二甲双胍溶液、格列吡嗪溶液、肉桂提取物溶液及淀粉溶液。
格列吡嗪阴性溶液:精密称取盐酸二甲双胍原料药125 mg、肉桂提取物150 mg、淀粉约70 mg,置100 mL量瓶中,加甲醇60 mL振摇使溶解,并加水稀释至刻度,摇匀,滤过即得。
混合溶液:精密称取盐酸二甲双胍原料药125 mg、格列吡嗪原料药2.5 mg、肉桂提取物150 mg、淀粉约70 mg,置100 mL量瓶中,加甲醇60 mL振摇使溶解,并加水稀释至刻度,摇匀,滤过即得。
分别精密量取上述溶液和60%甲醇溶液各20 μL进样,记录色谱图。试验结果表明,格列吡嗪阴性溶液色谱图中未见格列吡嗪色谱峰,其他各组分及溶剂色谱图显示均不会对格列吡嗪的含量测定产生干扰,混合溶液中格列吡嗪色谱峰与格列吡嗪原料药色谱峰保留时间一致,分离度符合要求。该方法专属性好,能有效分离待测组分与其他组分(图3)。

图3 混合对照品溶液(A);不含格列吡嗪阴性对照溶液(B)Fig.3 Mixture reference (A);Non glipizide negative sample (B)
4.2 线性考察
线性贮备液制备:精密称取格列吡嗪对照品25.0 mg,置100 mL量瓶中,加甲醇60 mL振摇使溶解,并加水稀释至刻度,摇匀,即得。
70%、80%、90%、100%、110%、120%、130%线性溶液:分别精密量取线性贮备液7.0 mL、8.0 mL、9.0 mL、10.0 mL、11.0 mL、12.0 mL、13.0 mL,置100 mL量瓶中,加60%甲醇溶液稀释至刻度,摇匀,即得。根据含量测定方法取上述7种不同浓度的线性溶液各20 μL进样。
试验结果表明,格列吡嗪在17.48~32.45 μg/mL范围内呈良好的线性关系,结果见图4。

图4 格列吡嗪线性关系考察结果Fig.4 The standard curve line of glipizide
4.3 精密度考察
参照格列吡嗪含量测定方法及3.3试验方法对仪器精密度及方法精密度进行考察,以峰面积计算精密度,仪器精密度RSD为0.45%,方法精密度RSD为0.43%,试验表明,仪器精密度与方法精密度均良好。
4.4 稳定性考察
精密称取样品1粒,照含量测定方法中供试品溶液配制方法处理,作为供试品溶液,放置在室温条件下,经0 h、1 h、2 h、4 h、6 h和8 h分别精密量取供试品溶液20 μL进样,记录色谱图,以峰面积计算稳定性,RSD为0.3%,试验结果表明:供试品溶液在8 h内稳定性良好。
4.5 回收率考察
精密称取格列吡嗪对照品25 mg,置200 mL量瓶中,加甲醇溶解并稀释至刻度,作为回收率贮备液。精密称取样品适量,以60%甲醇作为溶剂,加回收率储备液后制成高浓度样品溶液(120%)、中浓度样品溶液(100%)、低浓度样品溶液(80%)3份,照含量测定方法进样,记录色谱图,计算回收率分别为100.20%、100.10%、99.10%、99.46%、100.80%、99.25%、99.48%、98.82%、100.10%,平均回收率为99.7%,RSD为0.64%,试验结果表明,该方法回收率良好。
4.6 耐用性考察
分别使用正常色谱条件,不同柱温(30±5)℃、不同流速(1.0±0.1)mL/min 、不同流动相比例、不同色谱柱(Thermo C18、Agilent C18、SHESEIDO C18)以及不同的液相色谱仪(岛津、Agilent、Thermo)进行测试,分别计算,对盐酸二甲双胍含量进行考察。结果所有格列吡嗪含量的RSD为0.65%,含量测定方法耐用性较好。
5 样品含量测定
通过已建立的方法对3批样品的盐酸二甲双胍及格列吡嗪含量进行测定,结果显示:盐酸二甲双胍含量在97.53%~100.26%之间、格列吡嗪的含量在99.83%~101.71%之间。说明该方法可以测定盐酸二甲双胍格列吡嗪中盐酸二甲双胍和格列吡嗪的含量,结果见表1和表2。

表1 3批样品盐酸二甲双胍含量测定结果Tab.1 Determination results of metformin hydrochloride in 3 batches of samples
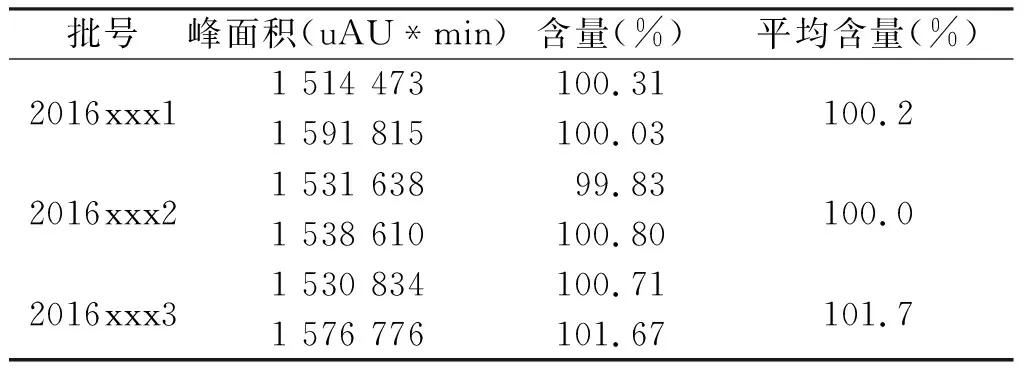
表2 3批样品格列吡嗪含量测定结果Tab.2 Determination results of glipizide in 3 batches of samples
6 讨论
复方二甲双胍格列吡嗪胶囊辽宁修和药业有限公司的独家品种,有临床试验数据显示,使用该复方制剂比单独使用二甲双胍或格列吡嗪更显著的降低II型糖尿病患者的糖化血红蛋白水平,同时患者的依从性、耐受性好,因此该制剂在临床上使用较为广泛[9-10]。按照本文建立的含量测定方法对盐酸二甲双胍格列吡嗪胶囊进行含量测定,在测定条件下其他物质对于盐酸二甲双胍及格列吡嗪的测定均无干扰,测定结果可信,耐用性好,表明建立的方法具有广泛的适用性,可以准确测定复方二甲双胍格列吡嗪胶囊中盐酸二甲双胍、格列吡嗪的含量,能有效控制复方二甲双胍格列吡嗪胶囊的质量,对复方二甲双胍格列吡嗪胶囊质量标准的制定有一定的提升作用。
