小儿腹腔镜肝切除的技术改进及疗效分析
2022-08-08郑百俊余辉李鹏程继文郭新奎田东浩熊娜高亚
郑百俊 余辉 李鹏 程继文 郭新奎 田东浩 熊娜 高亚
西安交通大学第二附属医院小儿外科,西安 710004
1991年Reich等[1]报道了世界首例腹腔镜肝脏楔形切除术,之后腹腔镜肝切除术(laparoscopic liver resection,LLR)在世界范围内逐渐开展。LLR早期主要用于肝脏边缘良性肿瘤的切除,随着外科医师对肝脏解剖的深入了解和腹腔镜技术的不断进步,LLR的手术适应证范围不断扩大,现已广泛应用于较大范围的肝切除以及肝脏恶性肿瘤切除。与成人相比,小儿LLR应用很少且进展缓慢,近年来西安交通大学第二附属医院小儿外科探索了LLR的临床应用,初步证实了其可行性与安全性[2-4]。2019年6月起,西安交通大学第二附属医院常规应用术前3D虚拟重建手术规划和术中吲哚菁绿(indocyanine green,ICG)荧光导航技术,并严格选择病例、探索完善手术技术,取得了一定成果,现报告如下。
材料与方法
一、临床资料
以西安交通大学第二附属医院2005年11月至2022年3月收治的42例肝脏肿瘤患儿为研究对象,其中前期组(2005年11月至2019年5月手术病例)25例,后期组(2019年6月至2022年3月手术病例)17例,两组均采用腹腔镜肝切除(laparoscopic liver resection, LLR)治疗。本研究获得西安交通大学第二附属医院伦理委员会批准(编号:001/2022)。
肝母细胞瘤(hepatoblastoma,HB)术前诊断依据包括血清甲胎蛋白(α-fetoprotein,AFP)、影像学检查结果、超声引导下穿刺活检结果。对PRETEXT分期Ⅱ期及以上的HB患儿,术前根据其危险度分层参考SIOPEL-4 (International Society of Paediatric Oncology Epithelial Liver Tumour Group)方案给予化疗2~4个疗程[5-6]。
后期组17例平均手术年龄21个月 (2~44个月),其中良性占位3例(肝血管内皮瘤、局灶性结节性增生、肝间叶错构瘤各1例),HB 14例(单灶13例,多灶1例)。肝脏占位最长径平均为6.2 cm(3.2~14.4 cm)。HB的 PRETEXT分期:Ⅰ期 1例、Ⅱ期8例、Ⅲ期5例(其中2例伴肺转移)。13例Ⅱ、Ⅲ期患儿接受以铂类为基础的术前化疗2~4个疗程,POSTTEXT Ⅰ期 4例、Ⅱ期9例,2例肺转移患儿转移灶均消失。前期组、后期组资料对比见表1,两组患儿年龄、性别、原发病及肿瘤最长径差异均无统计学意义(P>0.05)。
二、研究方法
(一)LLR手术适应证与禁忌证
LLR手术适应证包括: ①肿瘤距离第一和第二肝门均≥1 cm、预定切缘>1 cm、残肝体积大于标准肝体积25%(化疗后残肝体积大于标准肝体积的30%)的HB; ②最长径大于5 cm、持续增大或有症状的良性占位或不能排除恶性者。LLR手术禁忌证包括: ①肿瘤紧贴或侵及门静脉、肝静脉及下腔静脉; ②腹腔严重粘连。对存在LLR适应证者,选择LLR或开放手术由患儿家长决定并签署知情同意书。
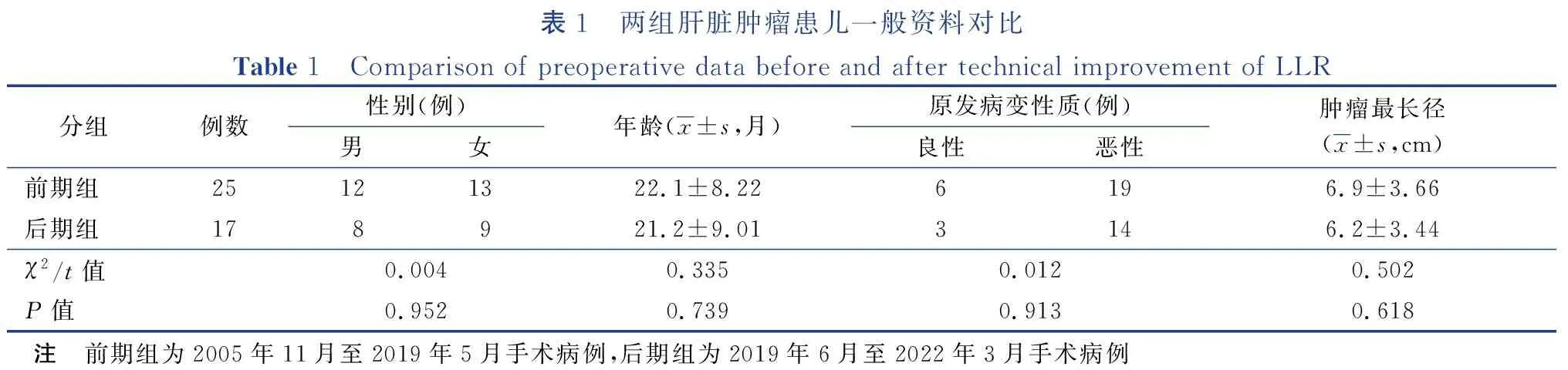
表1 两组肝脏肿瘤患儿一般资料对比Table 1 Comparison of preoperative data before and after technical improvement of LLR 分组例数性别(例)男女年龄(x±s,月)原发病变性质(例)良性恶性肿瘤最长径(x±s,cm)前期组25121322.1±8.226196.9±3.66后期组178921.2±9.013146.2±3.44χ2/t值0.0040.3350.0120.502P值0.9520.7390.9130.618 注 前期组为2005年11月至2019年5月手术病例,后期组为2019年6月至2022年3月手术病例
(二)主要技术改进
手术步骤参见作者已发表论文[3-4]。后期组与前期组相比,主要技术改进包括: ①术前行增强CT检查及三维重建,进行个体化虚拟手术规划; ②所有病例应用ICG进行术中导航(图1),术前48~72 h经外周静脉注射ICG 0.3~0.5 mg/kg(正染)或术中阻断目标肝段血供后经外周静脉注射ICG 0.05~0.1 mg/kg(反染); ③部分患儿行患侧一级或二级肝蒂Glisson鞘外解剖及阻断; ④肝实质离断时根据术中情况降低中心静脉压(2~4 cmH2O,1 cmH2O=0.098 kPa),如创面渗血明显则适当升高气腹压力[7-8]。
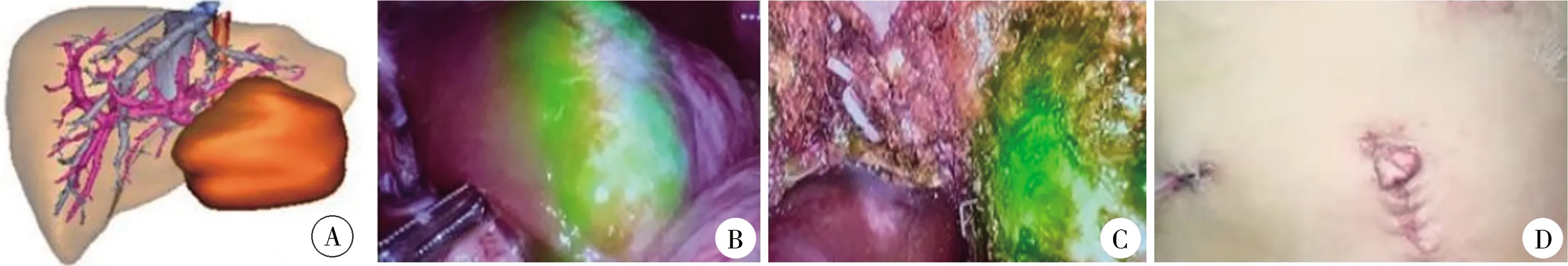
图1 1例肝脏肿瘤患儿腹腔镜肝左外叶切除手术照片A:术前三维CT重建; B:断肝前ICG正染显影; C:断肝中ICG正染显影; D:术后腹壁外观Fig.1 ICG positive staining image of laparoscopic left lateral hepatic lobectomy注 ICG指吲哚菁绿
三、观察指标
主要包括手术相关指标(手术时间、出血量、中转手术情况、HB切缘)、围手术期并发症发生情况(腹腔内出血、胆漏)、血生化检查结果(肝功能、甲胎蛋白变化情况)、是否再手术以及术后随访结果(肿瘤复发、转移情况)。
四、统计学处理

结 果
一、治疗结果
共行非解剖性切除2例(S71例,S4a1例),解剖性切除14例(左外叶1例,左半肝7例,右半肝3例,右后叶3例),联合肝脏分隔和门静脉结扎的二步肝切除术(associated liver partition and portal vein ligation for staged hepatectomy,ALPPS)手术1例[9]。后期组患儿平均手术时间234.4 min(70~360 min),出血量60.7 mL(20~300 mL),所有肿瘤均无破裂,HB均获R0切除,平均切缘1.2 cm(0.7~3.0 cm)。术后1~2 d即可下床活动及进食。ALPPS手术患儿出现胆漏,经引流25 d后自愈。其余患儿术后2~4 d拔管。围手术期无其他并发症及再手术患儿。术后肝功能恢复正常平均时间为7 d(5~12 d),HB术后平均开始化疗时间为12 d(10~16 d)。术后平均随访18个月(1~34个月),1例术前伴肺转移的HB患儿术后14个月出现肺部病变复发,无肝脏局部复发及其他部位转移,其余患儿均无肿瘤复发。与前期资料对比见表2,两组患儿手术方式、手术时间、出血量、中转开放情况、HB切缘和胆漏发生差异均无统计学意义(P>0.05)。

表2 两组肝脏肿瘤患儿手术资料及并发症对比 Table 2 Comparison of operative data and complications before and after technical improvement of LLR 分组例数手术方式(例)不规则解剖性ICG应用(例)手术时间(x±s,min)出血量(x±s,mL)中转手术(例)HB切缘(x±s,cm)胆漏(例)前期组257180246.5±54.3875.4±30.0521.0±0.314后期组1721517234.4±56.2260.7±36.4411.2±0.371χ2/t值0.767-0.6981.4280.0001.8970.295P值0.381-0.4890.1611.0000.0650.611 注 前期组为2005年11月至2019年5月手术病例,后期组为2019年6月至2022年3月手术病例;ICG指吲哚菁绿;HB指肝母细胞瘤
二、特殊病例介绍
1例肿瘤最小的患儿因癫痫住院检查发现左内叶上段肝脏肿瘤3.2 cm×2.0 cm,血AFP 996.2 ng/mL,诊断为HB(PRETEXT Ⅰ期),术中用腹腔镜下血管阻断夹行左侧肝蒂Glisson鞘外暂时性阻断,在正染ICG荧光引导下顺利完成S4a肿瘤非解剖性R0切除,手术时间70 min,术中出血20 mL。1例就诊时肝脏肿瘤大小为12.2 cm×9.5 cm×8.8 cm,呈不均质实性,伴双肺多发结节,血AFP>121 000 ng/mL,超声引导下穿刺活检为HB,术前化疗4个疗程(3个疗程顺铂/顺铂-表柔比星联合1个疗程异环磷酰胺+卡铂+依托泊苷)后肺部病变消失,肿瘤大小4.0 cm×2.5 cm×2.5 cm,位于S7,血AFP 329.2 ng/mL,经Pringle法阻断第一肝门+正染ICG荧光引导下顺利切除肿瘤,随访至今已31个月,患儿生长发育正常。
ALPPS手术患儿就诊时肿瘤大小为13.7 cm×8.9 cm×14.4 cm,三维重建显示肿瘤与肝脏大血管位置关系不明,预估完整切除肿瘤后FLR/TLV小于20%。两期手术均在腹腔镜下完成,Ⅰ期行门静脉右支结扎+部分肝实质分割术,手术时间180 min,围手术期未输血,术后残肝容积增长率为78.2%;Ⅱ期在ICG引导下完整切除右三叶,手术时间360 min,输血600 mL,术后12 d肝功能恢复正常。术后出现胆漏,最大引流量175 mL/d,经引流后自愈。术后病理报告为肝间叶错构瘤,目前恢复良好。
本组肝右后叶切除共3例,均在Rouviere’s沟内解剖右后肝蒂,行Glisson鞘外阻断+反染ICG荧光引导下完成手术[8]。1例右半肝切除患儿因第一肝门处理困难、手术进展缓慢而中转开腹手术。
讨 论
LLR治疗肝脏良性疾病的安全性和有效性已经得到确认。2008年第1届国际腹腔镜肝切除的Louisville Statement推荐:位于肝脏外缘(即S2、S3、S4b、S5、S6)直径小于5 cm的单发病灶,以及左外叶切除是LLR初级手术适应证[10]。之后,2014年第2届国际腹腔镜肝切除Morioka共识指出:超过3个肝段切除(如左半肝、右半肝、左三叶切除)手术,以及后上段、左内叶上段、中肝、尾叶切除属特殊或困难部位手术,建议由经验丰富肝脏中心实施[11]。随着手术经验的积累和技术的进步,LLR对恶性肿瘤的根治效果逐渐显现,除创伤小、出血少、住院时间短的优点外,在结肠癌肝转移、原发性肝癌根治切除效果上,五年存活率与开放手术接近或相似;手术技术从手辅助腔镜逐渐发展到完全腹腔镜,再由完全腹腔镜发展到机器人,重大手术比例从10%以下上升到20%,手术适应证从病灶切除发展到供肝切取(左外叶、左叶、右叶)。随着精准肝切除理念的引入,3D重建虚拟手术规划、术中超声、ICG实时导航技术逐渐应用,以肝蒂、肝静脉为基础的微创肝叶(sectionectomy)/肝段(segmentectomy)切除得以实现。
由于肝脏管道变异多且复杂,小儿肝脏肿瘤以巨块型(直径大于5 cm)居多,加之腹腔空间小,腹腔镜下止血困难、出现大出血风险较高等因素,使LLR在儿童群体中开展缓慢。本研究团队和Veenstra等[12]、Kwon等[13]及Wang等[14]的研究结果均显示了小儿LLR的安全性,LLR可以满足肿瘤根治性切除规范要求:整块切除、切缘阴性、避免术中瘤体破裂/溢出、淋巴结切取活检、保留足够肝实质。为了提高手术切除率、减少术中瘤体破裂、增加残余肝体积,我们进行了常规术前化疗,以达到肿瘤降级并降低手术风险的目的。
HB根治性切除适用于肿瘤预定切缘距离第一和第二肝门重要管道≥1 cm的患儿。小儿肝切除的残肝体积应达到标准肝体积的25%~30%(化疗后应大于标准肝体积的30%)。由于HB患儿就诊时中晚期患儿比例多达70%,HB生物学行为较肝细胞肝癌好,如果选择预设切缘≥1 cm,可能使相当一部分患儿丧失根治手术机会(转而行肝移植)。因此,如何把握根治性切除率、尽可能多保留肝实质需要个性化评估。近年来,我们对需肝切除术的患儿在术前常规行增强CT检查及三维重建,了解肿瘤的大小、位置及其与周围血管、胆管的立体解剖关系,评估可切除性并进行虚拟手术规划。我们认为,手术规划应以获得根治性切除为首要目的;如扩大手术范围不能增加根治的可能性,或可能出现残肝体积不足时,应选择基于门静脉供血和肝静脉引流为基础的肝叶(sectionectomy)/肝段(segmentectomy)切除,或采用ALPPS技术,术中根据肿瘤的位置、大小和相邻空间解剖位置关系,结合ICG荧光导航,确定并保持正确的断肝线/面;缺血线和肿瘤荧光边界不一时,应考虑ICG荧光反染或术中超声辅助。本组大部分病例采用正染法,术前48 h经周围静脉注射ICG,术中根据肿瘤组织内残留的荧光和缺血线确定肝表面切线,切开肝实质后依荧光和肝内主要管道走向引导断肝,标本切除后再次检查断面,确认有无肿瘤残存,证实了ICG术中导航在保证肿瘤R0切除方面的优势。
术中出血是LLR面临的主要挑战,也是中转手术的首要原因。目前我们常规预留Pringle阻断带,采用Pringle法阻断;右前叶、右后叶、右半肝切除采用Glisson鞘外解剖二级肝蒂,于肝实质内分别离断。如肿瘤距肝门较近,选择Pringle法阻断入肝血流,劈开肝实质浅面显露肝蒂并解剖出适当长度;如巨大右肝肿瘤或肝门部肿瘤妨碍显露,则选择前入路结合尾路手术。左右半肝切除时,断面上会遇到较大脉管,改为与管道平行方向将其游离出适当长度,明辨确认肝中静脉关系后再作处理。在保证循环稳定的前提下可降低中心静脉压,创面渗血明显时可适当升高气腹压力。在肝实质离断即将完成时游离出肝左/肝右静脉根部,采用hem-o-lock或Endo-GIA离断。
本研究中后期组和前期组相比,手术时间、出血量、术中中转、HB切缘和胆漏发生差异均无统计学意义[3-4]。但前期组的4例胆漏患儿中,有1例严重胆漏患儿共住院4次,总住院时间达11个月,经历3次手术治愈。后期组发生胆漏1例,经引流后治愈,一定程度上体现出技术改进后的优势,但仍需大样本研究进一步证实。
我们认为,严格把握手术适应证、术前通过三维重建掌握肝脏肿瘤的空间解剖关系、术中采用合理的手术入路并应用吲哚菁绿导航可有效减少小儿LLR的并发症。
利益冲突所有作者均声明不存在利益冲突
作者贡献声明论文设计调查为高亚、郑百俊、李鹏,数据收集与统计分析为余辉、程继文、田东浩、熊娜,论文结果撰写为郑百俊、郭新奎、田东浩,论文讨论分析为高亚、郑百俊
