溶剂萃取法从电解锰净化渣浸出液中回收锰钴镍的研究*
2022-08-01黎桂昌吴元花叶有明谢雪珍文美娜
黎桂昌,吴元花,叶有明,谢雪珍,文美娜
(1 广西科技师范学院,广西 来宾 546199;2 广西桂柳新材料股份有限公司,广西 柳州 545004)
钴镍是重要的有色金属资源,自然钴镍矿石中钴镍含量较低[1],而电解锰废渣中钴、镍含量均高于自然钴镍矿石中含量,所以从电解锰废渣中回收锰钴镍具有重要的意义。电解锰废渣常用硫酸浸出法回收有价金属,浸出液中主要含Mn、Ni、Co,均以硫酸盐的形式存在。钴镍化学性质非常相似,较难分离,且溶液中的杂质含量较高,需要进一步的除杂分离提纯。
锰钴镍分离的主要方法有[2-3]:化学沉淀法、离子交换法和溶剂萃取法。而溶剂萃取法因其具有选择性好、操作简单快捷、回收率高等特点,在钴镍的分离上得到了广泛的研究和应用。常用的萃取剂有胺类萃取剂、磷酸类萃取剂和羧酸类萃取剂等[1]。其中对于硫酸盐溶液,磷酸类萃取剂使用最为广泛,如P204、P507、Cyanex272、Cyanex302等[4-8]。但回收分离过程中遇到诸多的问题需要解决[4-9],如:①浸出液中的铁、铝、钙、镁等杂质严重影响萃取效果;②回收的锰溶液中铁含量过高不满足进一步深加工要求。目前,冶金工业中一般采用水解沉淀法除铁,如:黄铁矾法[10]、针铁矿法[11-12]和赤铁矿法[13-14]。根据锰浸出液的特点,文本采用赤铁矿法使用碳酸钙法除铁,然后使用氟化锰除钙镁,再用P204回收锰,最后使用P507进一步分离钴和镍,最终实现锰、钴、镍分离回收。
1 实验部分
1.1 实验原料和试剂
实验原料:浸出液,取自广西桂柳新材料有限公司电解锰净化渣硫酸多次浸出后溶液,组成见表1 所示。

表1 浸出液的主要化学成分
主要试剂:浓硫酸(AR),氨水(AR),P204(工业级),P507(工业级),磺化煤油(工业级)。
1.2 主要仪器
pH计,集热式恒温加热搅拌器,AA-6300C原子吸收光谱仪。
2 实验原理与方法
2.1 实验原理
2.1.1 除铁
萃取前用碳酸钙调节溶液的pH至Fe3+形成氢氧化铁沉淀去除,酸度减少到一定程度后碳酸钙不再溶解,而引入的钙离子在后续步骤中形成沉淀除去,反应式如下:
CaCO3+H+=Ca2++H2O+CO2↑
Fe3++H2O=Fe(OH)3↓+3H+
2.1.2 除钙、镁
萃取前用氟化锰除去引入了钙离子和溶液中的镁。常温时MnF2的溶解度为1.06 g/100 mL水,而氟化钙KSP=2.7 ×10-11,氟化钙KSP=6.4×10-9,可利用溶解度差异除钙镁,反应式如下:
M2++2F-=MF2↓
2.1.3 萃取分离锰、钴、镍
P204和P507均为磷酸类酸性萃取剂,其活性氢与金属进行离子交换,形成稳定的络合物。P204在一定条件下优先萃取铁和锰,萃余液继续用P507萃取可分离钴。萃取剂对金属离子的萃取顺序[1]:Fe3+>Mn2+>Co2+>Ni2+,受pH影响很大,可通过控制酸度分离回收锰钴镍。反应式为:
萃取:2HA+M2+=MA2+2H+
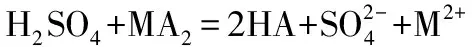
式中:HA为P204或P507;M2+为Mn2+、Co2+、Ni2+。
2.2 实验方法
除杂:在浸出液中加入缓慢碳酸钙调节浸出液pH,确定pH后,加热保温一段时间,过滤得清液。在溶液中加入氟化锰,加热,保温,再加入硫酸铝,静置一段时间后过滤得低钙、镁含量的溶液。
萃取:用硫酸和NaOH调pH,加入萃取剂,搅拌混匀 15 min,分离,检测水相中锰钴镍质量浓度,计算萃取率。
(2)
式中:E为萃取率,%;ρ0为初始离子质量浓度,g/L;V0为溶液体积,L;B(A/B)为A与B的分离系数;ρ余为萃余水相中离子质量浓度,g/L。
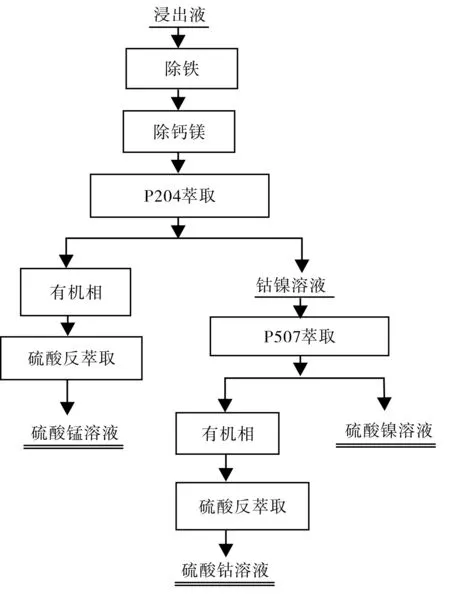
图1 工艺流程图
3 实验结果与讨论
3.1 碳酸钙除铁
3.1.1 pH对除铁的影响
在浸出液中加入碳酸钙调pH去除铁杂质,结果如图2所示。由图2可以看出:随pH提高,铁去除率提高;pH大于3.5后,铁去除率变化不大,铁已完全水解。继续增大pH,锰钴镍也会形成氢氧化物沉淀,造成有价金属的损失。综合考虑,确定适宜pH为3.5。

图2 线上线下混合实验教学模式
3.1.2 温度和时间对除铁的影响
浸出液加热到一定温度后,加入碳酸钙调pH值至3.5,保温一定的时间后,考查反应温度和保温时间对氢氧化铁的沉降的影响,试验结果见图3和表2所示。由图3可以看出,温度越高,除铁率越高,除铁效果越好,80 ℃除铁时,1.5 h时去除率已达最佳。同时,由表1可以看出,反应温度和保温时间会严重影响氢氧化铁的沉淀效果,80 ℃以上时,氢氧化铁颗粒成型较好,颗粒较大,较易过滤。综合考虑,最佳除铁温度为80 ℃,保温1.5 h。除铁后,浸出液的铁含量约2.5 mg/L,不会对萃取产生影响。
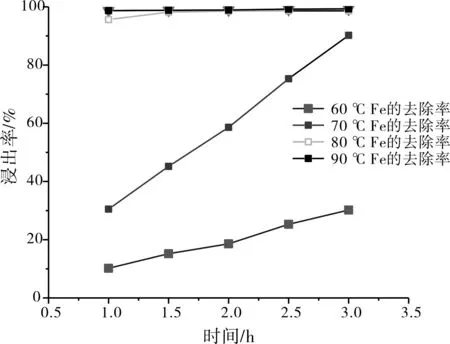
图3 温度和时间对溶液去除铁的影响
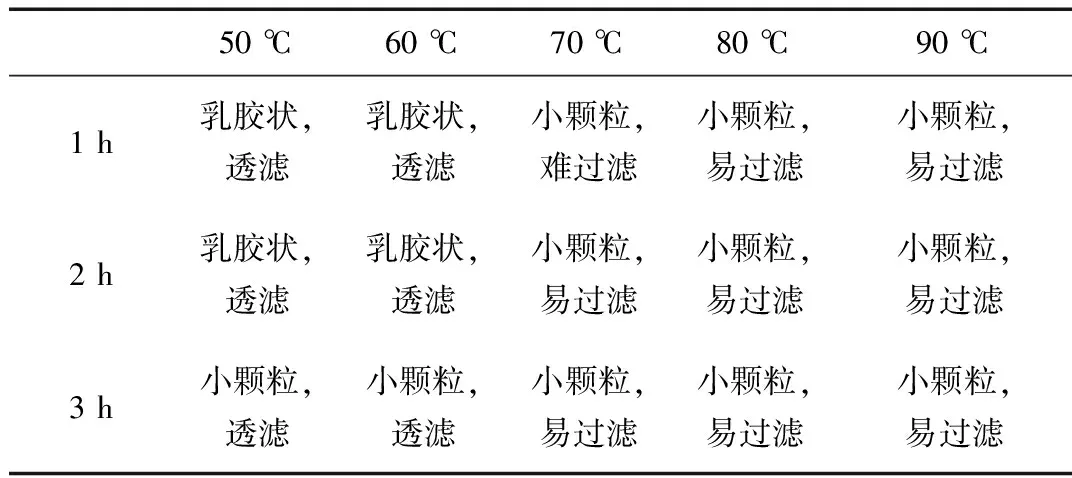
表2 反应温度和保温时间对除铁的影响
3.2 氟化锰除钙镁
3.2.1 氟化锰的用量对去除率的影响
在除铁后的溶液中加入不同过量系数的(按钙镁计算)的氟化锰,加热至60 ℃,搅拌反应1 h。考查氟化锰的用量对钙镁去除率的影响,结果如图4所示。由图4看出,随着氟化锰的用量的增加,钙镁去除率增加。氟化锰的用量与理论量之比大于1.5后趋于稳定。氟化锰用量少,钙镁离子去除不充分;氟化锰用量过多,则会导致溶液中氟离子含量增加,影响后续操作。故氟化锰的用量与理论量之比1.5时为最佳,此时钙、镁离子的去除率分别达到97.9%和96.6%。
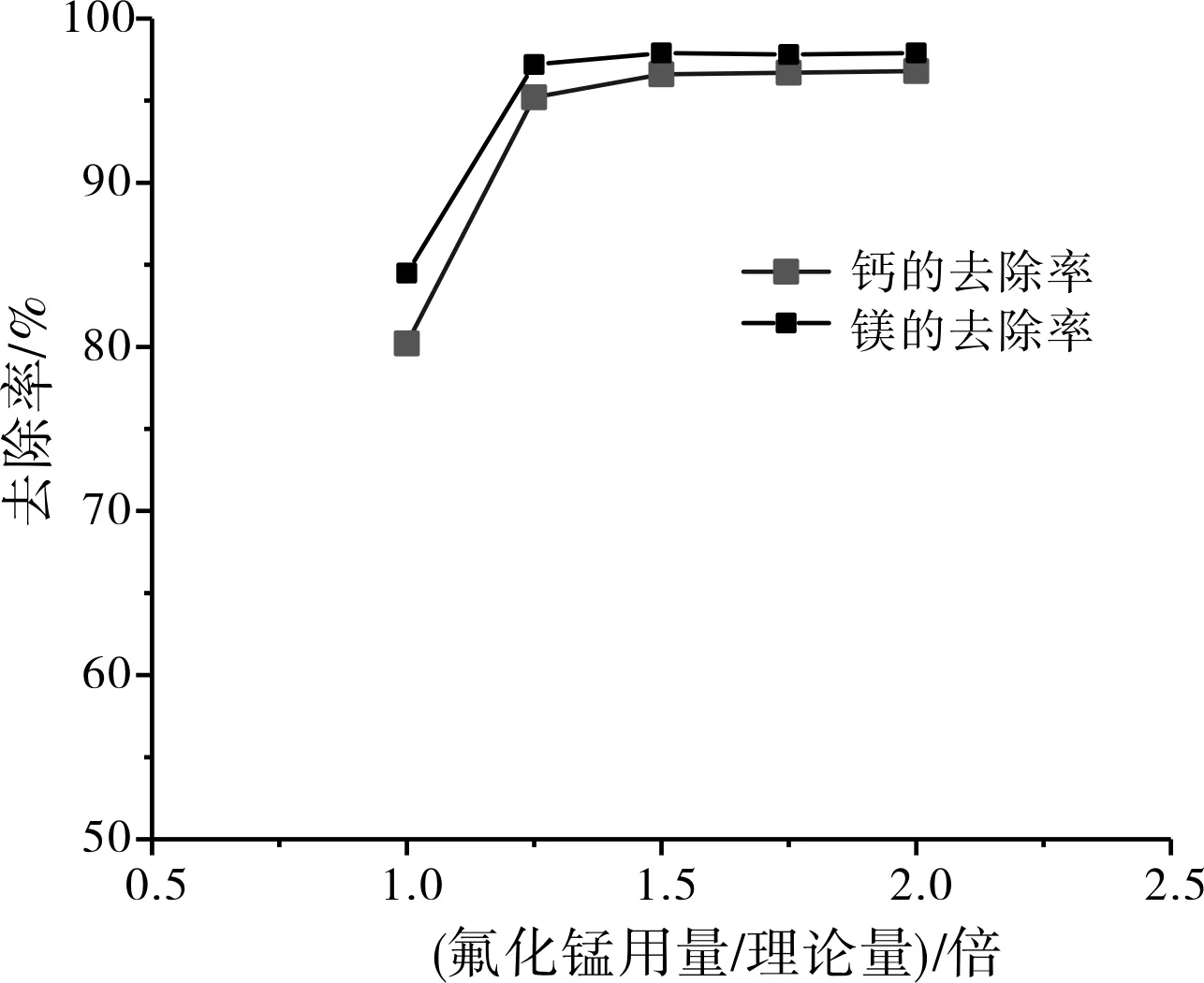
图4 氟化锰的用量对去除钙镁的影响
3.2.2 温度对去除率的影响
在除铁后的溶液中按理论量的1.5倍加入氟化锰,加热,搅拌反应1 h。考查温度对钙镁去除率的影响,结果如图5所示。由图5看出,随着反应温度的增加,钙镁去除率增加。钙镁的沉淀是吸热反应,温度升高利于氟化钙、氟化镁的生成,且温度较高时,氟化钙、氟化镁沉淀的沉降效果较好,利于分离。当温度大于80 ℃之后,钙镁去除率趋于平稳,此时钙、镁离子的去除率分别达到98.8%和97.5%。除钙镁后,浸出液的钙镁含量分别为1.5 mg/L和2.0 mg/L,对萃取影响较小,回收的锰溶液可直接返回流程使用。

图5 温度对去除钙镁的影响
3.3 浸出液中锰的回收
3.3.1 pH对P204萃取锰的影响
浸出液除铁和钙镁等杂质后,用P204萃取回收锰。固定条件:P204皂化率60%,有机相(30%P204+70%磺化煤油),有机相和液相相比Vo/Va=1:1,萃取15 min。考查pH对锰和钴镍的分离效果影响,其结果如图6所示。由图6可以看出,PH越高,萃取剂更易于萃取金属离子,锰钴镍萃取率均逐渐增加,PH>4时,锰萃取率趋于稳定。故最佳PH为4.0,此时锰萃取率为90.2%。
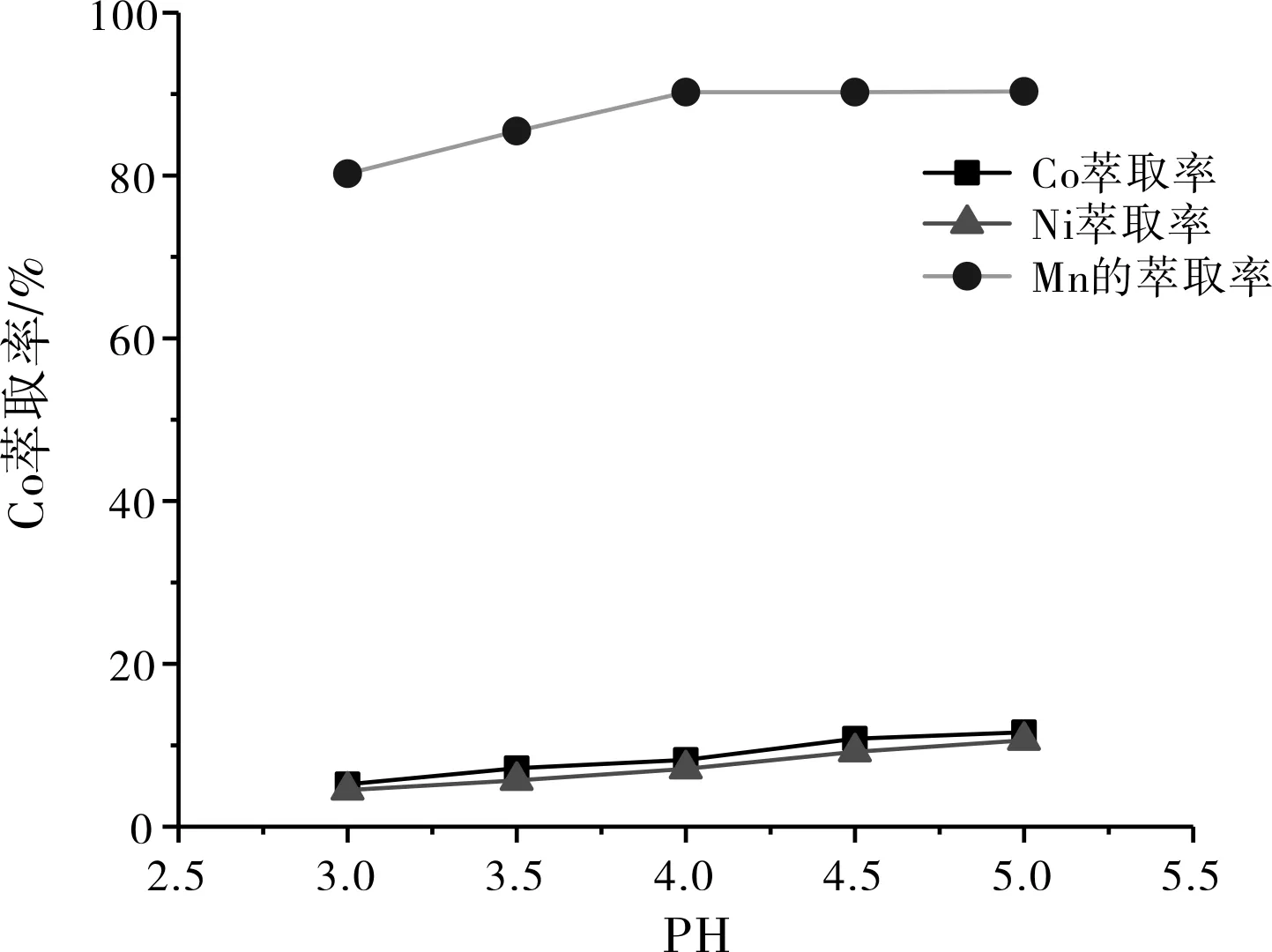
图6 pH对P204萃取锰的影响
3.3.2Vo/Va对P204萃取锰的影响
固定条件:P204皂化率60%,有机相(30%P204+70%磺化煤油),水相pH=4.0,萃取15 min。考查有机相与水相体积比Vo/Va对萃取的影响,结果如图7所示。由图7看出:Vo/Va相比增大,钴、镍萃取率均提高;Vo/Va大于1:2后,Co的萃取率基本不变。综合考虑,确定P204萃取锰时,有机相与水相体积比Vo/Va=1:2,此时锰萃取率为90.3%。
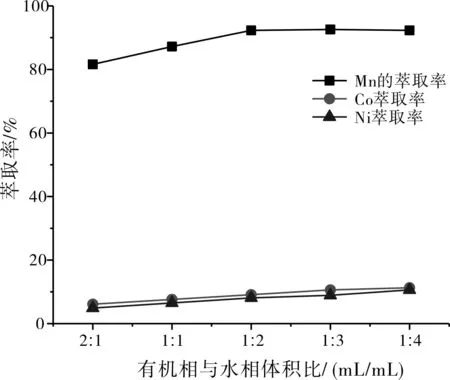
图7 相比对P204萃取锰的影响
3.4 钴镍的分离
3.4.1 pH对P507萃取钴的影响
浸出液除杂,P204萃取锰后,萃余水相继续用P507萃取分离钴镍。固定条件:P507有机相皂化率60%,有机相为30%P507+70%磺化煤油,有机相和与水相体积比Vo/Va=1:1,萃取15 min。考查pH对钴镍分离效果的影响,其结果如 图8所示。由图8可以看出,随pH增加,钴、镍萃取率均增加了,pH大于5.0后,钴的萃取率增加缓慢。综合考虑,确定P507萃取钴时水相pH以5为宜,此时钴萃取率为86.8%。

图8 pH对P507萃取钴的影响
3.4.2Vo/Va对P507萃取钴的影响
固定条件:P507有机相皂化率60%,有机相为30%P507+70%磺化煤油,水相pH=5,萃取15 min。有机相与水相体积比Vo/Va对萃取的影响试验结果如图9所示。由图9看出:随相比增大,钴、镍萃取率均提高;Vo/Va大于1:3后,Co的萃取率基本不变。综合考虑,P507萃取钴时,有机相与水相体积比Vo/Va=1:3,此时钴萃取率为88.9%。
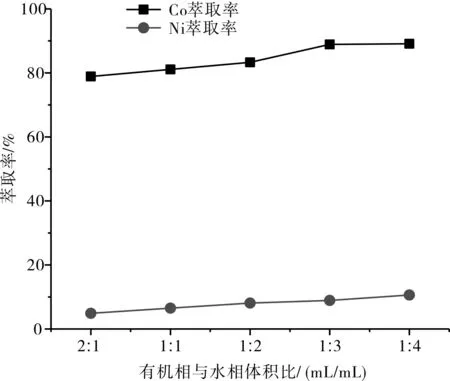
图9 Vo/Va对P507萃取钴的影响
4 结 论
(1)在浸出液pH=3.5、80 ℃、保温1.5 h条件下,铁的去除率可达到98.2%;
(2)在NCa+Mg:NF=1:1.5、80 ℃、搅拌反应1 h条件下,浸出液的钙镁含量分别为1.5 mg/L和2.0 mg/L;
(3)在P204皂化率60%、有机相(30%P204+70%磺化煤油)、水相pH=4.0、萃取时间15 min、相比1:2、锰的萃取率可达到90.3%;
(4)在P507皂化率60%、有机相(30%P507+70%磺化煤油)、水相pH=5、萃取时间15 min。相比=1:3,钴萃取率可达88.9%;
(5)锰、钴、镍回收率分别为90.3%、81.0%和80.5%,实现了浸出液中有价金属分离回收。
