霸王花药材的质量标准研究Δ
2022-07-29廖万忠蒋伟哲周贤强刘雪萍付书婕广西医科大学药学院南宁5300广西卫生职业技术学院医学基础部南宁53003
廖万忠,蒋伟哲,刘 微,周贤强,刘雪萍,付书婕#(.广西医科大学药学院,南宁 5300;.广西卫生职业技术学院医学基础部,南宁 53003)
霸王花为仙人掌科植物量天尺Hylocereus undatus(Haw.)Britt.et Rose 的干燥花,又名霸王鞭、三棱箭、剑花、龙骨花等,始载于《岭南采药录》。该药味甘、性微寒,常生长于海拔3~300 m处,在世界各地均有广泛栽培,于1645年引入我国,现被广泛种植于我国广东、广西、福建、海南等地[1]。霸王花具有润肺止咳、祛痰平喘、润肠通便、抑菌、抗氧化、提高免疫力等功效,主治咳嗽、支气管炎、肺炎、肺结核、便秘等疾病[2-4];此外,因富含多种人体必需氨基酸、植物纤维及微量元素等营养物质,霸王花又被广泛用作蔬菜食用[5]。相关研究表明,该药的活性成分主要为黄酮、多糖和皂苷等成分[6-8],其中山柰酚、异鼠李素等黄酮类成分对呼吸道疾病具有较好的治疗作用[9-10]。因此,结合霸王花的主要功效,上述黄酮类成分可作为定性定量指标以控制霸王花质量。目前,国家药材标准尚未收载霸王花,《中国植物志》第52卷、《中药大辞典》下册等中药典籍虽有收载,但仅有药材来源和性状鉴别,缺少显微鉴别、薄层鉴别、含量测定等相关质量控制内容。为此,本研究拟对15批霸王花药材进行性状、显微、薄层色谱(thin-layer chromatography,TLC)鉴别,测定其水分、总灰分、酸不溶性灰分、水溶性浸出物、醇溶性浸出物,并对其中山柰酚、异鼠李素进行含量测定,旨在建立霸王花药材的质量标准,为有效控制其药材质量提供理论依据。
1 材料
1.1 主要仪器
本研究所用主要仪器有LC-20AT 型高效液相色谱仪(日本Shimadzu 公司),101-3SB 型电热恒温干燥箱(绍兴市苏珀仪器有限公司),GMP3-10 型程控马弗炉(杭州卓驰仪器有限公司),KS-500DB 型数控超声清洗器(昆山洁力美超声仪器有限公司)等。
1.2 主要药品与试剂
异鼠李素对照品(批号110860-202012,纯度99.10%)购自中国食品药品检定研究院,山柰酚对照品(批号RP200312,纯度99.83%)购自成都麦德生科技有限公司;霸王花对照药材(批号290111-202107)购自江西佰草源生物科技有限公司;4%醋酸钠硅胶G 薄层板购自青岛海洋化工有限公司;甲醇(色谱纯)购自美国Merck公司,乙腈(色谱纯)购自天津市光复精细化工研究所,磷酸(分析纯)购自烟台市双化工有限公司,其余试剂均为分析纯,水为超纯水。
霸王花药材(编号S1~S15,具体来源信息见表1)均购自广西、广东,经广西中医药大学瑶医药学院谢阳姣研究员鉴定均为仙人掌科植物量天尺H.undatus(Haw.)Britt.et Rose 的干燥花。上述药材经粉碎后过3号筛,置于干燥箱中,备用。

表1 15批霸王花药材的来源信息
2 方法与结果
2.1 性状鉴别
本品为棕褐色或黄棕色干燥花,呈不规则的长条束状,长15~25 cm;萼管细长部扭曲呈条束状,但基部仍相连接;花外侧覆盖有皱缩的鳞片,内侧着生多数雄蕊,花丝线形,花药扁平呈黄白色;上端花被呈狭长披针形,有纵脉,往往数轮连在一起;气微,味稍甜。结果见图1。

图1 霸王花药材(编号S7)性状鉴别图
2.2 显微鉴别
按照2020 年版《中国药典》(四部)通则“2001 显微鉴别法”项下方法,取药材粉末(编号S7)适量,制片后观察[11]。本品粉末呈棕绿色或棕黄色;花粉粒呈黄色,类球形,直径18~26 μm,表面有颗粒状雕纹,具3 个萌发孔;非腺毛为单细胞,甚长,多弯曲;粉末中可见导管、薄壁细胞。结果见图2。

图2 霸王花药材粉末显微鉴别图
2.3 TLC鉴别
精密称取药材粉末1 g,加石油醚(60~90 ℃)20 mL,回流(水浴温度为80 ℃,下同)提取30 min;弃去石油醚液,药渣挥干后加甲醇25 mL,再回流提取30 min;滤过,取滤液15 mL与4 mol/L稀盐酸5 mL混合,回流提取15 min;滤过,得回流液;取回流液10 mL,浓缩至3 mL,加水15 mL,转入分液漏斗,用乙酸乙酯20 mL萃取2 次,合并乙酸乙酯层,蒸干,残渣加甲醇2 mL 溶解,即得供试品溶液。取对照药材粉末适量,同法制得对照药材溶液。另取山柰酚、异鼠李素对照品适量,用甲醇分别制成0.2 mg/mL山柰酚对照品溶液和0.1 mg/mL异鼠李素对照品溶液。按照2020年版《中国药典》(四部)通则“0502 TLC 法”项下方法操作[11]。吸取上述供试品溶液、对照药材溶液、对照品溶液各2 μL,分别点于同一4%醋酸钠硅胶G 薄层板上,以甲苯-甲酸乙酯-甲酸(10∶5∶1,V/V/V)溶液为展开剂展开;取出,晾干,喷以1%三氯化铝乙醇溶液,热风吹干至斑点清晰,然后在紫外灯(波长365 nm)下检视。结果显示,供试品色谱中,在与对照品和对照药材色谱相应位置上,显相同颜色的荧光斑点,且分离度较好。结果见图3。

图3 霸王花药材TLC图
2.4 水分、灰分、浸出物检测
2.4.1 水分 取各批次霸王花药材粉末,按照2020年版《中国药典》(四部)通则“0832 水分测定法”项下“第二法(烘干法)”进行检测[11]。每批样本平行测定3次,取平均值(表2)。结果显示,15批霸王花药材水分为10.70%~12.23%,平均值为11.44%。南方气候较为润湿,且15批药材水分最高值为12.23%,结合储藏过程中对水分控制的要求[12],拟定霸王花药材的水分不得过13.0%。
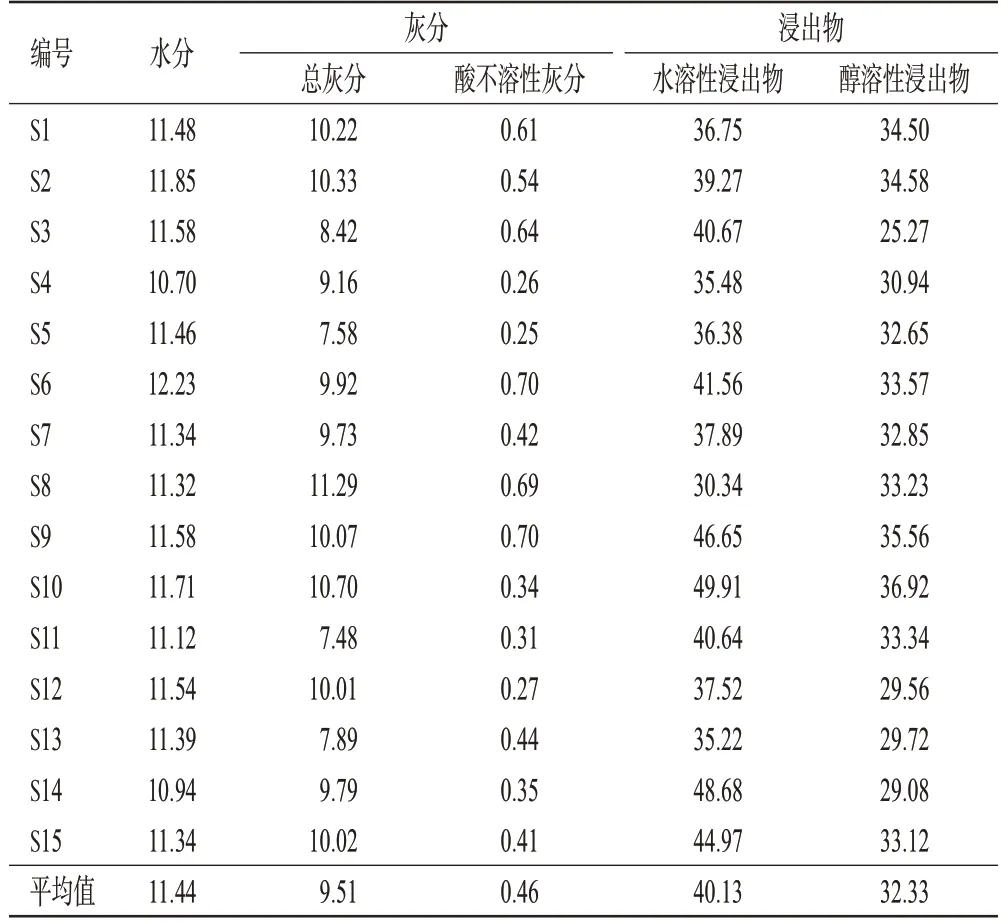
表2 霸王花药材中水分、灰分、浸出物测定结果(n=3,%)
2.4.2 灰分 取各批次霸王花药材粉末,按照2020年版《中国药典》(四部)通则“2302 灰分测定法”项下“总灰分测定法”和“酸不溶性灰分测定法”进行检测[11]。每批样本平行测定3次,取平均值(表2)。结果显示,15批霸王花药材总灰分为7.48%~11.29%,平均值为9.51%;酸不溶性灰分为0.25%~0.70%,平均值为0.46%。以平均值上浮20%为标准[13],拟定霸王花药材的总灰分不得过12.0%;酸不溶性灰分因实测值较小,暂不作限度要求。
2.4.3 浸出物 取各批次霸王花药材粉末,按照2020年版《中国药典》(四部)通则“2201 浸出物测定法”项下“水溶性浸出物(热浸法)”和“醇溶性浸出物测定法(热浸法)”进行检测,后者所用溶剂为60%乙醇[11]。每批样本平行测定3次,取平均值(表2)。结果显示,15批霸王花药材水溶性浸出物为30.34%~49.91%,平均值为40.13%;醇溶性浸出物为25.27%~36.92%,平均值为32.33%。以平均值下调20%为标准[13],结合15 批药材浸出物测得量,拟定水溶性浸出物不得少于30.0%,醇溶性浸出物不得少于25.0%。
2.5 含量测定
2.5.1 混合对照品溶液的制备 精密称取山柰酚、异鼠李素对照品适量,加甲醇制成上述2个成分质量浓度分别为100.356、58.730 μg/mL的混合对照品溶液。
2.5.2 供试品溶液的制备 精密称取药材粉末0.5 g,置于100 mL 锥形瓶中,加甲醇20 mL、4 moL/L 稀盐酸5 mL,称定质量,80 ℃加热回流提取1 h,放冷至室温,再次称定质量,用甲醇补足减失的质量,摇匀,用0.45 μm微孔滤膜滤过,取续滤液,即得。
2.5.3 色谱条件及系统适用性试验 以Xtimate C18(250 mm×4.6 mm,5 μm)为色谱柱,以甲醇-0.4%磷酸溶液(53∶47,V/V)为流动相;检测波长为362 nm;流速为1.0 mL/min;柱温为30 ℃;进样量为10 μL。分别取供试品溶液(编号S7)、混合对照品溶液和空白溶液[甲醇-4 mol/L稀盐酸(4∶1,V/V)],按上述色谱条件进样测定,记录色谱图(图4)。结果显示,各待测成分色谱峰与相邻色谱峰的分离度良好,理论板数均不低于3 000,且空白溶液对待测成分的测定无干扰,表明该方法的专属性较好。

图4 山柰酚和异鼠李素系统适用性试验的高效液相色谱图
2.5.4 线性关系考察 精密吸取“2.5.1”项下混合对照品溶液1、2、3、4、5 mL,用甲醇稀释至10 mL,得各稀释液。取混合对照品溶液和上述各稀释液适量,按“2.5.3”项下色谱条件进样测定,记录峰面积。以待测成分质量浓度为横坐标(x)、峰面积为纵坐标(y)绘制标准曲线,计算得山柰酚和异鼠李素的线性回归方程、相关系数(r)和线性范围(表3)。结果显示,各成分在其检测质量浓度范围内与峰面积的线性关系良好(r>0.999)。
2.5.5 检测限与定量限考察 取“2.5.1”项下混合对照品溶液适量,用甲醇逐步稀释,然后按“2.5.3”项下色谱条件进样测定,记录峰面积。分别以信噪比3∶1、10∶1计算山柰酚和异鼠李素的检测限、定量限(表3)。结果显示,山柰酚和异鼠李素的检测限和定量限均满足定量检测要求[11]。

表3 山柰酚和异鼠李素的回归方程、相关系数、线性范围、检测限和定量限
2.5.6 精密度试验 精密吸取“2.5.1”项下混合对照品溶液,按“2.5.3”项下色谱条件连续进样测定6次,记录峰面积。结果显示,山柰酚、异鼠李素峰面积RSD 分别为0.56%、0.56%(n=6),表明仪器精密度良好。
2.5.7 稳定性试验 取霸王花药材粉末(编号S7)适量,精密称定,按“2.5.2”项下方法制备供试品溶液,分别于室温下放置0、2、4、6、8、12、24 h时按“2.5.3”项下色谱条件进样测定,记录峰面积。结果显示,山柰酚、异鼠李素峰面积RSD 分别为0.56%、0.64%(n=7),表明供试品溶液在室温下放置24 h内稳定性良好。
2.5.8 重复性试验 取同一批霸王花药材粉末(编号S7)6份,精密称定,按“2.5.2”项下方法制备供试品溶液,再按“2.5.3”项下色谱条件进样测定,记录峰面积并按标准曲线法计算样品含量。结果显示,山柰酚、异鼠李素含量的RSD 分别为0.47%、0.90%(n=6),表明该方法重复性良好。
2.5.9 加样回收率试验 取已知含量的霸王花药材粉末(编号S7)6 份,每份约0.1 g,精密称定,精密加入“2.5.1”项下混合对照品溶液3 mL,按“2.5.2”项下方法制备供试品溶液,再按“2.5.3”项下色谱条件进样测定,记录峰面积并计算加样回收率。结果显示,山柰酚、异鼠李素的平均加样回收率分别为103.63%、98.00%,RSD分别为1.23%、1.15%(n=6),表明本方法的准确度良好。结果见表4。
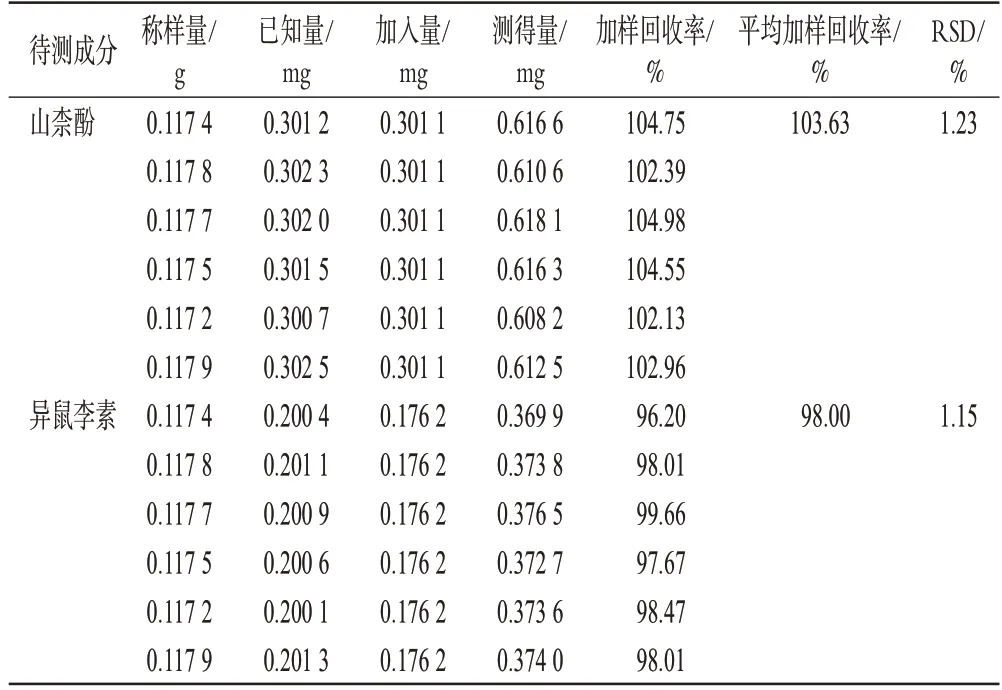
表4 山柰酚和异鼠李素的加样回收率试验结果(n=6)
2.5.10 样品含量测定 取15 批霸王花药材粉末,每份约0.5 g,精密称定,按“2.5.2”项下方法制备供试品溶液,再按“2.5.3”项下色谱条件进样测定,记录峰面积并按标准曲线法计算样品含量。每批样品平行测定3次,取平均值(表5)。结果显示,15批霸王花样品中山柰酚和异鼠李素含量分别为1.787~3.785、0.597~2.211 mg/g。因不同产地含量差异较大,故以含量最低值设限[14],即按干燥品计算,初步拟定霸王花药材中山柰酚和异鼠李素含量分别不得少于1.780、0.590 mg/g。

表5 15批霸王花药材中山柰酚和异鼠李素的含量测定结果(n=3,mg/g)
3 讨论
3.1 定性和定量分析指标的选择
现有研究表明,霸王花药材中含有丰富的黄酮类成分,如山柰酚、异鼠李素、槲皮素等[15]。山柰酚具有润肺止咳、抗炎、抗氧化、抗肿瘤和防治动脉粥样硬化的作用[16-17];异鼠李素具有抗支气管炎、抗氧化、抗肿瘤和降血压等作用[10,18]。山柰酚和异鼠李素的药理作用与霸王花润肺止咳、抗氧化的药用功效相似,提示这2个成分可能是该药的有效成分。因此,本研究选择山柰酚和异鼠李素作为霸王花药材定性和定量分析的指标成分。
3.2 TLC鉴别条件的选择
在TLC鉴别条件的选择中,本课题组考察了超声提取法与回流提取法对鉴别结果的影响,结果显示,超声提取法所得供试品溶液的杂质斑点多,主斑点不明显,故选择回流提取法;本课题组考察了不同薄层板对鉴别结果的影响,结果显示,山柰酚、异鼠李素与其他组分在硅胶G 薄层板中难以有效分离,而选择4%醋酸钠硅胶G 薄层板则可得到理想的分离效果;本课题组参考文献[19-20],考察了三氯甲烷-乙酸乙酯-甲酸(10∶3∶1,V/V/V)、正己烷-甲酸甲酯-甲酸(8∶4∶1,V/V/V)、石油醚-三氯甲烷-甲酸乙酯-甲酸(2∶10∶3∶1,V/V/V)、甲苯-甲酸乙酯-甲酸(10∶5∶1,V/V/V)等不同展开剂对鉴别结果的影响,最终选择了斑点清晰、圆整、分离度高、重复性好的甲苯-甲酸乙酯-甲酸(10∶5∶1,V/V/V)作为展开剂。
3.3 高效液相色谱条件和供试品溶液制备条件的选择
在高效液相色谱条件的优化研究中,本课题组通过将对照品溶液和供试品溶液于200~600 nm波长范围内进行光谱扫描,筛选出山柰酚、异鼠李素的最大吸收波长(362 nm)。本课题组对流动相组成(甲醇-水、甲醇-0.4%磷酸溶液、乙腈-水、乙腈-0.4%磷酸溶液)、甲醇-0.4%磷酸溶液比例(50∶50、53∶47、55∶45,V/V)、流速(0.8、1.0、1.2 mL/min)等色谱条件进行了考察,对比各成分分离度及基线平稳情况,最终选定“2.5.3”项下色谱条件。此外,本课题组还考察了样品提取方式(超声提取、回流提取)、提取溶剂(甲醇、水)、盐酸浓度(1、2、3、4、5 moL/L)等供试品溶液的制备条件[21],最终选择了待测成分色谱峰峰形对称无拖尾、杂质峰种类少且响应较弱的“2.5.2”项下供试品溶液制备条件。
3.4 样品含量测定结果分析
本研究表明,不同省份、同一省份不同产地之间的霸王花药材成分含量差异较大:广西6个产地样品中山柰酚的含量为1.902~2.809 mg/g,异鼠李素的含量为0.804~1.444 mg/g;广东9 个产地样品山柰酚的含量为1.787~3.785 mg/g,异鼠李素的含量为0.597~2.211 mg/g。这可能是因为药材产地地理位置、气候环境和采收时间等不同,导致指标成分的动态累积含量不同以及部分化学成分有所差异,加上此类药材体积较大、部位较多,使得样品采集不均一,最终导致各地样品成分含量差异较大。
综上所述,本研究对霸王花药材进行了定性鉴别和水分、灰分、浸出物测定,并对其中山柰酚、异鼠李素的含量进行测定,初步拟定了各指标的限度标准,为该药材的质量控制提供了参考方案,有利于推动其资源的开发与应用。但本研究收集的霸王花药材来源局限于广西、广东两地,为更加科学有效地完善其药材质量标准,本课题组今后将对更多产地的霸王花药材进行研究。
