水相法合成ZIF-8纳米颗粒及其水溶液中柚皮素的吸附性能*
2022-07-28袁思婧盛盈颖车金鑫陶能国陈秀梅
袁思婧, 盛盈颖, 车金鑫, 陶能国, 陈秀梅,2
(1. 湘潭大学 化工学院,湖南 湘潭 411105; 2. 湘潭大学 化工学院工程与技术博士后流动站,湖南 湘潭 411005)
0 引言
柚皮素是一种黄酮类化合物,广泛存在于化橘红、枳实、桃叶等天然植物中,已被证明具有抗炎[1]、抗动脉粥样硬化[2]和抗糖尿病[3]的潜能.目前,柚皮素的提取方法主要有酸水解法、超临界CO2萃取法和酶水解法[4]等.与这些方式相比,吸附法具有方便、能耗低、对温度和压力使用范围要求低等特点,具有很强的竞争力和可行性.
金属有机骨架材料(Metals-Organic Frameworks,MOF)是一种具有超高比表面积、孔结构可调、多功能的微孔材料[5].ZIF(Zeolitic Imidazolate Framework)系列材料是MOF重要的一个分支,广泛应用于吸附、储气、催化等领域[6],具有孔结构规则、比表面积大、热稳定性和化学稳定性好、结构和功能多样等特点[7].Son等[8]利用ZIF-8和ZIF-67吸附去除化合物硫芥子(使用2-氯乙基硫模拟),发现97%的2-氯乙基硫(2.5 mg/mL)在25 ℃下于9∶1(v/v)的水/乙醇溶液中在1 min内迅速被ZIF-8和ZIF-67吸附.Denning等[9]使用ZIF-8和ZIF-67将水和甲烷系统中的水转化为水合物的转化率分别从4.5%提高到85.6%和87.7%,从而使其储气量分别提高了14.4和14.7倍.ZIF-8用于柚皮素的提取具有材料合成工艺简单、吸附能耗低等优点,是一种提取柚皮素的潜在吸附剂.然而,目前关于ZIF-8对柚皮素吸附性能的研究较少.通常情况下,ZIF-8是由有机配体和金属离子在N, N-二甲基甲酰胺[10]、甲醇[11-13]等有机溶剂中合成,但使用有机溶剂作为合成介质会对环境产生潜在不利影响.
本文采用水相合成法制备了沸石咪唑酯骨架-8(ZIF-8),在室温下将六水合硝酸锌与2-甲基咪唑在超纯水中搅拌,并加入TEA对其进行改良,经混合、离心、干燥后得到ZIF-8样品(如图1所示).使用超纯水代替有机溶剂作为合成ZIF-8的介质,但这会导致有机配体浓度较高[14-16],增加制备成本.所以在合成介质中引入了碱性去质子试剂,有效地降低有机配体的浓度[17].将制备的ZIF-8应用于柚皮素的吸附和提取,分析了不同TEA加入量、不同原料、不同干扰物质、不同pH值条件下ZIF-8对水溶液中柚皮素吸附量的变化.通过吸附动力学和吸附热力学实验,探究了对柚皮素的吸附性能.此外,还考察了ZIF-8的重复使用性.这些研究结果为ZIF-8在柚皮素提取中的应用提供了理论依据.
1 实验材料和方法
1.1 材料试剂
六水合硝酸锌(Zn(NO3)2·6H2O,纯度99%),科密欧化学试剂有限公司;2-甲基咪唑(2-Hmim,纯度99%),麦克林生化科技有限公司;三乙胺(TEA,纯度99.5%)和柚皮素(纯度97%),阿拉丁生化科技股份有限公司;无水乙醇(纯度99.7%)、盐酸(HCl)和氢氧化钠(NaOH),湖南汇鸿药业有限公司.使用Milli-Q净水系统获得超纯水.其他所有试剂均为分析纯,无需进一步提纯即可使用.
1.2 ZIF-8样品的制备
分别加入2.95 g Zn(NO3)2·6H2O和6.5 g 2-Hmim到含200 mL的超纯水中.两种溶液在室温下磁力搅拌40 min后,用超纯水重复洗涤离心(9 000 r/min,12 min),并在60 ℃烘箱中干燥12 h得到ZIF-8样品,记为Y0.
添加TEA的ZIF-8样品是根据文献[18]制备的,具体制备条件略有修改.分别加入2.95 g Zn(NO3)2·6H2O和6.5 g 2-Hmim到含200 mL的超纯水中.分别将4 mL、5 mL、10 mL、15 mL和20 mL的TEA加入到2-Hmim溶液中,依次记为Y1、Y2、Y3、Y4和Y5.两种溶液在室温下磁力搅拌40 min后,用超纯水重复洗涤离心(9 000 r/min,12 min),并在60 ℃烘箱中干燥12 h.
1.3 表征方法
用扫描电子显微镜(SEM,Zeiss Sigma 300)观察ZIF-8样品的形貌.通过粉末X射线衍射仪(XRD,德国布鲁克仪器公司)测定ZIF-8样品的结晶度和晶体结构.使用傅立叶变换红外光谱仪(FTIR,美国尼高力仪器公司)采集400 ~ 4 000 cm-1的红外光谱图.通过热重法(TGA,1600HT,梅特勒-托利多集团)分析ZIF-8样品的热稳定性.采用气体吸附分析仪(美国,麦克默瑞提克仪器公司)测定ZIF-8样品的比表面积.紫外分光光度计(UV,日本岛津公司)测定柚皮素含量.
1.4 吸附实验
通过一系列吸附实验,考察了不同吸附剂类型、吸附剂添加量、溶液初始pH值、干扰物、吸附时间、吸附温度等因素对ZIF-8吸附柚皮素的影响.一般情况下,将10 mg的ZIF-8加入50 mL的柚皮素溶液中,然后在室温25 ℃下磁力搅拌1 h.用0.5 mol/L的盐酸和/或0.5 mol/L的NaOH溶液调节溶液pH值.吸附过程达到平衡后,用紫外分光光度计测定溶液中柚皮素的残留浓度.吸附量以qe(mg/g)表示,并用式 (1) 计算:
(1)
式中:C0为柚皮素溶液的初始浓度,mg/L;Ce为柚皮素溶液的吸附平衡浓度,mg/L;V为吸附实验中溶液的体积,L;m为ZIF-8样品的质量,g.
1.5 重复利用性实验
在25 mg/L柚皮素溶液中加入10 mg ZIF-8,室温下振荡1 h使ZIF-8充分吸附柚皮素.用80%的乙醇溶液解吸1 h,60 ℃的烤箱中烘干.将上述吸附-解吸步骤重复5次.
1.6 数据处理
所有实验均进行三次重复,采用Excel 2010进行实验数据统计,采用Origin(Pro 9.0)软件对实验参数和结果进行拟合分析及作图.
2 结果与讨论
2.1 表征
图2为不同TEA添加量条件下合成的ZIF-8系列样品的扫描电镜(SEM)图.从图2(a)和图2(b)可以看出,TEA用量较低时,在水溶液中不能合成完整的ZIF-8颗粒.当TEA的添加量增加到5 mL时,如图2(c)所示,从SEM图像中可以观察到ZIF-8颗粒的菱形十二面体结构,这说明制备ZIF-8颗粒所需TEA的最小用量为5 mL.当TEA体积从5 mL增加到20 mL(如图2(c~j)所示),样品的平均粒径从343 nm减小到124 nm.SEM结果表明,TEA的引入能显著促进水相中ZIF-8晶粒的形成,减小ZIF-8的粒径.这是因为ZIF-8晶体是由2-甲基咪唑中的-N与六水合硝酸锌中的Zn2+结合形成,而超纯水属于质子性溶剂,能提供质子与2-甲基咪唑中的-N形成N-H键,与Zn2+竞争.而在高TEA添加量的条件下,2-Hmim的快速去质子化使有机配体产生更多的反应位点,易与离子配合,加速与Zn2+的化学反应,从而合成小粒径的ZIF-8颗粒,提高水相合成中ZIF-8结晶度.
图3(a)为ZIF-8系列样品的BET比表面积以及孔径分布图3(b)情况图.可以看出ZIF-8系列样品曲线均为典型的Ⅰ类等温线,这说明所合成的样品均为微孔材料.ZIF-8系列样品的BET数据如表1所示,样品Y0(未添加TEA)的比表面积和孔容明显小于其他样品,而孔径明显大于其他样品,这说明合成样品的过程中添加TEA能明显改善ZIF-8的骨架结构.
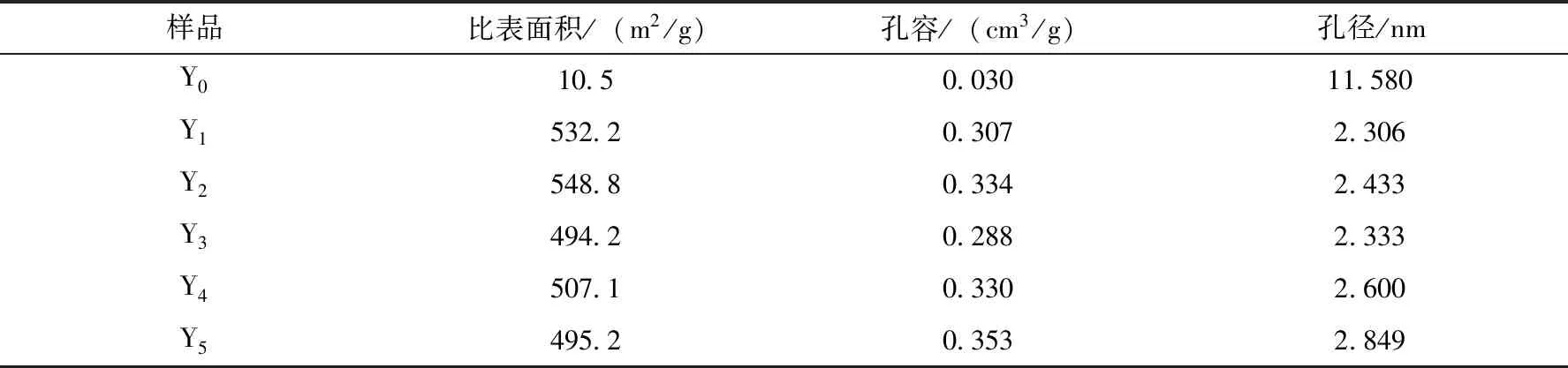
表1 ZIF-8系列样品的比表面积、孔容及孔径大小Tab.1 The surface area, pore volume and pore size of ZIF-8 with different addition of TEA
图4(a)为ZIF-8系列样品的X射线衍射(XRD)图.如图所示,样品Y0在(011)、(002)、(112)、(022)和(031)晶面的ZIF-8特征峰缺失,而样品Y1在(011)、(002)、(112)和(222)晶面上出现了ZIF-8的特征峰,这说明在超纯水中不能合成理想的ZIF-8颗粒,需要添加TEA来促进ZIF-8的合成,但在样品Y1中也观察到了杂质峰,说明仅加入4 mL的TEA不足以形成纯ZIF-8颗粒.当TEA体积分别增加到5 mL、10 mL、15 mL和20 mL时,可以清楚地看到样品Y2、Y3、Y4和Y5的XRD图谱与根据ZIF-8的理论结构模拟的XRD图谱趋于一致.结果与之前报道的ZIF-8结构相同[19].XRD的表征结果说明在水相合成法合成ZIF-8的过程中,TEA的加入改善了ZIF-8的晶体结构.这可能是因为超纯水中含有大量的质子,TEA的加入促进了溶液中的去质子化,得到了结晶度较高的ZIF-8颗粒.图4(b)为ZIF-8系列样品的红外光谱(FTIR)图.由图可以看出,ZIF-8样品在3 134 cm-1和2 930 cm-1处出现了咪唑单元和甲基的C-H伸缩振动特征峰;在1 585 cm-1处出现的峰与C=N的伸缩振动有关;在1 145和997 cm-1处出现的峰与C-N的伸缩振动有关;在422 cm-1处出现的峰为Zn-N的伸缩振动所产生.所得光谱与之前报道的ZIF-8光谱一致[20].XRD和FTIR检测结果进一步表明,在超纯水中加入TEA改良,能成功地合成较纯的ZIF-8纳米颗粒.图4(c)为ZIF-8系列样品的热重分析(TGA)曲线.从图中可以看出,在温度为260 ℃时,样品Y0和Y1发生了严重的失重现象,失重率约为10%,而其他样品的失重现象随着温度由30 ℃升至900 ℃而逐渐明显.说明低TEA添加量(0 mL、4 mL)合成的ZIF-8稳定性较差,这与图2中SEM图像呈现的趋势一致.通过计算失重曲线的导数来验证样品的热稳定性.图4(d)中ZIF-8样品的三个峰代表了样品失重的三个阶段.第一个峰出现在93 ℃,这可能与水分子的蒸发有关;第二个峰出现在259 ℃,这可能是由于ZIF-8样品中多余的2-Hmim挥发所致;第三次失重发生在600 ℃,这主要是由于ZIF-8骨架的分解[21-22].上述结果表明样品Y2、Y3、Y4和Y5在600 ℃内具有相对良好的热稳定性.
2.2 吸附实验
2.2.1 吸附性能为了研究不同TEA添加量制备的ZIF-8对柚皮素吸附效果的影响,分别用样品Y0、Y1、Y2、Y3、Y4和Y5吸附柚皮素,吸附时间为1 h.结果如图5(a)所示,添加TEA改良的ZIF-8样品对TEA吸附柚皮素的能力均优于原始ZIF-8(Y0).在TEA添加量为0 ~ 20 mL的范围内,随着TEA添加量的增加,ZIF-8对柚皮素的吸附量呈现出先增大后减小的趋势.当用TEA添加量为10 mL(Y3)时,样品的吸附量达到最大为132 mg/g.因此,后续的吸附实验都以样品Y3为吸附剂进行.
图5(b)为pH对样品Y3吸附柚皮素的影响.结果如图所示,当pH为3 ~ 6时,柚皮素吸附量随着pH的升高而增加;当pH为6 ~ 9时,柚皮素吸附量随着pH的升高而减小;但吸附量始终保持在57 ~ 64 mg/g内,这说明Y3具有良好的稳定性.后续选择在pH为5的条件下进行实验.
在吸附反应的接触时间为0 ~ 120 min的范围内,研究了样品Y3对柚皮素的吸附动力学.动力学拟合结果如图5(c)所示,Y3的吸附动力学曲线迅速上升.说明Y3对柚皮素的吸附过程在20 min内达到平衡,吸附率qt为102 mg/g.用动力学模型对实验数据进行拟合,拟一级动力学(2)、拟二级动力学(3)和颗粒内扩散(4)方程如下.
In(qe-q)=In(qe-k1t),
(2)
(3)
,
(4)
式中:qe为平衡时Y3对柚皮素的吸附量,mg/g;q为时间t(min)时的吸附量,mg/g;k1、k2和ki分别代表拟一级、拟二级和颗粒内扩散动力学常数.
表2为3种动力学模型拟合得到的各动力学参数,其中拟二级动力学模型 (R2= 0.999)比拟一级动力学模型(R2= 0.994)和颗粒内扩散动力学模型(R2= 0.296)更适合Y3对柚皮素的吸附过程,说明其吸附过程为化学吸附.

表2 Y3对柚皮素的吸附动力学模型参数Tab.2 Kinetic models parameters for adsorption of naringenin on ZIF-8 with Y3 in aqueous solution at 298 K
为了进一步评价Y3与柚皮素吸附位点的相互作用,用Langmuir模型和Freundlich模型对实验数据进行了拟合.模型拟合曲线如图5(d)所示,随着温度从289 K升高到309 K,Y3对柚皮素的吸附量逐渐增大,表明在高温下吸附反应更容易进行.Langmuir等温线模型假设吸附剂以单分子层的形式吸附在吸附质表面,如等式(5)所示.而Freundlich等温线模型假设吸附剂和吸附质之间存在多层吸附,如等式(6)所示.
,
(5)
,
(6)
式中:Ce为达到吸附平衡时柚皮素的浓度,mg/L;qm为Y3对柚皮素的理论最大吸附量,mg/g;kL为Langmuir模型中的常数;n和k分别为Freundlich模型常数和非均型因子经验常数.吸附等温线拟合参数如表3所示.Y3吸附剂表现出典型的Langmuir模型吸附行为,表明Y3对柚皮素的吸附过程为单分子层吸附.在309 K条件下,Y3柚皮素的qm值为867 mg/g.

表3 Y3对柚皮素的吸附等温线参数Tab.3 Isotherm models parameters for adsorption of naringenin on Y3 in aqueous solution
在上述实验数据的基础上,研究了温度(289 K、299 K、309 K)对吸附反应的影响.分配系数(K)由等式(7)计算.吉布斯自由能变化(△G0)、焓变(△H0)和熵变(△S0)分别由方程(7 ~ 9)得到.
(7)
△G0=-RTlnK,
(8)
(9)
式中:K为分配系数;T和R分别代表开尔文温度(K)和理想气体常数(8.314 J/(mol·K)).计算结果如表4所示.△H0为负值,表明Y3对柚皮素的吸附过程是放热反应.△G0为负值,证明此吸附过程可以自发进行.

表4 Y3对柚皮素的吸附热力学参数Tab.4 Thermodynamic paraments for adsorption of naringenin on Y3
2.2.2 干扰实验及可重复利用性为了判断样品Y3对柚皮素的选择性,在溶液中加入干扰物进行吸附实验,包括葡萄糖、CaCl2和KCl.吸附结果如图6(a)所示,在葡萄糖、Ca2+和K2+的干扰下,Y3对柚皮素的吸附量有所下降,但波动范围在10 mg/g以内.图6(b)为样品Y3的再生对其吸附性能的影响.由图可以看出,当重复5次吸附/解吸循环后,Y3对柚皮素的吸附率仍在50%以上,这表明Y3具有较好的重复利用性.
3 结论
本文采用水相合成法,在室温下制备了ZIF-8纳米颗粒.通过表征发现不同TEA的加入可以改善ZIF-8的晶体结构.10 mL TEA改良的ZIF-8为菱形十二面体结构,平均粒径约为166 nm.在合成ZIF-8的过程中加入足够的TEA可以使样品在600 ℃内具有良好的热稳定性.TEA改良的ZIF-8对柚皮素的吸附效果优于未改良的ZIF-8,当TEA用量为10 mL时,样品Y3对柚皮素的吸附效果最好.吸附动力学研究表明,Y3对柚皮素的吸附过程符合拟二级动力学模型,表明在柚皮素的吸附过程中化学吸附占主导地位.等温吸附结果表明,Y3对柚皮素的吸附过程符合Langmuir模型,表明Y3对柚皮素的吸附为单层吸附,理论最大吸附量为867 mg/g,并在Y3的再生实验中发现Y3具有良好的重复使用性.
