肥胖指标和甘油三酯对中老年人群糖代谢异常的预测价值
2022-07-28欧阳凌云张文龙
叶 鹏,陈 霞,魏 东,刘 雅,郑 莉,欧阳凌云,张文龙
(成都市第二人民医院 a.内分泌科, b.全科医学科,四川 成都610017)
随着经济发展和生活方式的改变,糖尿病的患病率逐年上升。最新的一项流行病学调查显示,2015~2017年中国成年人糖尿病和糖尿病前期的患病率分别为12.8%和35.2%[1]。大约3亿人处于糖尿病前期,发展为糖尿病的风险明显增加,而对糖尿病前期进行干预可降低糖尿病发病风险[2]。约一半的糖尿病患者没有被及时诊断[1],从而增加糖尿病并发症的发生风险。75%~80%的糖尿病患者最终会患上心血管疾病,糖尿病前期患者心脏病发作和中风的风险也明显升高[3,4]。由此可见,对于糖代谢异常患者的早发现、早预防尤为重要。据调查,成都地区中老年体检人群超重、肥胖和中心性肥胖普遍流行[5]。体质指数(body mass index,BMI)、腰围(waist circumference,WC)、腰臀比(waist-to-hip ratio,WHR)、腰高比(waist-to-height ratio,WHtR)是衡量超重、肥胖和中心性肥胖的常用指标。然而不同研究比较BMI、WC、WHR、WHtR与糖尿病或糖尿病前期相关性的结果并不一致[6~11],尚需进一步研究。甘油三酯(TG)与胰岛素抵抗密切相关。脂质蓄积指数(lipid accumulation product,LAP)结合了腰围和甘油三酯,在多个研究中证实是一个较好的识别糖代谢异常的指标[12,13]。但是在两项随访6年的研究中,LAP预测糖尿病的能力与WC、WHR、WHtR相似[14,15]。糖尿病已成为我国一个重大公共卫生问题,早期识别糖代谢异常高危人群十分重要,有助于早期预防。本研究是一项10年回顾性队列研究,旨在确定这些与肥胖相关的指标是否能预测糖代谢异常,寻找简便易行的指标。
1 资料与方法
1.1 一般资料2018年1~2月收集了四川省成都市大邑县蔡场社区的常住人口291例。纳入标准:①曾参与2008年成都“十一五”科技规划重大专项“城乡杜区常见多发慢性病防治”项目[16];②2008年糖代谢正常;③50~89岁。排除标准:①2008年诊断为糖尿病或糖尿病前期;②长期使用激素、恶性肿瘤、严重心脑血管疾病、严重肝肾功能不全、代谢性手术、截肢;③基线资料缺失较多。④未采血或不愿配合。根据世界卫生组织1999年标准,糖代谢正常定义为空腹血糖<6.1 mmol/L,且75 g葡萄糖耐量试验2 h血糖<7.8 mmol/L。本研究经过本院伦理委员会批准,受试者均签署知情同意书。
1.2 方法调查形式和内容与2008年保持一致,测量身高、体重、腰围、臀围、血压。采集空腹静脉血,采用全自动生化分析仪检测空腹血糖、餐后2h血糖、总胆固醇(TC)、TG、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)、血尿酸。2018年尚未诊断糖尿病的受试者需行75 g葡萄糖耐量试验。两位研究者独立完成受试者身份信息对比,收集2008年资料。LAP男性=(WC-65)×TG,LAP女性=(WC-58)×TG。糖代谢异常定义为空腹血糖≥6.1 mmol/L或糖耐量2 h血糖≥7.8 mmol/L,包括2018年以前已诊断糖尿病并进行药物治疗的受试者。根据中国肥胖问题工作组标准[17],BMI≥24 kg/m2为超重或肥胖;男性WC≥85 cm或WHR≥0.90,女性WC≥80 cm或WHR≥0.85,或WHtR≥0.5[8]为中心性肥胖。高TG血症定义为TG≥1.7 mmol/L。
1.3 统计学方法采用SPSS 20.0统计软件进行数据分析。计量资料以均数±标准差表示,首先进行正态性检验,若不符合正态分布则采用自然对数转换为正态分布资料。组间比较采用独立样本t检验,前后比较采用配对样本t检验。计数资料采用率描述,比较采用卡方检验。采用多因素Logistic回归校正混杂因素,分别计算不同指标糖代谢异常发病风险的比值比。采用MedCalc 12.7统计软件计算受试者工作特征(ROC)曲线,计算灵敏度、特异度及曲线下的面积(AUC)。不同ROC曲线下面积的比较采用DeLong′s检验。P<0.05为差异有统计学意义。
2 结果
2.1 患者的一般资料、肥胖指标及实验室检测指标
2018年调查时共发现92例受试者存在糖代谢异常(糖代谢异常组),其余199例为糖代谢正常组。糖代谢异常组中男38例,女54例,糖尿病前期63例,糖尿病29例。糖代谢正常组男77例,女122例。两组一般资料、肥胖指标及实验室检测指标见表1。
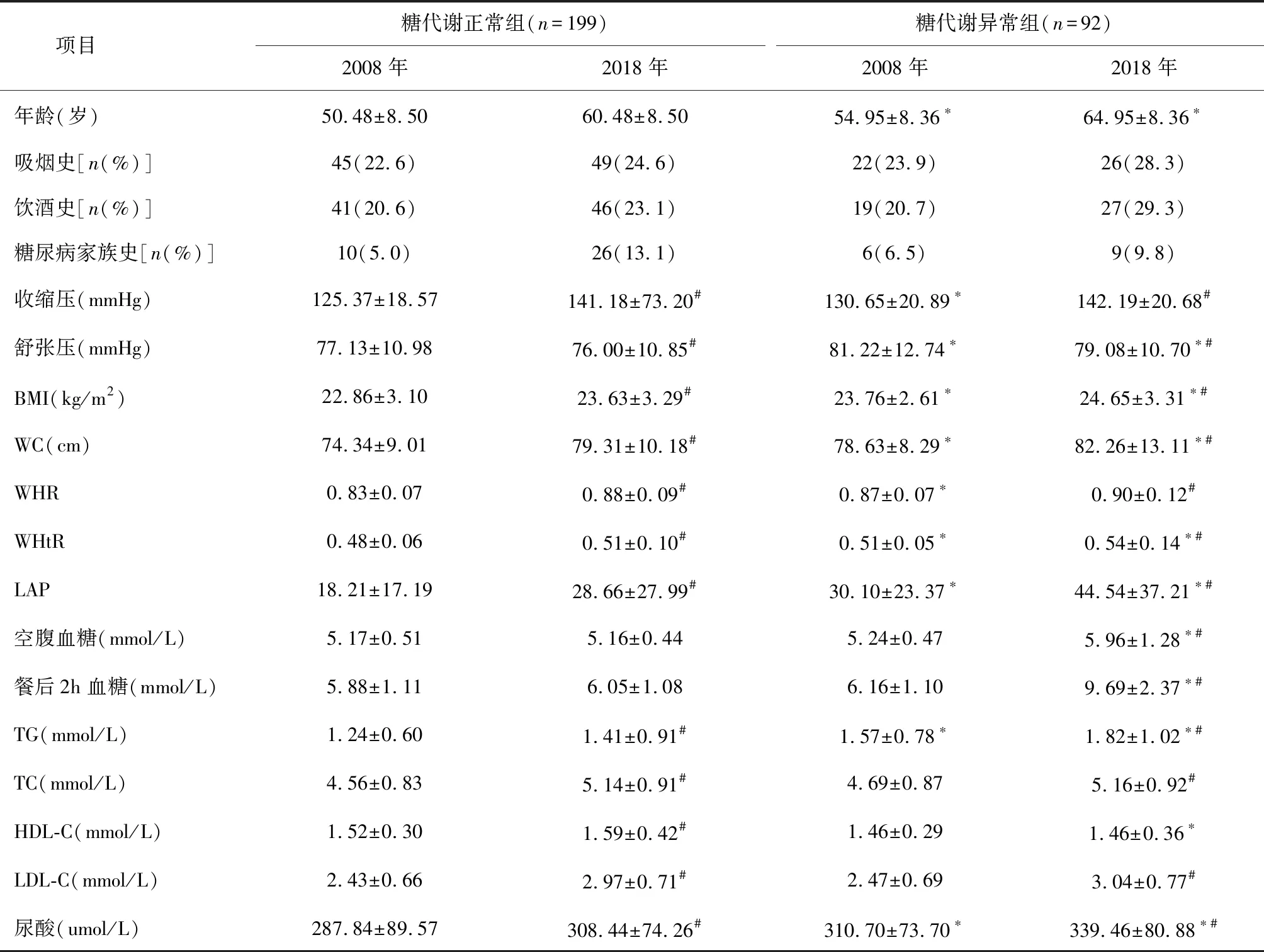
表1 患者的一般资料、肥胖指标及实验室检测指标
2.2 肥胖指标与TG对糖代谢异常发生风险的影响多因素Logstic回归发现,校正年龄、性别、糖尿病家族史、血糖、血压、血尿酸后,WC、WHR、WHtR每增加1标准差,10年后发生糖代谢异常的风险分别增加42.9%,40.9%,49.1%,差异有统计学意义(P<0.05)。由于TG、LAP不呈正态分布,根据三分位数将其分为三组,与下三分位组相比,TG和LAP上三分位组发生糖代谢异常的风险明显增加(P<0.05)。以正常指标为参照,中心性肥胖及高TG血症均增加10年后糖代谢异常发生风险(P<0.05)。见表2。

表2 肥胖指标及TG与糖代谢异常的多因素Logstic回归分析结果
2.3 肥胖指标与TG预测糖代谢异常的ROC分析
BMI、WC、WHR、WHtR、TG、LAP均可预测10年后糖代谢异常发生(P<0.05),其中LAP的ROC曲线下面积最大,WHtR次之,BMI最小。DeLong′s检验发现,LAP及WHtR预测糖代谢异常的能力明显高于BMI(P=0.020,P=0.033)。WC、WHtR、WHtR、TG、LAP预测糖代谢异常的能力比较,差异无统计学意义(P>0.05)。无论是男性还是女性,BMI的ROC曲线下面积均最小,男性WHtR曲线下面积最大,而女性LAP曲线下面积最大。见表3。
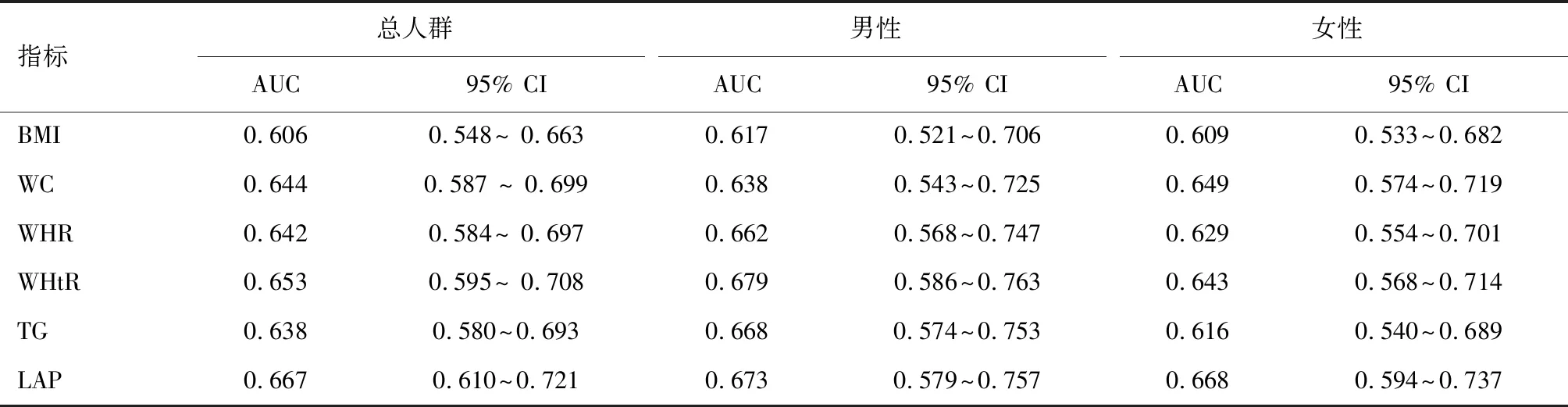
表3 肥胖指标与TG预测10年后糖代谢异常的ROC分析
2.4 肥胖指标联合高甘油三酯血症预测糖代谢异常的价值以超重、中心性肥胖作为切点联合高TG血症(TG≥1.7 mmol/L)预测糖代谢异常的的特异度均达到90%以上。见表4。

表4 肥胖指标联合TG增高预测糖代谢异常的特异度、灵敏度 (%)
3 讨论
近年多个糖尿病流行病学调查发现,糖尿病的患病率逐年升高,已成为严重的社会经济负担。本研究人群为成都地区的农村人群,研究显示糖代谢异常的10年累积发病率达31.6%,其中糖尿病前期占21.6%,糖尿病占10.0%。随着年龄增加和生活方式的改变,受试者的肥胖指标和TG均较10年前增加。糖代谢异常组的肥胖指标和TG较糖代谢正常组增加,而这种差异在10年前已经存在。因此对于高危人群的早期筛查和干预十分重要。
本研究发现,BMI、WC、WHR、WHtR均是糖代谢异常的预测因子,其中WHtR预测能力较强,BMI预测能力最弱。与我们的研究相似,一项针对四川人群的前瞻性研究发现,BMI、WC、WHR、WHtR可以提前3年预测糖代谢异常的发生,其中WHtR的预测能力最强[6]。Lawal等[18]和Xu等[7]研究也发现,WHtR较BMI、WC、WHR预测糖代谢异常的能力更强。也有研究与本研究不一致。一项针对皮马印第安人的前瞻性研究发现BMI和WHtR都是糖尿病的最佳预测指标[11]。Chei等[9]对日本人的队列研究发现,BMI、WC、WHtR仅在女性中是糖尿病的预测指标。这些研究提示不同肥胖指标在不同种族、性别和地区之间预测糖代谢异常的能力有所不同。
众多研究提示,TG是糖代谢异常的独立危险因素。本研究也发现,即使在校正混杂因素后,TG仍然是糖代谢异常的独立危险因素,预测糖代谢异常的能力与BMI、WC、WHR、WHtR相似。传统的肥胖指标无法准确地反映内脏脂肪的积累,而LAP联合了WC和TG,更能反应内脏脂肪积累和胰岛素抵抗。研究发现LAP可以有效识别糖代谢异常[19,20]。本研究和Wang等[14]的研究也发现,随着LAP增高,糖尿病和糖尿病前期的发病风险成倍增加。本研究还发现,LAP可以预测糖代谢异常的发生,优于BMI,但与WC、WHR、WHtR无统计学差异。安徽的一项研究显示,LAP与空腹血糖受损风险增高有关,优于BMI,在女性中还优于WC[21]。然而,Wang等针对中国农村人群随访6年的研究显示LAP预测糖尿病的能力与WC相似[14]。这些研究结果均提示LAP可以有效识别或预测糖代谢异常,然而是否优于传统肥胖指标,可能因研究人群、性别和研究设计的不同而不同。
由于LAP的计算较复杂,且缺乏适合中国人群的公认切点值,临床运用较少。因此,我们进一步计算了超重或中心性肥胖联合高TG血症预测糖代谢异常的特异度和灵敏度,结果发现特异度均达到了90%以上,假阳性率低于10%。这提醒我们,对于超重或中心性肥胖患者,如果合并高TG血症,应及早干预,预防糖代谢异常的发生。
本研究是一项随访10年的回顾性队列研究,采用糖耐量诊断糖代谢异常,很好减少因诊断不足带来的偏倚。但是,本研究也存在一些不足。研究人群为成都某社区的中老年人群,可能不能很好的代表广泛的中国人群。由于样本量相对偏小,本研究没有对糖代谢异常的程度进行亚组分析。在性别的亚组分析中,可能是由于样本量减少导致的检验效能不足,中心性肥胖指标预测糖代谢异常的能力较BMI仅有升高的趋势,这需要大样本研究进一步验证。
综上,BMI、WC、WHR、WHtR、TG、LAP均是成都某社区中老年人群糖代谢异常的危险因素和预测因子。中心性肥胖指标的预测能力,尤其是LAP和WHtR,优于BMI。对于超重或中心性肥胖合并高TG血症的患者应定期随访,早期干预,预防糖代谢异常的发生。
