从质量标准复核和审评视角浅析中药配方颗粒标准制定工作(I)
2022-07-21于姗姗刘洪超郭东晓郭衍珩袁炎炎林永强张秋红
于姗姗,刘洪超,郭东晓,郭衍珩,袁炎炎,林永强*,张秋红*
·中药配方颗粒标准制定专栏·
从质量标准复核和审评视角浅析中药配方颗粒标准制定工作(I)
于姗姗1,刘洪超2,郭东晓2,郭衍珩3,袁炎炎4,林永强2*,张秋红1*
1. 济南市食品药品检验检测中心,山东 济南 250102 2. 山东省食品药品检验研究院,国家药监局胶类产品质量评价重点实验室,山东省中药标准创新与质量评价工程实验室,中药配方颗粒共性技术山东省工程研究中心,山东 济南 250101 3. 菏泽市食品药品检验检测研究院,山东 菏泽 274000 4. 淄博市食品药品检验研究院,山东 淄博 255000
中药配方颗粒试点工作结束及质量标准制定技术要求实施后,国家及省级中药配方颗粒标准的制定均取得了阶段性成果。梳理了中药配方颗粒国家标准的研究历程及省级标准的探索研究成果,以山东省中药配方颗粒标准制定过程中的标准复核及审评中遇到的问题为切入点,主要包括药材基原、生产工艺、定性/定量指标成分合理性等问题,挖掘了上述问题产生的具体原因,提出了做好中药配方颗粒源头把控、寻求更加专属经济的检验方法、强化生产全过程质量控制,以及构建以企业为核心、相关各方应合作共享的质量标准制定体系等建议,推动中药配方颗粒标准的制定和完善,以期促进中药配方颗粒产业的高质量发展。
中药配方颗粒;标准制定;标准复核和审评;问题及对策分析;产业发展
中药配方颗粒是由单味中药饮片经水提、分离、浓缩、干燥、制粒而成的颗粒,在中医药理论指导下,按照中医临床处方调配后,供患者冲服使用[1]。自20世纪60年代至2021年,中药配方颗粒在我国长期处于试点研究阶段,国家对生产企业采取试点生产、从严管控的政策[2-4]。但是,因为中药配方颗粒没有统一的标准,不同企业生产中药配方颗粒时采用的原料药材来源不同,所用溶媒,提取、浓缩、干燥、制粒过程的工艺参数,辅料类型和用量,产品规格及临床折算剂量也不统一,给临床使用的安全性和有效性带来很大的隐患,也给市场监管带来不便,故尽快建立统一的中药配方颗粒质量标准,从而推动中药配方颗粒产业健康快速发展成为重中之重[5]。
1 中药配方颗粒标准制定的发展渊源及现状
1.1 中药配方颗粒国家标准的研究历程
国家药典委员会在中药配方颗粒国家标准制定方面主要分为3个阶段:第1阶段自2001年起,是以企业为主体制定企业标准;第2阶段自2012年8月起,是在国家药典委员会组织下以药检机构为主体制定标准;第3阶段自2016年8月起,是在国家药典委员会引领下以企业为主体制定标准。近年来,国家药品监管部门不断探索国家标准形成机制,让最熟悉产品的生产企业成为标准起草主体,标准管理部门专心做好管理和审评,使中药配方颗粒的标准制定流程更为规范,截至2021年11月1日,国家药品监督管理局分2批共颁布中药配方颗粒国家药品标准196个,其中第一批颁布160个,第二批颁布36个[6-7]。随着国家对中药配方颗粒产业愈加重视,对其质量要求也越来越高,上述196个品种全部收载了鉴别、特征(指纹)图谱、检查、浸出物、(多成分)含量测定等项目,使得其质量控制更加全面。
1.2 中药配方颗粒省级标准的探索与研究
2021年2月1日,国家药品监督管理局、国家中医药管理局、国家卫生健康委员会、国家医疗保障局联合发布《关于结束中药配方颗粒试点工作的公告》(2021年第22号)(以下简称《公告》)[1]。《公告》要求,中药配方颗粒应执行国家标准,国家标准没有规定的,应由省级药监部门自行制定标准。中药配方颗粒省级标准的制定应严格按照《中药配方颗粒质量控制与标准制定技术要求》(以下简称《技术要求》)执行[8]。经过不断地研究及探索,中药配方颗粒省级标准制定工作成绩斐然。山东、四川、陕西、河北、山西等10余个省区市积极出台除国家标准外的中药配方颗粒省级标准的公示稿及颁布件。截至2021年11月,省级中药配方颗粒共公示标准4117个,颁布其中2837个,山东省共分14批公示中药配方颗粒标准243个,分2批颁布其中159个[9-11]。
1.3 中药配方颗粒标准制定的相关流程及关键步骤
中药配方颗粒国家药品标准制定过程中,要经过标准研究起草、生产验证、标准复核、专家审评、公示征求意见、审核、标准颁布等流程。为了保证标准的科学性、重现性和可行性,企业自身起草或委托起草标准草案后,需由药品检验机构或其他具有相应资质的检验机构对制定的标准草案进行验证,以确保标准在后续执行中的适用性[12]。标准复核工作是中药配方颗粒标准制定流程中的重要一环。
2 标准草案常见问题、原因及对策分析
笔者所在项目组承担了山东省中药配方颗粒的标准复核及审评组织工作,本文针对药材基原、生产工艺、定性/定量指标成分合理性等中遇到的问题进行深入探讨及分析。
2.1 药材基原相关问题及建议
2.1.1 原料基原问题 《技术要求》规定,供中药配方颗粒用的中药材原料应固定基原。复核中发现,部分样品与其标示基原不符。如《中国药典》中山楂品种项下共有2种植物来源,分别为山里红Bge. var.N. E. Br.和山楂Bge.。在某企业提供的标示基原为山楂的山楂配方颗粒标准草案中发现,样品使用的药材基原疑似为山里红。后经咨询专家及市场调研,山楂为市场不常见品种。文献报道,我国使用的山楂资源,90%以上来自栽培变种山里红[13],山楂多为野生,分布及数量极少。建议企业广泛查阅文献,赴原产地收集原料,核对药材基原,必要时送检有资质的单位进行分子生物学鉴定,以保证研究用样品的基原准确无误。
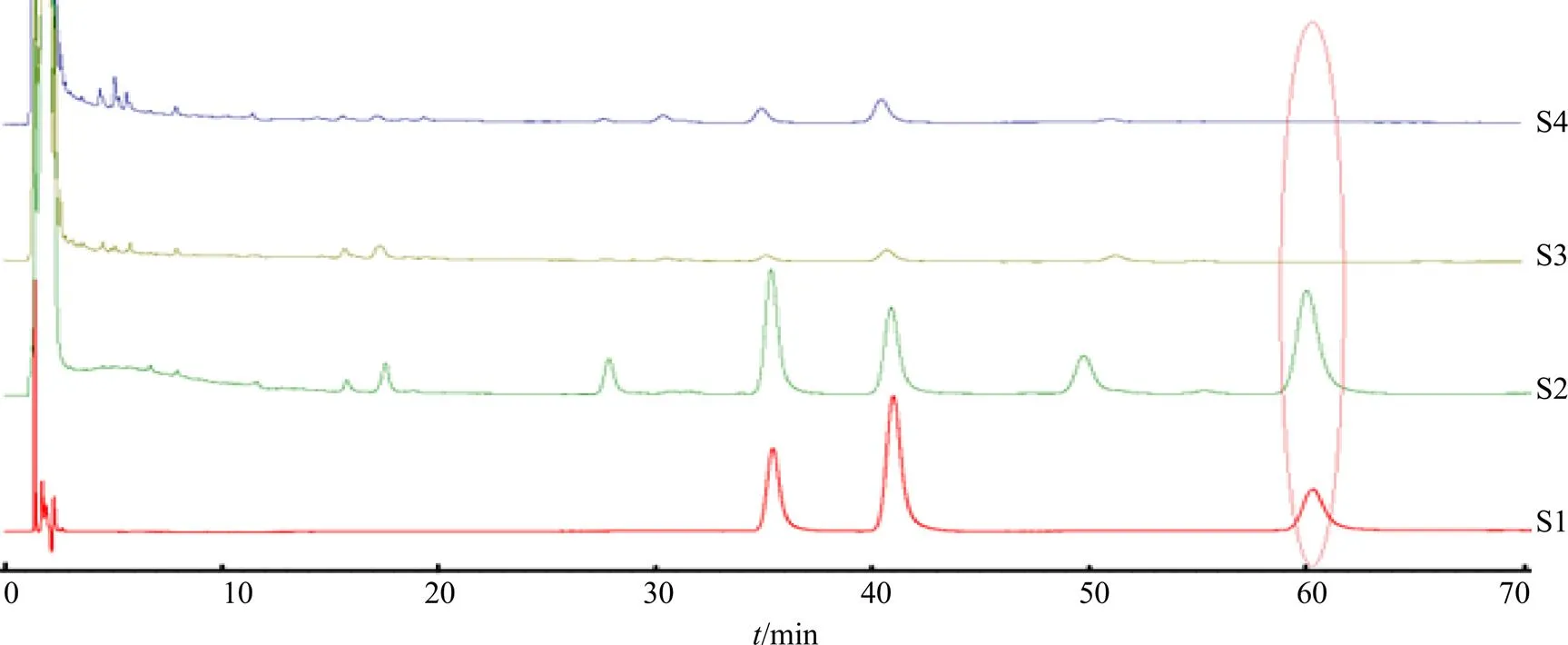
2.1.2 对照药材基原问题 多基原中药材的不同基原间存在成分差异。在标准复核过程中发现,某企业提交的威灵仙(基原为东北铁线莲Rupr.)配方颗粒标准草案中,【特征图谱】项下使用的对照药材为威灵仙Osbeck,导致样品与对照药材色谱行为差异很大。威灵仙(威灵仙)对照药材色谱中,灵仙新苷色谱峰峰面积非常小,而威灵仙(东北铁线莲)配方颗粒样品色谱中的灵仙新苷峰峰面积较大,见图1。

S1-威灵仙(东北铁线莲)配方颗粒 S2-灵仙新苷对照品 S3-威灵仙(威灵仙)对照药材 S4-威灵仙(东北铁线莲)药材
遵循《技术要求》相关规定,供中药配方颗粒生产用中药材原料应固定基原。而不同基原间成分的差异,会导致【特征图谱】项中特征峰不尽相同,作为随行参照物的对照药材,应尽量保证生产与检验间的一致性,从而满足方法适用性的要求。
2.2 生产工艺相关问题及分析
2.2.1 与生产工艺差异相关的性状问题 在穿心莲配方颗粒复核检验过程中,发现收集的不同厂家间的配方颗粒样品颜色差异明显,颜色跨度比较大。A厂家颗粒颜色为灰绿色至褐绿色,B厂家为棕色至棕褐色,C厂家为灰褐色,D厂家为灰黄色至棕褐色(图2)。企业提供的标准草案中,【性状】项下规定:“本品为灰绿色至灰黄色的颗粒”,不能涵盖各厂家样品的颜色范围。因此在颁布标准中,将其【性状】项修订为:“本品为灰绿色至棕褐色颗粒”。
在白扁豆配方颗粒复核检验中,发现标准草案中延续白扁豆药材的部分描述来规定颗粒的味道“嚼之有豆腥气”,但是性状检验中实际口感并无豆腥气。白扁豆药材及饮片嚼之确有豆腥气,但是经过相应工艺处理制成配方颗粒后,豆腥气基本消除。在中药配方颗粒的生产过程中,药材需要经过炮制、提取、分离、浓缩、干燥、成型等诸多工艺环节[14],企业间在原药材质量、生产设备、煎煮时间、滤过方式、浓缩干燥(喷雾干燥、带式干燥、真空干燥等)、辅料使用、制粒成型(湿法制粒、干法制粒等)上差异的影响,容易导致不同企业间产品外观及气味差异。故标准中对气味描述时应重新进行验证,不宜直接沿用相应药材描述。

图2 不同厂家的穿心莲配方颗粒
2.2.2 与生产工艺差异相关的含量测定问题 某企业提供的徐长卿配方颗粒标准草案研究资料中,【含量测定】的指标成分为丹皮酚,规定含丹皮酚(C9H10O3)应为6.0~44.0 mg/g,其样品测定结果为6.9~7.6 mg/g。另一家企业提供的样品,丹皮酚质量分数仅为0.03~0.04 mg/g。两家企业样品中丹皮酚含量差异巨大。
徐长卿药材中富含大量挥发油,研究表明其总挥发油成分中,丹皮酚约占九成[15],在传统处方中,此类饮片通常需要后下。《技术要求》规定,对于中药饮片含挥发油且其传统煎煮需后下的,商业规模生产时可先行提取挥发油,然后按“标准汤剂”中挥发油含量转移率范围,计算所含挥发油量,按比例重新加入。经与生产企业核对工艺,丹皮酚含量测定结果较低的样品,工艺中均缺少“先行提取挥发油,后按比例加入”的步骤,故建议企业在中药配方颗粒生产工艺研究过程中,应以标准汤剂为对照,以主要成分含量的一致性为考察指标,对原料、中间体及成品制备过程中的量质传递进行全面研究,制定合适的生产工艺,最大限度实现配方颗粒与饮片的功效一致化。
2.3 定性/定量指标成分的合理性探讨
2.3.1 定性指标与《中国药典》不一致的问题 某企业提供的蜜远志配方颗粒标准草案中,【鉴别】项同时采用远志酮III对照品和远志对照药材作为对照。但是项目组在复核中发现,薄层色谱中,远志酮III对照品的斑点不清晰,样品色谱中,在与远志酮III对照品相应的位置,斑点亦不清晰,且附近有干扰。《中国药典》2015年版远志的【薄层鉴别】项曾采用远志酮III对照品作为对照,而《中国药典》2020年版,相应项目已经修订为使用远志对照药材作为对照,删除了远志酮III对照品作为对照[16-17],应当是对《中国药典》2015年版方法验证和优化后进行了完善。
《中国药典》作为国家药品标准,标准的研究、起草、修订复核及审定工作工程中贯彻“四个最严”的要求,所选择的分析方法兼顾科学性、先进性、实用性[18],应当是中药配方颗粒标准起草及制定过程选择分析方法及测定指标的首选依据。在配方颗粒标准起草过程中,选择检验方法时应密切关注《中国药典》修订所带来的方法改进及调整。
2.3.2 【含量测定】项所选指标成分的合理性探讨 企业提供的大腹皮配方颗粒标准草案中,【含量测定】项的测定指标为计算去甲槟榔次碱、槟榔次碱、槟榔碱的总量。对不同企业提供的大腹皮配方颗粒样品进行复核检验,发现其他企业样品中槟榔碱目标峰缺失(图3)。
田莲超等[19]采用高效液相色谱法测定了大腹皮(槟榔果皮)及槟榔种子中4种生物碱(槟榔碱、去甲槟榔碱、槟榔次碱、去甲槟榔次碱)的含量,结果发现,大腹皮以槟榔次碱为主,几乎不含槟榔碱,建议通过测定槟榔次碱和去甲槟榔次碱的总量来控制大腹皮的质量。古桂花等[20]考察了不同烘烤时间和不同煮沸时间条件下,大腹皮中3种生物碱(槟榔碱、槟榔次碱、去甲基槟榔次碱)含量的变化,测定结果显示槟榔碱易溶于水且性质不稳定,可被碱水解,又易随水蒸气挥发,生物碱的含量随煎煮时间的延长而降低,煮沸0.5 h后损失率高达80%。选取槟榔碱作为定量指标,其合理性值得商榷。
S1-混合对照品溶液 S2-A厂家 S3-B厂家 S4-C厂家
Fig. 3 HPLC chromatogram of Dafupi formula granules
3 对中药配方颗粒标准制定的思考与展望
中药配方颗粒作为在中药饮片基础上进一步加工制成的颗粒,其标准化是整个产业进步的需求。在《技术要求》的指导下,高起点、高质量制定统一的配方颗粒标准,可以带动中药全行业的进步。为做好中药配方颗粒国家及省级标准的制定,更好地控制产品质量,提出以下几点看法。
3.1 固定药材基原、产地及相关炮制方法,做好药材源头把控
《技术要求》中规定,供中药配方颗粒生产用中药材原料应固定基原、采收时间、加工方法、药用部位等。这就要求强化中药质量源头管理,加强质量管理规范基地建设,实现中药材种植养殖规范化;采收加工环节应结合“道地药材”概念与可溯源的要求,探索建立与规范化种植/养殖基地相配套的产地加工中心,建立、完善中药材生产与产地加工技术规范[3],细化贵细药材等特殊类别中药材的加工处理标准,如趁鲜切制、直接干燥、发汗、煮后干燥、炙制等[21-23],实现从田间地头到生产车间的全程化管理,从源头上确保药材基原准确无误、质量安全可控、炮制方法科学合理,保障中药配方颗粒质量的一致性和稳定性。
3.2 持续进行【特征图谱】项的研究,致力寻求更加专属、经济的检验方法
特征图谱是选取供试品图谱中某些重要的特征信息,与对照药材的特征峰信息进行比对,同时选用一个或多个对照品进行定位,利用相对保留时间法对多个目标成分进行识别判断。特征图谱作为控制中药质量的重要鉴别手段,可实现同时对中成药、中药材中大量化学成分信息的提取、识别及量化[24],在已颁布的中药配方颗粒国家标准中,绝大部分均采用了特征图谱作为鉴别手段[25]。
但是,有些品种的【特征图谱】项存在一些问题:有些采用了专属性差的指标成分,无法评价原料药材的真伪优劣;有些使用的对照物质数量很多,导致检验成本高昂,给生产企业日常检验带来了沉重的经济负担;有些在不同色谱柱和不同色谱仪上重现性差。为了寻求更专属的鉴别方法,可在【特征图谱】项的研究中引入一些新方法,如基于中药质量标志物理论[26-27]提出的化学标识物[28],提高方法专属性,有效保障所用原料药材的真伪。为了有效解决对照品短缺、昂贵、不稳定等问题,可尝试采用新的替代标准物质法[29],如采用“双标线性校正法”[30]来进行特征峰的定位,以提高保留时间预测准确率和色谱柱符合率。
3.3 积极开展顶层规划和基础研究,做好生产全过程质量控制
在中药配方颗粒标准研究过程中,需要以标准汤剂作为研究基础,进行原料药材、中间产品、颗粒成品与“标准汤剂”的比对研究,分别建立相应内控标准,以明确关键质量属性,并说明生产全过程量质传递和各项指标设定的合理性。应以标准汤剂为对照,以干浸膏出膏率、主要质量标志成分的含量转移率、指纹图谱或特征图谱的一致性作为考察指标,在对量质传递和物料平衡进行全面研究的基础上,确定相关工艺参数。在大生产过程中,着重制定生产工艺的标准化程序,设置并固定工艺中饮片的煎煮时间、煎煮次数、料液分离及浓缩、干燥方式、辅料使用、制粒成型等,严格实施标准操作规范,确保产品持续满足质量标准要求。
3.4 构建以企业为核心、相关各方合作共享的质量标准制定体系
自2001年首批6家试点企业开始自主生产中药配方颗粒,到2021年11月1日结束试点放开生产,196个国家标准及山东、四川、陕西等省标准的正式颁布,中间经历了漫长而曲折的过程。这些标准出台前,不同生产企业间存在着原料基原、药材质量、生产工艺、仪器设备、颗粒与饮片折算比、标准控制指标等诸多差异,制约了中药配方颗粒产品质量的提高。制定完善的中药配方颗粒法定标准,能够促进整个中药配方颗粒行业的发展。
《公告》及《技术要求》的实施,标志着我国中药配方颗粒标准制定进入了新的阶段。为了质量标准制定工作更快速高效地推进,应构建以企业为主体的质量标准研究体系,由企业负责研究数据及报送标准的真实、完整、高效,按照质量标准起草的研究技术要求进行品种研究,明确起草什么品种、选择什么基原、用什么检测方法等,并积极向药品监督管理部门报送相关资料;药品检验及第3方检验机构要坚持公平、公正、公开的业务原则,按照质量标准草案的复核技术要求积极承担标准复核工作,给出科学、公正、合理的复核意见及改进措施。相关各方应合作共享,加快中药配方颗粒标准的制定和完善,共同促进中药配方颗粒产业的发展。
利益冲突 所有作者均声明不存在利益冲突
[1] 何军, 朱旭江, 杨平荣, 等. 中药配方颗粒的现状与发展新思路[J]. 中草药, 2018, 49(20): 4717-4725.
[2] 国家药品监督管理局. 国家药监局国家中医药局国家卫生健康委国家医保局关于结束中药配方颗粒试点工作的公告(2021年第22号) [EB/OL]. [2021-02-10]. https://www.nmpa.gov.cn/xxgk/ggtg/qtggtg/20210210145856159.html.
[3] 吴远波, 张鸿, 冷红文, 等. 中药配方颗粒政策发展及其质量标准发展概述 [J]. 江西化工, 2021, 37(4): 27-30.
[4] 鲁萍, 邓勇. 中药配方颗粒行业试点20年政策梳理与优化建议[J]. 中草药, 2022, 53(4): 1277-1284.
[5] 吕朝耕, 康传志, 周良云, 等. 中药配方颗粒标准化研究现状与思路探讨 [J]. 中国现代中药, 2017, 19(6): 748-752.
[6] 国家药品监督管理局. 国家药监局批准颁布第一批中药配方颗粒国家药品标准[EB/OL]. [2021-04-29]. https://www.nmpa.gov.cn/yaowen/ypjgyw/20210429094401110.html.
[7] 国家药品监督管理局. 国家药监局批准颁布第二批中药配方颗粒国家药品标准[EB/OL]. [2021-10-31]. https://www.nmpa.gov.cn/yaopin/ypjgdt/20211031205610177.html.
[8] 国家药品监督管理局.国家药监局关于发布《中药配方颗粒质量控制与标准制定技术要求》的通告(2021年第16号)[EB/OL]. [2021-02-10]. http://www.gov.cn/ zhengce/zhengceku/2021-02/11/content_5586817.html.
[9] 山东省药品监督管理局. 山东省中药配方颗粒标准(第十四批)公示[EB/OL]. [2021-11-29]. http://mpa.shandong. gov.cn/art/2021/11/29/art_101747_10312391.html.
[10] 山东省药品监督管理局. 山东省药品监督管理局关于发布实施《山东省中药配方颗粒标准》(第一批)的公告[EB/OL]. [2021-10-11]. http://mpa.shandong.gov.cn/art/ 2021/10/11/art_101747_10308472.html.
[11] 山东省药品监督管理局. 山东省药品监督管理局关于发布实施《山东省中药配方颗粒标准》(第二批)的公告[EB/OL]. [2021-10-26]. http://mpa.shandong.gov.cn/art/ 2021/10/11/art_101747_10308472.html.
[12] 冯丽. 中药配方颗粒省级标准制定关注要点[N]. 中国医药报, 2021-03-09(003).
[13] 郑伟, 周茗, 王双艳, 等. 不同来源山楂叶化学成分比较分析 [J]. 药学学报, 2021, 56(12): 3526-3539.
[14] 林环玉, 伍振峰, 曾丽华, 等. 中药配方颗粒发展现状及产业升级对策分析 [J]. 中国医药工业杂志, 2018, 49(8): 1161-1165.
[15] 李葆林, 杨梦婷, 支雅婧, 等. 徐长卿化学成分和药理作用的研究进展及质量标志物(Q-Marker)预测分析 [J]. 中草药, 2021, 52(12): 3725-3735.
[16] 中国药典[S]. 一部. 2015: 156-157.
[17] 中国药典[S]. 一部. 2020: 163-164.
[18] 何轶, 翟为民, 倪龙, 等. 中药国家药品标准修订技术要求 [J]. 中国食品药品监管, 2021(9): 40-43.
[19] 田莲超, 秦少荣, 易红, 等. 同源中药大腹皮与槟榔中4种生物碱的含量比较研究 [J]. 中国中药杂志, 2018, 43(14): 2850-2856.
[20] 古桂花, 胡虹, 曾薇, 等. 槟榔不同工艺处理品中3种生物碱的含量比较 [J]. 中国实验方剂学杂志, 2013, 19(4): 44-47.
[21] 李远辉, 伍振峰, 李延年, 等. 基于粉体学性质分析浸膏干燥工艺与中药配方颗粒制粒质量的相关性 [J]. 中草药, 2017, 48(10): 1930-1935.
[22] 易方, 刘会. 黄精“产地加工-炮制一体化”的药材及饮片质量研究 [J]. 湖南中医杂志, 2021, 37(6): 173-177.
[23] 吴红伟, 李东辉, 边甜甜, 等. 基于响应面法结合熵权法多指标优选黄芪药材产地加工炮制一体化工艺 [J]. 中草药, 2021, 52(19): 5854-5861.
[24] 姚令文, 刘燕, 郑笑为, 等. 指纹图谱、特征图谱技术在中药材和中成药中的应用 [J]. 中国新药杂志, 2018, 27(8): 934-939.
[25] 徐玉玲, 雷燕莉, 曾立, 等. 中药配方颗粒品种统一标准的有关问题探讨 [J]. 中草药, 2020, 51(20): 5389-5394.
[26] 刘昌孝, 陈士林, 肖小河, 等. 中药质量标志物(Q-Marker): 中药产品质量控制的新概念[J]. 中草药, 2016, 47(9): 1443-1457.
[27] 刘昌孝. 中药质量标志物(Q-Marker)研究发展的5年回顾 [J]. 中草药, 2021, 52(9): 2511-2518.
[28] 林永强, 林林, 焦阳, 等. 基于Q-Marker理论的化学标识物研究及应用 [J]. 中国药学杂志, 2020, 55(2): 161-166.
[29] 马双成, 王莹, 魏锋. 中药质量控制未来发展方向的思考 [J]. 中国药学杂志, 2021, 56(16): 1273-1281.
[30] 栾永福, 臧远芳, 刘洪超, 等. 基于双标线性校正法的银黄口服液多组分定性分析 [J]. 药物分析杂志, 2021, 41(6): 1091-1099.
Analysis on formulation of standard of traditional Chinese medicine formula granules from perspective of quality standard review and evaluation (Ⅰ)
YU Shan-shan1, LIU Hong-chao2, GUO Dong-xiao2, GUO Yan-heng3, YUAN Yan-yan4, LIN Yong-qiang2, ZHANG Qiu-hong1
1. Jinan Supervision and Inspection Center for Food and Drug Control, Jinan 250102, China 2. Shandong Engineering Research Center for Generic Technologies of Traditional Chinese Medicine Formula Granules, Shandong Engineering Laboratory for Standard Innovation and Quality Evaluation of TCM, NMPA Key Laboratory for Quality Evaluation of Gelatin Product, Shandong Provincial Institute for Food and Drug Control, Jinan 250101, China 3. Heze Institute for Food and Drug Control, Heze 274000, China 4. Zibo Institute for Food and Drug Control, Zibo 255000, China
After the completion of pilot work of traditional Chinese medicine formula granules (TCMFGs) and the implementation of technical requirements for the formulation of quality standards, the formulation of national and provincial standards have achieved milestones. Research process on national standard of TCMFGs and exploration and research results of the provincial standard are summarized in this paper. The entry point is the standard review and problems encountered in the review during the formulation of standard of TCMFGs in Shandong Province, such as raw material of TCM, production process, rationality of qualitative/quantitative index composition, etc. Specific reasons for above problems are excavated in this article, controlling the source of TCMFGs, seeking more exclusive and economic inspection methods, strengthening quality control throughout the production process are also proposed. The establishment of a quality standard formulation system with enterprises as the core and relevant parties should be cooperated and shared, so as to promote the formulation and improvement of the standard of TCMFGs, with a view to promoting the high-quality development of TCMFGs industry.
traditional Chinese medicine formula granules; standard formulation; standard review and evaluation; problem and countermeasure analysis; industrial development
R288
A
0253 - 2670(2022)14 - 4243 - 06
10.7501/j.issn.0253-2670.2022.14.002
2022-01-20
山东省重点研发计划重大科技创新工程项目(2021CXGC010511);山东省重点研发计划项目(2020RKB24001);山东省人文社会科学课题(2021-YYGL-44);山东省食品药品检验研究院平台课题(SDIFDC-KY-1-2021023,SDIFDC-KY-1-2021026)
于姗姗,女,副主任药师,研究方向为中药质量控制与研究。Tel: (0531)55515960 E-mail: yssyb@126.com
林永强,男,主任药师,博士,研究方向为中药质量控制及评价研究。E-mail: 13864067104@163.com
张秋红,主任中药师,硕士,研究方向为中药质量控制与研究。E-mail: zhangqh9886@163.com
[责任编辑 崔艳丽]