基于宏基因组测序的四川麸醋醋醅微生物组和风味形成相关基因分析
2022-07-16刘爱平吴洁王玉婷泽仁德西陈冉邓明琴李琴李建龙敖晓琳陈蓉刘书亮
刘爱平 吴洁 王玉婷 泽仁德西 陈冉 邓明琴 李琴 李建龙 敖晓琳 陈蓉 刘书亮
摘要: 四川麸醋因风味独特而备受消费者青睐,醋醅中微生物组与麸醋的风味密切相关。本研究旨在基于宏基因组测序技术揭示醋醅的微生物组和风味形成相关基因。结果表明,醋醅中的微生物隶属于70个门、885个属和3 168 个种,优势菌包括金山乳杆菌、耐酸乳杆菌、耐热芽孢杆菌和巴氏醋杆菌等。在COG数据库中注释到8 656 个COG功能单元,在KEGG数据库中注释到43个KEGG通路,氨基酸代谢、碳水化合物代谢是醋醅微生物发酵的主要代谢功能。从醋醅样品中检测到223个不同的碳水化合物活性酶,其中糖基转移酶丰度最高(reads数占比为37.09%);各氨基酸代谢途径之间的主要基因、酶存在较大差异;醋醅基因组中包含编码转氨、脱羧和脱氢等作用的基因,具备通过氨基酸代谢形成风味物质的基础。研究结果为阐明四川麸醋醋醅微生物组,揭示风味形成机制提供了参考。
关键词: 四川麸醋; 醋醅; 宏基因组; 微生物组
中图分类号: TS26;S188 + .4 文献标识码: A 文章编号: 1000-4440(2022)03-0806-07
Microbiota and flavor formation-related genes of Sichuan bran vinegar Pei : insights from metagenome
LIU Ai-ping1, WU Jie1, WANG Yu-ting1, ZEREN De-xi1, CHEN Ran1, DENG Ming-qin1, LI Qin1,LI Jian-long1, AO Xiao-lin1, CHEN Rong2, LIU Shu-liang1
(1. College of Food Science, Sichuan Agricultural University, Ya’an 625014, China; 2.Sichuan Baoning Vinegar Co., Ltd., Langzhong 637400, China)
Abstract: Sichuan bran vinegar has unique flavor and is favored by consumers. The microbiota in vinegar Pei is closely related to the flavor of bran vinegar. This study aims to reveal the microbial composition and flavor formation-related genes of vinegar based on metagenomic sequencing technology. The results indicated that the microorganisms in vinegar Pei belonged to 70 phyla, 885 genera, and 3 168 species, and the dominant bacteria included Lactobacillus jinshani , Lactobacillus acetotolerans , Bacillus sporothermodurans , and Acetobacter pasteurianus . 8 656 COG functional units were annotated in the COG database, and 43 KEGG pathways were annotated in the KEGG database. Amino acid metabolism and carbohydrate metabolism were the main metabolic functions of microbial fermentation in vinegar Pei . 223 different carbohydrate-active enzymes were detected, and the abundance of glycosyltransferase was the highest, accounting for 37.09%. The main genes and enzymes in amino acid metabolic pathway were quite different. Genes encoding amino acid aminotransferase, decarboxylation and dehydrogenase were found in vinegar Pei genome, possessing the basis for flavor development through amino acid metabolism. The results provide a reference for elucidating the microbiota and flavor formation mechanism of Sichuan bran vinegar.
Key words: Sichuan bran vinegar; vinegar Pei ; flavor; metagenome; microbiota
食醋是單独或混合使用各种含有淀粉与糖的物料、食用乙醇经微生物发酵酿制而成的液体酸性调味品(GB 2719-2018《食品安全国家标准 食醋》),具有诱人的颜色、风味和功能特性 [1] 。每个国家和地区均有各自独特的食醋产品,如欧美国家以水果为原料生产的果醋和东亚国家以谷物为原料生产的谷物醋 [2] 。食醋酿造在中国已有两千多年的历史,形成了以山西老陈醋、镇江香醋、四川保宁醋、福建永春老醋为代表的中国四大名醋 [3] 。传统食醋酿造主要分为固态发酵和液态发酵两大类,由于前者风味更佳,因此中国食醋酿造多采用固态发酵方式生产 [4-5] 。
保宁醋是四川麸醋的典型代表,而风味是评价麸醋品质的重要指标。随着现代分析技术的发展,基于GC-MS(气相色谱-质谱仪)、GC-O(氣相色谱-嗅闻仪)、氨基酸自动分析仪、高效液相色谱等技术 [6-8] 的食醋风味研究越来越深入。发酵食品的风味形成与发酵过程中微生物的演替息息相关,研究者常采用传统培养法或免培养法与高通量测序技术相结合的方法来研究发酵食醋过程中微生物的动态变化 [9-11] 。宏基因组测序可以系统展示发酵体系的微生物基因组信息,并可辅助开展功能及代谢通路的分析,便于挖掘菌群的生物多样性、群落结构、功能特性及其相互关系 [12-14] 。Lu等 [15] 基于宏基因组和克隆文库分析了乙偶姻合成机制,Wu等 [16] 基于宏基因组测序技术分析了镇江香醋的风味代谢途径,但是目前鲜有关于宏基因组测序技术用于四川麸醋的研究。本研究基于宏基因组测序技术分析了四川麸醋醋醅的微生物组成及其主要代谢通路,并注释其风味形成的功能基因,以期为四川麸醋风味形成机制及品质提升提供理论基础。
1 材料与方法
1.1 四川麸醋醋醅的采样与处理
参考Liu等 [8] 报道的方法进行醋醅采样,随机选择四川保宁醋有限公司一个刚完成发酵的发酵池,在发酵池前、中、后段的上、中、下层共取9个点,取出醋醅充分混匀,通过四分法舍去多余醋醅后,将200 g醋醅样品收集于无菌自封袋中,当天运回实验室(冰盒中保温),于-80 ℃ 保存。称取25 g醋醅置于含有200 ml无菌生理盐水的三角瓶内,低速振荡15 min(100 r/min )后在超净工作台内用无菌的4层纱布过滤,收集滤液,于300 r/min 离心5 min,收集上清液;于10 000 r/min 高速离心5 min,收集沉淀,将沉淀用无菌生理盐水洗涤3次;将所得沉淀分装于1.5 ml 离心管中,于-80 ℃ 保存。
1.2 醋醅总DNA的提取
称取0.5 g醋醅,按照FastDNA土壤试剂盒(FastDNA SPIN Kit for Soil,美国MP Biomedicals公司产品)说明书步骤提取醋醅总DNA,送至上海美吉生物医药科技有限公司进行宏基因组测序。
1.3 生物信息学分析
(1)数据拼接。基于Hiseq原始测序数据,使用fastp软件进行数据质量控制,获得高质量reads。使用Megahit拼接软件对序列进行拼接组装,选择最优组装结果。(2)非冗余基因集的构建。用MetaGene对拼接结果进行开放阅读框(ORF)的预测,用CD-HIT软件进行聚类,用SOAPaligner软件分别将高质量reads与非冗余基因集进行比对(默认参数为95%相似度),统计基因在对应样品中的丰度信息。(3)数据库注释。使用BLASTp将非冗余基因集与NR数据库、eggNOG数据库、KEGG数据库进行比对,完成丰度和功能注释。(4)统计分析和作图。用R软件完成。
以上生物信息学分析均依托美吉生物云平台(www.majorbio.com)。
2 结果与分析
2.1 微生物群落结构
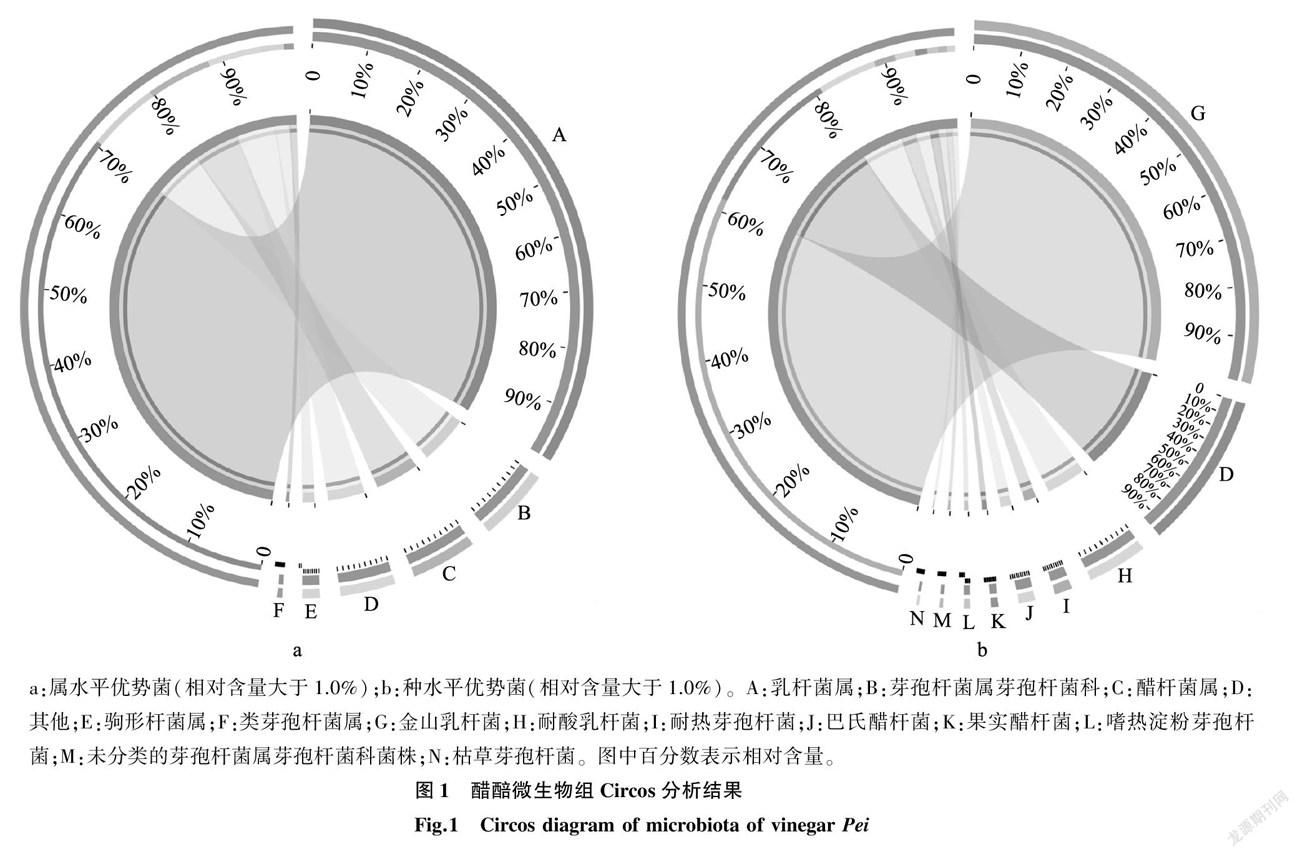
提取醋醅样品基因组,经宏基因组测序和去除低质量数据后,得到醋醅样品的基因组全长为66 379 836 bp,包含101 448 条序列。对醋醅基因组进行物种注释,共鉴定出来自70个门、118个纲、199个目、334个科、885个属和3 168个种的醋醅微生物,其中相对含量大于1%的优势菌群在属、种水平上的数量分别为5个(图1a)、8个(图1b)。
优势菌属包括乳杆菌属、芽孢杆菌属、醋酸杆菌属、驹形杆菌属和类芽孢杆菌属,前三者的相对丰度最高,分别为71.0%、9.3%和8.4%。相对含量大于1.0%的优势菌种包括金山乳杆菌、耐酸乳杆菌、耐热芽孢杆菌、巴氏醋杆菌、果实醋杆菌、嗜热淀粉芽孢杆菌、未分类的芽孢杆菌科芽孢杆菌属菌株和枯草芽孢杆菌,前三者的相对丰度最高,分别为62.0%、7.9%和2.8%。综上可见,乳杆菌是醋醅样品中占比最高的优势菌种,这与聂志强等 [17] 关于天立独流老醋的研究结果类似。
金山乳杆菌是具有异型乳酸发酵特性的革兰氏阳性、兼性厌氧菌株,由Yu等 [18] 首次从镇江香醋固态发酵过程中分离得到,该菌也广泛存在于白酒酿造产物中 [19] 。耐酸乳杆菌是白酒糟醅发酵过程中一种较具优势的菌 [20] ,易从谷物醋中分离得到。巴氏醋杆菌是食醋工业中应用得最广泛的醋酸菌,能够在有氧条件下将乙醇转化为乙酸。
2.2 数据库注释分析
2.2.1 COG数据库注释分析 将测序数据与EggNOG数据库进行比对,获得各基因对应的COG注释概况(图2),共鉴定到8 656 个COG功能单元,这些功能单元分属于23个主要的功能大类。其中基因数排名前10的功能类别是转录,碳水化合物转运和代谢,复制、重组和修复,氨基酸转运和代谢,细胞壁/膜/包膜生物合成,无机离子转运和代谢,能量产生和转换,次级代谢物生物合成,翻译后修饰、蛋白质周转、分子伴侣,辅酶转运和代谢;对应的基因数分别是448个、370个、355个、265个、254个、228个、202个、148个、144个和135个。从测序reads的丰度看,排名前5名的功能类别是未知功能类,复制、重组和修复,氨基酸转运和代谢,翻译、核糖体结构和生物合成,碳水化合物转运和代谢。
2.2.2 KEGG数据库注释分析 由图3可以看出,醋醅中的20 626 032 个reads匹配到KEGG数据库中6类共44个KEGG通路,其中reads最多的10个KEGG通路为碳水化合物代谢、氨基酸代谢、翻译、辅因子和维生素代谢、复制和修复、膜运输、核苷酸代谢、能量代谢、脂质代谢和信号转导。碳水化合物代谢、氨基酸代谢和翻译通路对应的reads数分别为1 717 454 个、1 364 306个 和1 107 840 个。该注释结果中与食醋风味成分形成密切相关的碳水化合物代谢和氨基酸代谢是主要的代谢活动,与COG数据库注释结果相符。四川麸醋醋醅中碳水化合物代谢、氨基酸代谢和翻译通路对应的reads数与Wu等 [16] 关于镇江香醋的研究结果相近,且远高于Wu等 [21] 关于山西老陈醋的报道,但四川麸醋、镇江香醋和山西老陈醋醋醅中碳水化合物代谢和氨基酸代谢对应的reads数占比均最高。
2.2.3 基于CAZy数据库的碳水化合物活性酶分析 碳水化合物是微生物重要的能源和碳源。COG、KEGG数据库注释结果均表明,碳水化合物代謝是醋醅微生物最丰富的功能类别之一。CAZy数据库包含糖苷水解酶( GH )、糖基转移酶( GT )、多糖裂解酶( PL )、碳水化合物酯酶( CE )、碳水化合物结合模块(Carbohydrate binding modules,CBM)和辅助活动模块(Auxiliary activities,AA)共六大类蛋白质家族。本研究从醋醅样品中检测到223个不同的碳水化合物活性酶,其中糖苷水解酶120个,糖基转移酶37个,碳水化合物酯酶14个,辅助活动模块10个,碳水化合物结合模块24个,多糖裂解酶18个。从各类酶的相对丰度看,糖基转移酶最高(reads数为299 206 个,占比37%),其次为糖苷水解酶(占比27%)和碳水化合物酯酶(占比24%)(图4)。食醋的固态发酵首先是将谷物原料转化为可发酵糖供微生物利用,因此碳水化合物活性酶广泛存在于固态发酵过程中。与本研究结果类似,汤涵岚 [22] 的研究结果也表明,食醋大曲中糖苷水解酶对应的基因数最多。
2.2.3.1 糖苷水解酶( GH ) 目前,CAZy数据库中有171个糖苷水解酶家族,醋醅宏基因组中共注释到81个 GH 家族。其中reads数较多的糖苷水解酶家族是GH25(reads数55 664 个,占比25.76%)、GH13(reads数27 232 个,占比12.60%)和GH32(reads数26 648 个,占比12.33%)。GH25具有溶菌酶活性,GH13具有 α -淀粉酶活性、支链淀粉酶活性等,GH32具有转化酶、菊粉内切酶、 β -2,6-果聚糖6-左旋糖化酶活性。
2.2.3.2 糖基转移酶( GI ) 目前,CAZy数据库中有114个糖基转移酶家族,醋醅宏基因组中共注释到37个 GT 家族,其中reads数较多的糖基转移酶家族是GT4(reads数87 924 个,占比37.09%)、GT41(reads数66 842 个,占比28.20%)和GT28(reads数25 994 个,占比10.97%)。GT4具有蔗糖合成酶、蔗糖磷酸合成酶、 α -葡萄糖基转移酶活性,GT41具有5′-二磷酸尿嘧啶核苷(UDP)- N -乙酰葡糖胺:肽 β - N -乙酰氨基葡萄糖转移酶、二磷酸尿苷葡萄糖:肽 N - β -葡萄糖基转移酶等活性,GT28具有1,2-二酰基甘油3- β -半乳糖基转移酶、1,2-二酰基甘油3- β -葡萄糖基转移酶、双半乳糖二酰基甘油合成酶等活性。
2.2.3.3 碳水化合物酯酶( CE ) 目前,CAZy数据库中有19个碳水化合物酯酶家族,醋醅宏基因组中共注释到14个 CE 家族。其中reads数较多的碳水化合物酯酶家族是CE10(reads数86 344 个,占比44.48%)、CE1(reads数45 110 个,占比23.24%)和CE7(reads数24 944 个,占比12.85%)。CE10具有芳酯酶、羧基酯酶、乙酰胆碱酯酶活性,CE1具有乙酰木聚糖酯酶、肉桂酸酯酶、阿魏酸酯酶等活性,CE7具有乙酰木聚糖酯酶、头孢菌素- C 脱乙酰酶活性。
2.2.3.4 碳水化合物结合模块(CBM) 目前,CAZy数据库中有88个碳水化合物结合模块家族,醋醅宏基因组中共注释到24个CBM家族。其中reads数较多的碳水化合物结合模块家族是CBM47(reads数800个,占比25.86%)、CBM32(reads数678个,占比21.91%)和CBM50(reads数550个,占比17.78%)。CBM47具有岩藻糖结合活性,CBM32具有与耶尔森氏菌聚半乳糖醛酸结合的活性,CBM50具有结合GH18、GH19、GH23、GH24、GH25和GH73等的活性。
2.2.3.5 辅助活动模块(AA) 目前,CAZy数据库中有17个辅助活动模块家族,醋醅宏基因组中共注释到7个AA家族。其中reads数较多的辅助活动模块家族是AA1(reads数42 548 个,占比43.56%)、AA3(reads数24 660 个,占比25.25%)和AA6(reads数20 420 个,占比20.91%)。AA1具有漆酶、邻二酚:氧氧化还原酶、铁氧化酶活性,AA3具有纤维二糖脱氢酶、葡萄糖1-氧化酶、芳醇氧化酶等活性,AA6具有1,4-苯醌还原酶活性。
2.2.3.6 多糖裂解酶( PL ) 目前,CAZy数据库中有42个多糖裂解酶家族,醋醅宏基因组中共注释到12个 PL 家族。其中reads数较多的多糖裂解酶家族是PL9(reads数1 060 个,占比41.25%)、PL11(reads数558个,占比21.71%)和PL12(reads数400个,占比15.56%)。PL9具有果胶裂解酶、外聚半乳糖醛酸裂解酶、硫肽聚糖裂解酶活性,PL11具有鼠李糖半乳糖醛酸内切酶、鼠李糖半乳糖醛酸外切酶活性,PL12具有硫酸肝素裂解酶、肝素裂解酶活性。
2.3 食醋风味物质形成的基因分析
四川麸醋富含氨基酸,表1列出了相对丰度排名前3的氨基酸代谢相关基因和酶,可以看出,各氨基酸代谢的主要基因与酶存在较大差异。氨基酸代谢形成风味主要依靠转氨作用,首先在转氨酶的作用下将氨基酸转化为 α -酮酸, α -酮酸再在脱羧酶催化下转化为醛,醛进一步在烟酰胺腺嘌呤二核苷酸脱氢酶( NADH )的辅助下转化为高级杂醇,高级杂醇还会在醇乙酰转移酶的催化作用下发生酯化反应生成乙酸酯类物质 [23] ,这些成分均为食醋中重要的风味成分 [8] 。醋醅基因组中参与转氨途径的酶及其编码基因见表2。醋醅基因组中的转氨酶基因主要包括支链氨基酸转氨酶基因(编号EC2.6.1.42)、天冬氨酸转氨酶基因(编号EC2.6.1.1)和 D -丙氨酸转氨酶基因(编号EC2.6.1.21),三者对应的reads数分别为13 450 个、3 894 个和1 406 个。支链氨基酸转氨酶主要参与缬氨酸、亮氨酸和异亮氨酸的生物合成,天冬氨酸转氨酶主要参与苯丙氨酸代谢, D -丙氨酸转氨酶主要参与 D -精氨酸和 D -鸟氨酸代谢。酮酸主要通过氧化脱羧直接转化为羧酸,依靠酮酸脱氢酶( KaDH )、磷酸转乙酰基酶( PTA )和酰基激酶( ACK ),在醋醅中存在 PTA 的编码基因 pta和ACK 的编码基因 ackA 。同时,醋醅中存在丰富的醛脱氢酶和醇脱氢酶的编码基因,催化醛类、醇类物质转化成相应的醇类、羧酸类物质。因此,四川麸醋醋醅具备以氨基酸为底物形成食醋风味的基础。氨基酸在各类食醋中均有检出,不同类别的食醋可能在氨基酸代谢的基因种类和基因丰度上存在区别。
3 结 论
醋醅中的微生物种类、数量和代谢在很大程度上决定了食醋的风味。本研究随机选择1个工业化生产规模发酵池,取9份发酵成熟的醋醅混合为1个样品进行宏基因组测序。宏基因组测序可揭示样本中存在的所有DNA信息,因此通过对1个成熟醋醅样品的测序即可较全面地揭示发酵体系中与风味形成相关的基因。
本研究结果表明,醋醅中丰度最高的优势菌属是乳杆菌属,占比为71%。氨基酸代谢、碳水化合物代谢是醋醅微生物最旺盛的代谢功能,醋醅样品中检测到大量碳水化合物活性酶和氨基酸转氨、脱羧和脱氢反应的基因,具有形成食醋风味的分子基础。本研究结果可为四川麸醋微生物组及风味形成机制解析提供理论参考,但由于宏基因组更多用于解析微生物潜力,后期可进一步结合宏转录组、代谢组定量分析发酵过程中核心微生物中与风味形成相关基因的表达,更深入揭示食醋风味形成机制。
参考文献:
[1] WU Q, LUO Q, XIAO J S, et al. Catechin-iron as a new inhibitor to control advanced glycation end-products formation during vinegar storage[J]. LWT, 2019, 112: 108245.
[2] 王 敏,沈廣玥,宋 佳,等. 中国谷物醋风味研究进展[J]. 食品科学技术学报, 2021, 39(4): 29-36.
[3] MELINI V, MELINI F. Asian grain-based food products and the European scheme for food protected designations of origin: a critical analysis[J]. Trends in Food Science & Technology, 2019, 91: 83-94.
[4] WU J J, GULLO M, CHEN F S, et al. Diversity of Acetobacter pasteurianus strains isolated from solid-state fermentation of cereal vinegars[J]. Current Microbiology, 2010,60(4): 280-286.
[5] LIU D R, ZHU Y, BEEFTINK R, et al. Chinese vinegar and its solid-state fermentation process[J]. Food Reviews International, 2004, 20(4): 407-424.
[6] 孙宗保,赵杰文,邹小波,等. 镇江香醋特征香气成分加工过程中的变化和形成机理分析[J]. 中国食品学报, 2010, 10(3): 120-127.
[7] 郑 宇,程 程,刘 静,等. 中国传统固态发酵食醋主要特征风味物质组成分析[J]. 中国食品学报, 2020, 20(8): 237-247.
[8] LIU A P, PENG Y, AO X L, et al. Effects of Aspergillus niger biofortification on the microbial community and quality of Baoning vinegar[J]. LWT, 2020, 131: 109728.
[9] 王俊奇,黄卫红,李双彤,等. 永春老醋不同生产阶段细菌和真菌多样性动态变化特征分析[J]. 食品与发酵工业, 2021, 47(2): 38-44.
[10] WU L H, LU Z M, ZHANG X J, et al. Metagenomics reveals flavour metabolic network of cereal vinegar microbiota[J]. Food Microbiology, 2017, 62: 23-31.
[11] WU J J, MA Y K, ZHANG F F, et al. Biodiversity of yeasts, lactic acid bacteria and acetic acid bacteria in the fermentation of ‘Shanxi aged vinegar’, a traditional Chinese vinegar[J]. Food Microbiology, 2012, 30(1): 289-297.
[12] BELLEGGIA L, AQUIANTI L, FERROCINO I, et al. Discovering microbiota and volatile compounds of surstrmming , the traditional Swedish sour herring[J]. Food Microbiology, 2020, 91: 103503.
[13] LI W, HAN Y S, YUAN X, et al. Metagenomic analysis reveals the influences of milk containing antibiotics on the rumen microbes of calves[J]. Archives of Microbiology, 2017, 199(3): 433-443.
[14] 黄祖新. 宏基因组学及其在大曲酒微生物研究中的应用[J]. 酿酒科技, 2009(10): 17-21.
[15] LU Z M, LIU N, WANG L J, et al. Elucidating and regulating the acetoin production role of microbial functional groups in multispecies acetic acid fermentation[J]. Applied and Environmental Microbiology, 2016, 82(19): 5860-5868.
[16] WU L H, LU Z M, ZHANG X J, et al. Metagenomics reveals flavour metabolic network of cereal vinegar microbiota[J]. Food Microbiology, 2017, 62: 23-31.
[17] 聶志强,韩 玥,郑 宇,等. 宏基因组学技术分析传统食醋发酵过程微生物多样性[J]. 食品科学, 2013, 34(15): 198-203.
[18] YU Y J, LI X, ZHANG J H, et al. Lactobacillus jinshani sp. nov., isolated from solid-state vinegar culture of Zhenjiang aromatic vinegar[J]. Antonie van Leeuwenhoek: Journal of Microbiology, 2020, 113(1): 43-54.
[19] 张 媛,廖卫芳,缪礼鸿,等. 采用实时荧光定量PCR法检测白酒酿造系统中的重要功能菌株 Lactobacillus jinshani [J]. 食品与发酵工业, 2021. DOI: 10.13995/j. cnki. 11-1802/ts. 027843.
[20] 张 霞,郑 佳,赵 东,等. 多粮浓香型白酒中特征酵母菌与耐酸乳杆菌的关系[J]. 微生物学通报, 2019, 46(7): 1571-1581.
[21] WU Y F, XIA M L, ZHANG X F, et al. Unraveling the metabolic network of organic acids in solid-state fermentation of Chinese cereal vinegar[J]. Food Science & Nutrition, 2021, 9(8): 4375-4384.
[22] 汤涵岚. 基于宏基因组分析增温对食醋大曲固态发酵过程中微生物菌群的影响[D]. 广州:华南理工大学, 2019.
[23] 解春芝. 基于氨基酸代谢的腐乳酱风味促熟及机理研究[D]. 贵阳:贵州大学, 2019.
(责任编辑:徐 艳)
收稿日期:2021-10-27
基金项目:四川省科技厅重点研发项目(2020YFN0133、2019YFN0112)
作者简介:刘爱平(1986-),男,湖北荆州人,博士,副教授,主要从事食品微生物研究。(E-mail)aipliu@sicau.edu.cn
通讯作者:刘书亮,(E-mail)lsliang999@163.com
