解毒定痛方对骨转移瘤放疗爆发痛患者疼痛程度的影响
2022-07-13王志芳
王 苗,张 楠,马 芹,张 亮,王志芳,张 萌
(河北省沧州中西医结合医院,河北 沧州 061000)
骨转移是晚期恶性肿瘤常见的并发症之一,以结直肠癌、肺癌、前列腺癌、乳腺癌、多发性骨髓瘤、恶性淋巴瘤骨转移等肿瘤常见,对骨转移患者进行放疗治疗后,约30%~40%的患者可能发生爆发痛[1]。爆发痛指癌症患者在逐步控制慢性疼痛后,机体发生的一种短暂性剧烈疼痛。爆发痛带来的痛感给患者带来极大的痛苦,对患者的生活质量治疗造成严重的影响,甚至可影响患者的心理健康,危及患者的生命[2]。目前,临床常采用止痛药物的三阶梯镇痛疗法、激素等治疗,但上述疗法易引发不良反应,且不良反应较大,尚未达成统一标准。因此,采用积极有效的方法缓解骨转移瘤放疗爆发痛患者的疼痛程度,提高生活质量,是临床一直研究的热点。近年来的研究指出,中医药可有效控制疼痛,但在骨转移瘤放疗爆发痛中的研究较少。因此,本研究将探讨解毒定痛方对骨转移瘤放疗爆发痛患者疼痛程度的疗效。
1 资料与方法
1.1 一般资料 以自2020年8月至2022年1月于我院收治的100例骨转移瘤放疗爆发痛患者为研究对象,按随机数字表法分为治疗组和对照组各50例。治疗组男29例,女21例;年龄42~76岁,平均(50.34±12.38)岁;骨转移:多发20例,单发30例;原发肿瘤:头颈3例,肝胆胰腺6例,胃肠7例,食管2例,泌尿5例,乳腺6例,肺部18例,其他3例;转移部位:颅骨3例,四肢骨7例,骨盆9例,脊柱20例,胸廓11例。对照组男28例,女22例;年龄42~75岁,平均(50.27±12.46)岁;骨转移:多发20例,单发30例;原发肿瘤:头颈3例,肝胆胰腺7例,胃肠6例,食管2例,泌尿4例,乳腺7例,肺部19例,其他2例;转移部位:颅骨2例,四肢骨9例,骨盆11例,脊柱22例,胸廓6例。两组患者一般资料比较差异无统计学意义(P>0.05),具有可比性。本研究的制定符合《世界医学协会赫尔辛基宣言》的相关要求。
西医诊断标准:根据《恶性肿瘤骨转移及骨相关疾病临床诊疗中国专家共识》制定关于恶性肿瘤骨转移的诊断标准[3]:①确诊为恶性肿瘤(经细胞学或组织病理学确诊),或经细胞学或骨病灶穿刺活检确诊为恶性肿瘤骨转移;②经影像学确诊为恶性肿瘤骨转移包括X线、CT扫描、MR扫描确诊。中医诊断标准:符合《中药新药临床研究指导原则》[4]中热毒蕴结型的诊断标准,主症:病变局部或皮肤温度较高、病变局部疼痛、肢体疲倦;次症:头晕目眩、纳差、口干渴;二便:尿短赤、便干结;舌脉:舌红苔黄、脉弦数。
病例纳入标准:①符合上述诊断标准;②伴疼痛、椎旁肿块、椎体压缩性骨折、神经压迫症状等无法行手术治疗,需进行放疗者;③接受放疗治疗;④依从性较好,且精神正常者;⑤能够准确评估自身疼痛者;⑥预计生存周期>6个月者;⑦放疗前1周停用激素及激素类药物;⑧患者均签订知情同意书。排除标准:①患有严重心、肺、肝、肾功能障碍类疾病者;②患有认知障碍、精神类疾病及无法准确判断阐述自身疼痛者;③合并急性炎症、风湿免疫病等疾病者;④对本研究药物过敏史或出现严重不良反应者。
1.2 治疗方法
1.2.1 对照组:给予常规西药治疗,根据疼痛程度,可给予口服布洛芬缓释胶囊(国药准字H10900089 )、口服羟考酮控释片,初始剂量为5 mg,2次/d;在爆发痛发生时给予肌肉注射吗啡注射液 5~10 mg。
1.2.2 治疗组:在上述治疗的基础上给予解毒定痛方治疗。组方:自然铜、桑寄生各30 g,地黄25 g,党参、牡丹皮、白芍、骨碎补、龟板各20 g,当归15 g,牛膝12 g,虫、川芎、川楝子各10 g,肉桂3 g。上述中药由我院中药方制成颗粒后,开水冲服,2次/d。
1.3 观察指标 对比治疗前后两组中医证候积分、炎症因子、疼痛因子、疼痛程度,统计疗效及不良反应。
1.3.1 中医证候积分[4]:将病变局部或皮肤温度较高、病变局部疼痛、肢体疲倦的严重程度依次分为无、轻度、中度、重度,评分分别为0、2、4、6分;将头晕目眩、纳差、口干渴的严重程度依次分为无、轻度、中度、重度,评分为0、1、2、3分,评分越高,病情越严重。
1.3.2 实验室指标:治疗前后抽取患者静脉血5 ml,离心取上清液送检。肿瘤坏死因子-α(TNF-α)、白细胞介素-6(IL-6)、去甲肾上腺素(NE)、β-内啡肽(β-EP)、P物质(SP)、前列腺素E2(PGE2)、5-羟色胺(5-HT)采用酶联免疫吸附法测定,试剂盒购自上海纪宁实业,需严格根据说明书进行操作。
1.3.3 疼痛程度:采用数字化评估量表评估。重度疼痛为7~10分;中度疼痛为4~6分;轻度疼痛1~3分;无痛0分。
1.3.4 不良反应:记录治疗过程患者出现的便秘、恶心呕吐、发热、白细胞减少等不良反应。
1.4 疗效标准[4]显效:病变局部或皮肤温度较高、病变局部疼痛等临床症状均改善明显,中医证候积分减少≥75%;有效:病变局部或皮肤温度较高、病变局部疼痛等临床症状均好转,中医证候积分减少≥50%;无效:上述均无变化或加重。总有效率=显效率+有效率。

2 结 果
2.1 两组临床疗效比较 治疗后,治疗组临床疗效高于对照组(P<0.05),见表1。
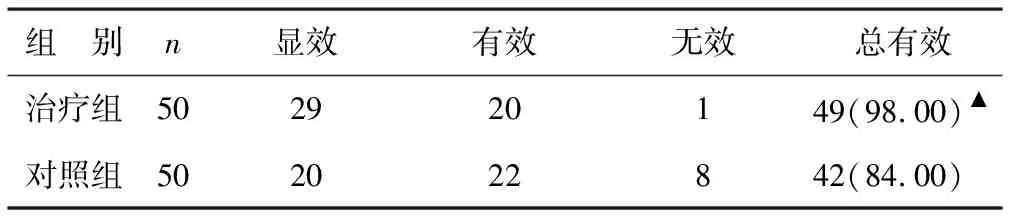
表1 两组临床疗效比较[例(%)]
2.2 两组治疗前后中医证候积分比较 治疗前,两组病变局部或皮肤温度较高、病变局部疼痛、肢体疲倦、头晕目眩、纳差、口干渴评分比较差异无统计学意义(P>0.05);治疗后,两组病变局部或皮肤温度较高、病变局部疼痛、肢体疲倦、头晕目眩、纳差、口干渴评分均较治疗前降低,与对照组相比,治疗组病变局部或皮肤温度较高、病变局部疼痛、肢体疲倦、头晕目眩、纳差、口干渴评分更低(P<0.05)。见表2。
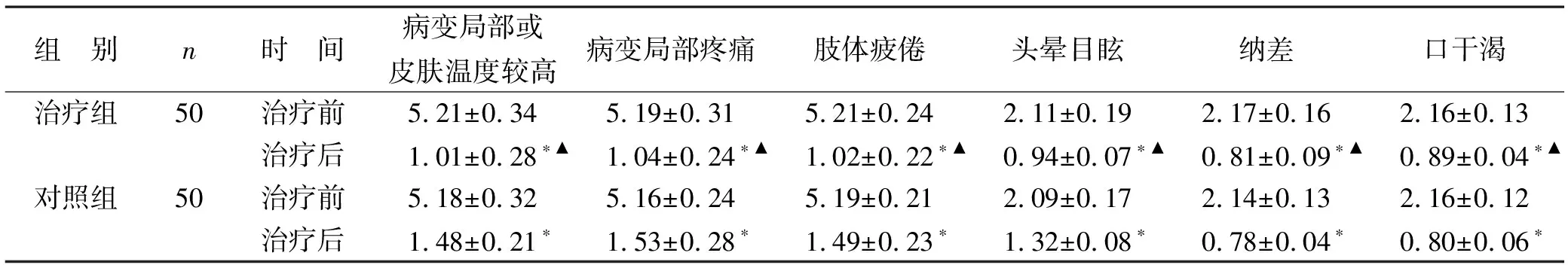
表2 两组治疗前后中医证候积分比较(分)
2.3 两组治疗前后炎症因子水平比较 治疗前,两组TNF-α、IL-6水平比较(P>0.05);治疗后,两组TNF-α、IL-6水平均较治疗前降低,与对照组相比,治疗组TNF-α、IL-6水平更低(P<0.05),见表3。

表3 两组治疗前后炎症因子水平比较
2.4 两组治疗前后疼痛因子比较 治疗前,两组NE、β-EP、SP、PGE2、5-HT水平比较(P>0.05);治疗后,两组NE、β-EP、SP、PGE2、5-HT水平均较治疗前降低,与对照组相比,治疗组NE、β-EP、SP、PGE2、5-HT水平更低(P<0.05),见表4。

表4 两组治疗前后疼痛因子比较
2.5 两组治疗前后疼痛程度评分比较 治疗前,两组疼痛程度比较(P<0.05);治疗后,两组疼痛程度均较治疗前降低,治疗组疼痛程度低于对照组(P<0.05),见表5。

表5 两组治疗前后疼痛程度评分比较(分)
2.6 两组不良反应比较 在治疗过程中,对照组出现15例便秘、12例恶心呕吐、3例发热、12例白细胞减少,总发病率为84.00%(42/50);治疗组出现3例恶心呕吐、1例发热、5例白细胞减少,总发病率为18.00%(9/50),治疗组总不良反应低于对照组(P<0.05)。
3 讨 论
近年来的研究指出,恶性肿瘤的发病率呈逐年递增趋势[5]。在临床上恶性肿瘤常伴骨转移,其中约50%~70%的恶性肿瘤伴骨转移患者伴疼痛[6]。放疗对恶性肿瘤伴骨转移疼痛具有缓解作用,其中约1/4患者经放疗后疼痛完全缓解,2/3患者经放疗疼痛减轻[7]。但放疗会伴不同程度的不良反应,其中爆发痛在临床常见。因此,寻找一种有效的方法减轻骨转移瘤放疗爆发痛的疼痛程度,降低不良反应,对临床尤为重要。
中医学根据骨转移瘤的临床症状将其归属于“骨痹”“骨瘤”等范畴,其认为该病的病因病机可能为内热或外热在机体内停留日久,形成痰瘀,热、瘀、痰互结,内蕴结毒产生火热毒邪,火热毒邪阻塞于经络脏腑,发为肿瘤;热毒伤阴,耗伤津液气血,累及脾胃肝肾,最终引发不荣则痛[8]。因此,治则为滋阴清热、解毒止痛。解毒定痛方中桑寄生、地黄共为君药,其中桑寄生补肝肾、强筋骨,地黄清热凉血、滋阴生津,两药合用共达滋阴清热,强骨生髓;自然铜、延胡索、党参、白芍、龟板、骨碎补、牡丹皮共为臣药,其中自然铜散瘀接骨止痛,延胡索活血散瘀止痛,党参补中益气,白芍养血止痛敛阴,龟板滋阴潜阳、益肾健骨,骨碎补活血补肾强骨,牡丹皮凉血破瘀泻火,六药合用共达滋阴潜阳、凉血破瘀、泻火止痛;当归、川楝子、川芎、牛膝、虫为佐药,当归补血活血止痛,川楝子行气止痛,川芎活血祛瘀,牛膝补肝肾、散恶血,五药合用共达活血祛瘀、养血止痛;肉桂为使药,引火归源、散寒止痛之效。诸药合用共达滋阴潜阳、清热养血祛瘀、健骨止痛。黄杰等[9]的研究指出,中药汤剂联合热疗干预可提高恶性肿瘤骨转移的疗效,可降低疼痛程度。本研究结果显示,治疗后,治疗组临床疗效高于对照组,治疗组病变局部或皮肤温度较高、病变局部疼痛、肢体疲倦、头晕目眩、纳差、口干渴评分更低,提示解毒定痛方可缓解骨转移瘤放疗爆发痛患者临床症状,降低中医证候积分,提高疗效。
TNF-α由内皮细胞及巨噬细胞产生,其在健康人体内可直接杀伤肿瘤细胞,发挥抗肿瘤和抗感染的作用;另外,其水平上升,参与肿瘤的发生发展。IL-6主要由成纤维细胞、局部巨噬细胞及单核细胞产生,对细胞增殖、分化及免疫反应具有促进作用,与肿瘤的发生发展密切相关。本研究结果显示,治疗后,与对照组相比,治疗组TNF-α、IL-6水平更低,提示解毒定痛方可降低骨转移瘤放疗爆发痛患者TNF-α、IL-6水平,降低炎症反应。这可能是虫中的虫水提取物可抑制肿瘤生长,虫总生物碱类成分具有显著的抗菌抗炎作用,虫中的酶解物具有显著的镇痛作用[10]。牡丹皮中的有效成分丹皮醇具有显著的抗肿瘤、抗菌、调节免疫、抗菌消炎等作用[11]。骨碎补中有效成分为黄酮类化合物具有抗氧化、抗炎、抗骨质疏松等作用[12]。
疼痛因子与恶性肿瘤疼痛程度密切相关,NE、β-EP、SP、PGE2、5-HT属于疼痛因子。SP对炎性反应具有增强作用,有利于血管生成,参与疼痛信号传递[13]。PGE2可增加外周组织中毛细血管的通透性,对其他多种疼痛介质在局部浸润具有促进作用,促使痛觉阈值降低,促使疼痛感觉产生。β-EP、SP是介导痛觉信号传导的神经多肽,可将痛觉信号传递向中枢神经,引发疼痛。5-HT是神经疼痛的关键调节者,是最为活跃的神经递质,其对急性疼痛的影响大于慢性疼痛。曹迪等[14]的研究指出,中药汤剂可有效降低癌性疼痛患者疼痛介质及炎症因子水平。但关于中药汤剂对骨转移瘤放疗爆发痛患者疼痛因子的报道少见。本研究结果显示,治疗后,治疗组NE、β-EP、SP、PGE2、5-HT水平更低,提示解毒定痛方可降低骨转移瘤放疗爆发痛患者NE、β-EP、SP、PGE2、5-HT水平,降低疼痛因子水平,这可能是解毒定痛方缓解骨转移瘤放疗爆发痛患者疼痛程度的作用机制,但需进一步采用动物研究证实。罗海恩等[15]的研究指出,中药汤剂可缓解骨转移癌患者疼痛程度,且不良反应少。本研究结果显示,治疗后,治疗组疼痛程度高于对照组,提示解毒定痛方可降低骨转移瘤放疗爆发痛患者疼痛程度。分析原因如下:延胡索中的有效成分为延胡索总碱具有显著的镇痛作用,与吗啡相比,其镇痛效价约40%,且低于吗啡类药物的成瘾率;另外,延胡索中的延胡索乙素具有较强的抗焦虑及镇静作用[16]。川楝子中的川楝素具有广谱抗肿瘤,川楝子醇提取物具有抗炎镇痛的作用[17]。地黄中地黄寡糖具有明显的抗肿瘤作用,不同浓度氯仿提取物、正丁醇浸膏、地黄醋酸乙酯浸膏等对枯草杆菌、金色葡萄球菌、大肠杆菌等具有明显抑菌作用[18]。当归提取物具有镇痛作用,当归多糖可抑制肿瘤的生长,诱导细胞凋亡,发挥抗肿瘤作用[19]。白芍中的有效成分白芍提取物可抗炎,白芍总苷具有调节免疫功能,白芍醇提取液具有镇静作用[20]。本研究进一步观察了解毒定痛方对骨转移瘤放疗爆发痛患者不良反应的影响,结果显示,治疗组总不良反应低于对照组,提示解毒定痛方可降低骨转移瘤放疗爆发痛患者不良反应,安全性较高。
综上所述,解毒定痛方可降低骨转移瘤放疗爆发痛患者中医证候积分,改善临床症状,降低炎症因子水平及疼痛因子水平,缓解疼痛程度,不良反应少。
