“U”路经皮椎间孔镜治疗中央型椎管狭窄术后1年临床效果研究
2022-07-11齐慧林福清占恭豪王兴鹏尹路
齐慧 林福清 占恭豪 王兴鹏 尹路



[摘要]目的探讨“U”路经皮椎间孔镜(PELD)手术治疗中央型椎管狭窄(LCSS)的安全性和术后1年临床疗效。方法回顾分析2017年1月至2019年6月上海市第十人民医院疼痛科及温州医科大学附属第二医院疼痛科第一诊断为LCSS并同意接受“U”路PELD手术治疗并完成术后1年随访的患者55例。记录患者性别、年龄、症状持续时间、手术持续时间和住院天数等基本临床资料,记录术后1d、1个月、3个月、6个月和1年的腰背部和下肢视觉模拟量表(VAS)评分,并采用Oswestry功能障碍指数问卷表(ODI)评估患者生活质量,术前、术后3个月、6个月和1年采用改良Macnab评估患者临床预后。结果1例患者失访,54例患者完成1年随访。术后无神经根损伤、硬膜囊撕裂、脑脊液漏或感染等并发症发生。术后各时间点腰背部和下肢VAS评分以及ODI较术前显著降低(P<0.05)。术后3个月、6个月和1年的改良Macnab评估“总优良率”分别为92.59%、92.59%和98.15%,有显著改善(P<0.05)。无患者因症状复发需要接受二次微创或开放手术治疗。结论“U”路PELD为治疗LCSS有效且安全的手术方式,可显著改善LCSS患者的临床症状、提高其生活质量。
[关键词]“U”路;经皮椎间孔镜;椎管狭窄;中央型
[中图分类号]R681.5
[文献标识码]A
[文章编号]2095-0616(2022)12-0121-05
中央型椎管狭窄(lumbar central spinal stenosis,LCSS)是老年患者最常见的腰椎疾病之一,可导致腰腿痛、间歇性跛行和下肢感觉异常等症状[1],发生率约27.2%[2]。目前临床上对这类患者的治疗仍然存在争议[3]。既往临床上多采用椎板切除减压等开放性手术方式治疗LCSS,但该方法创伤大、术后恢复时间长、经济费用较高。经皮椎间孔镜手术(percutaneous transforaminal endoscopic lumbar discectomy,PELD)是新近发展的脊柱微创手术方式,主要优点在于可通过椎间孔到达椎管内,对椎管内外神经、血管和骨性结构影响较小。最初主要用于治疗腰椎间盘突出症,目前椎管狭窄已被纳入PELD适用范围[4]。临床上PELD主要包括TESSYS(transforaminal endoscopic spine system)、YESS(Yeungendoscopicspinesurgery)和椎板间入路。“U”路PELD是在TESSYS上发展起来的手术方式,然而目前其治療LCSS的疗效未明,因此,本研究拟通过术后临床随访探索“U”路PELD手术方式治疗LCSS的安全性和临床疗效,为临床提供参考依据。
1资料与方法
1.1一般资料
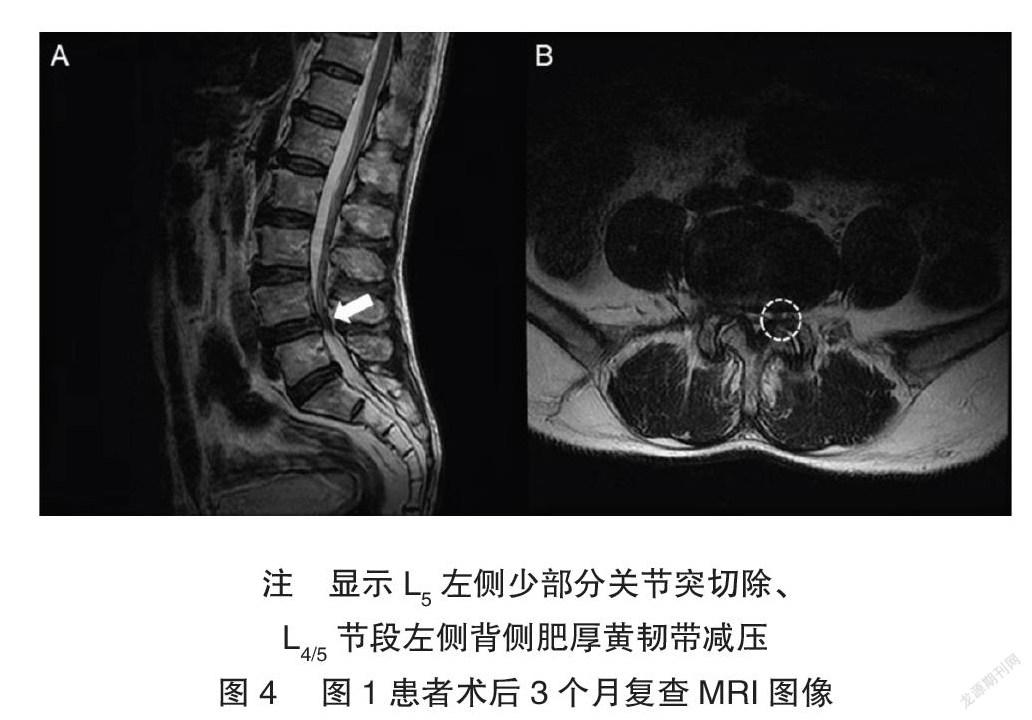
选取2017年1月至2019年6月上海市第十人民医院疼痛科及温州医科大学附属第二医院疼痛科诊断为“中央型椎管狭窄”(LCSS)并接受“U”路PELD手术治疗的患者。目前LCSS的诊断无统一客观标准,临床主要依据症状、体征和影像学检查结果综合判断[2]。纳入标准:1年龄18~85周岁;2临床表现为腰臀部疼痛、下肢痛、间歇性跛行和/或下肢感觉异常;3影像学(CT和/或MRI)表现与临床症状、体征相符,“中央型椎管狭窄”诊断明确,伴或不伴有侧隐窝狭窄(图1);4接受口服药物、理疗、硬膜外注射等保守治疗12周后疗效欠佳;5告知其他手术方式及手术风险后仍选择接受“U”路PELD治疗。排除标准:1由单纯腰椎间盘髓核突出导致的中央型椎管狭窄患者;2存在脊柱畸形或椎体不稳,需开放性手术治疗患者;3有全身感染、凝血功能障碍等异常患者;4有精神疾病无法配合手术患者;5拒绝接受术后1年随访患者。
最后共纳入接受“U”路PELD治疗的LCSS患者55例,其中男29例(52.73%)、女26例(47.27%),平均年龄(55.91±12.11)岁。患者症状持续时间18(12,156)周,手术持续时间(85.64±25.77)min,住院天数5(3,7)d。术前腰背部视觉模拟量表
(Visual analogue scale,VAS)评分6(4,7)分,下肢VAS评分5(3,5)分,Oswestry功能障碍指数问卷表(Oswestrydisabilityindex,ODI)为52(36,71)。手术节段分布为L2/3~L5/S1,其中L2/31例、L3/43例、L4/532例、L5/S114例、L3/4+L5/S11例、L4/5+L5/S14例。
1.2方法
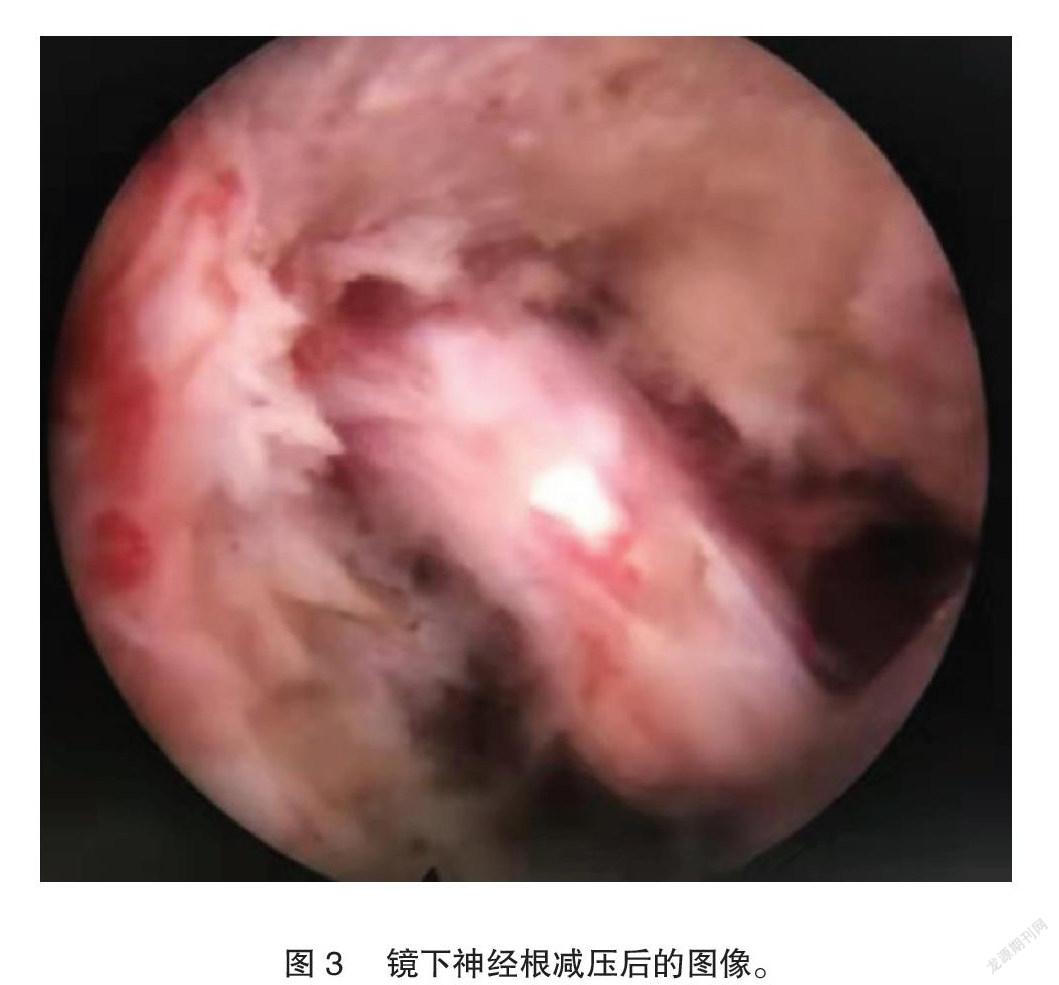
患者健侧卧位,术者在DSA透视下定位责任椎间盘相关位置,常规消毒铺巾,该椎间隙水平向左侧旁开12cm左右为穿刺点,皮下及筋膜层各注射0.5%利多卡因(山东华鲁制药有限公司,国药准字H37022147)5ml局部麻醉后,髓核穿刺针经椎间孔进入上述椎间隙,DSA侧位监测下,针尖到达下位椎体上关节突上缘位置后(图2),拔除穿刺针针芯,再次注射0.5%利多卡因10ml进行麻醉,然后插入导引钢丝、逐级扩张管及工作套管后,置入椎间孔镜及手术器械。在生理盐水持续冲洗及椎间孔镜监视下,切除下位椎体上关节突前上内侧部分(<1/3关节突),打磨行走根后外侧部分椎板,摘除黄韧带和/或增生骨质等组织充分减压,行椎管扩大成形。打开侧隐窝后在镜下进一步将工作套管置入至背外侧黄韧带和椎板之间的间隙内,充分对粘连的神经根和硬脊膜进行松解,同时进行神经探查;充分对硬膜囊背外侧黄韧带和椎板之间减压神经根和硬膜囊减压后,再将偏心环锯和工作套管进入至硬膜囊腹侧,切除病变髓核,予以纤维环射频消融成形,同时切除骨化的后纵韧带、黄韧带或椎体后缘等,手术路径宛如“U”字形。手术达到以下标准:镜下见,无明显渗血、神经根复位、神经血供充盈、硬膜囊搏动良好、直腿抬高90度时神经根移动明显(图3)。最后拔除工作套管,创口缝针后覆无菌敷贴。
1.3术后评估和随访
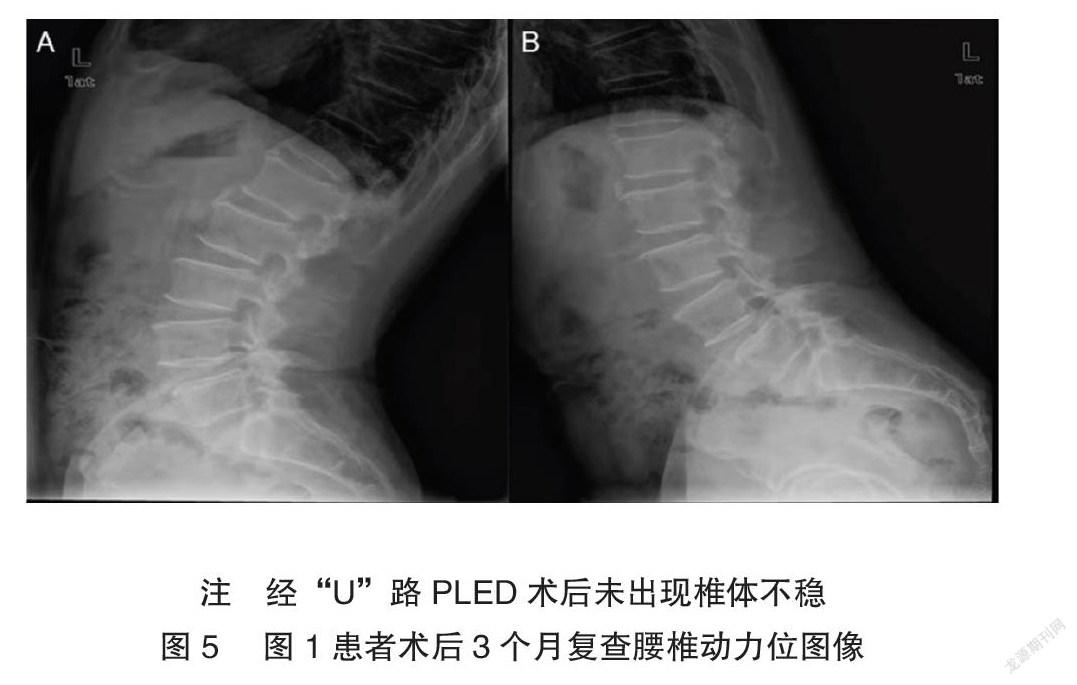
所有纳入患者术后复查腰椎动力位平片(图4)和磁共振(图5),并随访至术后1年。采用VAS评估患者术前、术后1d、1个月、3个月、6个月和1年的腰背痛和下肢痛程度[5],总分0~10分。采用ODI评估生活质量[6],并在术后3个月、6个月和1年采用改良Macnab标准评估临床预后[7],总分0~100分,改良Macnab评估结果分为4个等级:“差”为治疗前后症状无改善,甚至加重;“可”为症状减轻,活动受限,影响患者正常工作和生活;“良”为症状轻微,活动轻度受限,对患者工作生活无影响;“优”为症状完全消失,可恢复原来的工作和生活。优良率=(“优”+“良”)例数/完成随访的患者总人数×100%。随访方式主要通过来院随访进行。
1.4统计学分析
采用统计学软件SPSS25.0进行数据统计分析,所有计量资料采用Kolmogorov-Smirnov方法检验数据是否符合正态分布,符合正态分布的计量资料用均数±标准差(x±s)表示,采用方差分析,不符合正态分布的计量资料采用[M(P25,P75)]表示,采用相关样本Friedman秩和检验;计数资料用[n(%)]表示,采用等级秩和检验。P<0.05为差异有统计学意义。
2结果
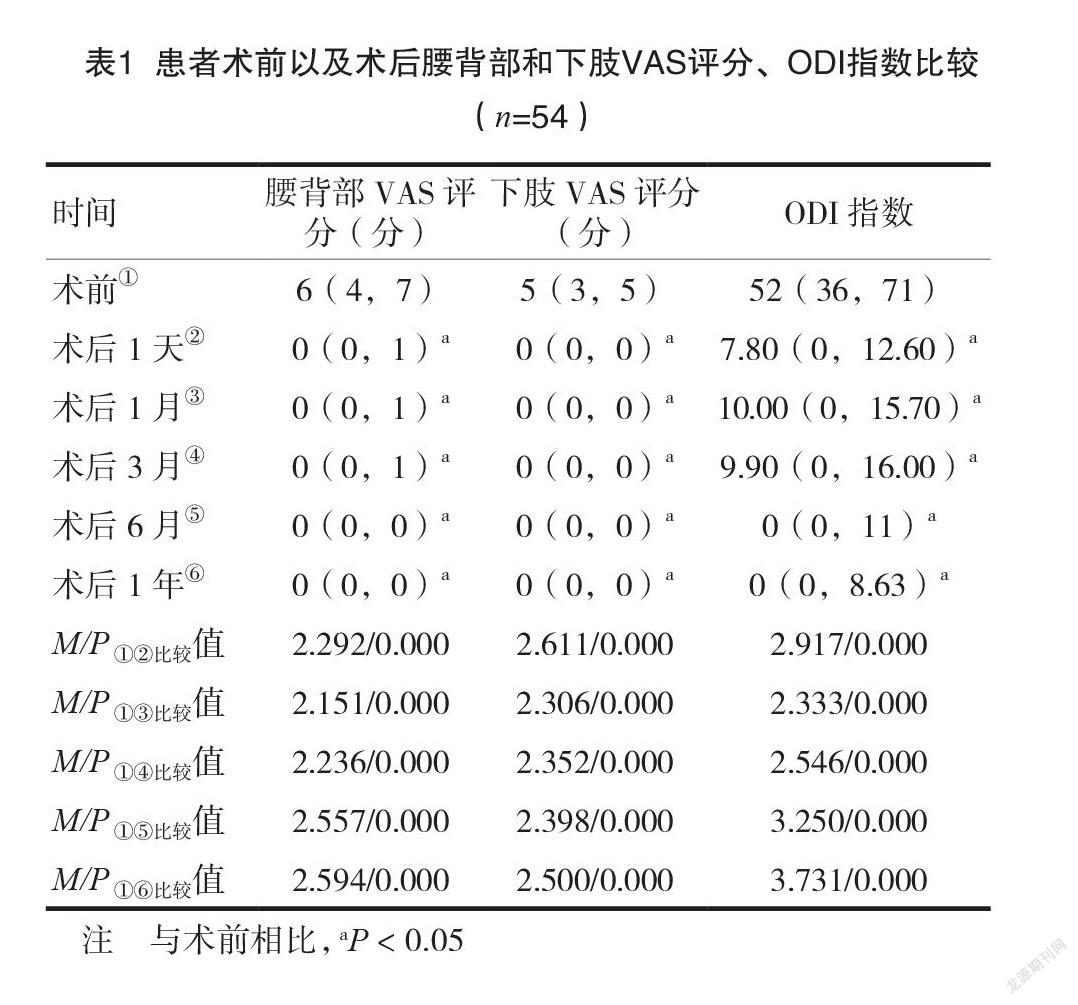
2.1患者术前以及术后腰背部和下肢VAS评分、ODI指数比较
有1例患者术后1月失访,另54例患者完成术后1年随访,无神经根损伤、硬膜囊撕裂、脑脊液漏或感染等并发症发生。结果显示患者腰背部VAS评分从术前6(4,7)下降至术后1年的0(0,0),术后各时间点腰背部VAS评分较术前显著降低(M=114.598,P=0.000),见表1;下肢VAS评分从术前的5(3,5)分下降至术后1年的0(0,0)分,术后各时间点下肢VAS评分较术前显著降低(M=142.924,P=0.000)。患者ODI从术前的52(36.71)降低至术后1年的0(0,8.63),术后各时间点ODI指数较术前显著降低(M=161.935,P=0.000)。
2.2患者改良Macnab评估结果比较
在术后1年随访中,纳入患者术后3月改良Macnab评估结果为32例“优”、18例“良”、2例“可”,2例“差”,优良率为92.59%;术后6月改良Macnab评估结果为40例“优”、10例“良”、3例“可”,1例“差”,优良率为92.59%;术后1年改良Macnab评估结果为40例“优”、13例“良”、1例“可”,优良率为98.15%,患者预后有显著改善,差异有统计学意义(Z=-4.838,P=0.000),见表2。无患者因症状复发需要接受二次微創或开放手术治疗。
3讨论
LCSS是由骨质增生、黄韧带肥厚、伴或不伴有椎间盘突出、髓核钙化等因素造成椎管容积减小、硬膜囊和神经根受压,是导致老年人腰腿痛的最常见原因之一[1]。LCSS通常发生于40岁以上成年人,随着人口老龄化和影像检查技术的普及和发展,LCSS检出率呈上升趋势[3]。既往临床对于LCSS患者主要采用传统开放性手术进行椎管减压治疗,伴或不伴融合。然而,早期研究提示开放性手术对LCSS的疗效欠佳,约23%的患者需要接受多次手术治疗、33%的患者术后仍存在严重腰背痛[8]。尽管术者在术中切除部分关节突组织以达到更彻底的减压,但是目前一致认为过度切除关节突与开放性手术后椎体不稳相关,这也可能是导致开放性手术疗效欠佳的原因之一[9]。
随着脊柱微创手术迅速发展,PELD已逐渐成为治疗脊柱源性疾病的主要微创手术方式之一。随着手术方式和器械的不断改进和发展,PELD的适用范围由最初的腰椎间盘突出症逐渐扩大[10],目前已涵盖腰椎椎管狭窄症的治疗[4,11]。“U”路作为近年新近发展的PELD手术方式,已有研究报道“U”路PELD可用于治疗胸椎椎管狭窄,且优良率达71.4%[12]。目前已有研究报道TESSYS和椎板间入路等对LCSS的安全性和临床疗效[4,13-14],但是临床上对于“U”路PELD治疗LCSS的安全性和疗效尚未明确,因此本研究致力于探索“U”路PELD治疗LCSS的安全性和临床疗效,具有重要临床意义。
本研究纳入55例接受“U”路PELD的LCSS患者,并进行术后1年随访,其中1例在术后1月失访,因此共纳入54例患者数据进行统计分析。研究结果提示,与术前相比,“U”路PELD可显著降低患者术后腰背部和下肢VAS评分、ODI指数(P<0.01)。术后3个月、6个月以及1年的改良Macnab评估优良率分别为92.6%、92.6%和98.1%,随着时间推移,术后患者预后有显著改善(P<0.01),但是对于术后3个月之前和术后1年之后的时间点未进行评估,在未来研究中可进一步完善和证实。为减少对脊柱稳定性的影响,术者在术中对下位椎体上关节突的切除范围小于1/3,经术后腰椎动力位证实对患者脊柱稳定性未造成不良影响。
PELD并发症主要包括神经和血管损伤、硬膜囊撕裂、脑脊液漏、感染、肌肉血肿、硬膜囊血肿等。在本研究随访中,对手术并发症进行记录,结果显示最初纳入随访的55例患者中无并发症报告,至术后1年随访结束时无患者需要接受二次开放或微创手术,提示“U”路PELD是治疗LCSS有效且安全的手术方式。此外,资料显示腰椎椎管狭窄患者中约有35%存在1个节段以上的中至重度椎管狭窄[15]。本研究中有5例(9.1%)患者接受2个节段的手术治疗,发生率低于文献报道,可能与本研究主要筛选LCSS患者进行随访,以及本研究样本量较小有关。
本研究探索“U”路PELD手术治疗LCSS的临床疗效和安全性,具有一定创新性,但存在以下不足:1未能纳入接受开放性手术治疗的LCSS患者作为阳性对照组;2均为病程>12周的慢性痛患者,随访中仅对疼痛评分、功能改善和生活质量提高等指标进行评估,未记录疼痛相关情绪量表;3随访周期仅为术后1年,未能报道远期的临床疗效;4未测量术前和术后椎间盘高度以及椎间孔直径等,所以未能从解剖学方面来进一步揭露“U”路PELD的优势。因此,结论还需随机分组的大样本临床研究进一步验证。
综上所述,“U”路PELD为治疗LCSS有效且安全的手术方式,可显著改善LCSS患者的临床症状、提高其生活质量。然而,由于本研究的局限性,研究结论还需未来大样本、随机对照的临床试验进一步证实。
[参考文献]
[1] Manchikanti L,Kaye AD,Manchikanti K,et al.Efficacy of epidural injections in the treatment of lumbar central spinal stenosis: A systematic review [J].Anesth Pain Med,2015,5(1):e23139.
[2] Kim YU,Park JY,Kim DH,et al.Ther role of the ligamentum flavum area as a morphological parameter of lumbar central spinal stenosis[J].Pain Physician,2017, 20(3):E419-E424.
[3] Hu D,Fei J,Chen G,et al.Treatment for lumbar spinal stenosis in elderly patients using percutaneous endoscopic lumbar discectomy combined with postoperative three- dimensional traction[J].Expet Rev Med Devices,2019, 16(4):317-323.
[4]邓敦,颜海波,林宪法,等.微创椎间孔镜治疗退行性腰椎管狭窄早期临床效果[J].温州医科大学学报,2017,47(4):273-276.
[5] Thong ISK,Jensen MP,Miró J,et al.The validity of pain intensity measures: what do the NRS, VAS, VRS, and FPS-R measures?[J].Scand J Pain,2018,18(1): 99-107.
[6] Lue YJ,Hsieh CL,Huang MH,et al.Development of a Chinese Version of the Oswestry Disability Index Version 2.1[J].Spine,2008,33(21):2354-2360.
[7] Wu B,Zhan GH,Tian XY,et al.Comparison of transforaminal percutaneous endoscopic lumbar discectomy with and without foraminoplasty for lumbar disc herniation: a 2-year follow-up[J].Pain Res Manag, 2019,2019:6924941.
[8] Katz JN,Lipson SJ,Chang LC,et al.Seven- to 10-year outcome of decompressive surgery for degenerative lumbar spinal stenosis[J].Spine,1996,21(1):92-97.
[9] Guo S,Sun J,Tan G.Clinical study of bilateral decompression via vertebral lamina fenestration for lumbar interbody fusion in the treatment of lower lumbar instability[J].Experimental and Therapeutic Medicine, 2013,5(3):922-926.
[10]王睿嫻,田心毅,占恭豪,等.经皮脊柱内镜下椎间盘切除术治疗腰椎间盘突出症1年疗效随访研究[J].中国疼痛医学杂志,2019,25(8):603-607.
[11] Lee CW,Yoon KJ,Ha SS,et al.Foraminoplastic Superior Vertebral Notch Approach with Reamers in Percutaneous Endoscopic Lumbar Discectomy: Technical Note and Clinical Outcome in Limited Indications of Percutaneous Endoscopic Lumbar Discectomy[J].J Korean Neurosurg Soc,2016,59(2): 172-181.
[12] Xiaobing Z,Xingchen L,Honggang Z,et al.“U” route transforaminal percutaneous endoscopic thoracic discectomy as a new treatment for thoracic spinal stenosis[J].International Orthopaedics,2019,43(3): 825-832.
[13]黄保华,钟远鸣,陈远明,等.经椎间孔经皮内镜治疗中央型椎管狭窄症[J].中国矫形外科杂志,2018,26(1):79-83.
[14]薛静波,陈浩翔,李学林,等.经皮全脊柱内镜经椎板间隙入路治疗中央型腰椎管狭窄症[J].中国微创外科杂志,2020,20(4):322-325,329.
[15] Tang S,Jin S,Liao X,et al.Transforaminal percutaneous endoscopic lumbar decompression by using rigid bendable burr for lumbar lateral recess stenosis: technique and clinical outcome[J].Biomed Res Int,2018,2018:2601232.
(收稿日期:2021-12-15)
