植物SWEET基因家族的研究进展
2022-07-10李旭楠李诗燕王锦达
黄 成,李旭楠,李诗燕,王锦达
(福建农林大学国家甘蔗工程技术研究中心,福州 350002)
0 引言
糖是植物体内一类重要的有机物,其含量约占植物干重的50%以上,植物中的糖通常可分为可溶性糖和不溶性糖,可溶性糖包括葡萄糖、蔗糖、麦芽糖等;不溶性糖包括淀粉、纤维素等[1]。植物通过光合作用将大气中的CO2转化为可利用糖源,通过长距离运输到达库组织进行储存或利用。糖对植物的生长发育起着重要作用,不仅作为能源物质维持植物自身基础代谢生命活动,另外糖的合成、转运分配以及代谢过程,也沟通了蛋白质的合成、脂类的合成等[2-4]。并且糖还作为植物细胞中的溶质,通过调节细胞中溶液渗透压进而影响气孔开关等活动[5-6]。此外,植物中的糖还是重要的信号分子,可以通过影响生长素的运输和分布来调节子叶的伸长和生长[7]。但植物并不能通过膜内外的浓度梯度差吸收糖分,必须借助转运蛋白完成糖分的运输及生物代谢。SWEET蛋白的发现恰好解释了糖分转运模式,研究表明SWEET转运蛋白可以促进糖类顺浓度梯度扩散以及调控植物体内糖类化合物的运输[8-10]。
已有的研究表明,SWEET基因在自然界生物中的存在范围极广,在多种植物中如拟南芥、木薯、桉树等以及动物中均已被发现,例如秀丽隐杆线虫、高等生物人和小鼠等[11]。在植物细胞中有3个基因家族编码的蛋白在糖分的转运的过程中起着重要的作用:单糖转运蛋白(Monosaccharide transporters,MSTs),蔗糖转运体/蔗 糖 载 体 (Sucrose transporters,/Sucrose carriers,SUT)和双向糖转运蛋白(Sugars will eventually be exported transporters,SWEET)[12]。其中MSTs和SUT 2个糖转运蛋白基因家族在过去已经得到了广泛的研究。本研究围绕SWEET基因编码蛋白结构,以及其在植物中参与的生物学功能进行总结,为进一步研究SWEET基因在动植物中的其他结构的生物学功能提供理论指导。
1 SWEET蛋白结构特征与糖分转运机制
1.1 SWEET蛋白结构特征
SWEET蛋白是通过葡萄糖荧光共振能量转移(fluorescence resonance energy transfer,FRET)传感器鉴定出的一个不依赖环境pH,只利用细胞内外浓度差实现糖跨越细胞膜浓度梯度运输的一类蛋白[13]。植物中的SWEET蛋白属于MtN3-like大族中的MtN3/saliva蛋白家族,在原核生物中的SWEET具有1个保守的MtN3/saliva跨膜结构,其中含有3个跨膜螺旋。真核生物具有的2个保守的MtN3/saliva跨膜结构(含7个跨膜螺旋)(图1-A)由原核生物3个跨膜的MtN3/saliva结构域发生了复制形成,由此来承担更复杂的蔗糖转运(图1-B)[13]。而真核生物中的7次跨膜螺旋则是由2个3-TMs和1个TM相互连接形成,3-TMs则是SWEET蛋白中心保守性较低的单个跨膜α-螺旋(α-helical transmembrane domain,TMs),连接分别位于SWEET蛋白N端和C端的相对保守的2个重复的具有3次跨膜α-螺旋构成的[14]。因此,SWEET蛋白的结构的差异性使得其在不同物种间行使着不同的生物学功能。
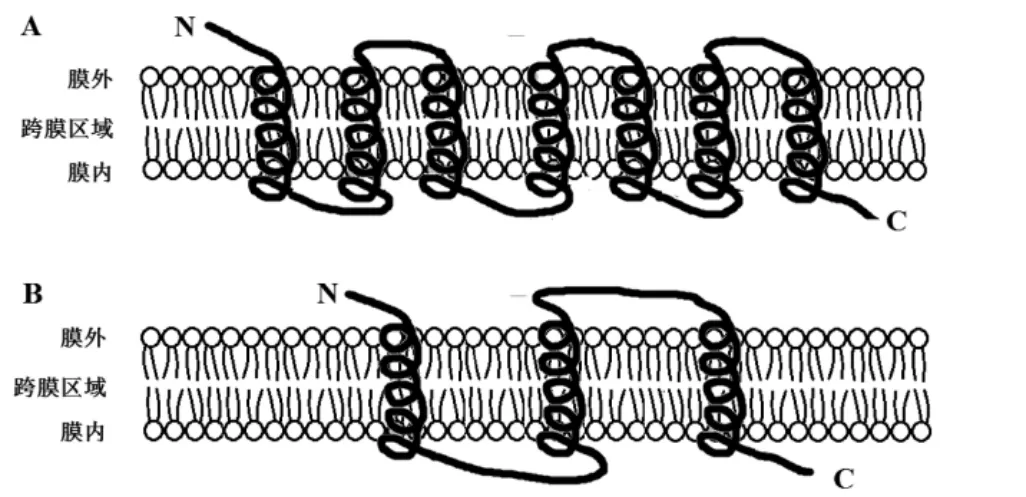
图1 SWEET基因家族结构模型[15]
1.2 SWEET蛋白糖分转运机理与叶片中糖转运过程。
水稻OsSWEET2b和大肠杆菌E.coil的SWEET结晶构象研究表明SWEET蛋白都通过形成底物结合口袋,并在相应位点氨基酸的协助下,实现糖的结合和转运[16]。其中在水稻OsSWEET2b蛋白中2个高度保守的天冬酰胺残基对底物结合起了重要作用,此外TM2的半胱氨酸、TM6的苯丙氨酸也是OsSWEET2b形成糖转运功能的关键位点。在拟南芥的研究中发现,拟南芥中的SWEET蛋白TM1、TM2、TM5和TM6 4个结构域中的脯氨酸通过改变蛋白构象(终止螺旋或诱导弯曲)从而实现蛋白对糖的结合与转运,缺少任何一个结构中的脯氨酸都会导致蛋白失去活性[16]。尽管已有的实验已经在一定程度上解释了SWEET蛋白糖转运机制,但目前对于SWEET蛋白是如何结合糖分以及转运糖分的详细机制还没有得到非常具体清晰的阐述,在未来我们要进一步分析SWEET蛋白的三维结构,才有可能对SWEET蛋白的糖分转运机制有更详细的了解。
在叶片中,叶肉细胞合成的蔗糖通过胞间连丝进入韧皮部薄壁细胞,位于韧皮部薄壁细胞质膜上的SWEET蛋白将蔗糖外排到韧皮部外质。筛管(SE)-伴胞(CC)复合体质膜上的蔗糖转运体(SUTs)从外质体摄取蔗糖,从而将蔗糖浓缩进入筛管中,进行下一步的糖分转移与再分配[(8]图2)。

图2 叶片中糖分转运模型[8]
2 SWEET基因家族在植物中的生物学功能
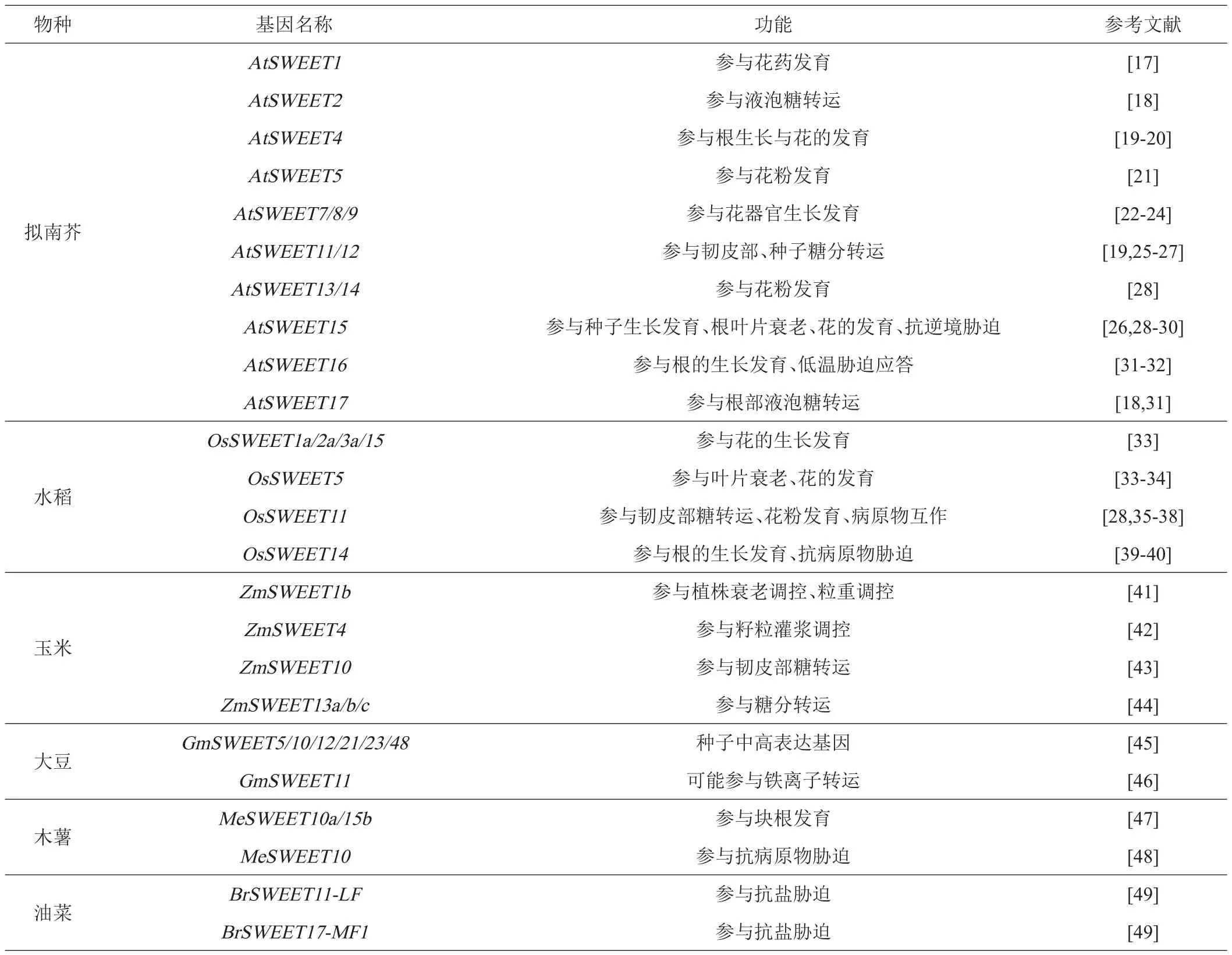
表1 不同植物SWEET基因研究进展
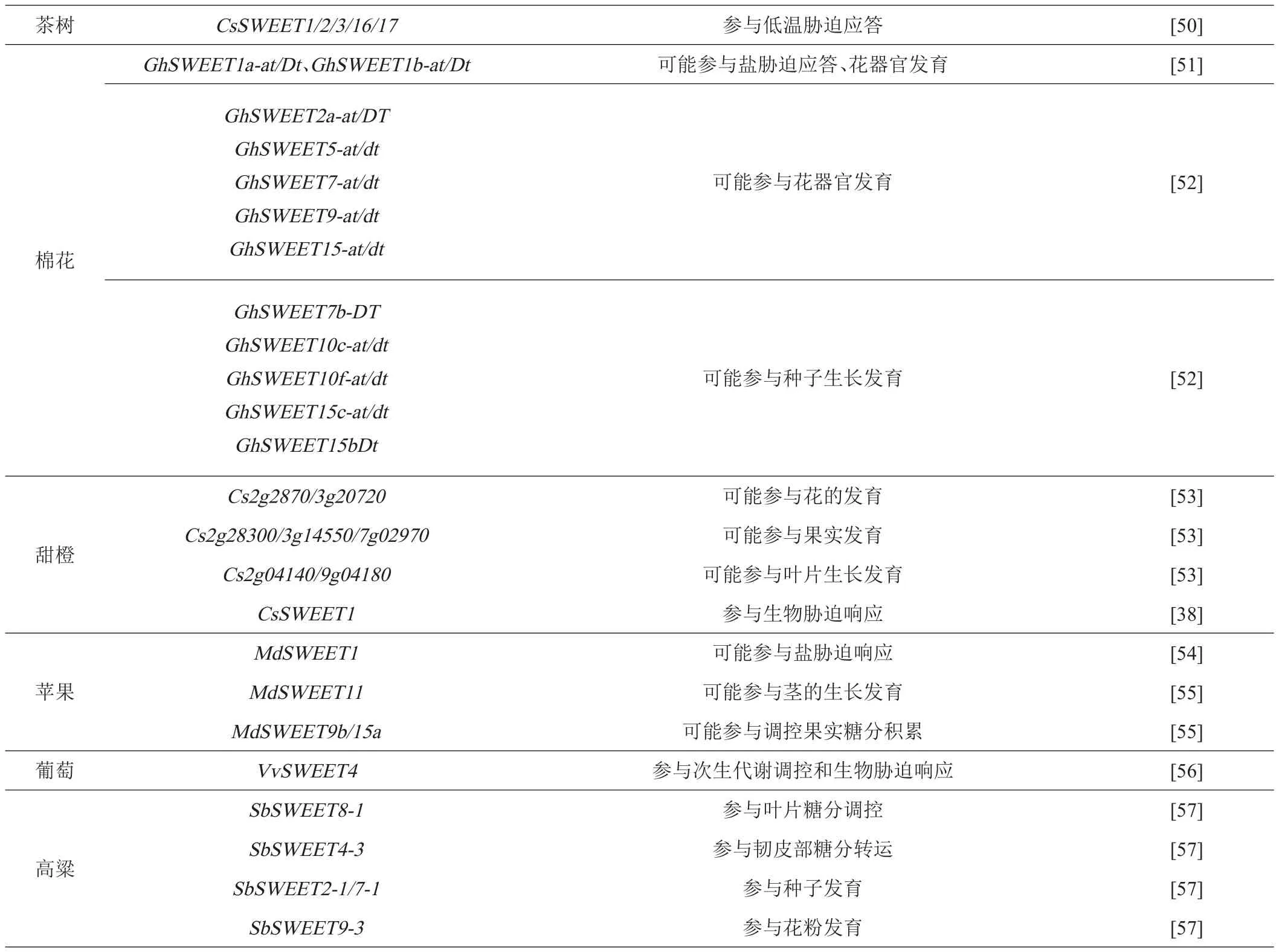
续表1
由于SWEET蛋白在原核与真核生物中的组成结构不同,使得SWEET蛋白在不同物种中行使着不同的功能。总体而言SWEET基因主要参与了糖分转运、生殖生长、营养生长以及抗逆胁迫过程。
2.1 SWEET参与植物生长发育过程
2.1.1 参与糖分转运 植物通过光合作用合成的糖原,主要以蔗糖的形式完成糖分的长距离运输。而植物有机物质的长距离运输主要通过质外体或共质体途径进行,蔗糖可以通过质外体的途径向韧皮部进行扩散也可以通过共质体途径利用细胞胞间连丝进入韧皮部质外体[15]。而蔗糖转运蛋白只能协助蔗糖从筛管-伴胞复合体外转运到筛管-伴胞复合体内,但不能负责蔗糖从韧皮部薄壁细胞转运到筛管-伴胞复合体分子附近[28]。如何实现蔗糖向韧皮部薄壁细胞转运成为蔗糖质外体途径能否实现的关键。定位在拟南芥叶片细胞质膜上的AtSWEET11和AtSWEET12蛋白的发现首次证明了SWEET蛋白在糖分转运过程中的重要作用,AtSWEET11和AtSWEET12在叶片中的高表达表明其能够协助糖分转运到筛管-伴胞复合体分子附近,从而实现蔗糖质外体途径的转运,并且在高光条件下AtSWEET11/12蛋白突变株的叶子中出现了淀粉和糖积累现象[19]。随后发现的OsSWEET11在水稻韧皮部中特异性表达,也表明该蛋白可能参与了蔗糖在韧皮部的转运过程。另外,玉米ZmSWEET10a基因表达分析显示,其对授粉后糖的输出起关键作用并且在玉米维管束鞘细胞的特异性高表达,也表明了SWEET蛋白可能参与了韧皮部糖分转运的过程[43];同样的结论在缺失ZmSWEET13a/b/c的突变体上也得到了印证,ZmSWEET13a/b/c突变体缺失玉米光合作用受损,叶片积累了大量的淀粉和可溶性糖,影响了蔗糖在韧皮部的装载[44]。
虽然大部分的SWEET蛋白都主要行使着转运蔗糖的作用,但目前发现也存在少部分SWEET蛋白参与了果糖等单糖的转运过程。如拟南芥AtSWEET17在根和叶的液泡膜上表达,通过转运果糖来维持根部胞质果糖稳态;AtWEET17的同系物AtSWEET16也可能具有果糖转运功能,研究发现AtSWEET16主要在根系液泡中表达,果糖过量作用下突变体的根系生长抑制现象表明AtSWEET16通过调节液泡中果糖含量维持胞质稳态[31]。相信随着被挖掘SWEET蛋白数量的增多,结构进一步明晰,SWEET蛋白更多糖分转运功能将被发现。
2.1.2 影响根、茎、叶生长发育 糖在根系的生长发育中起着重要的作用,光合作用产生的糖经过长距离运输到达根系,进而参与根系的生长发育,葡萄糖可作为关键营养信号分子促进根尖分生组织活性,蔗糖可促进根伸长和激活根分生组织[58]。糖还可与激素作用调控主根的生长发育[59]。Chen[19]等首次发现拟南芥AtSWEET4参与了植物根的生长,证实了SWEET蛋白在植物根系生长上起着重要作用。随后发现的AtSWEET16/17蛋白再次证明SWEET蛋白在根系生长发育中的作用[31]。在水稻中发现OsSWEET14基因突变会导致水稻侧根生长发育受到一定影响[39]。另外,在药用植物铁皮石斛中也发现SWEET蛋白在根系中起着明显作用,DoSWEET11基因在石斛根中高效表达,意味着其可能主要参与了根中糖分转运和贮存[60]。近年来,越来越多的植物中均发现SWEET基因在根部有表达,如小麦TaSWEET6基因、木薯MeSWEET基因、马铃薯StSWEET5基因等[47,61-62]。
茎作为植物的六大器官之一,参与了植物众多的生理生化过程。糖是茎在生长发育过程中必不可少的有机物质,对于以块茎为收获产物的植物而言,糖分在茎中的运输储存则显得更为重要。路静等[55]研究发现苹果MdSWEET11基因在茎中出现高表达现象,其表达量是根的7.5倍,表明MdSWEET11可能参与了苹果茎的生长和发育。同样的结果在番荔枝中也得到了证实,番荔枝AT-SWEET16-1基因在茎中的表达量比其他组织都高,可以推测AT-SWEET16-1在番荔枝茎中具有一定的功能[63]。在块茎作物马铃薯中发现StSWEET5基因在茎中有表达,说明StSWEET5可能参与了马铃薯块茎的形成与膨大过程[62]。在众多的植物中均发现了SWEET蛋白在茎中的存在,但均未有较为详细清晰的阐述,相信在未来进一步挖掘SWEET蛋白的组织表达特异性的过程中,茎中SWEET蛋白的生物学功能能够得到更为详细的阐述。
SWEET基因家族也参与了叶片的生长发育。Seo等[29]研究发现,拟南芥SAG29(AtSWEET15)基因在衰老的叶片中转录水平显著提高,高表达的转基因植株出现了加速衰老现象,但T-DNA插入基因突变体与野生型植物的表型差异并不明显,说明SAG29(AtSWEET15)没有直接参与叶片衰老的前期过程,而与衰老过程的后续步骤有关。Zhou等[34]发现,水稻OsSWEET5基因编码的蛋白具有转运半乳糖功能,其在衰老的叶片中表达,过表达的OsSWEET5基因导致糖代谢及转运异常,并且还抑制了生长素信号的转导和易位,从而导致水稻苗期生长迟缓和早熟早衰。进一步实验发现,敲除OsSWEET5基因的植株并没有出现明显的表型变化,说明水稻中可能还有其他糖转运蛋白可以实现转运半乳糖的功能。目前对于SWEET基因在植物叶片中的功能研究较少,该基因在叶片中的功能还有很大的开发空间,有没有可能通过调节SWEET基因在叶片中的表达来延长叶片寿命,进一步提高叶片的光合作用时间及光能利用率从而有效增产增收等等的一些列可能的猜想,都有待科学家的进一步深入研究去验证。
2.1.3 参与花、果实、种子的生长发育 SWEET基因家族在植物花的生长发育中发挥着重要作用,目前SWEET基因在花器官中所起作用研究较为详细的2种植物分别为拟南芥和水稻。其中拟南芥中9个SWEET基因都主要在花中表达:AtSWEET1、AtSWEET4/5、AtSWEET7/8/9、AtSWEET13/14/15。AtSWEET1在花原端和雄蕊原基中有较高的表达,说明AtSWEET1可能为配体子的发育提供营养[17]。AtSWEET4在花瓣、花药和花丝中积累,而不在雌蕊中积累[20]。AtSWEET5在花粉发育后期的营养细胞中活跃表达,表明AtSWEET5(又称AtVEX1)为花粉的发育提供营养物质[21]。AtSWEET7基因被认为是“优先基因”在花粉发育时表达[22]。AtSWEET8(又称PRG1)在雄性减数分裂过程中,在小孢子细胞(或小孢子)和绒毡层中强烈表达,是拟南芥小孢子外显子形成的必须基因。AtSWEET8突变体由于突变微孢子在四分体阶段异常,导致小孢子和小室壁上有缺陷的孢粉沉积,并且小孢子细胞出现破裂和细胞质渗漏现象,最终使得突变体表现为雄性的育性降低[23]。AtSWEET9主要在蜜腺中表达,SWEET9突变体表现出花蜜分泌受阻现象[24]。ATSWEET13/14主要在雄蕊中表达,ATSWEET15则主要在花瓣中表达[28]。在水稻中主要有6个基因在花的不同组织中表达,分别为OsSWEET1a、OsSWEET2a、OsSWEET3a、OsSWEET5、OsSWEET11、OsSWEET15。其中OsSWEET11基因在水稻中的作用被研究的较为清晰,OsSWEET11突变体小孢子发育停止在单细胞花粉粒期,未成熟花粉逐渐退化,导致植株育性降低或者丢失[35],而其余5个OsSWEET基因则在水稻不同发育阶段的花或圆锥花絮中有较高表达,表明它们在水稻花的生长发育阶段起着重要作用[33]。除了拟南芥和水稻,其他植物中也存在与植物花的生长发育过程有关的SWEET基因。在牡丹中有10个SWEET基因家族成员 (PsSWEET1、PsSWEET2、PsSWEET3、PsSWEET4、PsSWEET5、 PsSWEET6、 PsSWEET7、 PsSWEET8、PsSWEET9、PsSWEET10)调控着牡丹的开花过程[64];在高粱中SbSWEET4-1和SbSWEET4-2主要在花序中表达,SbSWEET9-3与AtSWEET8在同一进化支,推测其在花粉中糖分运输和花粉发育过程中发挥关键作用[65]。除此之外,在大豆、烟草和毛竹等物种中也存在相关的SWEET基因[66-68]。
糖是果实积累的主要营养物质,果实的成熟度与其内部的糖含量有着密切关系,糖也是果实的口感风味和商品价值的重要指标。SWEET作为双向糖转运蛋白可能参与了果实发育和成熟阶段的糖分转运工作。王梓然等[69]研究发现在葡萄果实发育的Ⅰ期、Ⅲ期有9个SWEET基因家族成员的参与,其中有2个主要参与糖分的转运,分别是定位在质膜上的VvSWEET10和液泡膜上的VvSWEET16,二者基因的表达量从Ⅰ期到Ⅲ期都出现了强烈的上升现象。番茄中的SISWEET7a基因在绿熟期果柄、果实维管束相对表达量最高,说明其对果实发育起着调控作用[70]。同样的结果也出现在番荔枝作物中,番荔枝ATSWEET16-1基因在成熟果的果柄部位中表达量最高,也说明该基因在番荔枝果实的发育阶段起到一定作用[63]。此外在甜橙、苹果植物中SWEET基因家族中也发现有许多有果实发育有关的基因[53,71]。
种子的生长不仅需要氧气、水分、温度,还需要充分的营养物质。在大豆中发现6个基因在大豆种子中出现高表达,其中GmSWEET12和GmSWEET21在种子中的表达量甚至超过了花梗和豆荚中的表达量之和 , GmSWEET5、 GmSWEET10、 GmSWEET23、GmSWEET48在种子中表达量也超过其它组织,被认为是种子特异表达基因[45]。拟南芥AtSWEET11和AtSWEET12在质膜中大量表达,这可能与SWEET蛋白的糖转运功能有关系,将种皮中的蔗糖运输到胚组织,从而促进种子的萌发和发育。AtSWEET11也被检测到参与种皮糖的运输和种子发育[25]。在高粱中SbSWEET2-1和SbSWEET7-1与水稻SWEET11在同一进化分支,参考OsSWEET11基因的功能,推测SbSWEET2-1和SbSWEET7-1在高粱种子发育过程具有重要作用[57]。另外,在豌豆中也发现相应SWEET基因参与种子的萌发和发育[28]。
2.2 SWEETs参与响应各种胁迫应答
2.2.1 SWEETs参与响应各种生物胁迫应答 大部分病原物、害虫、杂草等的主要能量物质都是糖,植物与生物胁迫在互作的过程中,植物常常通过上调或者下调SWEET基因表达量从而调控体内糖分含量,以应对各种生物胁迫。目前,水稻中的SWEET基因在生物胁迫过程所起作用被研究的较为透彻。水稻OsSWEET11基因可以通过调节转录水平,从未促进或抑制白叶枯病菌的生长。当白叶枯病菌侵染水稻时,该细菌会通过T3分泌系统分泌TALES转录激活效应子,随后TALES激活因子与SWEET基因上游启动子顺式作用原件结合,从而调控靶标基因SWEET的表达,促进糖向白叶枯菌中转移,引起病情加重[28,72]。此外,李丽等[72]研究发现,白叶枯病菌non-TALE效应子XopN对病菌促进OsSWEET11基因的表达起到促进作用。OsSWEET14与OsSWEET11具有同源性,抑制OsSWEET14的表达可以提高植物对白叶枯病的抗性[40]。同样的结果在抑制OsSWEET11表达时也得到了证实,并且通过抑制OsSWEET11的表达还可以提高水稻对条纹枯病的抗性[36-37]。除了水稻之外,甜橙CsSWEET1基因可被细菌性溃疡病菌TAL转录激活因子诱导表达;葡萄VvSWEET4能够与灰霉病菌相互作用;辣椒中SWEET基因(UPA16)受细菌性疮痂病菌诱导表达量上升[38,73-74]。另外在拟南芥中也存在响应病菌胁迫的8个SWEET基因[15]。不仅如此,植物在受害虫侵害时,植物体内SWEET基因也存在表达量变化的现象。拟南芥植物受到南方根结线虫侵染时,拟南芥植物体内的多个SWEET基因出现表达量变化[75];西红柿叶片受到根际线虫侵染时,SWEETs基因出现明显的上调[76]。目前SWEET基因参与响应病原物胁迫的研究大部分还只停留于基本表达量水平,至于SWEET基因或蛋白是如何、在哪里调控糖分转运、什么时候开始调控,怎么调控等一系列的问题还有待进一步的研究。
2.2.2 SWEETs参与响应各种非生物胁迫应答 植物在逆境条件下,往往会通过提高体内糖含量,来降低体内渗透压;或是通过调节糖分转移再分配,维持渗透压的平衡,以安全度过逆境。SWEET作为重要的糖分转运蛋白,在许多植物中都发现这类基因对非生物胁迫有响应。
干旱环境条件下,作物能够调节其生理生化反应降低干旱对其产生的不良影响。SWEET基因家族成员已被证实是植物对干旱胁迫机制的一部分。拟南芥AtSWEET11、AtSWEET12和AtSWEET15在干旱胁迫条件下,三者在叶片中的表达量上调,提高蔗糖转运效率,促进糖向根系转移,从而降低根系渗透压,提高根系吸水量[26]。小麦TaSWEET6基因在干旱胁迫条件下表达量上调[61];青扦PwSWEET1在受到干旱胁迫下表达量也出现显著上调[77]。不仅如此,在耐旱植物木薯中也发现相关SWEET基因表达量也存在上调现象[47]。
高盐环境下植物的渗透压平衡被打破,植物会出现吸水困难现象,最后萎蔫死亡。不仅如此,盐胁迫会严重破坏植物光合器官结构,叶绿体类囊体膜膨胀、基粒消失且出现巨型淀粉粒,叶绿体结构遭破环,相关酶失活等等不良反应[78]。已有的研究表明,拟南芥AtSWEET15受高盐诱导,过表达的AtSWEET15会使植物对盐胁迫更加敏感,并加速叶片衰老[30]。而缺乏AtSWEET15的拟南芥对盐分胁迫不敏感。此外,拟南芥中异源表达尖叶石竹DsSWEET12和DsSWEET17,可以提高果糖和葡萄糖的积累量,并且提高对盐胁迫[79-80]。定位在液泡膜上的苹果MdSWEET1在番茄中异源表达,盐胁迫下,转基因番茄中积累了更多的可溶性糖,表明MdSWEET1基因可以通过调节糖的积累从而提高植物的耐盐能力[55]。在其他植物中也存在盐胁迫下,SWEET基因表达量上调的现象,如桉树中EgSWEET,油菜中 BrSWEET11-LF和 BrSWEET17-MF1,棉花中GhSWEET1a-at/Dt、GhSWEET1b-at/Dt等等[12,51,81]。
温度胁迫是限制植物生长发育的主要原因之一,低温/高温条件下都会影响植物光合酶的活性、水分代谢、呼吸作用等。为了应对不同的环境限制,就必须准确调控液泡中糖的储存和运输。拟南芥AtSWEET16和AtSWEET17是控制叶片和根内葡萄糖和果糖含量的主要因素,在寒冷胁迫下出现组成型过表达,过表达的AtSWEET16会增强植物的抗冻性,这可能是由于液泡中积累了更多的可溶性糖而导致的[32]。拟南芥AtSWEET11和AtSWEET12可以通过促进糖向次生在、木质部转移为此次细胞壁提供更多营养,进而提高拟南芥对低温的耐性[27]。在花卉植物萱草中也发现SWEET参与响应低温胁迫,定位在细胞膜上的萱草HfSWEET2a在低温诱导下出现了高表达[82]。不仅如此,在木本植物茶树中也存在响应低温胁迫的SWEET基因,茶树中CsSWEET1和CsSWEET17在低温下表达量急剧增加,CsSWEET2、CsSWEET3、CsSWEET16表达量下调[50]。SWEET基因不仅参与了低温胁迫应答的响应,也参与了高温胁迫应答的响应。高温胁迫下,水稻叶片中的OsSWEET2a表达量有着明显的变化[83]。种种现象都表明SWEET基因在植物响应高/低温逆境下发挥了重要作用,但具体的作用机理还有待进一步的研究。
激素在植物生长过程中发挥着重要作用,例如适宜浓度的ABA能够促进马铃薯形成块茎、抑制植物生长等等;GA能够促进茎的生长、促进节间伸长等,但过高浓度的激素往往会起反作用。目前已有的研究表明SWEET基因参与了激素胁迫的应答。在甘蔗中,ABA胁迫下,ShSWEET2a基因在24 h出现了明显上调,这可能与其上游启动子中相应ABA的顺式作用元件相关[12]。ABA胁迫处理下,小麦TaSWEET6基因表达量也出现了上调[78]。
在不同的逆境胁迫下,SWEET基因均出现了不同的应答反应,未来我们要进一步深入研究SWEET对逆境响应地机理,更好地将SWEET基因应用于育种,从根本上解决不良环境条件对植物产生的危害。
3 总结与展望
本研究综述了目前SWEET基因在植物中的蛋白结构、转运机制与部分生物学功能。SWEET还可以调控植物离子转运(如紫花苜蓿共生根瘤发育过程MtN3/saliva/SWEET基因在硼/钙离子平衡中可能发挥作用)、可能参与植物激素运输(如拟南芥AtSWEET13/14缺失突变体不能转运外源赤霉素)[84-85]。但是这些功能的研究仅在个别植物中有所报道,是否与植物特异性有关,有待未来进一步研究阐明。
SWEET蛋白作为植物中一类重要的糖分转运蛋白,参与了植物生长发育中的多个生理过程。目前的研究层面多数还只是集中在理论层面,对于实践层面的研究还有待加强。并且目前对于SWEET基因家族的挖掘、鉴定也仅限于几种模式植物,对于SWEET蛋白的鉴定和功能分析还需要大量的工作来阐明。未来需要综合运用各种现代研究手段,研究SWEET基因在植物营养生长、生殖生长、抗逆过程中的分子机制为分子育种提供良好基因资源,最终服务品种选育工作。
