维持性血液透析患者不宁腿综合征的影响因素
2022-07-08张蓝月田秀珣王晓华吴建华李金红薛志强谢敏妍胡明亮段文娟郑智华
张蓝月 田秀珣 雷 艳 王晓华 刘 洋 吴建华 李金红 薛志强 谢敏妍 胡明亮 段文娟 郑智华
不宁腿综合征(RLS)是维持性血液透析(MHD)患者常见的并发症[1],又称为尿毒症性RLS。但由于人们对其认识不足,易被忽视,常影响患者的生活质量和预期寿命[2]。由于MHD患者RLS的病因和危险因素尚未明确,目前还没有较好的防治手段,因此,本研究拟对珠三角地区的MHD患者进行多中心的横断面研究,以探讨RLS的影响因素,为其防治提供依据。
对象和方法
研究对象采用多中心横断面研究的方法,选择2020年7月至2020年11月在珠三角6个不同地区的血液净化中心行MHD治疗的769例患者(包括中山大学附属第七医院、中山大学附属第一医院惠亚医院、广州医科大学附属第六医院、广东省广州市番禺中心医院、广东省深圳市龙华人民医院和中山大学附属第一医院东院)。纳入标准:(1)年龄≥18岁;(2)规律血液透析3个月以上,每周至少透析2次;(3)签署了知情同意书者。排除标准:(1)合并严重感染或危重病者;(2)患有帕金森氏病[3]、周围神经病变、神经根病和类风湿性关节炎[4]等;(3)精神疾病、认知损伤或无法沟通者;(1)妊娠者及产妇[5]。退出标准:患者主动撤回知情同意书。本研究方案已获得中山大学附属第七医院医院伦理委员会批准(审批文号:KYAF/SC-07/01.0)。
研究方法(1)RLS的评估:根据国际RLS研究组织的标准[6]将患者分为RLS组和非RLS组。(2)记录MHD患者的一般资料,如人口学特征(性别、年龄)、透析龄、透析处方(透析方式、频率、抗凝剂)等。(3)记录患者的病因和药物治疗情况。(4)留取患者每周第1次透析的外周静脉血,即周一、周三、周五透析的患者于周一采血,检测血常规(白细胞、血小板、血红蛋白);血生化指标(β2微球蛋白、血糖、肝、肾功能指标);慢性肾脏病矿物质和骨异常(CKD-MBD)相关指标[血钙、血磷、全段甲状旁腺激素(iPTH)];铁代谢相关指标(铁蛋白、血清游离铁)。
统计学分析使用《SPSS 25.0》统计软件进行数据描述及分析。缺失值采用均值填补法。符合正态分布的计量资料使用均数±标准差描述,组间比较采用独立样本t检验;不符合的选用中位数 (Q1,Q3)表示,组间比较采用Mann-Whitney U检验。计数资料使用频数或百分比(%)描述,组间比较采用χ2检验、连续校正的χ2检验或Fisher精确概率法。使用二元Logistic回归分析尿毒症性RLS的各影响因素:首先进行单因素分析,再将结果中P<0.1的变量纳入多因素分析。P<0.05为差异有统计学意义。
结 果
一般资料珠三角6个透析中心共769例MHD患者,最终有527例被纳入研究,其中男性288例(54.6%),中位年龄57.0(47.0,67.0)岁。RLS 38例(7.2%),其中男性22例(57.9%),中位年龄54.0(45.0,61.0)岁。
差异性分析显示,RLS组的透析前血磷(P=0.005)和尿素氮(P=0.008)水平显著高于非RLS组,但两组患者间的人口学特征(性别、年龄)和透析龄、透析处方、高血压患病比例均无显著差异,其余肝、肾功能、血糖及血红蛋白等指标等均无显著差异(表1)。
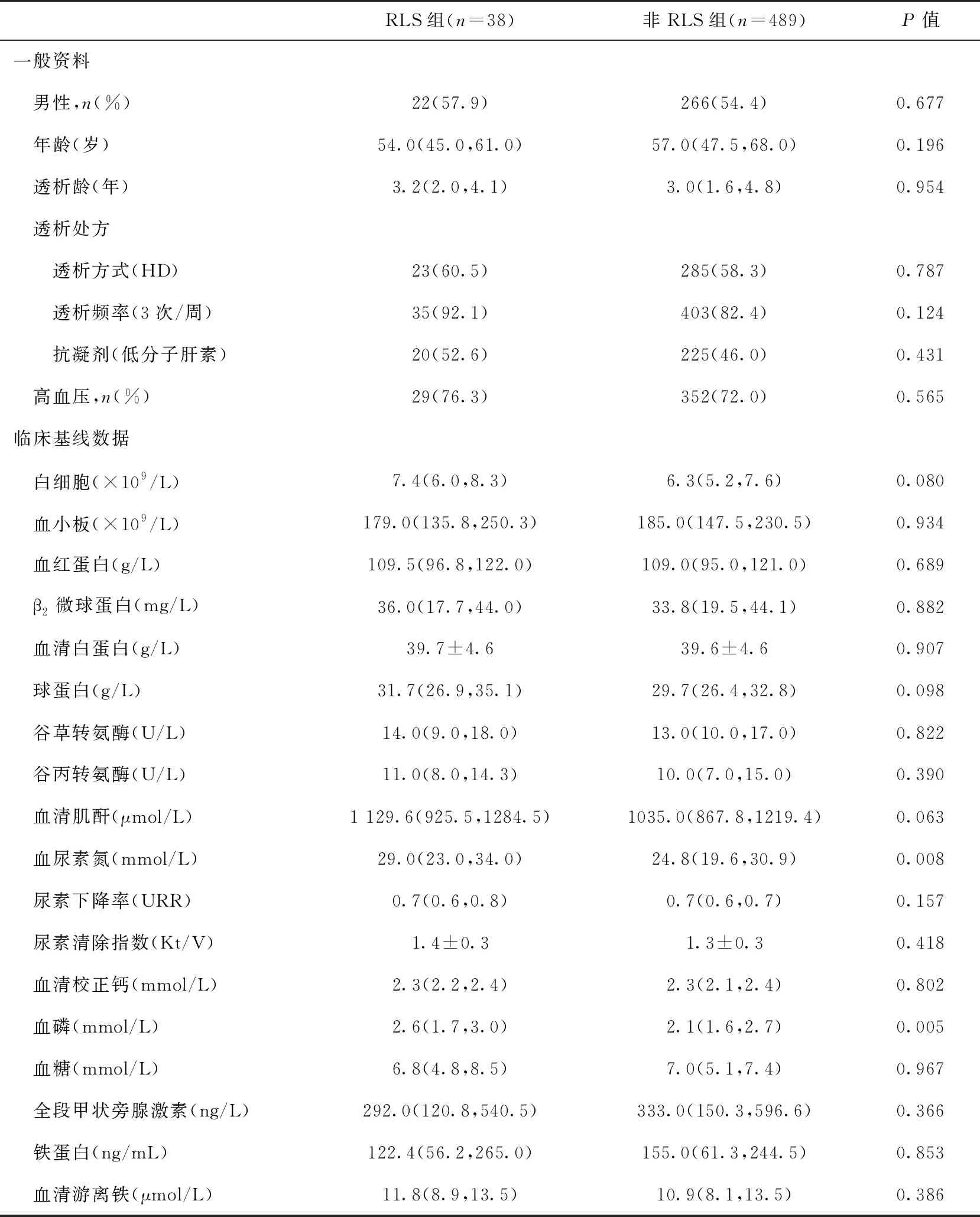
表1 两组间患者一般资料与临床检验参数比较
病因及药物治疗差异性分析结果提示,RLS组以高血压肾损害为原发病的患者比例显著高于非RLS组(P=0.005)。RLS组服用镇静安眠类药物的患者比例更高(P=0.002),其余药物如钙剂等在两组患者间则未见统计学差异(表2)。
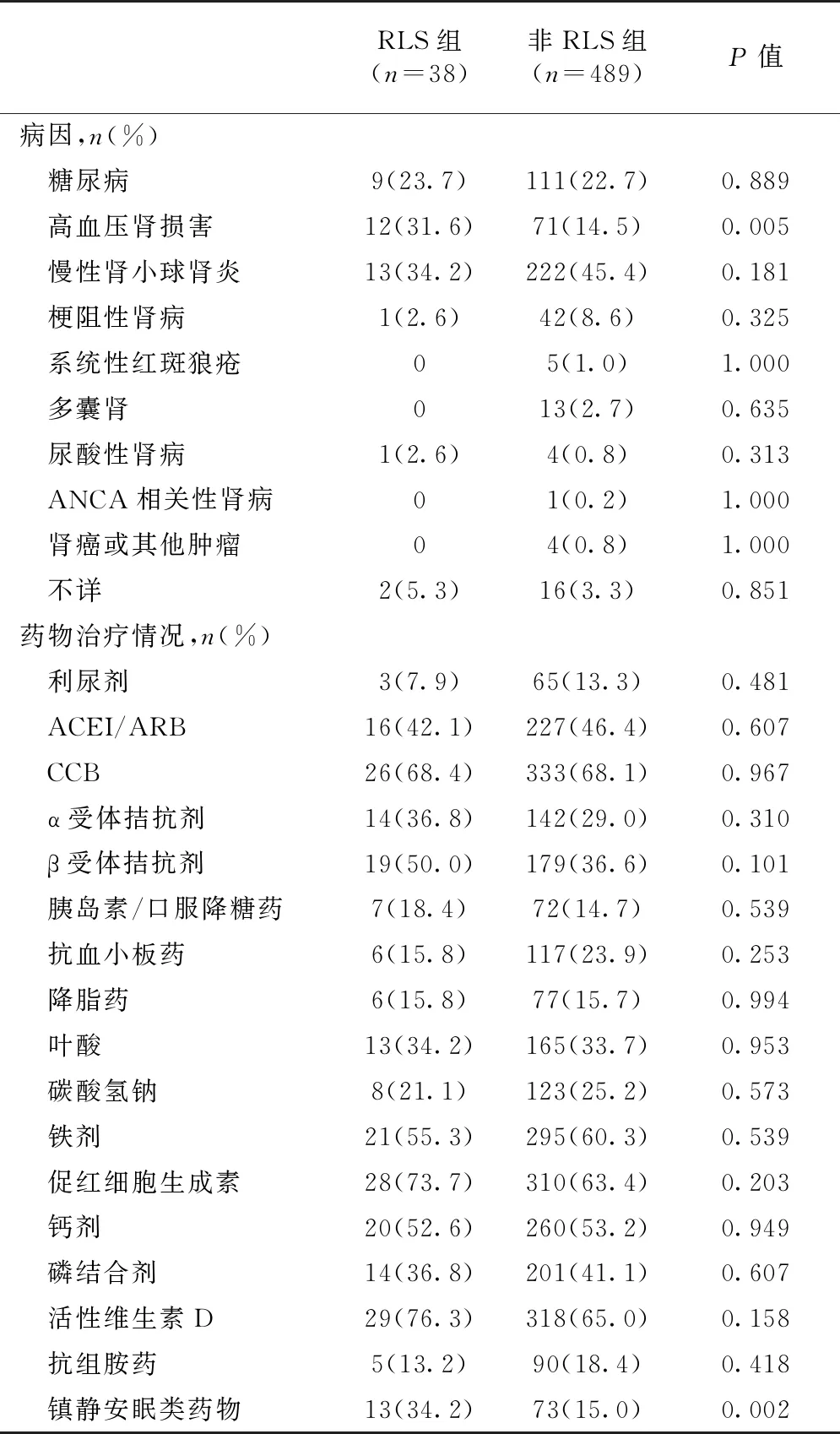
表2 两组间患者病因与药物治疗比较
RLS的独立影响因素分析以是否患RLS为因变量做二元Logistic回归分析,先进行单因素分析。结果提示,白细胞计数(P=0.090)、透析前血清肌酐(P=0.092)、血磷(P=0.004)水平及高血压肾损害(P=0.007)均是RLS的危险因素;对以上变量进一步采用多因素分析,结果提示,血磷水平(OR=1.709,95%CI 1.121~2.607,P=0.013)和高血压肾损害(OR=2.790,95%CI 1.311~5.938,P=0.008)是MHD患者患RLS的独立危险因素(表3)。
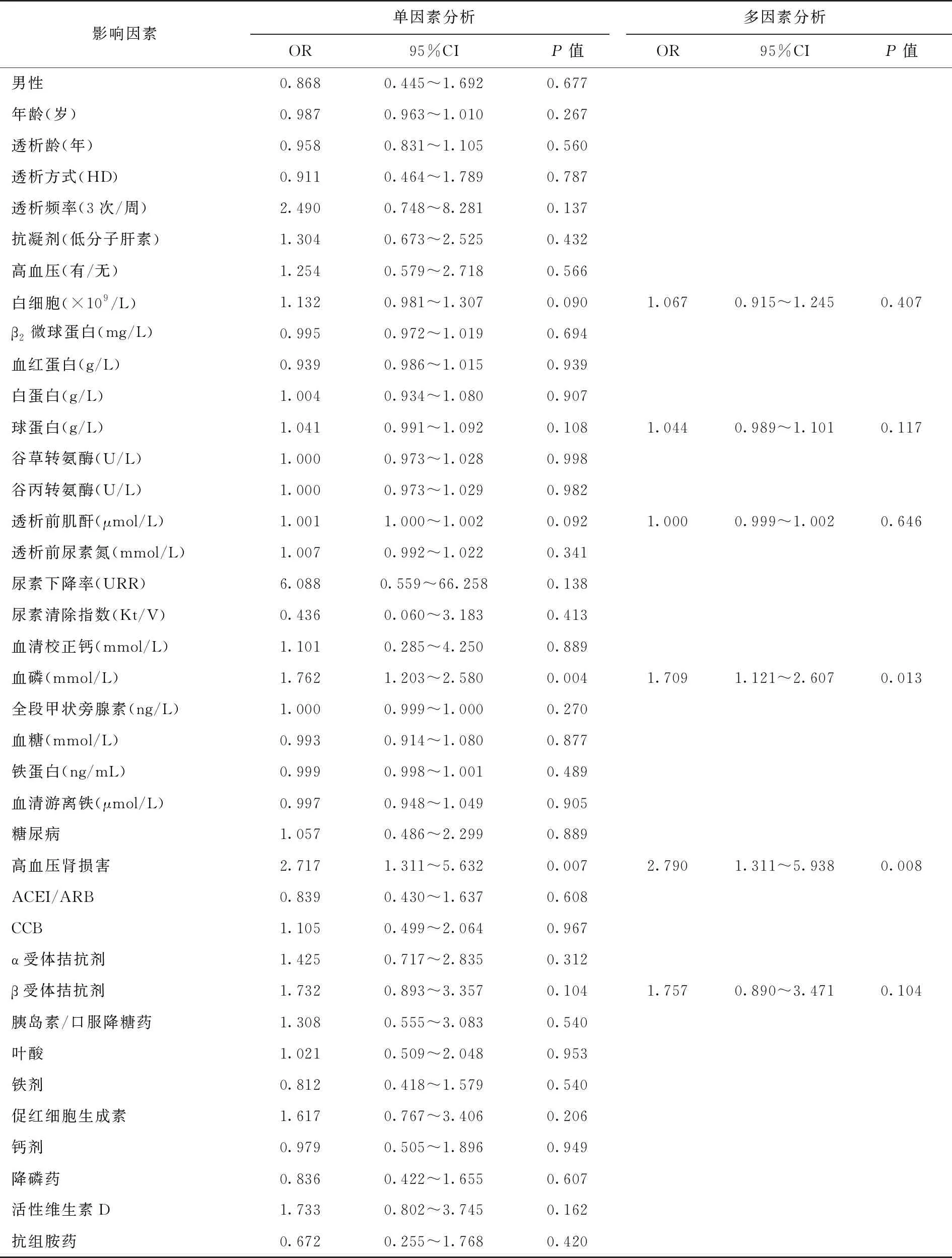
表3 维持性血液透析患者不宁腿综合征的影响因素分析(二元Logistic回归)
讨 论
目前中国慢性肾脏病(CKD)患者约有1.2亿,且有近百万CKD患者进入了MHD[7],这对社会和患者均造成了严重的经济负担。由于透析技术的改善,患者的生存率明显提高,但其生存质量仍然较差[8]。 MHD常见的并发症如心脑血管疾病、CKD-MBD及肾性贫血等已广受重视,但RLS、瘙痒、失眠、抑郁等精神神经方面的并发症研究较少,虽然目前已有越来越多的学者开始关注,但尚无较好的防治方法。
RLS是神经元的运动感觉失调障碍,患者有强烈活动双腿的冲动和不适感,这些症状在休息时或者夜间加重,并可在活动后暂时减轻[6]。RLS更多的是会给患者带来精神抑郁、生活水平下降等痛苦。RLS病因十分复杂,各个研究得出的影响因素常互相矛盾,尚无明确结论[2,4,9-11]。
本研究中,MHD患者RLS的患病率为7.2%,说明其在MHD患者中是一个不可忽视的并发症,与国外同类研究得到的12%~25%相比略低[12]。或许反映了珠三角地区的医疗技术及随访管理比较完善,患者的依从性好,并发症相对较低。Lin等[13]比较了各个地区同类研究得出的患病率,也发现不同血液透析中心的不同管理策略可能解释这一差异。种族差异也可能是影响因素之一[14]。
本研究结果表明,血磷可作为尿毒症性RLS的独立危险因素,这与之前的研究结论一致[9,15-16]。我们推测高血磷水平可导致CKD-MBD,诱发或加重RLS。值得注意的是,以往研究表明,采用血液透析滤过(HDF)可降低透析患者的骨代谢指标[17],因此,CKD-MBD对RLS的影响可能是一个很有意义的课题,需要更深入地研究。
高血压肾损害也是MHD患者发生RLS的独立危险因素。我们推测,高血压相关的交感神经激活和代谢失调等因素在RLS的发生发展中起到了关键作用[18]。同类研究也提示,RLS患者发生高血压或心血管疾病的风险超过了非RLS患者2倍以上[19]。因此,控制患者的血压十分重要,并有必要进一步探讨血压在尿毒症性RLS中的作用机制。
研究提示, RLS组的MHD患者透析前尿素氮水平明显高于非RLS组,这与Kim等[20]的报道一致。但本研究未能证实尿素氮是否是RLS的独立影响因素,可能原因之一是其水平很容易受到蛋白质的摄入量、人体体积和能量代谢的影响。
许多研究均表明,糖尿病患者患RLS的比例较高,是RLS可能的危险因素[21-23],还需要更深入的临床研究和机制探讨。此外,失眠作为RLS的诊断依据之一[6],常严重降低患者的睡眠质量。本研究的MHD患者主要是由于出现了失眠和焦虑等症状而服用镇静安眠类药物,其中RLS组的用药比例显著高于非RLS组,反映了RLS对患者睡眠的负面影响。失眠作为MHD患者另一个重要的并发症,本课题组其他成员正在进行相关的研究。
目前,国内大多数关于尿毒症性RLS的临床研究样本数较少,且多为单中心研究。本研究为地区性多中心研究, 两组MHD患者间的药物治疗情况基本无差异,提示各个血液透析中心的治疗方案异质性较小,结果较可靠。但是,本研究存在橫断面观察性研究所共有的局限性,因此还需做进一步的前瞻性队列研究来证实。
综上所述,RLS是MHD患者不可忽视的并发症,其发病机制不明,防治效果不佳。高血磷水平及高血压肾损害可能是MHD患者患RLS的独立危险因素,找出并研究以上各种因素对尿毒症性RLS的影响,可为RLS的机制探讨及临床实践提供重要依据,并改善患者的生活质量,提高其长期生存率。
