饮品中苯甲酸和山梨酸的检测
2022-07-05邬学清高晓博
邬学清 高晓博 金 宏
(集宁师范学院 化学与化工学院,内蒙古 乌兰察布 012000)
1 引言
1.1 研究意义
目前,食品安全问题备受社会瞩目,而食品添加剂含量也是关注点。其中苯甲酸、山梨酸是食品中常用的添加剂和防腐剂[1]。苯甲酸是酸型食品防腐剂的一种,能抑制霉菌、酵母和细菌在酸性条件下的生长[2]。山梨酸也能抑制霉菌、酵母菌和好氧性细菌的生长活性,二者都能达到食品防腐目标,但是两者均不能食用过多和经常食用,否则会影响人体健康[3]。
根据资料,苯甲酸慢性中毒会导致头痛、晕眩、记忆力急剧下降、失眠、乏力、神经衰弱等症状;有的可能会导致体内免疫细胞数量降低,造成再生障碍性贫血[4]。一般认为,适量添加苯甲酸并不会在人体形成积累,是相对安全的。但是,苯甲酸能损坏细胞膜有序结构,使细胞膜的功能发生紊乱,干扰细胞内的各种平衡机制,使人体内各组织系统功能紊乱,出现呕吐、腹痛和心率变快等严重征状[5],所以食品、饮品相对安全不可忽略;虽然山梨酸(钾)能够对霉菌、酵母菌和好氧性细菌的活性产生抑制作用,还能防止肉毒杆菌、葡萄球菌、沙门氏菌等有害微生物的生长和繁殖[6]。但是经常食用含有过量山梨酸的饮品,在一定情况下会抑制骨骼生长,对肾脏和肝脏造成损伤[7]。目前已经将山梨酸列入国家食品安全检测项目。
饮品是以水为原料,用不同配方制作而成供人们经常饮用的液体食品,不同的成分饮料对人体有着不同的作用,有的以补充人体水分为主,有的以缓解人体疲劳为主,有的含有丰富的维生素,有的还具有抗疲劳作用[8]。它的制作原料有蔬菜、水果、乳品类等,商家为保障储存、运输会适当加入防腐剂和添加剂,由此市场饮品有可能存在安全隐患。苯甲酸和山梨酸是饮品生产一般防腐剂,GB2760-2008 中明确规定饮料类山梨酸最大使用量0.5 g/kg、苯甲酸最大使用1 g/kg[9],可见对不同饮品苯甲酸和山梨酸的检测是食品安全检测的重要项目[8]。
1.2 研究现状及目的
如今,对于饮料中的苯甲酸和山梨酸含量的测定方法有多种,其中主要有高效液相色谱法和气相色谱法[9]。色谱法准确度高,但除了使用仪器价值高之外,还由于使用色谱柱填充料和流动相的特殊,使检测成本较高。梁奇峰教授等应用的比值倒数光度法,在不经分离的情况下,同时测得吸收光谱重叠严重的苯甲酸和山梨酸两组分的含量,此方法使用仪器简单,操作方便,广泛用于苯甲酸、山梨酸含量测定,但是数据处理复杂[10]。针对以上情况,对市场上不同饮品中的苯甲酸及山梨酸进行了抽样检测,一方面了解市场供应产品的质量安全指标,另一面为相关食品检测机构提供方便、经济、适用的检测方法。
1.3 研究思路及方法
苯甲酸具有芳烃结构,其吸收光谱在波长228 nm和272 nm处有K吸收带和B吸收带,且在非极性溶剂中B吸收带具有精细结构,随溶剂极性增大吸收带以一定的规律发生变化。山梨酸具有α、β不饱和羰基结构,在250 nm处有π跃迁的K吸收带[11]。综上所述,可以通过绘制物质溶液的紫外吸收光谱图,并在相同条件下与标准物光谱图进行比对,从而进行定性、定量分析。由于苯甲酸在水中溶解度小,而且容易升华;山梨酸难溶于水,所以本实验通过乙醚萃取和恒温蒸馏纯化饮品中的苯甲酸和山梨酸,在碱性条件下使其转化为可溶性的钠盐,利用紫外吸收分光光度法绘制它们的吸收光谱,确定最佳测定波长,利用分光光度法中的外标法定量测定苯甲酸和山梨酸的含量。
2 实验部分
2.1 主要仪器及试剂
756S 型紫外可见分光光度计(上海棱光技术有限公司),FA2204B 电子天平(上海精密科学仪器有限公司),HH-2 数显恒温水浴锅(江苏金坛市荣华仪器制造有限公司),分液漏斗,蒸馏装置等仪器。
碳酸氢钠(分析纯),天津市化学制剂三厂;苯甲酸(分析纯),天津市风船化学试剂科技有限公司;山梨酸(化学纯),国药集团化学试剂有限公司;乙醚(分析纯),上海马陆制药厂;氯化钠(分析纯),国药集团化学试剂有限公司;无水硫酸钠(分析纯),天津市塘沽邓中化工厂。
2.2 溶液的配制
2%的NaHCO3配制:称取40 g NaHCO3溶解稀释到2000 mL 作为溶剂。
82.4 mg/L 苯甲酸标准储备液的配制:称取苯甲酸0.0206 g 于50 mL 烧杯中,以2% NaHCO3溶解转移至250 mL 容量瓶中准确定容,待用。
25.0 mg/L山梨酸标准储备液的配制:精确称取山梨酸0.0625 g置于50 mL烧杯中,以2%NaHCO3为溶解转移至250 mL 容量瓶中准确定容,为250 mg/L 标准储备液,再准确移取山梨酸标准储备液10mL 准确稀释到100 mL 待用。
苯甲酸系列标准溶液的配制:分别移取1.00 mL、2.00 mL、3.00 mL、4.00 mL、5.00 mL 的苯甲酸储备液于5 个50 mL 的容量瓶中,然后用2%的NaHCO3溶液定容至刻度,摇匀,静置,得到苯甲酸系列标准溶液(浓度间隔为1 mg/L)。
山梨酸标准系列溶液的配制:分别移取0.50 mL;1.00 mL;1.50 mL;2.00 mL;2.50 mL 的山梨酸储备液于5 个50 mL 的容量瓶中,然后用2%的NaHCO3溶液定容至刻度,摇匀,静置,得到山梨酸系列标准溶液(浓度间隔为0.5 mg/L)
苯甲酸-山梨酸的混合溶液的配制:移取苯甲酸B1(1.00 mL);B2(2.00 mL);B3(3.00 mL);B4(4.00 mL);B5(5.00 mL)至50 mL 容量瓶中,按照下表移取山梨酸S1(0.50 mL);S2(1.00 mL);S3(1.50 mL);S4(2.00 mL);S5(2.50 mL)至相应的50 mL 容量瓶中,用2%% NaHCO3定容至刻度,摇匀,作为标准混合系列溶液,待用。
2.3 样品的来源
随机购买商品饮料:怡泉柠檬味汽水(2018.8.17)可口可乐公司;浩明苏打水(2018.5.30)北京浩明品牌管理有限公司;可乐(2018.11.16)可口可乐公司;雪碧(2018.8.13)可口可乐公司;美年达(青苹果味2018.8.17)百事公司。
2.4 实验方法
2.4.1 样品中苯甲酸、山梨酸的提取
取2.3 中各样品20.00 mL,放于小烧杯中加入1mL 的HCl(6 mol/L)酸化,然后放置在250 mL分液漏斗中,依次用30 mL、20 mL、20 mL 的乙醚各萃取一次,每次萃取后都静置5 分钟。待分液漏斗中静置分层,将上层乙醚提取液转移到小烧杯中。合并3 次萃取液用5mL 的HCl 和NaCl 混合溶液洗涤,然后加入适量的无水硫酸钠用作吸收残余水份,搅拌,恒温加热到40℃,45 分钟后将其中残留乙醚蒸发出去,用2.0% NaHCO3 溶液溶解,移至100 mL 容量瓶中定容,待用。
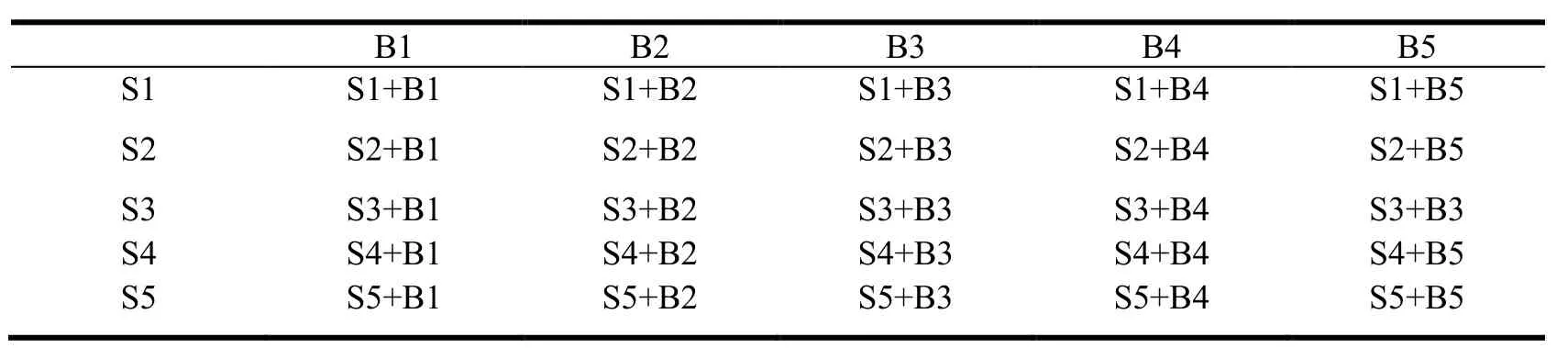
表1 山梨酸苯甲酸混合系列溶液
2.4.2 样品中苯甲酸含量的检测
移取苯甲酸1.00 mL、2.00 mL、3.00 mL、4.00 mL、5.00 mL 分别放置在5 个50 mL 的容量瓶,再分别依次准确滴加山梨酸1.00 mL,用2% NaHCO3定容。利用双波长分光光度法,在测定λ2 为230 nm;参比λ1 为276 nm 的条件下,绘制测定苯甲酸的标准曲线,线性方程为c=10.0695A-0.2677;相关系数r 为0.9995;线性范围为1.6 mg/L~8.0 mg/L;检出限量0.028 mg/L。准确移取2.4.1 中处理好的各样品提取液直接测量或稀释5 倍后测量其吸光度并计算其浓度。
2.4.3 样品中山梨酸含量的检测
移取山梨酸0.50 mL、1.00 mL、1.50 mL、2.00 mL、2.50 mL 分别放置在5 个50 mL 的容量瓶,再分别依次准确滴加苯甲酸3.00 mL,用2% NaHCO3定容。利用双波长分光光度法,在测定λ2 为255 nm;参比λ1 为276nm 的条件下,绘制测定山梨酸的标准曲线,线性方程为c=6.5135A+0.1726;相关系数r 为0.9999;线性范围为0.25 mg/L~5 mg/L;检出限量0.04 mg/L。准确移取2.4.1 中处理好的各样品提取液直接测量或稀释5 倍后测量其吸光度并算出其浓度。
3 结果与讨论
3.1 吸收光谱的绘制
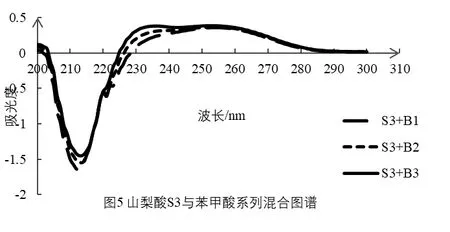
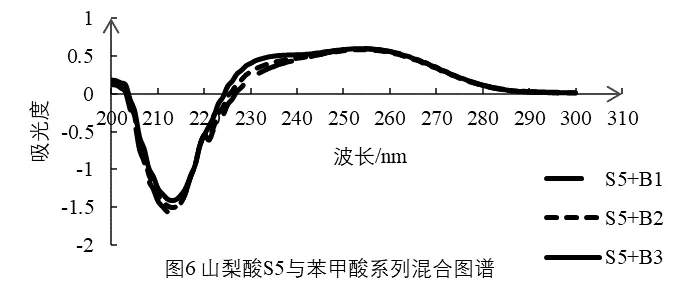
用2% NaHCO3 溶液作为参比,分别测定苯甲酸、山梨酸系列标准溶液以及二者系列混合溶液的紫外吸收光谱(扫描范围为200~300 nm,波长间隔为1 nm,扫描速度为中速,扫描间隔为0.5 nm)。根据光谱图的峰值变化或光谱图比较确定苯甲酸、山梨酸的定量测定波长。具体见图1 至图9。
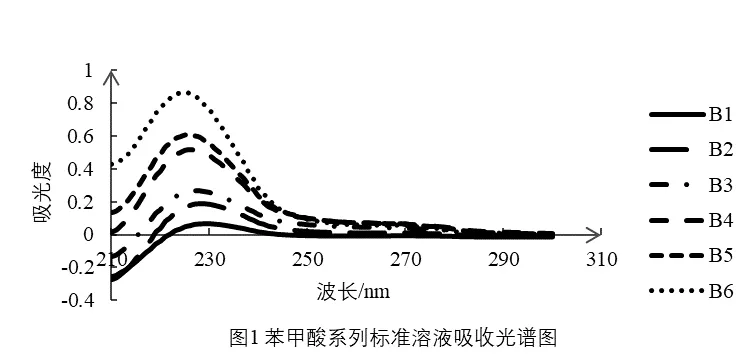
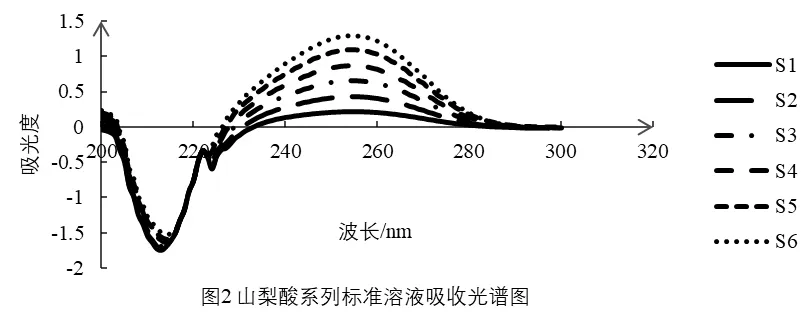

3.1.1 苯甲酸测定波长的确定
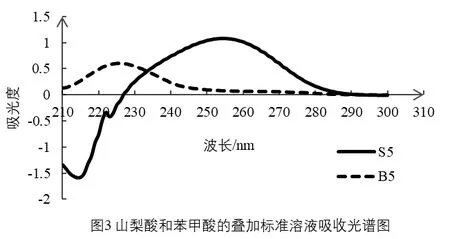
由图1、图2可知,随浓度的增大苯甲酸系列标准溶液的最大吸收波长有蓝移现象,而山梨酸的最大吸收波长随浓度增大无变化,苯甲酸的最大吸收波长225 nm处山梨酸有负吸收,在山梨酸的最大吸收波长255 nm处苯甲酸有正吸收,可见它们在最大吸收波长处都各有相互干扰,所以不能在它们最大吸收波长处进行分别测定。根据双波长分光光度法,吸收光谱相互重叠的两组份共存时可测定一种物质,而把另一种物质作为干扰物,所以在苯甲酸的测定波长处找山梨酸的等吸收波长。由图3可知,山梨酸在苯甲酸的最大吸收波长处有负吸收,难以确定等吸收波长;根据系数倍率法的原理也无法确定合适的参比波长[12],而在苯甲酸吸收波长227 nm处有山梨酸的等波长点,但是随苯甲酸含量的变化,吸光度变化不均匀。由图2、图4、图5、图6可知,在230 nm处吸光度随苯甲酸浓度均匀变化,在276 nm处吸光度随山梨酸浓度的均匀变化而变化,因此苯甲酸测定可利用230 nm为测定波长,276为参比波长;以系列混合溶液绘制标准曲线进行苯甲酸含量测定。所有混合系列所得线性方程相关性很好,线性方程的斜率和截距相差不大,具体见表2。
3.1.2 山梨酸测定波长的确定
根据吸收光谱相互重叠的两组份共存时,双波长测定规则,测定山梨酸,把苯甲酸作为干扰;山梨酸的最大吸收波长处苯甲酸的等吸收波长有286 nm、225 nm,具体见图3。根据双波长选择规则,当两波长距离相近时,可认为背景吸收是相等[12],待测组份吸收差最大。所以选择测定波长是255 nm,参比波长为286 nm,测定山梨酸系列溶液吸光度,并绘制标准曲线,显示线性方程相关性极差;由图7、图8、图9可知在255 nm处山梨酸的吸光度随均匀浓度变化。在276 nm处苯甲酸吸光度也随浓度均匀变化,因此,选择山梨酸的测定波长255 nm,参比波长276nm进行多组份混合液中山梨酸的测定,测定系列混合溶液吸光度,并分别绘制标准曲线,各线性方程的斜率、截距基本相同,相关系数符合分析测定一般要求,具体见表2。
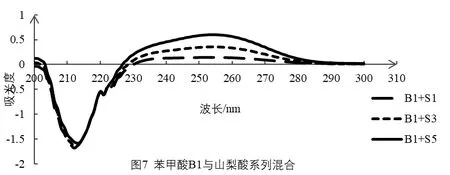
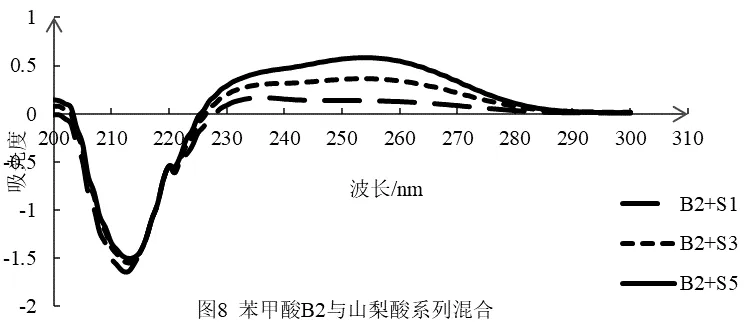
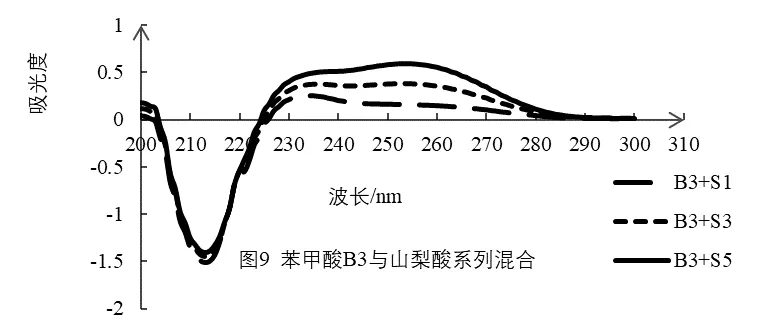

表2 线性方程及相关系数的比较(X=1、2、3、4、5)
3.2 样品中苯甲酸、山梨酸的测定
用2.4.1的提取方法对五种样品各取两份提取处理后,用2.4.2、2.4.3苯甲酸和山梨酸的测定方法,对每一提取液各平行测定5次,同一样品的两份测定结果通过F、t检验都不存在显著性差异(95%的置信度),所以数据处理结果为两份提取液的平均值,利用合标准偏差进行精密度分析,即测定次数为10,自由度为8计算合标准偏差[13];将B3+S3苯甲酸与山梨酸混合液在相应的线性方程下进行3次准确度测定,苯甲酸相对误差为+2.2%、山梨酸的误差是+9.3%(真值:苯甲酸4.94 mg/L山梨酸0.75 mg/L),结果见下表3。将各种饮料密度以1g/mL折算计算,五种饮料中防腐剂苯甲酸、山梨酸均无超标。测定方法供饮品质量检测参考使用或进一步验证。
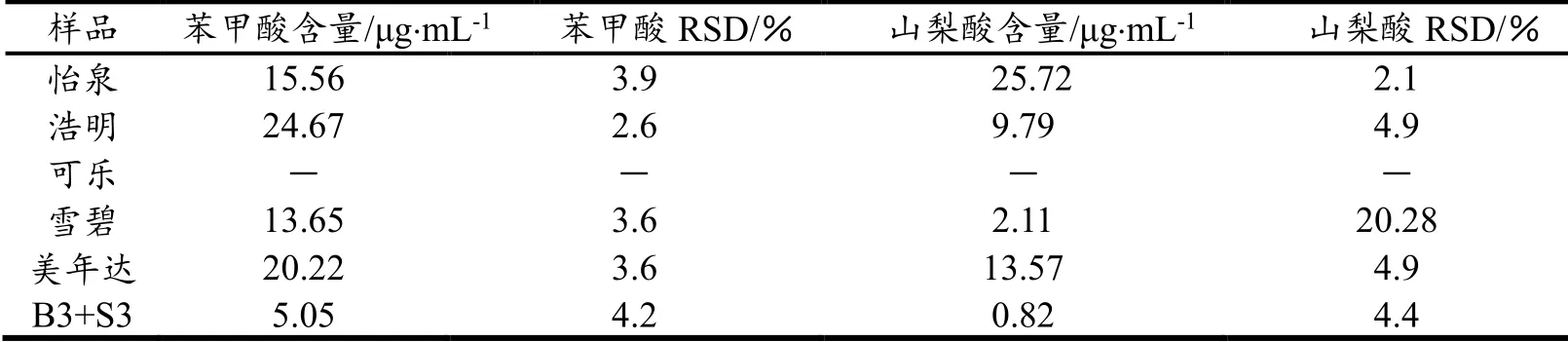
表3 样品测定数据及结果分析
