玻耳兹曼熵的演变过程
2022-06-30苏都毕力格
苏都毕力格,咏 梅
(内蒙古师范大学 科学技术史研究院,内蒙古 呼和浩特010022)
玻耳兹曼(Ludwig Boltzmann,1844—1906)是奥地利物理学家、哲学家,统计力学奠基人之一,他的贡献主要集中于气体理论,晚年继任马赫从事哲学研究。其气体理论研究包括从热力学第二定律的力学阐释转向麦克斯韦分布律的推广及非平衡态过程研究,逐步深入到热力学第二定律的统计力学解释,进一步提出著名的玻耳兹曼熵关系式。玻耳兹曼在气体动理论过程中采用的离散值方法,与19 世纪活跃的连续能量为基础的研究方式有差异,这正是“量子”概念的雏形。
物理学知识一方面来源于实验观察归纳总结,另一方面来自数理演绎推理。19 世纪之前热学研究以生活或实验现象获得理性认识并归纳总结出普遍规律,19 世纪开始热学研究先理论演绎而后实验验证。玻耳兹曼采用理论演绎方法开展研究工作。当时经典力学理论体系雄厚强大,物理学家们相信一切热学现象都能用力学理论描述,然而克劳修斯(Rudolf Julius Emanuel Clausius,1822-1888)、麦克斯韦(James Clerk Maxwell,1831—1879)、玻耳兹曼将概率统计思想引入物理学研究,开启新的理论研究方式。玻耳兹曼用这种研究方式完善他毕生为之奋斗的气体理论,尤其熵概念的统计解释最为深入人心。斯蒂芬·乔治·布鲁什(Stephen G.Brush)、马丁·克莱恩(Martin J.Klein)、爱德华·E·多布(Edward E.Daub)、亚历山大·巴赫(Alexander Bach)等都是著名物理学史家,对玻耳兹曼深有研究。斯蒂芬·布鲁什在《气体动理论》《热运动理论发展史》[1-2]中梳理了18、19 世纪气体理论和热学理论发展史,大量篇幅探讨了玻耳兹曼的气体动理论研究工作,认为玻耳兹曼的研究工作是19 世纪物理学和20 世纪物理学的桥梁。此外《玻耳兹曼统计思想的发展》《概率和热力学:热力学第二定律的简化》《玻耳兹曼1877 年的概率分布》等[3-5]文章也阐述玻耳兹曼统计的发展、演变。另外,玻耳兹曼传记《笃信原子的人》[6]以及《玻耳兹曼熵与统计规律的建构初探》[7]、《热力学第二定律的微观解释与统计思想的引入》等文章探讨了玻耳兹曼统计思想观念。玻耳兹曼对熵概念的统计解释经历的过程,在此期间玻耳兹曼的量子化观念鲜为人知。本文以玻耳兹曼的论文集和国内外玻耳兹曼研究文章、著作为基础,重新梳理玻耳兹曼提出著名熵关系式的历史线索和熵概念统计解释历程,探讨伟大探索者思想的萌生和变迁。
1 玻耳兹曼对热力学第二定律(熵)的力学解释
19 世纪60 年代,气体理论研究在维也纳非常活跃。计算出分子大小的洛喜密脱(Joseph Loschmidt,1821—1895)在维也纳大学从事研究工作。此时玻耳兹曼正在维也纳大学求学,深受导师斯忒番(Josef Stefan,1835—1893)和洛喜密脱的影响进而开展他的研究工作。
1865 年克劳修斯明确提出熵概念后不久[9],1866 年玻耳兹曼发表《论热力学第二定律的力学意义》[10],文中提到热力学第一定律和活力(动能)原理已被接受,热力学第二定律也被提出,但没有一个明确证明。玻耳兹曼试图对热力学第二定律给出一种数学解析证明并予以相应的力学意义。
《论热力学第二定律的力学意义》第一部分解决了温度概念问题。温度表示物体的冷热程度,人们已经可以借助温度计来测量,但玻耳兹曼认为温度没有一个精确一致的微观定义,尤其不确定温度与分子运动之间有何联系。因此,需要研究分子运动的哪些物理量与温度有关联。
伯努利碰撞理论提出之后,温度概念也不断深化。赫拉帕斯(John Herapath,1790—1868)明确提出温度取决于分子运动的思想,克劳修斯也认为温度是分子动能的平均值。玻耳兹曼相信即使是在热平衡状态下,系统内部分子相互碰撞,分子速度发生变化,分子过一段时间后总能回到同一位置,且速度大小方向相同,并且此后以类似的方式循环运动。假设运动时间段为t2-t1,则该分子温度为

式中T表示温度,表示分子动能。玻耳兹曼认为温度是原子运动的时间平均值,表明他已经接受统计学思想。
玻耳兹曼用动能守恒定律逐步推导了温度定义式。然而玻耳兹曼对温度的解释思辨性强,因而他的温度定义普适性受到局限。
玻耳兹曼的观点为:宏观量(温度)是相应微观量(分子动能)的长时间平均值,而微观量随时间的变化遵循力学规律。按照这种观点原则上可以解决宏观性质,但由于系统粒子数巨大,运动轨迹极复杂,找寻众多粒子的运动规律遇到困难。
在《论热力学第二定律的力学意义》第四部分中,用力学原理论证热力学第二定律。克劳修斯提出的热力学第二定律为克劳修斯定义的熵用于说明物理过程的方向性,而玻耳兹曼探寻熵的微观意义。
相互碰撞过程中,各个原子得到微小的能量ε之后都改变其运动增加其动能。即使在刚开始没有多大变化,过一段时间总有动能的增加。进而系统的压力和体积都有微小的变化,每个原子的轨迹也发生改变[10]24-25。
在一次循环过程中,计算原子动能变化的时间平均值,得到如下关系

再利用(1)式所得T值,则得

如果使物体保持一定温度,并假设把总热δQ均分给了各部分,那么总和

如果物体的温度各小部分不同,拆解成相同小单元dk,再求积分得到表达式对δQ积分,则得

这是玻耳兹曼最初得到的熵表达式,其中log 指的是自然对数ln。玻耳兹曼用力学运动方程得出熵关系式,但力学运动方程都是时间对称的,因此这并不能有力说明不可逆性问题。
玻耳兹曼1866 年的文章显然尝试着用纯力学原理给出熵的数学解析证明[10]。玻耳兹曼起初认为热力学第二定律可以用力学原理解释,主要是因为力学为研究纲领解决热学问题是当时主流研究方法。力学定律甚至应用于解决热学、电学等问题。
在伽利略时代以后的200 年间,这样一种企图有意识地或无意识地表现在几乎所有的科学著作中。亥姆霍兹(Hermannvon Helmholtz,1821—1894)约在19 世纪中叶把它表达得特别清楚:物理科学的任务,在我们看来,归根结底在于把物理现象都归结为不变的引力或斥力,而这些力的强度只与距离有关。要完全了解自然,就得解决这个问题[11]。
力学研究纲领在热学和气体动理论中应用的局限性在于力学原理去描述大量分子的碰撞会遇到无法克服的困难。就像日本科学史家广重彻(Tetu Hirosige,1928—1975)所说:“从今天的观点来看,这种处理极不充分,更重要的是缺乏统计考察。”[12]说明玻耳兹曼最初的尝试受到当时物理学家们研究思路的限制。
概率统计方法应用于物理学与经典力学分析方法有区别,是一种新兴的思考方式。可见玻耳兹曼本人也意识到了热力学第二定律力学解释的局限性,1866 年之后玻耳兹曼的文章采用概率统计。
2 玻耳兹曼推广麦克斯韦速度分布律
1860 年麦克斯韦发表了《气体动理论的解释》[13]。这篇论文中,麦克斯韦把分子类比成完全弹性球,分子很小、坚硬、完全弹性,只有碰撞时相互作用。麦克斯韦把气体内部运动与弹性球碰撞力学规律类比。事实证明,类比方法更易于理解问题、解决问题,对科学家本身也更方便。
克劳修斯、麦克斯韦都认为这些大量分子相互碰撞之后各个方向的概率相等,每次碰撞都改变速度,一定时间过后动能被分配到各个分子。麦克斯韦研究气体动理论的突出成果在于给定速度范围分子数的计算,计算出速度在v与v+dv之间的分子数其中N为弹性球的总数目,α是有关于平均速度的常量。
1866 年麦克斯韦又发表《关于气体动理论》[14]。以上两篇文章中麦克斯韦提出并证明麦克斯韦速度分布律,并用这个理论解释黏性、扩散、热传递现象。麦克斯韦速度分布率描述了处于平衡态系统分子运动的统计规律,甚至以此有效地解释一些自然现象。
1866 年之后,玻耳兹曼将注意力转向研究麦克斯韦速度分布律。1868 年玻耳兹曼发表《运动质点活力平衡的研究》[10]49-96。玻耳兹曼这篇论文目的是分析热力学平衡的性质。论文中将麦克斯韦速度分布定律推广为外场作用下麦克斯韦‐玻耳兹曼速度分布率。玻耳兹曼坚信各态历经假说(ergodic hypothesis):在长时间的过程中,分子坐标和速度的所有可能值都应符合气体的固定总能量[3],在此基础上拓展平衡态速度分布函数的意义。尤其重要的是1868 年玻耳兹曼的文章出现Quantum[10]49-96,可见他的思路是创新的,是他后续研究的萌芽。1877 年玻耳兹曼的文章中进一步解释他所说“量子”的意义[17],他认为气体分子相互影响,即气体分子运动存在关联性。
在非常大的封闭区域内有n个质点,其质量m1,m2,…,mn,速度c1,c2,…,cn,在某种力的作用下在极小的范围内运动。质点的速度介于有限范围之内,不仅仅是由概率决定。第二个质点取决于第一个质点的速度,最后一个质点的速度完全由(n-1)个质点的速度决定,因为整个系统的能量恒定[10]80-81。
1871 年玻耳兹曼争优先权发表一篇论文声称,1870 年克劳修斯关于热力学第二定律的解析证明与他1866 年的文章基本一致[10]228-236,所得到的熵关系式

玻耳兹曼用mc Ti代替公式(1)中的玻耳兹曼认为式(6)与克劳修斯所得到的熵相符。克劳修斯承认玻耳兹曼的优先权,同时提出熵概念的这种解释的缺陷,应该考虑系统的势能变化对粒子内部运动的影响[4]。玻耳兹曼采纳了克劳修斯的建议并在之后的研究工作中纠正。
1871 年玻耳兹曼的主要工作在于推广麦克斯韦速度分布律,寻求普适规律。1871 年《关于多原子气体分子之间的热平衡》这篇文章中提道:
如果每个气体分子都是一个质点,麦克斯韦已经确定了不同运动状态的概率。在这种情况下,一旦知道分子速度的大小和方向,分子的状态就完全确定。当然,因为空间中每个速度方向都同样可能,你只需要确定速度不同大小的概率。…当我们把分子视为某些内部力作用下几个原子构成的系统时,我们似乎更接近于真理[10]237。
玻耳兹曼肯定麦克斯韦的成果,同时认为应该推广麦克斯韦速度分布律。因为在自然界中发现的气体分子不是单原子,有必要进一步研究把麦克斯韦速度分布律扩展到多原子构成的分子运动,建立通用定理。
1871 年另一篇文章《关于热平衡一些一般陈述》中,玻耳兹曼在麦克斯韦速度分布律之中加入势能的因素“系统包含的功(系统内能)等于平均活力(动能)和平均势能的总和”[10]258-287。玻耳兹曼扩展麦克斯韦速度分布律,使得这种描述自然现象更接近真实自然界中的气体运动。此后,玻耳兹曼在《从活力平衡命题对热力学第二定律解析证明》这篇文章中将麦克斯韦速度分布律应用于热力学第二定律的证明中,推导出熵[10]288-308

式中用T表示温度,λ表示分子数量,v是体积。1871 年玻耳兹曼做出关键性的突破,然而1871 年的文章很少受到学界关注[4]。这篇文章的深远历史意义在于探索热力学第二定律的微观意义,1872、1877 年玻耳兹曼推导熵关系时,总是将每一个新进展与方程(7)联系起来。1871 年熵概念发生变化,最终在玻耳兹曼1877 年的文章中有力解释熵与概率的关系。
3 玻耳兹曼对热力学第二定律的解释
1871 年玻耳兹曼推广了麦克斯韦分布律,对熵概念的微观意义做出突破,但仍没能彻底解决不可逆性问题。对这个问题的攻克是在1872 年的文章《气体分子热平衡的进一步研究》中[1]262-349,玻耳兹曼揭示麦克斯韦速度分布和克劳修斯热力学第二定律之间的关联性。解决问题的关键在于如何用概率统计找到规律,因此可以说热力学理论问题也是概率问题。玻耳兹曼用函数的增减来表示物理过程的方向性,函数的减小是一个方向,函数的增大是另一个方向。
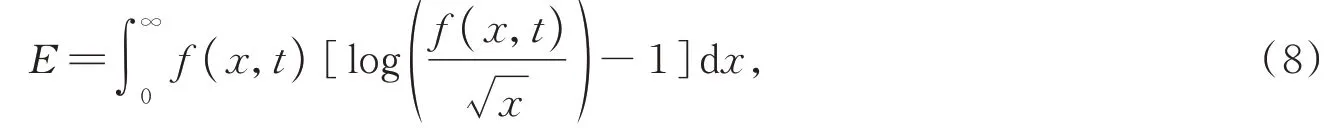
对E求导发现,所以E是减小或者保持不变,其对应于麦克斯韦速度分布律。玻耳兹曼在他的《气体理论讲义》(lectures on gas theory)中将E改用H表示,这就是著名的玻耳兹曼H定理,值得一提的是文中用离散值替换积分方法再次证明H定理的合理性。
无论动能的初始分布是什么,随着时间的推移它必须总是趋向麦克斯韦发现速度分布率。然而,在这里,我们成功地证明了在一般情况下是负的,并且只有在极限情况等于零,这当然是可逆过程[1]291。
玻耳兹曼认为H定理能说明热力学第二定律,甚至相信E就是熵,文章的第六节对熵进行进一步推导得出
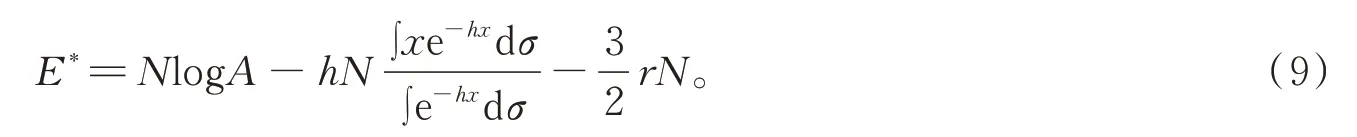
该式的意义在于玻耳兹曼从麦克斯韦‐玻耳兹曼速度分布律推导得出气体物理状态的概率。
19 世纪数学物理蓬勃发展,数学与物理关系密切,物理定律用数学公式给出。玻耳兹曼在麦克斯韦工作的基础上进一步研究非平衡态过程。玻耳兹曼1872 年的文章从麦克斯韦的研究成果深入到非平衡态过程研究[1]262-349,试图从微观动力学原理来证明热力学第二定律。玻耳兹曼将H随时间的演化(随时间单向变化)与热力学第二定律的熵增建立联系[16],并对之后1877 年的研究指明方向。
1874 年威廉·汤姆逊(William Thomson)关于自然界中的不可逆性问题提出疑问。洛喜密脱也指出:“根据力学定律从一些指定的初始条件经历一系列状态变化到达平衡态,如果把所有粒子的速度逆转也会经历同样的顺序,反过来回到初始状态。”这似乎与热力学第二定律不符。热力学第二定律认为在任何这样的状态序列中,熵必然总是增加的。1877 年玻耳兹曼先发表《力学原理与热力学第二定律的关系》中做出回应并指出不可逆性问题的关键是概率[1]362-367。就像玻耳兹曼所言:“均匀分布比非均匀分布多很多,随着时间的推移变得均匀,可以证明在一定的时间段之后,无穷多的初始状态可以导致一个均匀的状态。可以从不同状态分布的相对数量,计算它们的概率,可以用这方法来计算热平衡,并且用同样的方法来处理热力学第二定律。由于均匀分布的状态比非均匀分布的状态多出很多,非均匀状态概率极小,实际上可以认为是不可能的。例如如果一个氧气和氮气混合于一个容器,将发现下半部分化学成分纯氧,而氮在上半部分的概率非常小,但也不是不可能。”玻耳兹曼着重强调不可逆性问题应该当作概率问题去解释。
1877 年玻耳兹曼发表《关于热力学第二定律与热平衡条件概率计算的关系》深化他的想法[17]。假设粒子系统在时间为零时具有一定的状态,通过粒子之间的相互作用,状态发生变化。根据热力学第二定律,这种变化必须以粒子的总熵增加的方式变化,就像玻耳兹曼所说,“除了所有粒子的整体状态的概率会越来越大之外没有什么其他变化”。文中论证熵增单向变化不是别的就是所有粒子整体状态的概率所决定,并深入探讨这种概率与热力学第二定律的数学关系。玻耳兹曼沿袭他之前的量子化观念,即假设分子动能具有离散值,以此论证熵[5]。
这个假设并不对应任何现实的力学模型,但它在数学上更容易处理。每个分子的动能只能有有限个数的值。作为进一步的简化,我们假设每个分子的动能形成一个等差数列,如下所示:
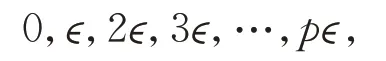
在碰撞前,两个碰撞分子的动能范围也如下:
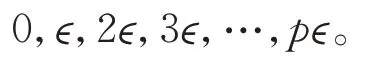
这意味着在碰撞后,每个分子仍然有上述动能值之一。假设有n个分子,它们动能取以上值中的一个。假设这些能量任意地分布在n分子中,且总能量是一个常数λϵ。用ω0表示动能为0 的分子个数,ω1动能为ϵ的分子个数,ω2是动能为2ϵ的分子个数,以此类推ωp动能为pϵ的分子个数。物理条件必须满足下式:
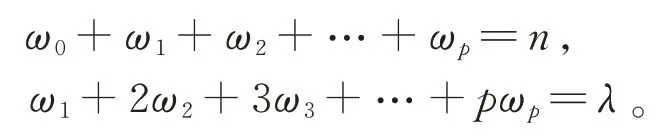
为了更为直观地理解,取n=7,λ=7,p=7,则分子动能最大值只能P=7ϵ。7 个分子动能可取以下8 个值中的一个
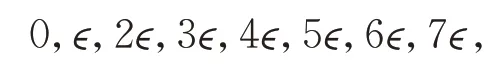
且分子最大动能表明总动能7ϵ,那么只有以下15 种分配方式,表格中第10 是概率最大的分布[17]1976-1978(图1)。
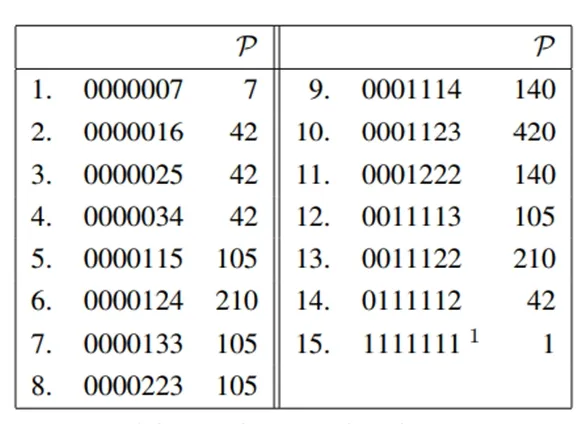
图1 动能分配的概率Fig.1 Probability of kinetic energy distribution
计算表格中排列,断定玻耳兹曼计算过程为
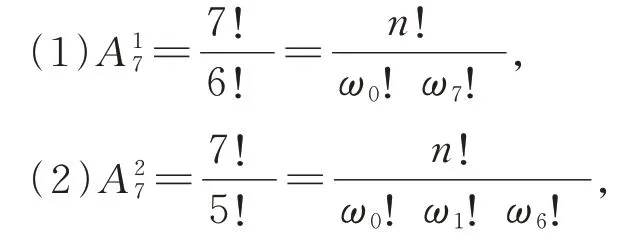
以此类推,扩展到n个分子排列数P=其中ω0,ω1…是不为零的有意义的数。若想求排列的最大值,因分子是常数,求分母的最小值。因为P的分母是乘积,所以最容易确定其对数的最小值M=ln[ω0!]+ ln[ω1!]+…。若是扩展到非整数值,应用微分学从而找到表达式的最小值M1=lnΓ[ω0+1]+lnΓ[ω1+1]+…,它表达的意思与上一个式子相同[17]1979-1981。
玻耳兹曼采用的方法认为能量是离散值,这观念在他那个历史时期不被采纳。所以他想方设法用伽马函数(Gamma function)及伽马函数斯特林(Stirling)公式,数学近似等方法在离散值的排列和连续的积分之间建立联系[18]。这样就可以消除离散的能量与连续的能量之间的矛盾。进而玻耳兹曼提出一个新概念排列测度(permutability measure)Ω与当今统计力学著作中的微观状态数或容配相对应,现今统计力学著作中把所有可能的微观状态的实际数目表示为体积(V),分子数(N)和能量(E)的函数,用符号Ω(V,N,E)来表示,并且玻耳兹曼强调熵的可加性。玻耳兹曼推演出计算排列测度Ω公式
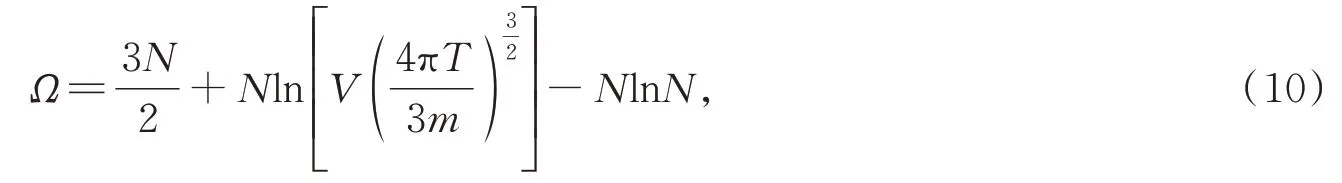
式中T表示平均动能,V表示体积,N表示分子数。进而推演出

玻耳兹曼认为1877 年得出熵符合玻耳兹曼1871 年的熵关系式。
在物体的系统中,如果发生了许多可逆的变化,那么所有这些物体的总熵保持恒定。另一方面,如果这些过程是不可逆的,那么所有物体的熵必然增加,正如众所周知的事实,在一个不可逆循环过程上的积分是负的。根据排列方式计算物体ΣΩ和总排列测度必须具有相同的增加。因此,在热平衡时在一个附加常数范围内,排列测度乘以一个常数的大小与熵相等;但在一个不可逆的过程中,它也保留了意义,不断增加[17]2004-2005。
玻耳兹曼得出的熵与现在人们理解的熵基本一致。玻耳兹曼关系式给出了熵的微观意义,物理系统的熵以相应微观状态的对数来表示。不足之处是玻耳兹曼能量子(quantum)纯数学计算方便而采纳,与实验或者物理性质关联不突出。
物理学家和科学史家都对熵关系式的评价很高。我国物理学家冯端认为“玻耳兹曼关系式把宏观量熵(S)与微观状态数(Ω)联系起来,在宏观与微观之间架起了一座桥梁,既说明了微观状态(Ω)的物理意义,也给出了熵函数的统计解释(微观意义)。物理概念第一次用几率形式表达出来,意义深远。”玻耳兹曼熵关系式演变见表1。玻耳兹曼墓碑上刻有著名熵关系式S=klnΩ,此式最早在普朗克关于“热辐射”的著名讲义中出现,但此公式冠以玻耳兹曼之名,确实当之无愧[19]。

表1 玻耳兹曼熵关系式演变Tab.1 Evolution of Boltzmann entropy
4 结语
熵概念一直是物理学家和哲学家广泛讨论的话题。玻耳兹曼的统计解释适用范围最广,影响最大。玻耳兹曼对熵的理解是随着研究逐渐深入的过程。他的研究方法推动了20 世纪从经典力学到量子论的转变。在19 世纪它仅仅处于倡议阶段,他的理论也不被认可或可以称为超前的,20 世纪玻耳兹曼的研究方法得到广泛应用。
物理概念和思想并不是凭空产生,而是钻研前人成果,研究中遇到种种难题,要去理解问题的本质,想方设法解决。物理学家就是创造性地解释困扰的问题。若将玻耳兹曼对熵概念统计解释历程应用于统计物理教学,学生更生动地理解熵概念和概率统计思想的发展以及变革,并从中得到启示。物理学就是这样在前人的创造性的思想(idea)和探索性的实验(experiment)基础上得到建立的。麦克斯韦描述了气体运动的规律,玻耳兹曼用熵的统计解释进一步阐释非平衡态过程规律,即麦克斯韦在微观层面上描述物理现象,玻耳兹曼进一步探究物理现象背后的原因。玻耳兹曼经过与其他科学家的探讨过程中坚定他的信念,可以使用概率统计方法来研究气体动理论,并将气体动力学理论与热力学融合在一起。热力学研究宏观物理量之间遵循的规律,而气体动理论从微观层面用分子的运动去解释物理现象。熵概念是在热力学第二定律研究中产生,玻耳兹曼研究热力学第二定律“熵”为中介,在热力学与气体理论之间建立了联系,在宏观量与微观量之间搭起了桥梁。
致谢:感谢内蒙古师范大学物理与电子信息学院那日苏老师和朝克夫老师提出的修改建议。
