Ni/Fe盐原位催化松木粉热解特性和动力学研究
2022-06-27聂明康殷浩鑫王佳兴
聂明康,殷浩鑫,王佳兴
(南京理工大学能源与动力工程学院,南京 210094)
热解是生物质资源利用的一种有效方式,主要是在高温条件下将生物质转化为清洁的高品位气体或液体燃料。与直接燃烧和填埋等传统生物质处理方法相比,热解不仅可以减少SO2和氮氧化物等污染物的产生,而且可以实现生物质的资源化利用,缓解我国资源短缺的问题。
生物质直接热解产物比较复杂,油品质量较低。催化热解技术的发展是一个必然的研究方向。在生物质催化热解过程中,催化剂是影响热解产物质量的核心。因此,选择合适和性能优良的催化剂是提高热解产物质量的重要途径。
采用金属盐浸渍生物质进行原位催化热解是降低生物质焦油含量和提高燃气质量的有效方法。生物质中大分子的含氧基团可以作为金属阳离子的吸附位点,这种现象导致生物质木质基质中分散着大量的金属前驱体[1]。PUTUN 等人[2]将MgO与棉籽混合后进行热解实验,结果发现MgO提高了半焦和气体的产率。ZHAO等人[3]发现NaCl与稻壳共热解中可以提高 H2的产量。冯东东等人[4]证实碱金属和碱土金属可以抑制生物质热解过程焦油的生成,进而提高气体产量。
生物质热解过程的动力学分析可以了解反应的程度,进一步分析反应机理,对热解特性的研究非常有帮助。因此,为了分析生物质的热解过程,需要研究热解反应的动力学[5]。本文研究了Ni/Fe盐原位催化松木粉热解特性,分析了添加Ni盐/Fe盐后松木粉热解过程的动力学,对降低生物质热解的焦油产率有积极影响。
1 实验部分
1.1 实验方案设计
本实验所用的实验原料为松木屑,购自于木材加工厂。将松木屑放入干燥箱中,在105 ℃下鼓风干燥24 h。随后将其粉碎和打磨,用不锈钢分样筛筛分粒径为0.12~0.18 mm松木屑,在105 ℃的环境下在干燥箱中干燥24 h,得到干燥的松木粉。将NiCl2·6H2O溶解在乙醇中,制备NiCl2乙醇溶液,随后将溶液倒入松木粉中(液面略高于松木粉),充分搅拌10 min,制成NiCl2-乙醇-松木粉混合物(金属镍与松木粉的质量比为1∶100)。最后,将得到的混合物在干燥箱中105 ℃下干燥24 h,制备出NiCl2松木粉混合物,本文将其称为NiCl2-SD。用同样的方法制备Ni(NO3)2松木粉混合物、FeCl3松木粉混合物和Fe(NO3)3松木粉混合物,分别称为Ni(NO3)2-SD、FeCl3-SD和Fe(NO3)3-SD。制备Ni盐/Fe盐-SD所用的化学试剂情况见表1。
根据国家标准GB/T 28731-2012《固体生物质燃料工业分析方法》以及JY/T 017-1996《元素分析仪方法通则》,对制备的Ni盐/Fe盐-SD样品进行工业分析和元素分析。工业分析过程中使用马弗炉对样品进行烧制,元素分析时采用德国艾力蒙塔公司的Vario MACRO Cube元素分析仪。Ni盐/Fe盐-SD的工业分析和元素分析见表2。
从表2中工业分析部分可以看出,Ni盐/Fe盐-SD的主要成分是挥发分和固定碳,其中挥发分的比例超过70%,固定碳的比例超过15%。Ni盐/Fe盐-SD相比于松木粉,灰分都有明显的提高,挥发分占比有一定程度的降低,固定碳占比也有较大幅度的提高。由于添加了Ni盐/Fe盐,Ni盐/Fe盐-SD的C元素和H元素的含量都有所降低。同时,由于添加了硝酸盐,Ni(NO3)2-SD和Fe(NO3)3-SD中N元素含量明显提升。Ni盐/Fe盐-SD与松木粉S元素和O元素含量没有明显的差别。
1.2 实验系统及方法
本实验利用德国耐驰公司的热重分析仪进行。实验的每份样品选用了10 mg(±0.5 mg)小试样,置于氧化铝坩埚内,并将样品在100 ml/min的N2气氛中从室温加热至800 ℃,加热速率分别为10 ℃/min、20 ℃/min、30 ℃/min和40 ℃/min。为了减小实验仪器误差和随机误差,每组实验重复三次,同时对空的氧化铝坩埚进行相同条件的热重实验,并以此对实验结果进行修正。
1.3 特征热解参数
由热重和热重一阶微分曲线可以得到特征热解参数(失重率TG,失重速率DTG),并以此来参考评价Ni盐/Fe盐-SD的热解行为。其中涉及到的参数主要有初始热解问题(Tv)、平均失重速率(-DTGmean)、热解残留物质量(WR)、最大失重速率(-DTGmax)以及最大失重速率时的温度(Tm)等。评价时,经常使用综合脱挥发分指数D对热解特性进行说明[6],计算公式如下:
(1)
式(1)中,ΔT1/ 2表示为(-DTG)/(-DTGmax)为 0.5时的温度区间。
1.4 热解动力学
生物质热解过程的动力学分析可以了解反应的程度,进一步分析反应机理,对热解特性的研究非常有帮助。对于本文的热重实验,反应是松木屑热解产生固体生物质焦炭和气体挥发物的过程。其中,气态挥发物包括气态产物如H2和CO以及气态焦油。整个反应的反应速率受加热速率等因素的影响。
通过分析样品的TG曲线,可以得到一些热解动力学参数,不仅可以定性解释和比较样品的热解特性,还可以定量计算。实验中样品的分解率可表示为:
(2)
式(2)中,k为阿伦尼乌斯化学反应速率常数,f(x)为热解反应机理函数;α为反应物的转化率,即α=Δm/m,Δm为样品减少的质量,m为样品初始质量;非均相固态热降解的动力学公式为:
(3)

表1 制备Ni盐/Fe盐-SD所用的化学试剂情况
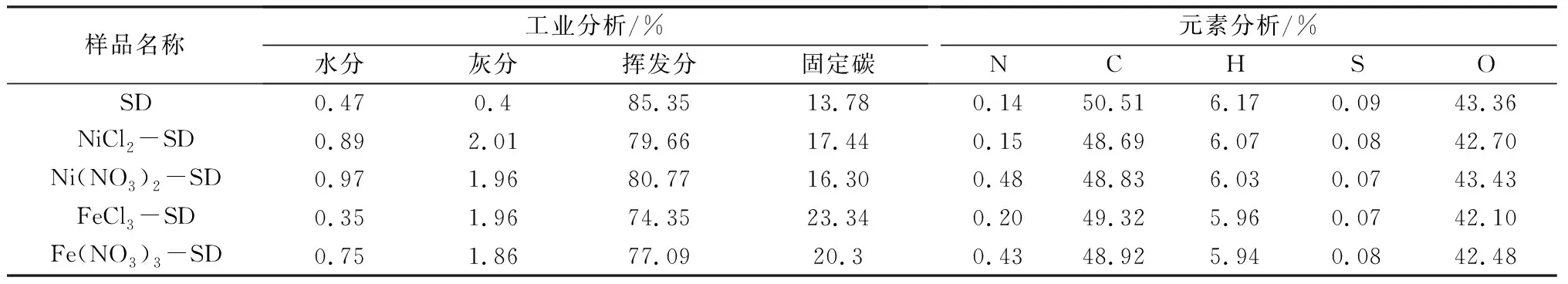
表2 Ni盐/Fe盐-SD的工业分析和元素分析
式(3)中,A是反应频率因子,可以表示为1/s;β为升温速率,可以表示为dT/dt;Eα为表观活化能;R是理想气体常数,其数值为8.314 J/(mol·K)。
联立式(2)和式(3)可以得到热解过程的动力学模型:
(4)
对其进行积分,可以得到:
(5)
式(5)中,G(α)为转换依赖函数f(α)的积分形式。
在使用Flynn-wall-Ozawa(FWO)和Kissinger-Akahira-Sunose(KAS)对活化能Eα进行计算时可以不受模型限制,且具有较高的准确性,是评价固体材料热解动力学的常用方法[7-9]。
利用FWO法计算活化能的表达式为:
(6)
分别设置10 ℃/min、20 ℃/min、30 ℃/min和40 ℃/min的不同升温速率,以1/Tα为横坐标,以ln(β)为纵坐标,基于FWO法绘制松木粉催化热解反应的动力学模型曲线。根据所得到的动力学曲线,计算得到基于FWO方法的活化能Eα。
利用KAS法计算活化能的表达式为:
(7)
分别设置10 ℃/min、20 ℃/min、30 ℃/min和40 ℃/min的不同升温速率,以1/Tα为横坐标,以ln(β/Tα2)为纵坐标,基于KAS法绘制松木粉催化热解反应的动力学模型曲线。根据所得到的动力学曲线,计算得到基于KAS方法的活化能Eα。
2 实验结果分析
2.1 Ni/Fe盐原位催化松木粉热解特性分析
图1为Ni盐/Fe盐-SD在升温速率为10 ℃/min下热解的TG和DTG曲线。首先是预热解阶段(室温~250 ℃),主要是内部水的析出,并伴有少量化学反应。其中部分组分分解成CO和CO2等物质,表明发生了热解反应。随后是生物质分解阶段(250~700 ℃),是热解过程的主要阶段,涉及温度范围大,化学反应复杂,包括纤维素和木质素的分解。样品质量减少的速度明显加快,大部分有机挥发物得到了析出。生成的液体产物主要有焦油和水,气体产物主要有CO、CO2和H2等小分子气体。最后是残余生物质的热解阶段(700~800 ℃),主要是C-O键和C-C键的进一步断裂,残余样品质量下降并逐渐趋于稳定,焦油等反应产物发生各种二次热解反应。同时,该阶段还包括少量的无机反应,如Ni盐和Fe盐还原生成单质Ni和Fe等。与不含Ni/Fe盐的松木粉样品相比,Ni盐-SD具有更高的质量损失。这可能与Ni金属粒子对生物质热解的不同影响有关。
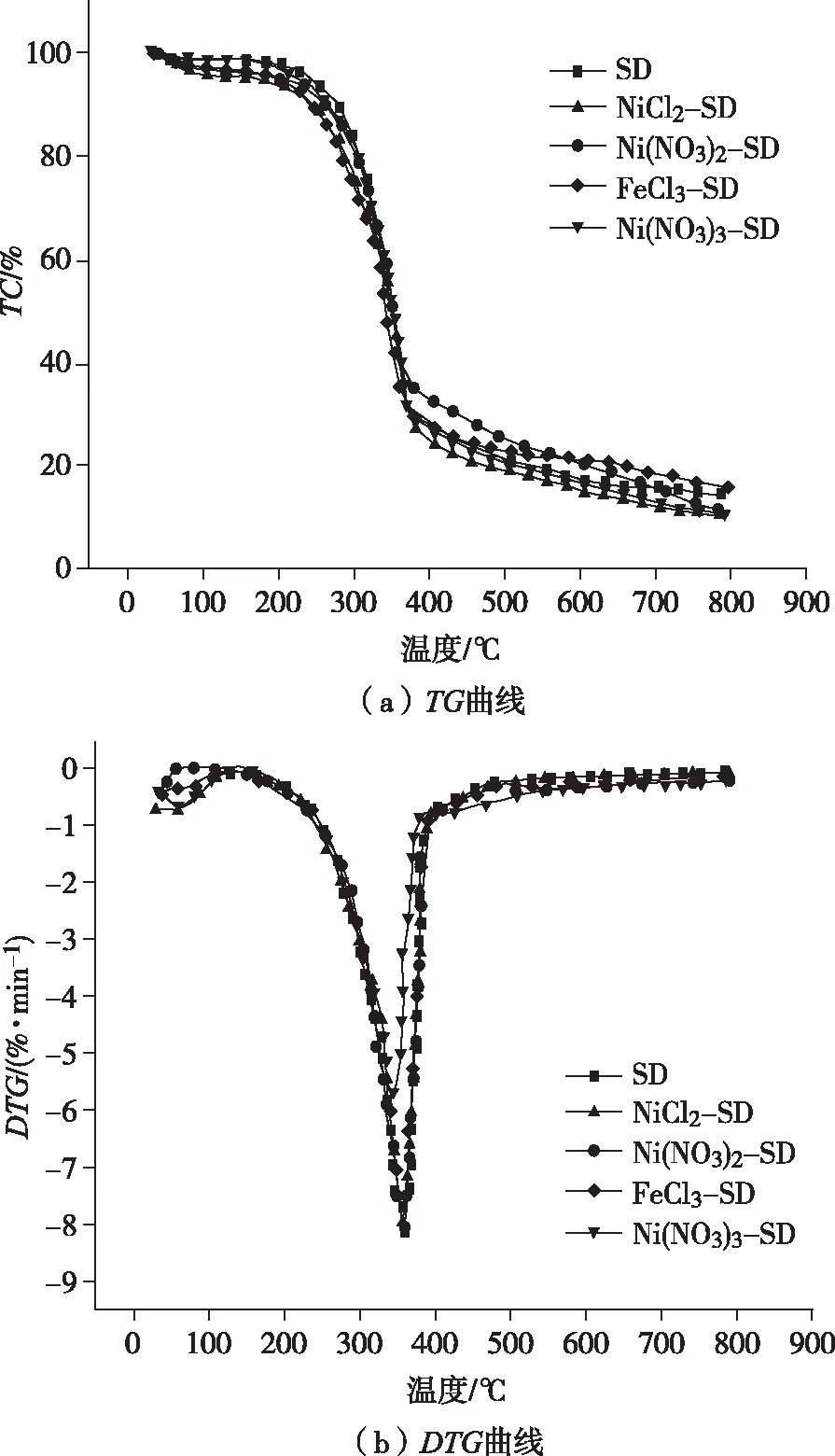
图1 Ni盐/Fe盐-SD在升温速率为10 ℃/min下的TG和DTG曲线
根据表3,松木粉(SD)样品的初始分解温度Tv最低为 213.77 ℃。添加Ni盐和Fe盐后,样品的Tv增加,Fe盐样品的Tv增加幅度大于Ni盐样品的Tv增加幅度。这说明加入Ni盐和Fe盐后,松木粉初始热解温度更高,热稳定性更强。氯化盐样品中Tv的增加幅度也高于硝酸盐样品。这表明Ni盐-SD的热解需要更高的温度。添加Ni盐和Fe盐的样品的最大失重率(-DTGmax)和平均失重速率(-DTGmean)均有所下降,Fe盐样品的最大失重率和平均失重速率的下降率高于Ni盐样品,表明Ni盐/Fe盐的添加降低了热解速率,这与Tv变化的一致。在热解残渣质量(WR)方面,Ni盐/Fe盐-SD的WR增加,与工业分析中灰分增加的结果相符。与普通松木粉样品相比,Ni盐/Fe盐-SD的综合脱挥发分指数D有所下降,说明Ni盐/Fe盐的加入可以抑制松木粉的热解性能,降低松木粉热解时的焦油产率。
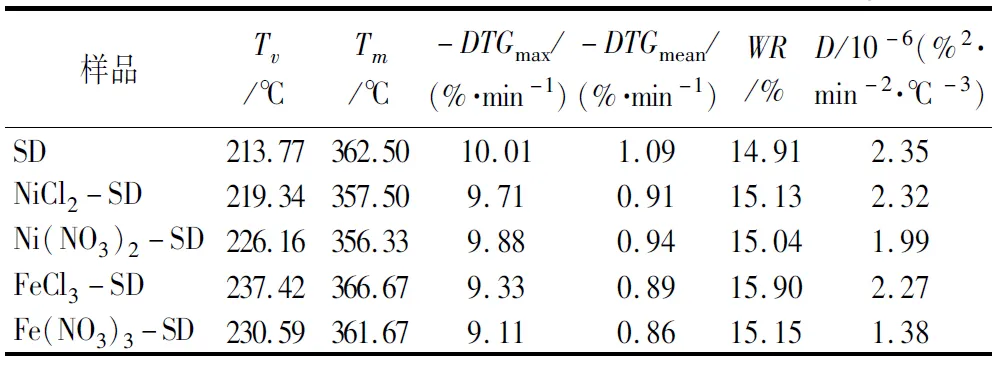
表3 升温速率为10 ℃/min时样品的特征热解参数
2.2 Ni/Fe盐原位催化松木粉热解动力学分析
分别在10 ℃/min、20 ℃/min、30 ℃/min、40 ℃/min的不同加热速率下对样品NiCl2-SD、Ni(NO3)2-SD、FeCl3-SD、Fe(NO3)3-SD热解进行热重分析,并运用FWO法和KAS法对热重结果进行分析计算。以1/T为横坐标、以ln(β)和ln(β/Tα2)为纵坐标用FWO法计算分析所得的拟合直线和用KAS法计算分析所得的拟合直线分别见图2和图3。根据两图中拟合直线的斜率,分别计算出基于FWO法和KAS法的表观活化能Eα。本文选取的α的取值范围为0.3~0.75。基于选取α的范围,Eα的相关系数R2都在93.172~99.017之间,表明拟合效果良好。对Ni盐/Fe盐-SD用FWO法KAS法计算分析所得Eα的平均值见表4。
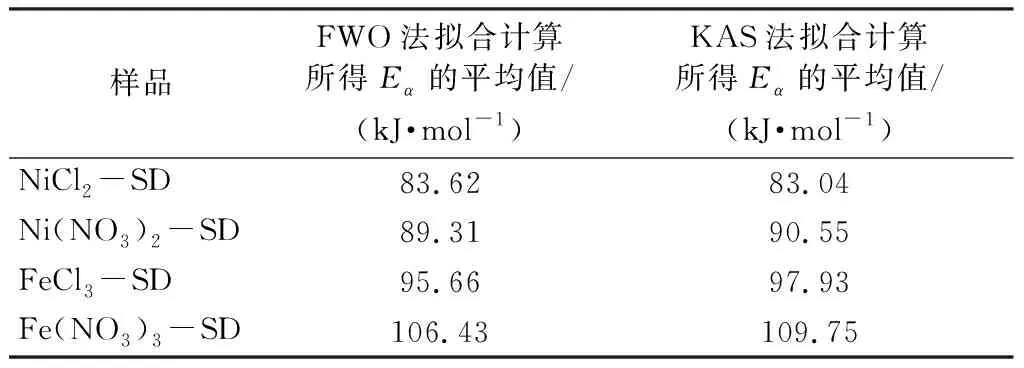
表4 对Ni盐/Fe盐-SD用FWO法KAS法计算分析所得Eα的平均值

图2 对Ni盐/Fe盐-SD用FWO法计算分析所得的拟合直线图
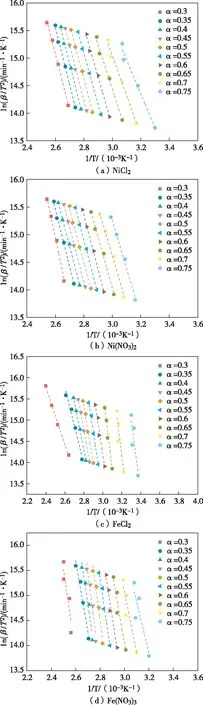
图3 对Ni盐/Fe盐-SD用KAS法计算分析所得的拟合直线图
分别用FWO法和KAS法对Ni盐/Fe盐-SD热解的热重结果拟合计算Eα值,结果如下:NiCl2-SD基于FWO法拟合计算的Eα值为79.94~87.72 kJ/mol,基于KAS法拟合计算的Eα值为73.75~86.16 kJ/mol;Ni(NO3)2-SD基于FWO法拟合计算的Eα值为71.18~95.79 kJ/mol,基于KAS法拟合计算的Eα值为73.13~97.17 kJ/mol;FeCl3-SD基于FWO法拟合计算的Eα值为73.85~122.84 kJ/mol,基于KAS法拟合计算的Eα值为76.07~130.22 kJ/mol;Fe(NO3)3-SD基于FWO法拟合计算的Eα值为81.98~130.62 kJ/mol,基于KAS法拟合计算的Eα值为86.96~131.60 kJ/mol。由此可以发现,依据FWO法和KAS法拟合计算得到的Eα具有一致性。
与普通松木粉相比(热解表观活化能为40~80 kJ/mol)[10],Ni盐和Fe盐的加入明显提高了材料的表观活化能,Fe盐的加入提高表观活化能的程度更大。这一现象与样品工业分析结果一致。造成这种结果的原因可能是加入Ni盐和Fe盐后,热解过程中产生的挥发分发生了聚合反应,样品中的灰分和固定碳增加,热解反应活性降低,引发热解反应所需的能量增加(即表观活化能增加),样品的热稳定性提高,热解过程中焦油的产率降低。
3 结语
本文利用热重实验(包含TG和DTG)对Ni/Fe盐原位催化松木粉热解过程的特性进行分析,对热重实验的结果运用FWO法和KAS法对Ni/Fe盐原位催化松木粉热解过程进行动力学分析,得到的结论如下:
(1)加入Ni盐/Fe盐后,样品的初始分解温度Tv均有不同程度增加,最大失重率(-DTGmax)和平均失重速率(-DTGmean)均有所下降,热解残渣质量(WR)一定程度增加,综合脱挥发分指数D有所下降,且在Fe盐的原位催化作用下以上特征热解参数变化更为明显。这表明Ni/Fe盐的添加提高了松木粉的热稳定性,降低了热解速率,降低松木粉热解时的焦油产率,且Fe盐的这种催化作用更为明显。
(2)加入Ni盐/Fe盐后,松木粉的表观活化能Eα不同程度增加,且Fe(NO3)3-SD的增加幅度最大,其基于FWO法拟合计算的Eα为81.98~130.62 kJ/mol,基于KAS法拟合计算的Eα为86.96~131.60 kJ/mol。相比于不加催化剂的松木粉,两种拟合计算的表观活化能Eα分别增加了77.4%、82.9%。这表明Ni/Fe盐的加入使得松木粉引发热解反应所需的能量增加(即表观活化能增加),样品的热稳定性提高,热解过程中焦油的产率降低。
