皂素氧化脱色工艺及性能表征研究*
2022-06-24刘传杰朱莉伟陈殿松蒋建新
刘传杰 朱莉伟 陈殿松 吉 骊 蒋建新
[1.北京林业大学材料科学与技术学院,国家林业和草原局木本香料(华东)工程研究中心,北京 100083;2.广州德谷个人护理用品有限公司,广东 广州 510800]
皂素广泛存在于单子叶植物和双子叶植物中,是糖基化植物的次生代谢产物。其可应用于饮料[1]、化妆品[2-3]、医药[4]以及人造板材[5-6]等领域,是许多中药、中成药、中草药、植物药和天然药的主要成分,在人造板材工业上作为乳化剂乳化石蜡效果好,可大幅度提升板材档次。皂荚皂素是从皂荚属植物中提取出来的一种三萜皂苷,其结构中含有糖体、有机酸等亲水性极性基团,皂素水溶液振摇后能产生持久的泡沫(类似肥皂水溶液泡沫),是一种非离子型表面活性剂,具有显著的去污[7-8]和抑菌能力[9-10]。目前,生产皂荚皂素的方法主要有水提法和有机溶剂提取法[11-15]。由于这两种方法均存在生产工艺粗放的问题,导致工业上生产的皂素产品颜色深、纯度低,产品附加值较低,在洗护、生物医药和食品等领域的应用受到了较大限制。皂荚皂素颜色较深主要有两方面的原因:一是源于其自身的天然色素充当了显色物质,且种类复杂多变,不易分离和纯化;二是由皂素加工提取过程中产生的,如加热过程中发生的美拉德反应、多糖的水解等。
为拓宽皂素产品的应用领域,提升其经济效益,对其颜色品质的控制和调节势在必行。皂素脱色的手段主要有两种:一种是在工业化生产过程中细化生产工艺,减少人为因素,控制色素类物质的溶出和进一步生成;另一种则是通过加入特定的脱色剂淡化其颜色。常用的脱色方法有物理吸附法、化学吸附法和化学氧化脱色法[16-21]。物理吸附法主要是利用分子之间的吸引力对皂素进行分离和纯化,从而达到物理脱色的效果,该方法样液不易过滤,皂素损失较大。化学吸附法是使用离子交换树脂选择性吸附皂素中存在的一些酚类、黄酮类和醌类色素。相较于物理吸附脱色的方法,化学吸附法脱色的能力较大,而且目标产物的损失也较小,皂素得率较高。色素类物质一般都含有共轭双键发色基团,因此可以通过化学氧化的方法破坏发色基团的共轭双键系统达到脱色目的。该方法脱色效率高且得到的皂素产品颜色自然均匀。目前,使用较多的化学氧化脱色剂主要有双氧水、过氧化苯甲酰、氯酸钠、高锰酸钾、臭氧等。本研究选用过氧化氢作为脱色剂,对粗提皂荚皂素进行脱色研究,取得了良好的脱色效果,该方法条件温和、不残留、处理范围广、效率高、不需要专用设备等,具有广泛的应用前景和工业化生产潜力。
1 材料与方法
1.1 材料
皂荚(Gleditsia sinensisLam.)果采摘于河南省三门峡市凯达农业技术推广有限公司皂荚林种植基地。无水乙醇、过氧化氢(30%)、氯化氢、氢氧化钠、吸附树脂(AG501-X8 Resin)购于上海阿拉丁生化科技股份有限公司,产品等级均为分析纯。
1.2 仪器
傅里叶变换红外光谱仪(Bruker-ALPHA,Bruker,德国);高效液相色谱仪(Waters 2695,Waters,美国),配备HPX-87P柱子和2414示差折光检测器;自动表面张力仪(BZY 系列,上海方瑞仪器有限公司,中国);分光辐射亮度计(PR715,Photo Research,美国);场发射扫描电子显微镜(SU8010,Hitachi,日本)。
1.3 试验方法
1.3.1 皂荚皂素脱色
皂荚皂素粗品采用无水乙醇索氏抽提的方法制备,皂荚果去籽、干燥、粉碎后将其放入索氏抽提中,在85 ℃下进行抽提12 h,然后将抽提液进行浓缩、真空干燥、研磨后得到粗提皂荚皂素(其色度值为L*: 58.09,a*: 9.60,b*: 3.57)。皂荚果和粗提皂荚皂素的宏观形貌如图1所示。称取一定量的粗提皂荚皂素溶于20 mL 90%的乙醇溶液中,用10% NaOH溶液调节pH至10,加入皂素质量6%的H2O2(30%),在70 ℃水浴的条件下磁力搅拌2 h,然后加入60 mg吸附树脂搅拌15 min,反应后将反应液过滤,调节滤液至中性,加入60 mL丙酮,不停搅拌直至得到固体沉淀,倒掉上层丙酮澄清液,将固体放入60 ℃烘箱,真空干燥得浅黄色粉末即为脱色皂荚皂素样品,样品真空密封保存备用。

图1 皂荚果和粗提皂荚皂素图Fig.1 The pictures of saponin pods and crude saponins
1.3.2 脱色率计算
参考严峻等[22-24]的方法,使用分光辐射亮度计对样品颜色进行测量,并将测定记录的数据(L*、a*和b*值)进行综合分析。L*是明度值,表示色彩的明暗度,其范围为0~100,0时亮度最低,100 时亮度最高。a*和b*值是色彩的色度值,其中a*值从红(正值)到绿(负值)渐变,b*值则由黄(正值)到蓝(负值)渐变[25]。L*值是衡量样品亮度的一个重要的指标,故使用L*值作为脱色效果的衡量标准。脱色率用如下公式进行计算:

式中:表示皂荚皂素脱色前的*值;表示皂荚皂素脱色后的L*值。
1.3.3 表面张力测定
根据文献[26]中的方法,并做了一定调整。取适量干燥后的粗提皂荚皂素和脱色皂素样品配置成0.35 g/L的皂素水溶液,加热至30 ℃,取一定量的皂素水溶液置于表面皿,采用自动表面张力仪测定溶液表面张力,每个样品重复五次。
1.3.4 泡沫高度测定
采用量筒震荡法对脱色前后皂素的泡沫高度进行测量,准备洁净的50 mL具塞量筒若干,取适量干燥后的脱色皂素配置成0.35 g/L的皂素水溶液。在室温下,取10 mL皂素水溶液加入具塞量筒,剧烈震荡,观察泡沫产生的高度作为溶液起泡性能的量度,记下从停止振荡到泡沫高度衰减到原来泡沫高度的一半所用的时间,即半衰期t1/2,用于表征泡沫的稳定性[27],每个样品重复五次。
1.3.5 傅里叶红外光谱表征
采用红外光谱仪和KBr压片的方法进行傅里叶红外光谱测试表征。将粗提皂荚皂素和脱色皂荚皂素样品绝干后和KBr充分研磨,置于压片机中压制透明的薄片后进行测试,条件为400~4 000 cm-1。
1.3.6 能谱测试
将粗提皂荚皂素和脱色皂荚皂素样品研磨后绝干,将粉末置于导电胶上,并进行喷金处理,借助场发射扫描电子显微镜搭载的能谱仪测试皂素样品中Fe和Cu的相对含量。
1.3.7 皂荚皂素水解
精确称取皂荚皂素25 mg,溶于25 mL 0.25 M硫酸中,30 ℃恒温震荡0.5 h,100 ℃回流水解2 h。然后将水解液冷却至室温,取3 mL上清液于离心管,加入碳酸钙进行中和,调节pH至5~7。将中和后的水解液高速离心(12 000 r/min)10 min,然后取1.5 mL上清液加入6 mg吸附树脂,吸附1 h。然后过0.22 μm水系膜后装入液相小瓶进行高效液相色谱分析[分析条件:HPX-87H柱(300×7.8 mm),流动相为5 mmol/L H2SO4,流速为0.5 mL/min,柱温为65 ℃,进样量为5 μL[28]。
2 结果与分析
2.1 处理时间对脱色效果的影响
对皂荚皂素进行脱色处理,不同的处理时间(编号1-4)、处理温度(编号5-8)和脱色剂用量(编号9-12)的试验方案见表1。
由表1、2可以看出,在H2O2用量(4%)和处理温度(70 ℃) 一定的情况下,脱色时间越长皂荚皂素的脱色率越高,随着时间的增加,皂素水溶液的表面张力呈现先降低后增加的趋势。此条件下最小脱色率为62.98%,对应的脱色时间为1 h,表面张力为41.90 mN/m;最大脱色率为76.50%时,对应的脱色时间为2.5 h,表面张力为43.25 mN/m,值由58.09提高到90.15。2号样品表面张力最小为41.55 mN/m,脱色时间为1.5 h。对比可知,脱色时间会影响皂荚皂素的脱色效果,且脱色的过程是缓慢进行的,并没有发生剧烈脱色反应,有利于脱色工艺的控制和进一步优化。

表1 皂荚皂素脱色试验方案、表面张力和得率Tab.1 Decolorization scheme, surface tension and yield of saponin from Gleditsia sinensis

图2 不同处理时间的脱色皂素图Fig.2 Decolorized saponins with diあerent treatment time
2.2 H2O2用量对脱色效果的影响
由表1和图3可以看出,在处理时间(1.5 h)和处理温度(70 ℃)一定的情况下,脱色剂用量越多皂荚皂素的脱色率越高而且皂素水溶液的表面张力也呈现先降低后增加的趋势。在脱色过程中,H2O2会产生游离的羟基自由基,这是一种高度反应的、非选择性的氧化剂,能够破坏色素类物质的共轭双键断裂或者发生异构,从而破坏其发色基团,达到脱色效果。此条件下最小脱色率为63.68%,对应的脱色剂用量为2%,表面张力为42.15 mN/m;最大脱色率为75.51%时,对应的脱色剂用量为8%,表面张力为43.60 mN/m,L*值由58.09提高到89.74。此外,当脱色剂用量为6%和8%时,两种脱色皂素的颜色并无显著差异,在考虑成本和安全性的情况下,H2O2用量不宜过多。

图3 不同脱色剂用量处理的脱色皂素图Fig.3 Decolorized saponinstreated with diあerent dosage of decolorizing agent
2.3 处理温度对脱色效果的影响
由表1、图4可知,在脱色剂用量(6%)和处理时间(1.5 h)一定的情况下,随着脱色温度的不断升高,粗提皂荚皂素的脱色率呈现先升高后下降的趋势,温度升高后皂素水溶液的表面张力未发生太大变化。此条件下最小脱色率为75.35%,对应的处理温度为55 ℃,表面张力为40.9 mN/m;当最大脱色率为78.12%,对应的处理温度为85 ℃,表面张力为42.65 mN/m,L*值由58.09提高到90.83。9号样品表面张力最小为40.90 mN/m,脱色温度为55 ℃。由此可以推测,脱色剂的反应活性会受到温度的影响,温度过高,脱色剂急剧分解影响脱色效果。此外,还可能是由于过高的温度使得反应体系发生了美拉德反应,从而影响脱色效果。

图4 不同处理温度条件下的脱色皂素图Fig.4 Decolorized saponins at diあerent treatment temperatures
2.4 脱色前后皂素的泡沫高度
由图5可以看出,脱色前后皂素水溶液的泡沫高度有着明显的变化,未脱色皂素的泡沫高度(图5a)为12 mm,脱色后皂素水溶液(图5b)的泡沫高度超过36 mm,且脱色皂素的半衰期t1/2≥12 h,远远高于未脱色皂素的半衰期t1/2= 40 min,说明皂荚皂素脱色工艺对皂素水溶液的泡沫稳定性起到了促进作用。脱色皂素的泡沫半衰期显著高于粗提皂素,加之粗提皂素颜色有了明显改观,由红褐色变成米黄色,实现了粗提皂荚皂素脱色纯化的目的,这有利于拓宽皂荚皂素在生物医药、食品饮料、照相复印等高端制造领域的应用。

图5 H2O2处理前后皂荚皂素水溶液的泡沫高度图Fig.5 Foam height map of saponin aqueous solutionbefore H2O2 treatment
2.5 脱色机理分析
2.5.1 脱色前后皂荚皂素Fe和Cu变化情况
粗提皂素中金属离子的含量对皂素的颜色会有一定的影响,金属离子吸附在皂素上会使皂素颜色加深。通过扫描电子显微镜搭载的能谱仪对皂荚皂素(未脱色样品)、1号脱色皂素(脱色率为62.98%)和11号脱色皂素(脱色率为78.12%)进行能谱分析,对皂荚皂素微区Fe和Cu及其相对含量进行测定。由表2可知,与未脱色皂素相比,脱色皂素两种元素的相对含量值均有所减少,且脱色率越高,金属离子相对含量越低。这可能是因为粗提皂荚皂素中存在色素类杂质,该类物质吸附金属离子后皂荚皂素颜色变深。经H2O2法处理后,其双键系统被破坏,其吸附的金属离子也随之被解吸附,相应的皂荚皂素颜色变浅。所以在工业生产中皂荚皂素的粗提或纯化过程应尽可能的避免金属离子的带入[16]。

表2 皂荚皂素脱色前后Fe和Cu的相对含量值对比Tab.2 Comparison of relative contents of Fe and Cu before and after decolorization of Gleditsia saponin
2.5.2 脱色前后皂荚皂素红外光谱分析
图6为粗提皂荚皂素和脱色皂荚皂素的红外光谱图。可以看出,皂荚皂素在3 000~3 700 cm-1之间存在一个较宽的振动峰,对应于糖基和苷元上所连O—H的伸缩振动;在1 500~1 800 cm-1之间的光谱区域对应COOH的振动峰;2 920 cm-1为亚甲基的C—H伸缩振动峰;1 725 cm-1和1 635 cm-1的吸收峰表明结构中存在C==O;900~1 130 cm-1中的吸收峰是由C—O—C振动引起[29-30]。脱色前后皂荚皂素在2 855 cm-1处发生了明显的变化,2 855 cm-1处应为脂肪链中的C—H振动峰,这应该是在脱色的过程中脱去了油脂类物质。脱色皂素在1 600 cm-1位置处出现了新的峰,而未脱色皂素中1 635 cm-1位置的峰消失,这可能是因为色素类杂质的双键被破坏导致的[20]。
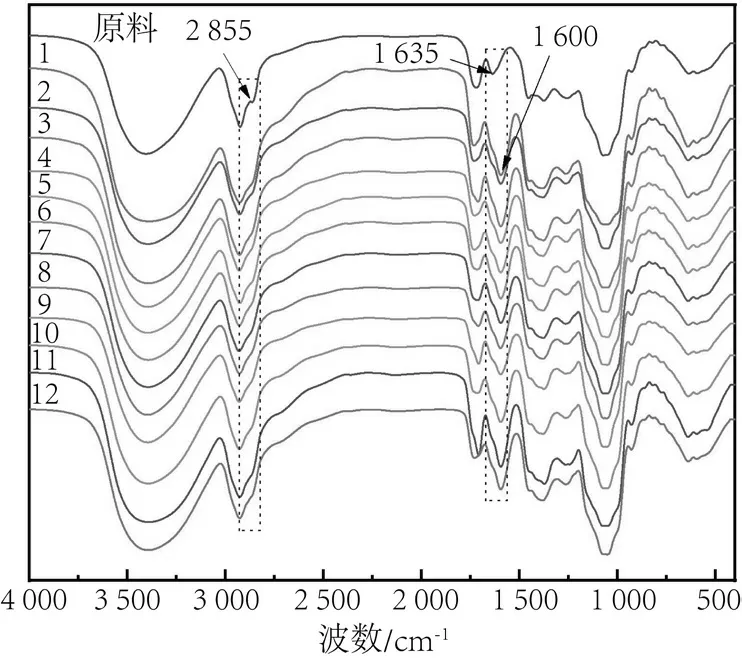
图6 H2O2处理前后皂荚皂素的红外光谱图Fig.6 Infrared spectra of gleditsia saponin before and after treatment with H2O2
2.5.3 脱色前后皂荚皂素糖含量变化
粗提皂荚皂素和脱色皂荚皂素样品水解后的糖含量如图7所示。由图可知,水解液中主要含有葡萄糖、木糖、鼠李糖和阿拉伯糖。相比于粗提皂荚皂素原料,脱色皂素各单糖含量均略有增加,皂素水解液中木糖含量最高,均在20%以上。其次是葡萄糖,含量均在15%以上。鼠李糖和阿拉伯糖含量相近,在5%左右。总糖含量最高值为7号和10号脱色样品,含量为51.05%。这说明H2O2法皂素脱色工艺能够有效去除粗提皂荚皂素中的部分杂质,提高脱色皂素产品纯度,具有工业化生产的可行性。

图7 皂荚皂素水解后的糖含量趋势图Fig.7 Trend chart of sugar content after hydrolysis ofgleditsia saponin
3 结论
1)采用H2O2法处理粗提皂素制备脱色皂素产品,该工艺简洁、条件温和、反应时间短。处理后的皂素颜色为米黄色,颜色自然。通过综合评价脱色剂用量、脱色温度、脱色时间、脱色皂素外观色貌、表面张力和总糖含量等参数和性质,确定了H2O2法脱色皂荚皂素的优化工艺为脱色剂H2O2用量6%、脱色时间2 h、脱色温度70 ℃。
2)红外光谱分析表明:脱色前后样品的结构基本不变,而且脱色样品的泡沫高度明显高于未脱色样品,说明色素类的杂质不仅会影响皂素产品的色泽而且会影响皂素水溶液的表面活性。
3)H2O2脱色反应主要破坏的是色素类杂质的双键,在脱色过程中,H2O2会产生游离的羟基自由基,能够破坏色素类物质的共轭双键系统。在去除杂质和油脂物质的同时,粗提皂荚皂素吸附的Fe和Cu的含量也随之降低,导致粗提皂荚皂素颜色变浅。
