锡酸锌纳米材料的制备方法及应用研究进展
2022-06-24马殿普李俊覃德清袁英杰潘飞符泽卫
马殿普,李俊,覃德清,袁英杰,潘飞,符泽卫
(云南锡业集团(控股)有限责任公司研发中心,云南 昆明 650200)
锡酸锌(ZnSnO)是一种性能优良的宽带隙N 型半导体材料,禁带宽度达到3.6eV。ZnSnO属于立方晶系,晶格常数为8.65Å(1Å=0.1nm),空间群为Fd3m。锡酸锌由于具有较高的电子迁移率、稳定性和高电导率,优异的吸附性能和光学性能以及优异的阻燃抑烟性能等,被广泛应用于锂离子电池负极材料、气敏材料、光催化、电触头材料以及阻燃抑烟剂等领域。不同的应用所对应的制备方法也有所不同,粒径的控制一直是锡酸锌超细化面临的主要挑战,研究还表明,材料的形貌、结构对ZnSnO性能影响较大。因此,需要根据不同应用要求的粒径尺寸、形貌、结构等选择合适的制备方法。锡酸锌自1953 年被首次合成,1993 年日本三菱公司研究人员对锡原料及工艺进行优化制备出粒径2~5μm 的锡酸锌,2001 年云南锡业创新性地发明了锡酸锌新工艺,制备出粒径0.4μm的锡酸锌。近年来,随着纳米技术迅猛发展,锡酸锌纳米化已逐渐成熟,目前已开发出多种ZnSnO纳米材料的制备方法,如水热法、化学沉淀法、固相化学法、微波合成法、模板法等,以及两种及以上方法联用的合成方法,通过调节反应条件可控制备出不同形貌结构、粒径的ZnSnO。此外,研究还表明材料的形貌结构对ZnSnO性能影响较大。因此,需要根据不同应用要求的粒径尺寸、形貌等选择合适的制备方法。
本文综述了国内外关于锡酸锌纳米材料的主要制备方法、原理及应用研究进展,分析了各种制备方法的优缺点及存在问题,并指出每种制备方法中不同结构的形成机理以及不同结构是如何对ZnSnO相关性能产生影响的,以期为锡酸锌纳米材料的深入研究提供思路。文章最后对锡酸锌纳米材料未来发展方向进行了展望,阐述了锡酸锌纳米材料的应用领域以及未来还需要解决的问题。
1 锡酸锌的制备方法
锡酸锌目前常用的制备方法主要有水热法、共沉淀法、固相法、溶胶-凝胶法等,已工业化的方法主要是化学沉淀法。已报道制备出的锡酸锌晶体有不同的形貌,如颗粒状、立方体(实心、空心)、球形、八面体、纳米棒/线(环)、片状、纳米花状等。制备方法的不同会影响ZnSnO晶体的结构、微观形貌以及热稳定性,进而对锡酸锌材料性能产生影响。
1.1 水热法
水热法是指在高温高压密闭反应釜中,以水或其他溶液为介质制备纳米材料的一种方法。ZnSnO晶体的水热生长大多使用锌盐[ZnCl、ZnSO、Zn(NO)等]与氯化锡水溶液反应,添加不同种类碱,然后在密闭高压环境、温度200~250℃下制得。方军等用ZnAc和NaSnO为原料,(Zn)/(Sn)为2,温度180~200℃,采用水热法在聚四氟乙烯内衬的不锈钢反应釜反应48h,制备得到正八面体尖晶石型ZnSnO纳米粒子,其形貌如图1所示。

图1 水热法制备的正八面体Zn2SnO4的扫描电镜(SEM)图
除调控水热反应过程中的物理化学参数来影响晶体生长外,使用不同矿化剂和添加剂也可以控制锡酸锌晶体的微观形貌。Chen等以乙酸锌和锡酸钠为原料,添加乙二胺(EDA)和十六烷基三甲基溴化铵(CTAB),采用水热法在180℃下反应24h制备出由纳米棒构成的具有三维结构的锡酸锌纳米花,花簇平均直径为350nm,纳米棒直径为10~15nm,EDA和CTAB对形成三维花状结构起着重要作 用。Zhu 等以ZnSO·5HO 和SnCl·5HO 为 原料,NaOH为矿化剂,采用水热法制备出尖晶石结构的ZnSnO,适当调节NaOH 浓度及水热温度可以得到纯度较高以及结晶较好的ZnSnO晶体,其反应见式(1)~式(3)。

王 欣 等以Zn(CHCOO)·2HO 和SnCl·5HO为原料,NaOH为矿化剂,采用一步水热法制备出ZnSnO,随着NaOH 含量的增加,ZnSnO逐步由纳米级颗粒状向微米级针状和棒状结构转变,同时ZnSnO负极材料也逐步由纯相向杂相转变,原因在于ZnO和SnO等杂质物质的出现,如图2所示。

图2 NaOH添加量与Zn2SnO4结构关系的SEM图
空心结构的ZnSnO用于阻燃时能显著提升材料的阻燃效率和力学性能,原因在于空心结构能为锡酸锌提供更高的比表面积和更好的隔热功能。胡伟东等以碳球为模板,SnCl和Zn(NO)为原料,采用水热法制备出空心结构的ZnSnO(如图3 所示),直径约500nm,球壳厚度约50nm,将其应用于聚氯乙烯(PVC)阻燃。与纯PVC 相比,添加10g ZnSnO,PVC 材料极限氧指数(LOI)提升6.5%,(热释放速率峰值)、(烟释放速率峰值)、(烟释放总量) 分别降低24%、50.1%和53.6%,残炭率提升9%。
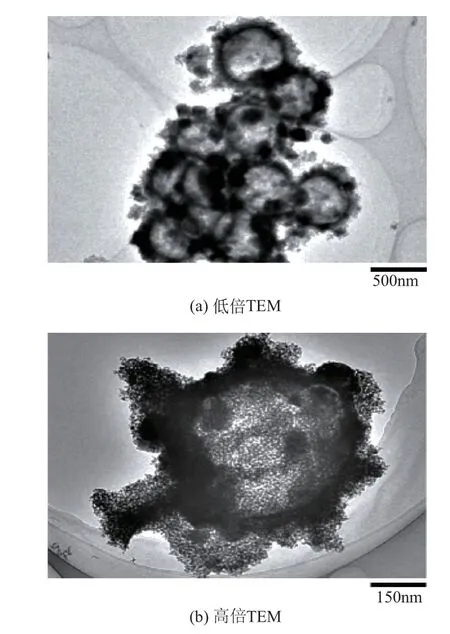
图3 水热法制备的Zn2SnO4空心球的透射电镜(TEM)图
水热法因具有产率高、纯度高、结晶效果好以及粒度均匀、操作简便、成本低廉等优点,能够制备出其他方法难以制备的超细锡酸锌颗粒,且在水热反应过程中可通过调节反应温度、反应时间、表面活性剂种类等因素调控晶体的生长,因此该法已被广泛应用于ZnSnO纳米材料的制备。水热法目前存在的最大问题是对设备要求较高,且安全性较差,难以连续操作,离工业化还有一段距离。
1.2 化学沉淀法
化学沉淀法是在可溶性溶液中添加沉降剂或在一定温度下利用水解反应将金属离子沉淀为氢氧化物或金属盐,经煅烧后得到氧化物粉末。常用的化学沉淀法有共沉淀法和均相沉淀法等。在制备ZnSnO纳米材料方法中,共沉淀法是较为常用的方法之一,共沉淀法主要在Zn/Sn盐溶液中添加碱性物质,在碱性环境中生成ZnSn(OH)纳米颗粒,然后经高温煅烧后得到ZnSnO纳米颗粒。化学沉淀法中锌盐种类、沉淀剂种类以及煅烧温度都可影响ZnSnO的形貌,而煅烧温度还能进一步影响粉体的结晶程度。
叶晨琳等以SnCl·5HO 为锡源,ZnCl为锌源,(Sn)∶(Zn)=1∶2,NaCO为沉淀剂,制得锡酸锌前体,然后在箱式电炉中1000℃下煅烧3h,成功制得尖晶石型高纯度ZnSnO纳米颗粒。郑秀君等以ZnSO·7HO 和SnCl·5HO 为原料,摩尔比2∶1,NaOH调节pH至7左右,采用化学共沉淀法制备出羟基锡酸锌,在700℃下煅烧7h,制得颗粒大小均匀的尖晶石型纳米ZnSnO,粒径小于30nm。Stambolova等通过0.5mol Zn(NO)·6HO和0.3mol SnCl·2HO与0.5mol NaCO的共沉淀法制备出ZnSnO的氢氧化物前体,再将前体在750℃下煅烧后获得平均尺寸为20nm的ZnSnO纳米晶粒。刘凤敏等按Zn/Sn 摩尔比2∶1 称取Zn(CHCOO)·2HO 和SnCl·5HO,加入去离子水将其溶解,滴加稀盐酸抑制其水解,配制20%稀NH·HO 作为沉淀剂,采用共沉淀法制备出ZnSn(OH),将其在马弗炉中煅烧2h 后得到粒径约20nm 的ZnSnO颗粒。何汉兵等以NaSn(OH)和ZnSO为原料进行ZnSnO共沉淀法制备研究,结果表明,NaSn(OH)和ZnSO分别为1.2mol/L 和1.3mol/L,室温反应4h,终点pH 9.4,转速900r/min 时,制得纯度99%、粒径3.8μm 的白色球形ZnSnO颗粒。其化学形成过程见式(4)~式(6)。

Wang等以SnCl·5HO和Zn(NO)为原料,摩尔比1∶2,溶解于水中,在搅拌条件下将混合溶液逐滴加入氨水中,控制pH 至8 得到前体,用去离子水洗涤除去前体中的Cl和NO,将干燥后的前体在1000℃下煅烧1h,制得粒径为300~500nm的ZnSnO空心球,如图4所示。

图4 沉淀法制备的Zn2SnO4空心球的SEM图
化学沉淀法具有工艺简单、条件易于调控、生产周期短、成本低、产物颗粒小且均匀,以及低能耗等优点,也是目前工业化生产ZnSnO最主要的方法。但该法存在的最大问题是ZnSnO容易团聚,且一般需要退火处理。
1.3 固相化学合成法
固相化学合成法是将金属盐或金属氧化物粉末按一定比例混合研磨,用去离子水洗涤,再经高温煅烧后形成固相粉体的一种方法。徐甲强等以ZnSO·7HO、SnCl·5HO、NaOH 为原料,室温下对混合物进行研磨,研磨过程中混合物发生反应生成ZnSn(OH),在600℃下高温热处理1h后得到平均粒径为30nm的ZnSnO颗粒。王中长等以同样的方法,按(ZnSO·7HO)∶(NaOH)∶(SnCl·5HO)=1∶1∶6,将原料混合放于玛瑙研钵中研磨反应,经去离子水洗涤后制得前体ZnSn(OH),后经高温煅烧得到ZnSnO纳米颗粒。其形成过程的化学式见式(7)~式(11)。

李杰康等以SnO和ZnO 为原料,按1∶1 摩尔比加入粉体研磨缸中,同时加入600mL 水,先低速研磨预混30min,后高速研磨12h,陈化30min,经去离子水洗涤过滤干燥后制得粒径1μm左右的ZnSnO粉体,如图5 所示。在合成ZnSnO过程中,为了避免ZnO的蒸发,目前已提出了不同的热处理方法。

图5 固相法制备的立方体形Zn2SnO4粉体的TEM图
固相化学合成法能否进行取决于固相反应的热力学函数,即总反应吉布斯函数改变值小于零。固相化学合成法的优点是反应过程为无溶剂反应,反应在室温下就可进行,且工艺流程简单,易于工业化,成本低廉,获得的粉体均匀无团聚等。该法的缺点是反应过程中会放出大量热,成核速度大于生成速度,超细颗粒的获得只能自然生成而不能完全控制,所以合成的晶粒粒径偏大且分布不均,存在较严重的团聚现象。此外,固相化学合成法存在能耗较高、对设备性能较高、反应时间长,且反应过程中容易混进杂质等问题。
1.4 微波合成法
微波合成法不同于传统的加热制备方法,由于微波可直接穿透样品对其进行加热,极大地加速了反应的进行和晶化的速度。自20 世纪80 年代被引入纳米材料合成领域以来,由于绿色环保且操作简便,越来越受到研究人员的青睐。Parthibararman等以SnCl·2HO 和ZnCl·2HO 为原 料,摩尔比1∶2,将其溶于去离子水中,然后强烈搅拌下滴加NH·HO,直至pH达到8,反应完成时,得到天蓝色沉淀物,后用去离子水清洗10 次以上,直至AgNO检测不到Cl,NH则用乙醇洗涤出去,将所得沉淀物转移至聚四氟乙烯内衬的微波炉(900W、2.45GHz)中,空气气氛照射10min,最后得到直径20~50nm、长度700nm 的纳米棒状ZnSnO,如图6所示。

图6 微波法合成的纳米棒状Zn2SnO4的SEM图
Zhang 等以锌盐和锡盐为原料,通过微波辅助方法合成了ZnSn(OH),后经高温煅烧得到平均粒径700nm 的锡酸锌微球。实验显示,通过调节Zn和Sn的比例可合成各种形貌(正八面体、正方体、球形)的ZnSnO,其比例及形貌如图7所示。

图7 采用微波法,在不同锌/锡比下合成的Zn2SnO4的形貌及X射线衍射(XRD)图
微波合成法最显著的优点是操作简便、能高效且快速地合成出粒度分布均匀的纳米颗粒,且生成的产物产率高、易纯化,具有比常规合成法更优异的性能。但该法存在的最大问题是成本较高,且工业化难度较大,目前只适合小批量生产。
1.5 溶胶-凝胶法
溶胶-凝胶法通常选择易于水解的无机盐或金属醇盐作为原料溶解于液相溶剂中,加入有机酸使之发生水解和单体缩聚反应后得到凝胶前体,后将凝胶进行陈化、干燥、煅烧后得到纳米颗粒。Wang 等采用溶胶-凝胶法制备出锡酸锌纳米粉体,其制备方法根据文献报道首先合成Sn(OH)(5mL/L)和Zn(OH)(2.8mL/L)胶体溶液,将胶体溶液混合后缓慢加入GO(氧化石墨烯)水悬浮液(0.4mg/L)中,随后逐渐出现棕色沉淀,将沉淀物离心并用去离子水洗涤3次,在60℃下干燥6h,最后将GO还原为还原氧化石墨烯(rGO),随后在氮气氛围中高温煅烧2h后,获得粒径4nm的ZnSnO/石墨烯阳极材料。
溶胶-凝胶法制备ZnSnO的优点主要是简单经济、纯度高、烧结温度低等。其存在的问题主要是其晶体生长取向几乎未受到外部限制,产物形貌可控性较差,产物多为不规则的小颗粒。
1.6 模板法
黄保军等以Zn(CHCOO)·2HO、SnCl·5HO和NaOH为原料,定量滤纸为模板,用生物模板法合成微纳米ZnSnO。结果显示,(Zn)/(Sn)=2时,可获得无杂质的立方晶型ZnSnO晶体,ZnSnO的结晶度随煅烧温度升高而增大,900℃为最佳,ZnSnO的形貌与定量滤纸形貌相似。陈灵智等以NaSnO为锡源,ZnSO为锌源,活性炭为模板,搅拌状态下使Zn充分进入活性炭微孔中,搅拌结束后将混合溶液移入水热釜中,220℃反应10h,经干燥煅烧后得到AC-ZnSnO复合材料。
模板法可借鉴和利用天然生物结构来实现特殊结构材料的制备,具有高效、便捷以及经济的优点。此外,模板法的特殊优点是可获得其他方法难以得到的高比表面积,但存在的问题是高温下模板去除后常伴随着孔结构的坍塌,从而大大降低材料的比表面积。因此,如何解决模板去除后材料的热稳定性是模板法应用的关键。
1.7 其他制备方法
唐香珺等以Al、CuO、ZnO、SnO 为原料,采用高温燃烧合成-喷射法制备出ZnSnO微纳米颗粒。其摩尔比按Al∶CuO∶ZnO∶SnO=10∶5∶4∶6,100 目过筛后混匀,倒入自制的燃烧合成装置中,用钨丝点火,引发反应,在反应器、炉壁、透气筛及接物盘中收集到大量ZnSnO,经SEM 分析其形貌有球形、纳米线,也有棱形,并趋于团簇状,如图8所示。经机理分析得反应式为式(12)。

图8 高温燃烧合成-喷射法制备的Zn2SnO4微纳米颗粒

纳米线的形成分析认为是SnO发生歧化反应生成SnO和Sn,而SnO的沸点是2073K,当被连续喷射出来时,便形成了纳米级的SnO纤维。
刘中奎以ZnO、SnO和活性炭粉末作为原料,按摩尔比1∶1∶1混匀,采用碳热还原热蒸发法成功合成出秧苗状的ZnSnO纳米线,如图9所示。

图9 碳热还原热蒸发法制备的秧苗状Zn2SnO4纳米线
近年来,随着新技术的发展,还出现了一些新的ZnSnO制备方法,如液相组装法、溶液燃烧法、球磨法等,以及将多种方法联用的制备方法,为ZnSnO功能化制备提供了新选择。
综上所述,不同制备方法及同一种方法下不同制备条件,会得到不同形貌结构、比表面积、粒径大小及分布不同的锡酸锌纳米颗粒,这些因素的不同会影响其相关应用性能。制备纳米锡酸锌的方法较多,每种方法都有优缺点及存在的问题,可根据具体应用需求选择合适的制备方法。水热法和化学沉淀法作为目前ZnSnO的主要制备方法,工业化应用相对成熟,多数不同形貌的ZnSnO多采用这两种方法来合成。但这两种方法目前仍有短板,未来可把重点放在研究水热法、化学沉淀法与其他方法的联用制备工艺上,综合利用各自优势,取长补短,有效控制锡酸锌的形貌结构及粒径分布。
2 锡酸锌的应用
锡酸锌凭借独特的结构、形貌优势,优异的导电性能、化学稳定性、吸附性和光学性能以及独特的阻燃抑烟性能等优势,近年来被广泛应用于锂离子电池负极材料、气敏材料、光催化、电触头材料以及阻燃抑烟剂等领域。
2.1 在锂离子电池中的应用
纳米ZnSnO具有独特的电子结构、良好的化学稳定性和较高的导电性,其较大的比表面积有效缩短了离子的扩散路径,获得了优异的电化学性能。其作为锂离子负极材料的优势在于理论容量高,达到1231mA·h/g,具有较高电导率(250S/cm),且其嵌锂电位较低、制备简单、环境友好等,在锂离子电池应用领域表现出良好的应用前景。
锡酸锌的制备方法决定了ZnSnO晶体的结构、热稳定性和微观形貌,进而影响其锂离子电池性能,锡基材料纳米化是提高其电化学性能的有效途径之一。2006 年,南开大学Rong 等采用水热法合成了ZnSnO,并首次将ZnSnO作为负极材料应用于锂离子电池,获得了988mA·h/g 的电化学容量,通过采用XRD 和TEM 对完成一次循环过程的电极材料进行分析,提出了ZnSnO属于合金储锂机制,与SnO和ZnO类似。Yuan等则进一步在水热法合成ZnSnO的配方中添加葡萄糖,经碳热还原法制备出ZnSnO/C 复合材料,该复合材料经40次充放电循环之后,电容量仍高达563.5mA·h/g,远高于纯ZnSnO的404.9mA·h/g。Jiang等也采用类似工艺制备出核壳结构的ZnSnO/C 纳米棒,直径8nm,将其用作锂离子电池负极材料,展现出较大的可逆容量和优异的循环性能,见图10。

图10 Zn2SnO4/C电接触材料Li存储容量和循环寿命
Wang 等则通过改变ZnSnO形貌,经水热法制备出花状ZnSnO复合材料,首次充放电容量高达1750mA·h/g。该复合材料具有较高的结晶度且不含杂质,独特三维结构的ZnSnO具有较大的比表面积,从而提供了较多的电化学活性位点,有利于电解质的扩散,减弱了电池在合金化及脱合金化过程中的体积改变,从而提升电池的循环性能。
虽然ZnSnO的储锂机理受其结晶度、形貌、晶体结构等因素影响,各研究团队对其机理分析不尽相同,但目前普遍认同ZnSnO属于合金化储锂机制。ZnSnO的电化学容量受晶体结构、粒径大小和形貌等影响,同时还与制备方法相关。锡酸锌用作锂电负极材料时,通常选择水热法进行合成。研究表明,采用水热法制备ZnSnO过程中,碱的种类及用量、表面活性剂种类及水热时间都会对ZnSnO形貌产生重要影响,进而影响其电化学性能。对锡酸锌纳米材料在锂电池负极材料中的应用,今后的研究重点应是对ZnSnO进行结构设计,进一步提高材料的储锂性能。
2.2 在气体传感器中的应用
与固体颗粒相比,中空结构的纳米材料因其密度低、比表面积大、高孔隙率和表面渗透性能,可以提供更多的表面活性位点、大比表面积和快速扩散能力,使气体更容易渗透到传感层,使其在气体传感器领域有较大的应用潜力。ZnSnO由于具有优异的结构优势以及光电性能和化学敏感性,因此近年来在气体传感器领域获得广泛关注。目前,已有多种形貌的ZnSnO用作气敏材料的研究,其对NO、正丁胺(CHN)、液化石油气(LPG)、CHOH、三乙胺(TEA)、HS 等气体表现出优异的气敏特性,见表1。

表1 Zn2SnO4对不同气体的气敏性能
Ma 等以ZnAc、SnCl和NaOH 为原料,Zn/Sn/Na摩尔比1/1/10,采用水热法130℃反应6h,经洗涤煅烧后得到空心八面体结构的ZnSnO,将其用作气体传感器时最佳工作温度为260℃,对HS 和CHOH 表现出高响应和快速恢复时间,灵敏度较高,对体积分数50×10的HS灵敏度为46,最低检测限为1×10,显然该灵敏度和恢复时间的提升归功于ZnSnO空心结构提供了更高的比表面积,如图11所示。

图11 Zn2SnO4空心八面体结构传感器对不同种类气体的灵敏度选择性图及对不同浓度H2S的响应图
Jiang 等将ZnCl、SnCl·5HO 及四乙基氢氧化铵加入CHOH 与HO 的混合液中,220℃反应6h,制得分层立方体结构的纳米ZnSnO,将其用作气体传感器时,其最佳工作温度350℃,对体积分数400×10的正丁胺灵敏度较好,达到102.2,重现性及选择性也较好,如图12所示。

图12 Zn2SnO4立方体与不规则结构传感器对不同气体的灵敏度图
具有高比表面积和完全电子耗尽的ZnSnO纳米结构显然对提高气体灵敏度是有利的,更大比表面积的空心结构以及花球形结构的锡酸锌显然对其气体传感性能也是有利的。目前,多数不同形貌的ZnSnO都选用水热法来制备,原因在于该法可对其形貌进行精准调控,高比表面积和良好限定的多孔结构能改善材料的气体响应速度。
2.3 在电触头材料中的应用
在低压接触器领域,MeO/Ag 电触头应用最为广泛,其中CdO/Ag性能较好,但Cd污染令其应用受限,SnO是最有可能替代CdO 的,但SnO存在与Ag 润湿性差的问题,而ZnSnO与Ag 同属面心立方结构,其结合性优于SnO,将其用于电触头,能获得优于现有电接触材料的性能。
叶晨琳等以四氯化锡和氯化锌为原料,碳酸钠作沉淀剂,通过沉淀法制备出ZnSn(OH),在1000℃箱式电炉中煅烧3h 后得到ZnSnO,经粉末冶金法制备出Ag/ZnSnO复合电接触材料,并对其做SEM、金相、电阻率、硬度及密度等分析。结果表明,Ag/ZnSnO的导电性能远优于相同条件制备的纯相ZnSnO,但硬度性能仍需改善,见表2。
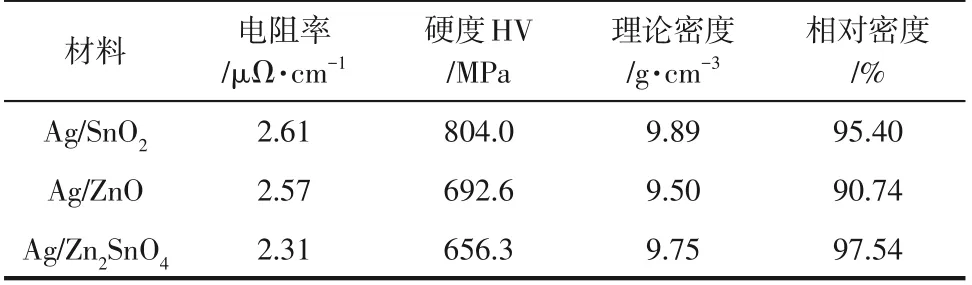
表2 不同增强相制得的Ag基电接触材料性能对比
隋晓涵等采用球磨-固相烧结法制备了粒径100nm的ZnSnO,经混粉(200r/min球磨4h)及初压(200mPa)-初烧(860℃、2h)-复压(1200MPa)-复烧(840℃烧结2h),制备出Ag/ZnSnO电触头材料,其相对密度达到97.1% 以上,硬度达到79.3HV,与商用Ag/SnO电触头相比,具有更明显的优势。
电触头材料的性能好坏取决于基体与第二相之间的润湿性,ZnSnO与Ag 有较好的结合性。此外,同一添加相不同粒度尺寸的ZnSnO对电触头材料性能的影响也较大,添加相尺寸减小能够提高电触头材料的导电性,这就涉及不同制备方式对其性能产生的影响。由此可见,制备性能优异的电触头,不仅要选择第二相材料,还要确定有益的制备工艺。
2.4 在染料敏化太阳能电池(DSSC)阳极材料中的应用
ZnSnO有较低的电子复合速率、高电子迁移率和光稳定性,在紫外条件下比TiO等稳定且开路电压更高,以及较高的电子迁移率和耐酸性,因此成为染料敏化太阳能电池光阳极材料的热门研究对象。
2007 年,Tan 等采用水热法合成粒径10~60nm 的ZnSnO颗粒,将其用作DSSC 光阳极,结果表明,在薄膜厚度小于6μm 时,ZnSnO太阳能电池效率高于TiO太阳能电池,在5.6μm时光电转化效率最大值达到3.8%。Al-Attafi等采用溶剂热反应合成了具有立方堆积结构的ZnSnO纳米颗粒,然后将其作为光阳极与D149染料组装成DSSC,测试结果表明,光电转换率达到4.9%。Chen 等首次将ZnSnO纳米线用作DSSC光阳极,尽管其染料吸附量不高且电池效率相对较低,但与ZnSnO纳米颗粒作DSSC 光阳极相比,其开路电压提高了0.1V 以上,原因在于纳米线有利于电子的传递,从而抑制了背电子传递过程。
除将ZnSnO用作光阳极外,对ZnSnO光阳极进行改性研究的报道也较多。Li等采用一锅法制备出ZnSnO纳米线,与SnO结合制备成由纳米线组成的SnO/ZnSnO中空微球,随后将SnO/ZnSnO微球作为光阳极,DSSC的整体光转换率为4.72%,比使用基于纳米棒分层结构的SnO微球DSSC提高了240%。杂化微球也被确定为高性能光催化剂,具有更好的可回收性,可用于模拟阳光照射下染料的光降解,太阳能利用率的提高主要归功于SnO和ZnSnO之间形成的异质结构提高了电子传输和电荷分离效率。Wang 等采用水热法合成ZnSnO,然后在10μm 厚的ZnSnO薄膜上印刷上一层TiO散射层,与未涂散射层时的ZnSnO相比,其使用效率从3.74%提升至5.72%。而Li等则选择在FTO表面印刷ZnSnO薄膜后,将其放入Al(NO)溶液中浸泡10min 进行钝化处理(如图13 所示),经测试后发现Al处理后开路电压降低了,ZnSnO的平带具有正偏移,Al引入ZnSnO晶格中并占据Sn位置,导致倒带边缘减小,但电子注入的驱动力大大增强,导致电池效率显著提升。

图13 Zn2SnO4表面处理工艺及反应机理
较多报道指出,ZnSnO纳米材料存在着团聚严重、粒径不一且形貌各异等问题,阻碍了ZnSnO透明半导体的发展,严重影响了DSSC光电转换效率,所以解决此类问题是提高DSSC 光电转换效率的关键所在。
2.5 在光催化中的应用
尖晶石型氧化物光催化剂在环境及能源领域应用前景广阔,ZnSnO作为高效稳定的光催化剂,由于带隙较大,在催化降解有机污染物及光解水制H等方面表现优异。2017 年,Seyed 等通过一步水热-原位合成法将ZnSnO颗粒成功负载在CNT 表面,制备出ZnSnO-CNTs 复合材料,将其用作光催化材料,对该材料的结构、形貌、光催化性能和光生载流子迁移效率进行了表征,同时探讨了该材料可见光活性增强的机理,其机理如图14 所示。结果表明,该复合材料用于光催化时,CNTs 不仅增强了ZnSnO的吸附性能,而且首次提出CNTs 能作为一种适当的自由基抑制材料,进而提高ZnSnO光生载流子的分离效率,如图14所示。

图14 CNTs增强Zn2SnO4光催化活性机理
赵春美通过研磨-煅烧法制备了ZnSnO负载g-CN的ZnSnO-CN光催化剂,XRD 结果表明,ZnSnO仍是立方晶系,反尖晶石结构,g-CN仍是石墨型结构,紫外-可见分光光度(UV-Vis)测试结果则表明该复合材料具有良好的可见光吸收能力。光催化实验结果表明,10% (质量分数)ZnSnO-CN对罗丹明B(RhB)的光催化降解效率为99.69%,对对硝基酚(PNP)的降解效率可达到96.75%,如图15所示。

图15 Zn2SnO4-C3N4降解RhB和PNP的机理图
陈强等等采用水热法和沉淀法合成了立方体、八面体和球体3种形貌的锡酸锌样品,经表征及光催化性能测试,实验结果表明,不同合成方法制备的3种锡酸锌样品均与纯相晶体结构一致,与具有八面体和球体形貌的锡酸锌相比,立方体形貌的锡酸锌具有更大的比表面积和更好的光催化性能,在模拟太阳光下照射180min 后对罗丹明B 的降解率可达到82%。
单一使用锡酸锌应用于光催化时,可见光利用率有限,效果欠佳,因此可通过改变ZnSnO制备方法,对其进行掺杂改性,能够增强光催化活性。此外,相对于八面体和球体,立方体形貌的锡酸锌粒径较小,分散性较好,比表面积相对较大,能够暴露更多的催化反应活性位点,获得最佳的光催化活性。
2.6 在阻燃领域的应用
锡酸锌由于具有优异的阻燃和抑烟性能,因此将其用作阻燃型高分子材料的阻燃剂和烟雾抑制剂,锡类阻燃剂作为一类新型高效、环保阻燃抑制剂,有望成为替代SbO的环保型阻燃产品。徐建中等将锡酸锌作为协效剂加入聚丙烯/聚磷酸铵/季戊四醇膨胀阻燃体系中,实验显示添加1%ZnSnO的聚丙烯(PP)/膨胀型阻燃剂(IFR)体系极限氧指数高达30.2%,且对材料力学性能影响较小,热重分析(TGA)表明,ZnSnO的加入提高了PP/IFR 体系的最大分解温度,降低了最大热失重速率,增加了成炭量,部分离子流也有所降低,与IFR有很好的阻燃协同作用。徐建中等又采用化学沉淀法制备出纳米级锡酸锌,将其用于软质PVC 的阻燃。实验显示,随着ZnSnO添加量的增加,阻燃软质PVC 的烧失量逐渐增大,烟密度等级(SDR)逐渐减小,当ZnSnO添加量为15 份时,LOI 可达36.0%,烟密度等级降低至86.2%,拉伸强度为25.47MPa,断裂伸长率为168%,见表3。
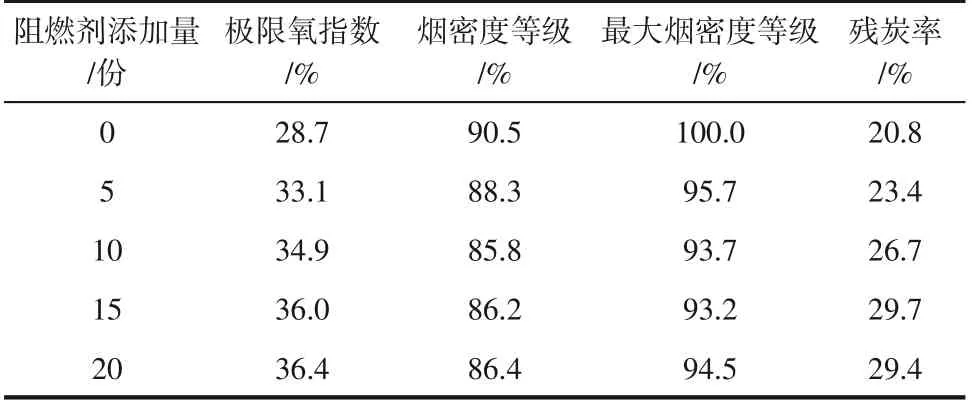
表3 Zn2SnO4对软质PVC阻燃消烟性能的影响
Horrocks等选用锡酸锌、磷酸芳基酯[间苯二酚(二苯基磷酸酯)]、环状有机磷酸酯、二乙基亚膦酸铝、三聚氰胺多磷酸酯,以及三聚氰胺尿酸酯单独或组合形式应用到聚酰胺(PA6)中,经导数热重-差热分析(DTA/DTG)、LOI、防火等级UL94、锥量及力学性能测试,结果表明,锡酸锌的添加对PA6阻燃性能的提升较为明显。
锡酸锌对PVC、聚丙烯(PP)、丙烯腈-苯乙烯-丁二烯共聚物(ABS)等高分子材料具有显著的阻燃和抑烟效果,是替代三氧化二锑的首选,但其价格昂贵,且与基材相容性较差,不适合大量添加,通常将其与CaCO、Al(OH)、Mg(OH)、高岭土、蒙脱土等复配来协同阻燃。研究表明,球形和无定形的锡酸锌都能明显改善PVC 的阻燃抑烟性能,但球形ZnSnO的阻燃抑烟效果优于无定形的ZnSnO。锡酸锌作为一类新型高效、环保阻燃抑制剂,在阻燃领域展现出很好的应用前景,如何降低成本、提高效率以及拓宽在高分子材料领域的应用范围仍是锡基阻燃剂市场化面临的挑战。
3 结语
ZnSnO纳米材料由于优异的性能在诸多领域已获得广泛应用,发挥着越来越重要的作用,不同形貌、结构及粒径的ZnSnO纳米材料具有不同的性质。理想的锡酸锌颗粒应该是高纯度、粒径小且处于单分散状态,因此欲制备出性能较好的ZnSnO纳米材料,需要控制最终产物的形貌、结构、粒径及较窄的粒径分布范围,减少颗粒团聚现象。
纳米锡酸锌的主要制备方法有水热合成法、化学沉淀法、固相化学合成法、微波合成法等,每种制备方法各有优缺点,水热法和化学沉淀法是目前最常用的两种工业化生产方法,但水热法制备锡酸锌目前还缺乏对其动态生长的系统性观察和研究。为弥补采用单一方法制备锡酸锌的缺陷,可将两种及以上的制备方法进行互补联用,如在溶胶-凝胶法中加入水热合成法的环节,可减少ZnSnO前体高温煅烧时的团聚现象等;引入超声波替代传统的搅拌操作,可有效控制晶粒大小及防止团聚。目前科研工作者已成功制备出颗粒状、立方体(实心、空心)、球形、八面体、纳米棒/线(环)、片状、纳米花状等形貌的ZnSnO复合材料,将这些材料应用在锂离子电池负极材料、气体传感器、电触头材料、光催化、DSSC及阻燃等领域。
锡酸锌纳米材料最重要的应用领域主要是锂电池负极材料、气敏材料和阻燃等。对ZnSnO纳米材料的制备和应用的研究还方兴未艾,随着其应用领域的扩大,对其综合性能提出了更高要求,目前仍有许多问题亟待解决。为此,制备锡酸锌纳米材料未来的研究重点应该围绕以下几点:①如何高效可控制备特定形貌和晶粒尺寸的锡酸锌仍是一个挑战;②深入研究纳米ZnSnO的合成机理,不同结构如何影响相关性能以及不同形貌控制机制。
