血管生成抑制剂治疗恶性胸膜间皮瘤的有效性及安全性的Meta分析
2022-06-23张彩苹
李 晶,张彩苹
0 引言
恶性胸膜间皮瘤(Malignant pleural mesothelioma,MPM)是一种治疗方法有限的恶性疾病,极为罕见,具有高侵袭性的特点[1]。MPM的标准治疗策略:①可手术切除的肿瘤,首选手术治疗,通常结合放疗和/或化疗;②不可切除的肿瘤则选择化疗或放疗[2]。考虑到超过50%的MPM患者在确诊时已居于晚期阶段,手术不能实施,因此,化疗成为首选的治疗方案。目前,唯一公认用于MPM的首选一线化疗方案为培美曲塞联合铂类[1]。然而,MPM肿瘤具有相对的化疗耐药性[3],以及MPM患者的预后近10年来未见明显改善[4],对于MPM的化疗已到达平台期。新的靶点和诊疗方法正在研究中,迫切需要改善患者预后,提高MPM治疗的标准[4]。对于MPM肿瘤细胞的生长,血管系统起着重要的作用,多种血管生长因子参与其中[5]。在MPM治疗中,血管生成抑制剂已与化疗药物联合使用,如尼达尼布联合培美曲塞[6]、西地尼布联合培美曲塞[7]、贝伐珠单抗联合培美曲塞[8],但目前国内外尚无血管生成抑制剂治疗恶性胸膜间皮瘤的系统评价。本研究对血管生成抑制剂治疗MPM的有效性及安全性进行Meta分析,为恶性胸膜间皮瘤的临床治疗提供循证学依据。
1 资料与方法
1.1 检索策略 全面通过计算机检索PubMed、The Cochrane Library、Embase、中国知网(CNKI)等数据库,检索自建库至2020年12月10日发表的文献,随后人工检索纳入RCT的相关参考文献。检索词为主题词+自由词的随机组合,中文检索词:胸膜间皮瘤,血管生成抑制剂;英文检索词:“Malignant pleural mesothelioma”,“Angiogenesis inhibitors”。
1.2 文献的纳入与排除标准
1.2.1 纳入标准 ①研究类型:随机对照试验(Randomized controlled trials,RCT),语种限定为中文及英文;②研究对象:经病理组织学确诊为MPM,且年龄>18岁的患者;③干预措施:干预组给予血管生成抑制剂+化疗,对照组为安慰剂+化疗或单独化疗;④测量指标:总生存期(Overall survival,OS)、无进展生存期(Progression-free survival,PFS)、3~5级不良反应。
1.2.2 排除标准 ①文献类型为摘要、综述、经验交流或会议报告;②文献内容重复、报告的信息量少导致数据无法被利用;③无法提取到相关数据的文献。
1.3 资料提取 由2名研究人员独自进行资料提取,若出现分歧则通过商议或由第3人决定。提取的数据包括:第一作者、发表年份、样本量、治疗措施、OS、PFS的危险比(Hazard ratio,HR)和95%可信区间(Confidence interval,CI)、3级以上不良反应例数。
1.4 质量评价 按照Cochrane系统评价手册对纳入的RCT进行质量评价,包括:随机性、分配隐藏、盲法的实施、数据的完整性、发表偏倚、其他偏倚等方面。
1.5 统计学处理 采用Cochrane系统评价软件Revman 5.3对所提取的相关数据进行Meta分析。从文献中直接提取PFS、OS的HR及其95%CI,若无法直接提取,则通过Kaplan-Meier生存曲线间接提取[9];不良反应发生率以相对危险度(Relative risk,RR)及其95%CI表示。异质性使用卡方检验,如果I2>50%或P<0.1,表示研究之间有异质性,采取随机效应模型,并对异质性的可能缘由进行查找,如果异质性非常大,需更改为描述性分析;反之,若I2<50%或P>0.1,表示不存在异质性,则采取固定效应模型。P<0.05为差异有统计学意义。
2 结果
2.1 文献筛选结果 经过检索中英文数据库获得相关文献222篇,21篇因重复发表被移除,剩余201篇。随后对文献标题及摘要进行简单阅读,排除不相关文献185篇,余16篇则通篇详细阅读。同时人工纳入1篇参考文献,最终共获得4篇文献[6-8,10],均为RCT。文献检索流程见图1。
2.2 纳入文献的基本特征及质量评价 4篇相关研究均为英文RCT,涉及1 384例患者。研究组均为血管生成抑制剂+化疗,分别为NGF-hTNF+化疗(吉西他滨、阿霉素或长春瑞宾)[10]、尼达尼布+培美曲塞[6]、西地尼布+培美曲塞[7]、贝伐珠单抗+培美曲塞[8],共690例患者;对照组为安慰剂+化疗或单独化疗,694例患者被纳入。文献基本特征见表1,质量评级见图2、图3。文献质量评分均为4分以上,质量尚可。
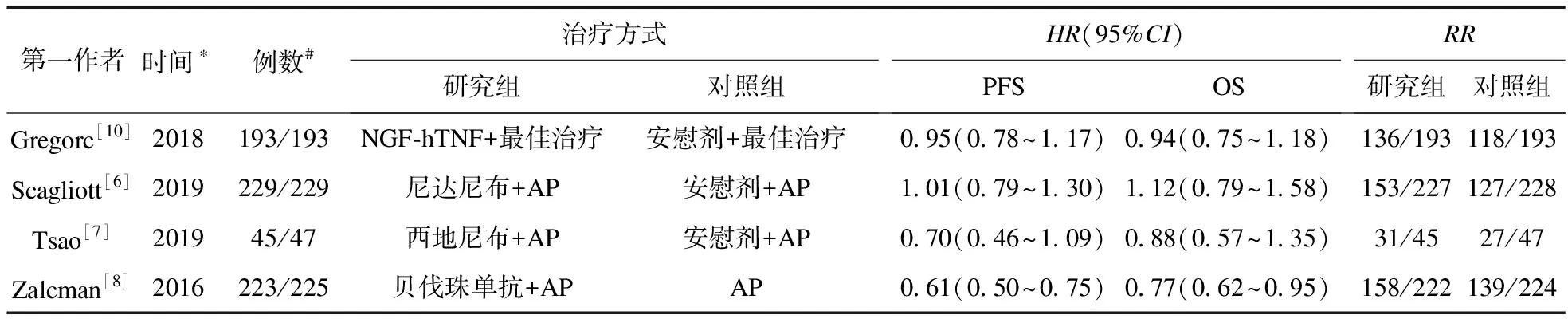
表1 文献基本特征

图2 偏倚风险比例

图3 偏倚风险总结
2.3 Meta分析结果
2.3.1 总生存期 纳入的4篇研究均包含OS的HR及95%CI,各研究结果之间无明显异质性(P=0.31,I2=17%),采用固定效应模型。结果显示,两组在OS方面差异无统计学意义(HR=0.89,95%CI:0.77~1.02,P=0.08)。进行亚组分析,既往有放疗或手术史的患者OS差异有统计学意义(HR=0.79,95%CI:0.65~0.96,P=0.02),表明既往有放疗或手术史的患者OS高于对照组。见图4。
2.3.2 无进展生存期 分析纳入文献的PFS,各研究之间有明显异质性(P=0.003,I2=78%),采取随机效应模型。结果显示,研究组和对照组在PFS方面差异无统计学意义(HR=0.81,95%CI:0.62~1.06,P=0.08)。随后对异质性过大的原因进行寻找,可能与既往史有关,随后采用亚组分析。亚组分析结果表明,既往有放疗或手术史的患者PFS优于对照组(HR=0.63,95%CI:0.52~0.75,P<0.000 1)。见图5。

图4 两组患者OS的Meta分析森林图
2.3.3 3~5级不良反应 纳入的4篇研究均涉及3级以上不良反应事件,进行异质性检验(P=0.95,I2=0%),使用固定效应模型。结果显示,血管生成抑制剂组的不良反应率是对照组的1.17倍,两组比较差异有统计学意义(RR=1.17,95%CI:1.08~1.27,P<0.000 1)。见图6。
3 讨论
血管生成是肿瘤生长和发展必不可少的因素[4],因此,血管生成靶向治疗一直被认为是多种癌症的选择方案[3]。研究表明,靶向血管生成可能与MPM特别相关[3]。培美曲塞与铂类联合应用是当下MPM患者的标准一线化疗方案,但过去10年MPM的预后基本保持不变[4]。目前,关于血管生成抑制剂治疗MPM的相关临床试验正处于进展中。
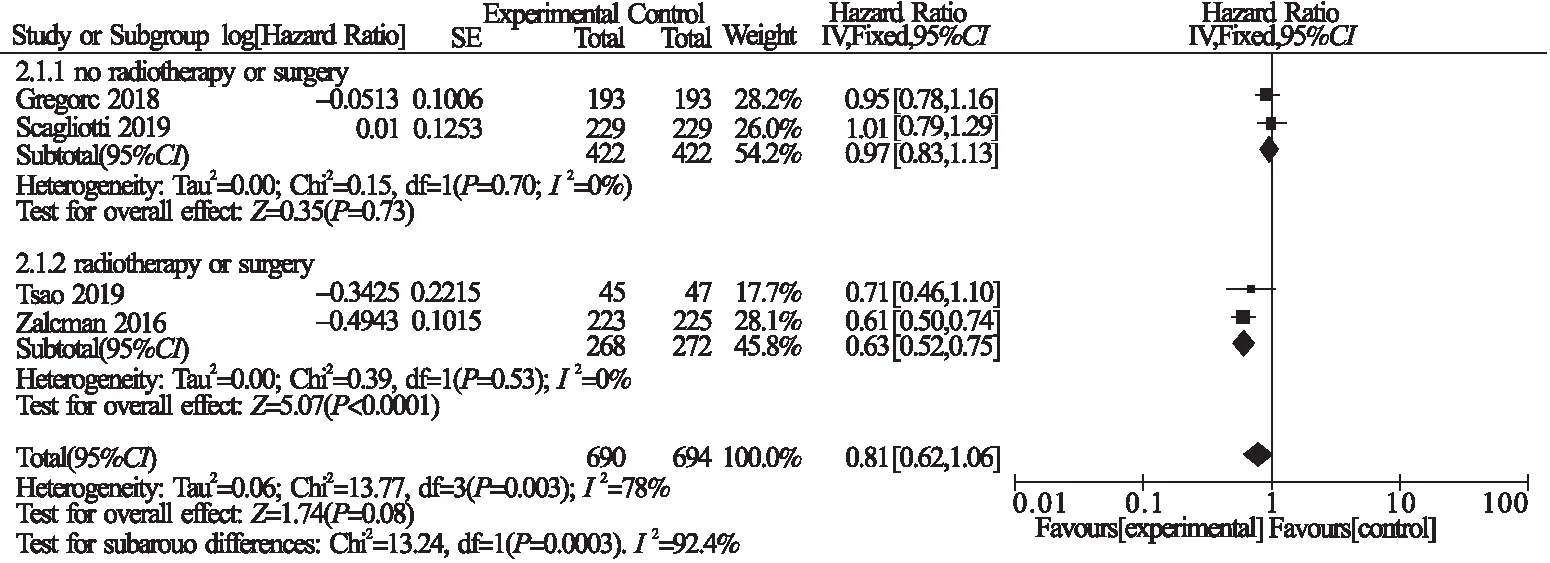
图5 两组患者PFS的Meta分析森林图
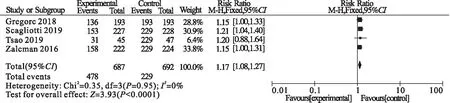
图6 两组患者RR的Meta分析森林图
Buikhuisen等[11]进行了一项随机Ⅲ期临床试验,首次研究了血管生成抑制剂沙利度胺治疗恶性间皮瘤(Malignant mesothelioma,MM)的有效性。研究随机分配了222例患者,试验组给予沙利度胺+积极支持治疗,对照组仅为积极支持治疗。积极支持治疗包括适当的镇痛、针对胸膜积液恰当的处理、必要时给予氧疗、关注患者的心理社会需求,以及必要时的联合治疗(如物理治疗)[11]。结果显示,沙利度胺组的中位进展时间为3.6个月(95%CI:3.2~4.1),而积极支持治疗组为3.5个月(95%CI:2.3~4.8)(HR=0.95,95%CI:0.73~1.2,P=0.72)。研究表明,在一线化疗中加入沙利度胺未使恶性间皮瘤患者获益。贝伐珠单抗是一种单克隆抗体,可与血管内皮生长因子(Vascular endothelial growth factor,VEGF)相结合,以破坏驱动血管生成的关键信号通路发挥效应[3]。Kindler等[12]评估了贝伐珠单抗联合吉西他滨/顺铂治疗MM的有效性。115例MM患者被纳入研究,试验组给予贝伐珠单抗+吉西他滨/顺铂,对照组为安慰剂+吉西他滨/顺铂。贝伐珠单抗组中位PFS为6.9个月,安慰剂组为6.0个月(P=0.88)。贝伐珠单抗组和安慰剂组的中位OS分别为15.6个月和14.7个月(P=0.91)。研究表明,贝伐珠单抗联合吉西他滨/顺铂并没有显著改善MM患者的PFS或OS。因以上两项研究中研究对象包含恶性腹膜间皮瘤,不符合纳入标准,故未纳入。
本研究一共纳入4篇英文文献,Meta分析结果显示,血管生成抑制剂组与对照组在OS和PFS方面差异无统计学意义[HR=0.89,95%CI:0.77~1.02,P=0.08;HR=0.81,95%CI:0.62~1.06,P=0.08]。随后进行亚组分析发现,既往有放疗或手术史的血管生成抑制剂研究组OS和PFS均高于对照组[HR=0.79,95%CI:0.65~0.96,P=0.02;HR=0.63,95%CI:0.52~0.75,P<0.000 1]。原因可能如下:①假设放疗和手术可以诱导促血管生成因子,随后靶向治疗可以提高抗肿瘤效果[7];②放疗和手术可以缩小肿瘤的体积,可能会使生存率提高[7];③纳入研究的数量较少,合并的样本数较低。年龄、MPM的病理分型、合并症等因素可能会对药物的有效性产生影响,因纳入文献数量有限以及数据的不完整性,故仅对既往有放疗或手术史因素进行了亚组分析。
在安全性方面,常见的不良反应包括血液学毒性和非血液学毒性,血液学毒性包括中性粒细胞减少、贫血及血小板减少,非血液毒性则包括恶心、呕吐、乏力、腹泻等[6-8,10]。结果显示,血管生成抑制剂组的3~5级不良反应率是对照组的1.17倍,两组差异有统计学意义。与化疗相比,增加血管生成抑制剂并未显著增加不良反应的发生率。
本Meta分析的局限性:①由于更多的血管生成抑制剂正在研究中,故可进行分析的RCT数目不多,样本量较少,可进行亚组合并的相关文献少,可能会对研究结论有影响;②其中纳入的一篇文献显示,MPM患者既往有培美曲塞一线化疗史,在用药期间或之后疾病进展[10],而其他文献纳入的患者既往无化疗史。该文献与其他文献有一定差异,对结果的产生可能会有影响。
综上所述,血管生成抑制剂对既往有放疗或手术史的MPM患者有一定疗效,且安全性尚可,但考虑到纳入RCT的数目较少、质量参差不齐等因素,未来还需更多大型、Ⅲ期随机对照临床试验来证实血管生成抑制剂对MPM的疗效。
利益冲突:所有作者均声明不存在利益冲突
