基于色泽量化与UPLC指纹图谱的不同产地荆芥药材质量评价△
2022-06-22王寿富田甜谢明晏崔婷姚晓璇程钰洁魏梅孙冬梅
王寿富,田甜,谢明晏,崔婷,姚晓璇,程钰洁,魏梅,孙冬梅
广东一方制药有限公司 广东省中药配方颗粒企业重点实验室,广东 佛山 528244
荆芥最早以“假苏”为别名记载于《神农本草经》[1],被列为中品,其药用部位为唇形科植物荆芥Schizonepeta tenuifoliaBriq.的干燥地上部分。荆芥采收季节为夏、秋二季,花开到顶、穗绿时割取地上部分,除去杂质,晒干。荆芥属临床上常用的解表类中药,其味辛,性微温,具有解表散风、透疹、消疮的功效,主要用于感冒、头痛、麻疹、风疹、疮疡初起等表证[2]。荆芥的种植产地众多,早期品种包括江苏产的“苏荆芥”、浙江产“浙荆芥”、河北产“祁荆芥”,随着栽培技术的进步,现今在全国各地区均有种植,主要包括安徽、河北、浙江、河南等地区[3]。
颜色是中药材及中药饮片鉴别和质量评价的常用指标之一,《中华人民共和国药典》(以下简称《中国药典》)2020 年版对荆芥的性状描述为“茎呈方柱形,表面呈淡黄绿色或淡紫红色,断面呈类白色。叶呈黄绿色,多已脱落。花冠黄绿色或淡棕色。小坚果外表呈棕黑色”[2]。药材性状中植株表面颜色和花冠颜色跨度较大,考虑药材产地分布较多,推测是由于不同产地药材差异较大,导致荆芥药材质量难以控制。
近年来,色泽量化原理被广泛应用于中药材及饮片颜色测定中,为中药材和饮片的质量评价提供技术支持和参考[4-5],但关于荆芥药材质量与色度值的相关性研究未见国内外文献报道。本研究采用超高效液相色谱法(UPLC)测定不同产地荆芥药材的指纹图谱,采用分光测色仪测定药材粉末颜色,同时测定醇溶性浸出物、水溶性浸出物及指标成分含量,运用SPSS 26.0 软件分析粉末颜色与各项测定指标的相关性,运用聚类分析、正交偏最小二乘法-判别分析(OPLS-DA)、熵权TOPSIS 法对不同产地荆芥药材进行质量评价研究,以期为荆芥药材的产地优化、质量评价提供依据。
1 材料
1.1 仪器
TS7700 型分光测色仪(深圳市三恩时科技有限公司);H-Class 型液相色谱仪(沃特世仪器公司);ME204E 型万分之一天平、XP26 型百万分之一天平(梅特勒-托利多仪器有限公司);KQ-700DE 型数控超声波清洗器(昆山市超声仪器有限公司);DHG-9147A 型电热恒温干燥箱(上海精宏实验设备有限公司);Milli-Q-Direct 超纯水系统(默克股份有限公司)。
1.2 试药
对照品迷迭香酸(批号:111871-201706,纯度:90.5%)、橙皮苷(批号:110721-201818,纯度:96.2%)、胡薄荷酮(批号:111706-201907,纯度:99.8%)均购自中国食品药品检定研究院;甲醇(分析纯,西陇科学股份有限公司);乙醇(分析纯,天津富宇精细化工有限公司);甲醇、乙腈(色谱纯,默克股份有限公司);磷酸(色谱纯,天津市科密欧化学试剂有限公司);水为超纯水(实验室自制)。
13 批荆芥药材经广东一方制药有限公司孙冬梅主任中药师、魏梅主任药师鉴定,均为唇形科植物荆芥Schizonepeta tenuifolia Briq.的干燥地上部分。安徽省亳州市产样品编号为S1~S3,河北省安国市产样品编号为S4~S6,浙江省萧山市产样品编号为S7~S10,河南省周口市产样品编号为S11~S13。样品均为10 月份花开到顶、穗绿时采割,药材的叶、花冠均多已脱落。
2 方法与结果
2.1 水溶性浸出物、醇溶性浸出物测定
按照《中国药典》2020 年版(四部)浸出物测定法(通则2201)项下的热浸法规定[6],分别以水、70%乙醇作溶媒,测定不同产地的荆芥药材水溶性浸出物、醇溶性浸出物含量,结果见表1~2。结果表明,水溶性浸出物、醇溶性浸出物值最高的样品分别为S5、S6;产自河北安国的样品水溶性浸出物均值、醇溶性浸出物均值最高,质量较为稳定。
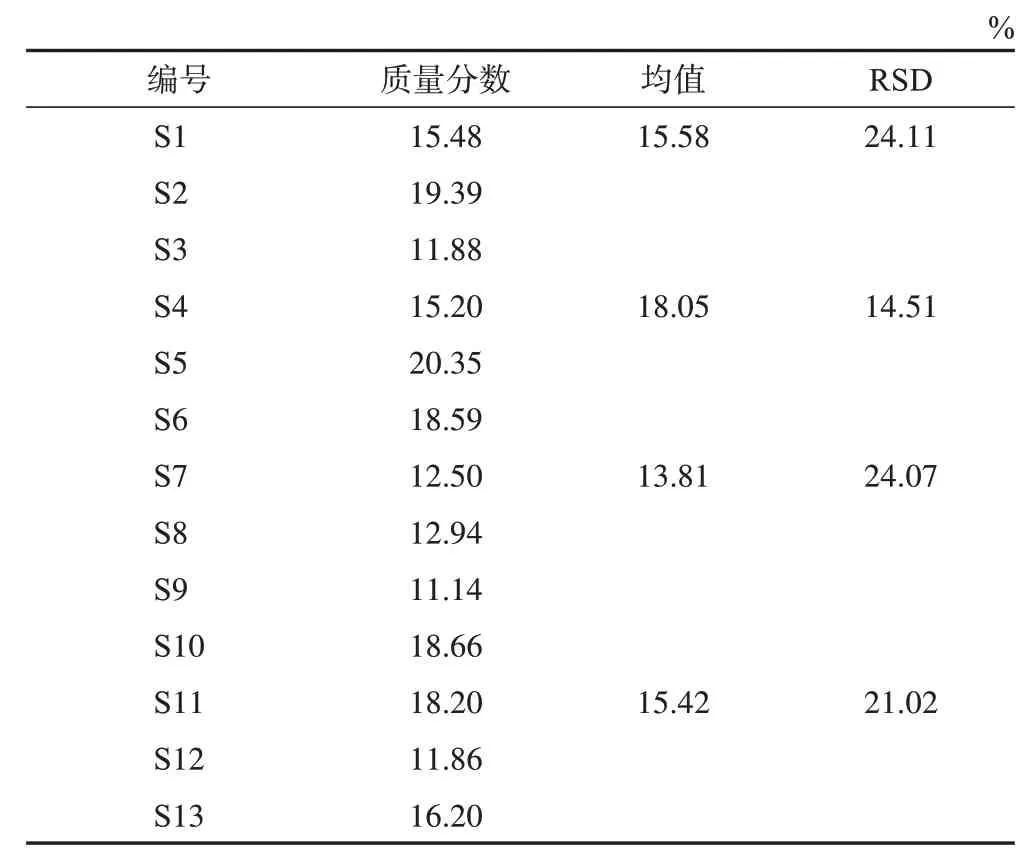
表1 荆芥药材水溶性浸出物质量分数
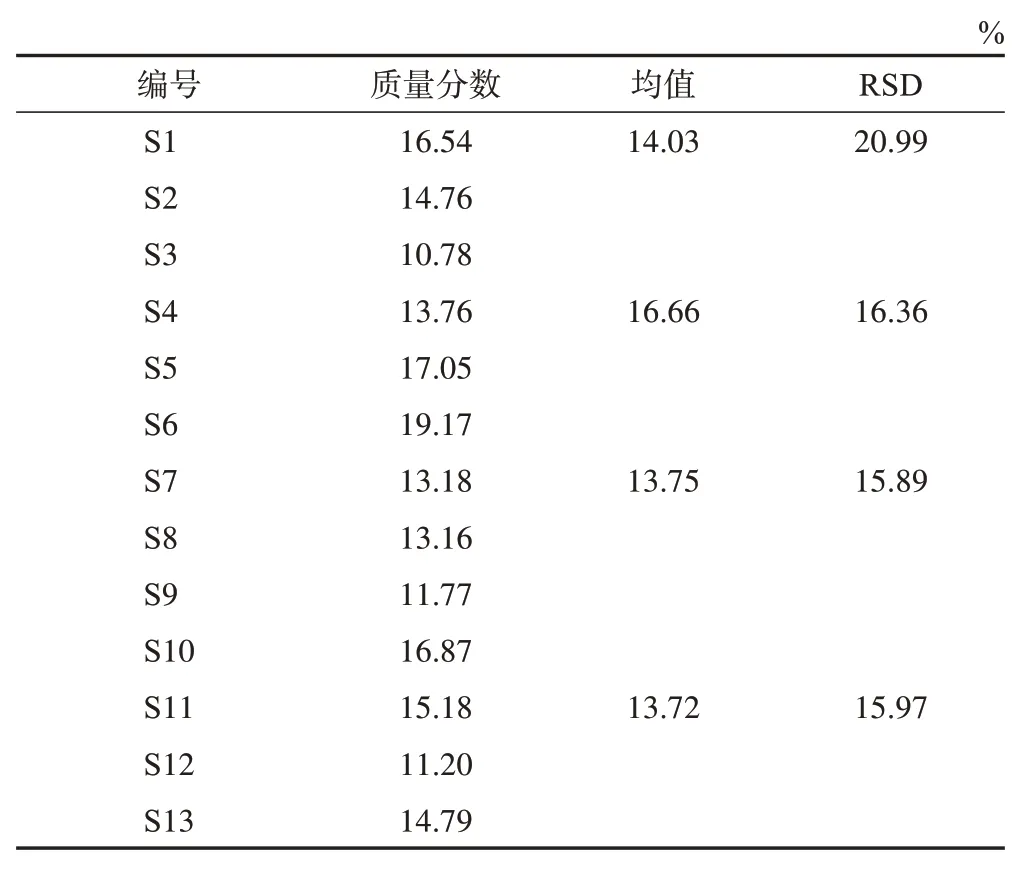
表2 荆芥药材醇溶性浸出物质量分数
2.2 指纹图谱的建立
2.2.1 色谱条件 色谱柱为Waters CORTECS UPLC T3 柱(150 mm×2.1 mm,1.6 μm);以乙腈为流动相A,0.1%磷酸水溶液为流动相B,梯度洗脱(0~6 min,10%A;6~11 min,10%~13%A;11~14 min,13%~15%A;14~27 min,15%~20%A;27~46 min,20%~30%A;46~56 min,30%~50%A;56~66 min,50%~60%A);检测波长为235 nm;柱温为30 ℃;流速为0.30 mL·min–1;进样体积为2µL。
2.2.2 单一对照品溶液的制备 分别取对照品橙皮苷、迷迭香酸、胡薄荷酮适量,精密称定,加甲醇制成分别含橙皮苷346.815 µg·mL–1、迷迭香酸245.725 µg·mL–1、胡薄荷酮148.078 µg·mL–1的单一对照品母液,备用。
2.2.3 供试品溶液的制备 取荆芥药材粉末(过二号筛)约0.5 g,精密称定,置具塞锥形瓶中,精密加入70%甲醇25 mL,密塞,称定质量,超声(功率250 W,频率40 kHz)处理30 min,取出,放冷,再称定质量,用70%甲醇补足减失的质量,摇匀,经0.22 μm微孔滤膜滤过,取续滤液,即得。
2.2.4 精密度试验 精密吸取同一供试品溶液(S1),按2.2.1项下色谱条件连续进样6次,以橙皮苷为参照峰,计算各色谱峰的相对保留时间和相对峰面积,结果表明各色谱峰的相对保留时间RSD 均小于0.5%,相对峰面积RSD 均小于3.0%,表明仪器精密度良好。
2.2.5 重复性试验 按2.2.3 项下方法平行制备同一供试品溶液(S1)6份,按2.2.1项下色谱条件测定,以橙皮苷为参照峰,计算各色谱峰的相对保留时间和相对峰面积,结果表明各色谱峰的相对保留时间RSD 均小于1.0%,相对峰面积RSD 均小于3.0%,表明该方法重复性较好。
2.2.6 稳定性试验 精密吸取同一供试品溶液(S1),按2.2.1 项下色谱条件分别在0、2、4、8、12、24 h 进样测定,以橙皮苷为参照峰,计算各色谱峰的相对保留时间和相对峰面积,结果表明各色谱峰的相对保留时间RSD 均小于1.0%,相对峰面积RSD 均小于3.5%,表明供试品溶液在24 h 内稳定性良好。
2.2.7 指纹图谱的建立 取不同产地的荆芥药材(S1~S13),按2.2.3 项下方法制备供试品溶液,按2.2.1 项下色谱条件进行测定,记录各批次荆芥药材的色谱图。运用“中药色谱指纹图谱相似度评价系统”(2012A 版),将13 批荆芥色谱图导入评价系统,以荆芥药材(S1)色谱图为参照,时间窗宽度设为0.1 min,采用多点校正法进行Mark 峰匹配,选择中位数法生成相应对照指纹图谱R,建立荆芥药材的UPLC 指纹图谱。13 批荆芥药材共标定21 个共有峰,通过与对照品比对,确定9 号峰为橙皮苷、10 号峰为迷迭香酸、17 号峰为胡薄荷酮。13 批荆芥药材的UPLC 叠加指纹图谱、对照指纹图谱R、单一对照品溶液色谱图见图1。
《自动化生产线综合实训》课程已于2018年秋期开放网上资源用于学生使用,让学生体验线上线下的“混合式”教学。目前已开发了网上资源,学生正在使用过程中。对于平台上的资源,大多数学生认为比较丰富,而且使用方便,尤其是视频课堂,短小易懂,可以在较短时间内学习相关知识和技能,学生认为经过网络课程和虚拟实训的学习,再动手操作实训,技能能得到提高,锻炼了分析问题、解决问题以及动手能力和小组协作能力的培养。
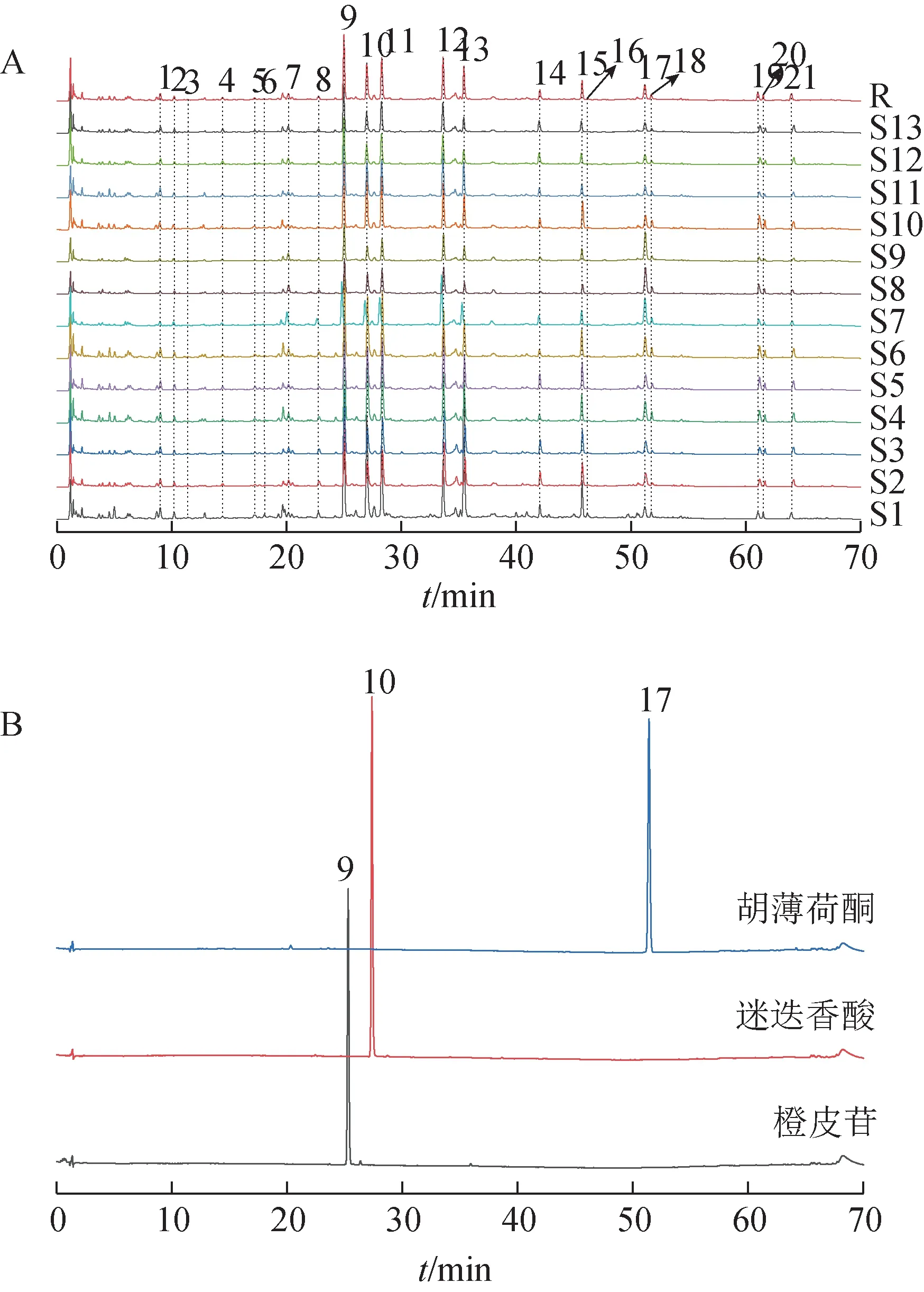
图1 荆芥UPLC叠加指纹图谱、对照指纹图谱R和单一对照品溶液色谱图
2.2.8 相似度评价 采用“中药色谱指纹图谱相似度评价系统”(2012A 版)分析软件,以荆芥药材对照图谱R 为参照,对不同产地的荆芥药材样品进行相似度一致性评价。结果显示,13 批荆芥药材(S1~S13)指纹图谱相似度依次为0.984、0.944、0.992、0.977、0.988、0.964、0.942、0.908、0.908、0.960、0.992、0.984、0.994,相似度均在0.9 以上,表明各批荆芥药材指纹图谱与对照图谱相似度较高。
2.3 含量测定
2.3.1 标准曲线制备 分别精密吸取2.2.2 项下单一对照品母液0.5、1.0、2.0、4.0、6.0、8.0 mL,置于25 mL 量瓶中,加甲醇稀释至刻度,得到系列混合对照品溶液。分别吸取上述混合对照品溶液适量,按2.2.1 项下色谱条件进样测定,以各成分的质量浓度为横坐标(X),以各成分对应的峰面积为纵坐标(Y),绘制标准曲线,得到橙皮苷、迷迭香酸、胡薄荷酮的线性回归方程分别为Y=11 100.0X–1 958.9、Y=4 866.8X–2 375.7、Y=15 794.0X–57 036.0,r分别为0.998 4、0.999 0、0.999 8,表明橙皮苷、迷迭香酸、胡薄荷酮质量浓度分别在6.936 3~110.980 8、4.914 5~78.632 0、2.961 6~47.385 0µg·mL–1与峰面积线性关系良好。
2.3.2 精密度试验 精密吸取2.3.1 项下混合对照品溶液(橙皮苷质量浓度为55.490 4 µg·mL–1、迷迭香酸质量浓度为39.316 0 µg·mL–1、胡薄荷酮质量浓度为23.692 5µg·mL–1),按2.2.1 项下色谱条件连续进样6 次,记录各成分的色谱峰面积。结果表明,橙皮苷、迷迭香酸、胡薄荷酮峰面积RSD分别为0.77%、0.89%、2.40%,表明仪器精密度良好。
2.3.3 稳定性试验 精密吸取同一供试品溶液(S1),按2.2.1 项下色谱条件分别在0、2、4、8、12、24 h 进样测定,记录各成分的色谱峰面积。结果表明,橙皮苷、迷迭香酸、胡薄荷酮峰面积RSD分别为0.94%、0.70%、3.20%,表明供试品溶液在24 h内稳定性良好。
2.3.4 重复性试验 按2.2.3 项下方法平行制备同一供试品溶液(S1)6份,按2.2.1项下色谱条件进行测定,记录各成分的色谱峰面积并计算质量分数。结果表明,橙皮苷、迷迭香酸、胡薄荷酮质量分数的RSD 分别为0.54%、0.87%、0.96%,表明该方法重复性较好。
2.3.5 加样回收率试验 称取已知含量的荆芥药材粉末(S1)9份,每份0.25 g,精密称定,按对照品加入量与供试品中待测定成分含量之比0.5∶1.0、1.0∶1.0、1.5∶1.0 的原则,精密加入橙皮苷、迷迭香酸、胡薄荷酮对照品,按2.2.3 项下方法制备供试品溶液,按2.2.1 项下色谱条件进样测定,计算得到橙皮苷、迷迭香酸、胡薄荷酮的加样回收率和RSD,结果见表3。结果显示,橙皮苷、迷迭香酸、胡薄荷酮含量测定分析方法回收率分别为96.51%~100.51%、96.68%~101.04%、96.52%~100.51%,RSD 分别为1.45%、1.50%、1.45%,符合《中国药典》2020 年版9101 药品质量标准分析方法验证指导原则要求。

表3 荆芥药材中3个成分的加样回收率试验结果
2.3.6 样品含量测定 取荆芥药材粉末,按2.2.3项下方法制备供试品溶液,按2.2.1 项下色谱条件对荆芥药材的橙皮苷、迷迭香酸、胡薄荷酮含量(以干燥品计)进行测定,结果见表4。结果表明,橙皮苷含量、胡薄荷酮含量最高的分别为安徽亳州、浙江萧山产荆芥,河北安国产荆芥药材的橙皮苷含量RSD、迷迭香酸含量RSD 相对较低,质量较稳定。

表4 荆芥药材中指标成分质量分数
2.4 色度值测定

2.4.2 精密度试验 取同一样品粉末(S1)适量,按2.4.1项下方法连续测量6次,记录色度值,结果表明L*、a*、b*值的RSD 均小于3.5%,表明仪器精密度良好。
2.4.3 重复性试验 取同一样品粉末(S1),平行测定6 份,记录色度值,结果表明L*、a*、b*的RSD均小于3.0%,表明该方法重复性良好。
2.4.4 稳定性试验 取同一样品粉末(S1),按2.4.1 项下方法压制成薄片,在室温下放置0、2、4、6、8、10、12 h后,测定色度值。结果表明,L*、a*、b*的RSD均小于3.0%,表明样品稳定性良好。
2.4.5 样品色度值测定 取13 批不同产地的荆芥药材,按2.4.1 项下方法进行色度值测定并计算E,每批样品平行测定3次,取平均值,结果见表5。
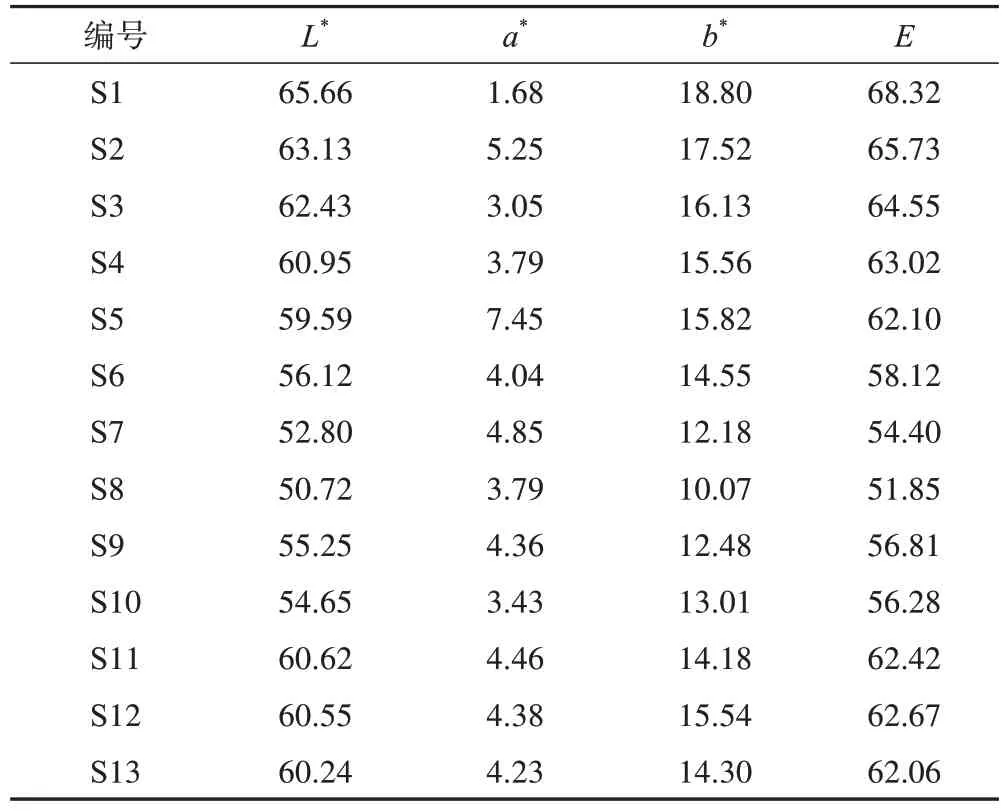
表5 荆芥药材色度值
2.5 荆芥药材数据分析
2.5.1 荆芥色度值与各项测定指标的相关性分析 利用SPSS 26.0 软件对荆芥药材浸出物、指标成分含量及色谱峰面积与色度值参数进行皮尔逊(Pearson)分析,结果见表6。结果表明,峰1分别与L*、b*、E值呈高度正相关,胡薄荷酮含量、峰17分别与L*、b*、E值呈显著负相关,橙皮苷含量、峰9分别与b*值呈显著正相关;峰3 分别与L*、b*、E值呈显著正相关,橙皮苷含量、峰9分别与L*、E值呈显著正相关,峰7、18 分别与L*、E值呈显著负相关,峰5、11、13、14、16 分别与b*值呈显著正相关,表明荆芥药材中化学成分含量与药材颜色具有较高的相关性。此外,水溶性浸出物、醇溶性浸出物含量与色度值相关性较低,表明从药材粉末色度值无法辨别浸出物含量的高低。

表6 荆芥药材色度值与浸出物含量、指标成分含量、色谱峰面积相关性分析
2.5.2 荆芥药材色度值聚类分析及质量标志物分析 将荆芥药材的色度值参数导入SIMCA 14.1软件进行层次聚类分析(HCA)。由图2 可知,当相对聚类距离为15 时,13 批样品可聚为两类:S6~S10 聚为一类,以浙江萧山产荆芥为主;S1~S5、S11~S13聚为一类,以安徽亳州、河北安国、河南周口产荆芥为主。
基于色度值的聚类分析结果,对13 批荆芥药材的测定指标进行OPLS-DA。模型参数累积方差贡献率(R2Y)为0.954,预测优度系数(Q2)为0.783,均大于0.5,表明此模型为优质模型。进而对OPLSDA 模型中变量重要性投影(VIP)进行分析,结果见图3。对各指标的VIP 值大小进行排序,选择VIP值>1 的成分变量作为区分荆芥药材的质量标志物,包括峰17(胡薄荷酮,VIP 值为2.370 8)、9(橙皮苷,VIP 值为2.083 1)、13(VIP 值为2.013 2)、10(迷迭香酸,VIP 值为1.547 7)、11(VIP 值为1.479 2)、12(VIP 值为1.231 8)、14(VIP 值为1.128 6),说明基于色度值聚类分析的结果,峰9~14、17 对不同产地荆芥药材的质量具有显著影响,可以作为区分不同产地荆芥药材的质量标志物。

图3 荆芥药材各测定指标OPLS-DA模型VIP分析
2.5.3 不同产地荆芥药材熵权TOPSIS 法分析 熵权TOPSIS法是基于评价指标的信息熵大小,根据评价对象与理想化目标的接近程度进行顺序优选的一种多指标决策分析方法[7-9],该分析方法能客观评价不同批次荆芥药材的质量。对13 批荆芥药材的色度值参数、指标成分含量、浸出物含量及色谱峰峰面积等指标建立初始决策矩阵,根据公式(2)~(3)将矩阵转化为标准化决策矩阵,计算越大越优型指标和越小越优型指标(Rij);按照公式(4)~(5)计算熵值(Ej)和权重(vj)。根据公式(6)确定加权决策矩阵(Z);根据公式(7)~(8)计算得出最优方案(Z+)与最劣方案(Z–),再根据公式(9)计算每个样品与最优方案(Z+)、最劣方案(Z–)的距离得到最优解的欧氏贴近度(Ci),并进行排序,结果见表7。结果显示,排名前5名的是安徽亳州产S1 样品、河北安国产S4~S6 样品、浙江萧山产S10 样品。根据13 批样品的欧式贴近度值(Ci),安徽亳州、河北安国、浙江萧山、河南周口4个产地荆芥的平均Ci值分别为0.432 3、0.475 0、0.362 0、0.251 3,表明河北安国所产荆芥的质量整体高于安徽亳州、浙江萧山、河南周口产样品。
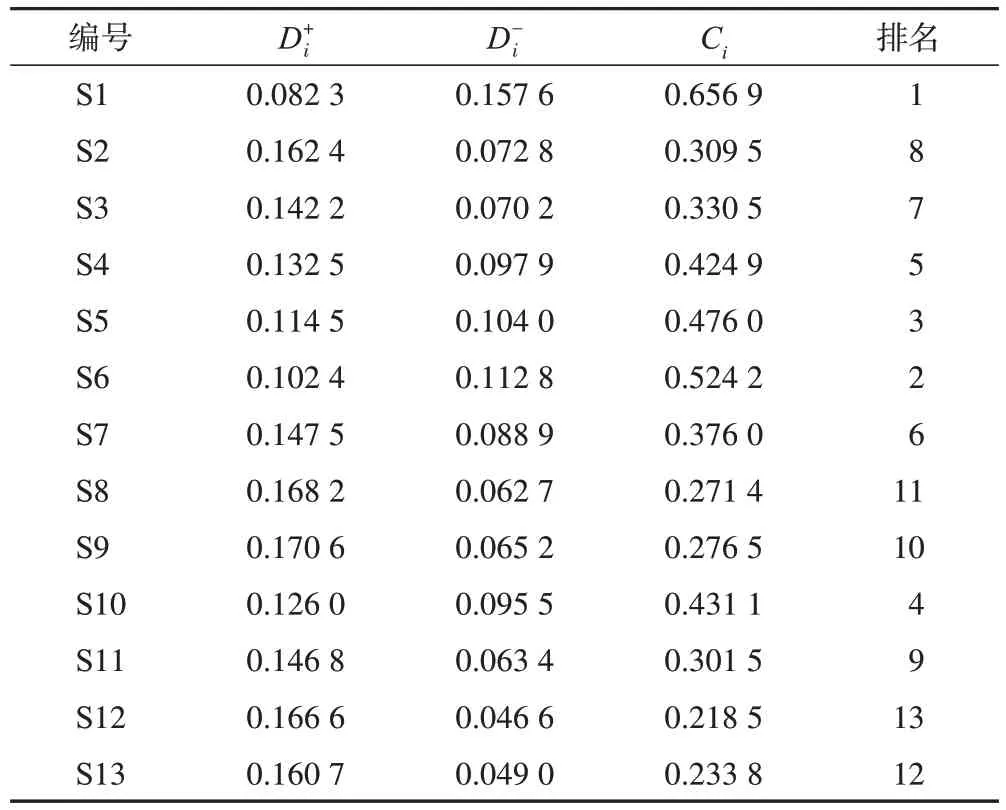
表7 荆芥药材的熵权TOPSIS分析

式中,i为样本数(i=1,2,……,m),j为评价指标(j=1,2,……,n)。
3 讨论
随着中药材人工种植的推广,对药材进行质量检测和控制显得尤为重要,而颜色作为中药最直观的外在特征之一,与中药质量密不可分[10]。《中国药典》2020 年版对荆芥药材性状中颜色描述较为宽泛,且药材产地分布较多,不同产地药材有差异,难以有效控制荆芥药材的质量。本研究基于CIELAB 色彩空间理论,利用分光测色仪测定荆芥药材的色度值,以期通过外在表征快速评价药材质量。荆芥药材表面颜色与内部颜色不均一,而粉末具有较好的均一性和稳定性,故本研究采用荆芥药材粉末进行实验。通过色度值与各指标的相关性分析,发现峰1、3、9、17,胡薄荷酮含量,橙皮苷含量均分别与L*、b*、E值密切相关;峰7、18 分别与L*、E值密切相关,峰5、11、13、14、16 分别与b*值密切相关。由此说明荆芥药材中的化学成分含量高低与其粉末色度值具有紧密相关性,测定药材粉末的色度值可初步预估其中化学成分的含量高低,为荆芥药材的质量评价提供依据。此外,水溶性浸出物、醇溶性浸出物含量与色度值相关性较低,说明从药材粉末色度值无法预测浸出物含量的高低。
荆芥在全国大部分地区均有种植,早期江苏太仓产“苏荆芥”、浙江萧山产“浙荆芥”、河北安国产“祁荆芥”质量较优,如今随生态环境变化、栽培技术的发展,产地成为影响荆芥药材质量的重要因素之一[3]。苏畅等[11]研究表明,山东、河北、安徽等中部地区土地肥沃,土壤含水量较高,且挥发油含量高,是荆芥最适宜的种植区。本研究以13 批荆芥药材为研究对象,运用HCA、OPLS-DA对不同产地荆芥药材进行分析。由色度值的聚类分析结果可知,浙江萧山产荆芥聚为一类;安徽亳州、河北安国、河南周口产荆芥聚为一类,表明此3 个产地的药材颜色性状较为相似。OPLS-DA 发现峰17(胡薄荷酮)、9(橙皮苷)、13、10(迷迭香酸)、11、12、14 共7 个成分的VIP 值均大于1,是重要的成分变量,提示此7 个成分可作为不同产地荆芥药材的质量标志物。结合熵权TOPSIS 法对13 批荆芥药材中的色度值参数、指标成分含量、浸出物及色谱峰峰面积进行综合质量评价,结果表明河北安国所产荆芥质量较佳,同时河北产“祁荆芥”的L*、b*值均较大,由此可以推测L*值越大、b*值越大(即药材粉末颜色越亮、越黄),荆芥药材质量越好,这与《中华道地药材》荆芥项下规定“色淡黄绿色”[12]相呼应。
本研究所建立的荆芥药材的UPLC 指纹图谱测定方法稳定可靠,并通过研究各项测定指标与色度值的相关性,结合多种统计分析方法对不同产地的荆芥药材进行整体质量差异研究,可为荆芥药材的质量评价提供参考。
