鸭公树子中生物碱类成分及抗炎镇痛活性研究△
2022-06-22李君梁晓
李君,梁晓
1.湘潭医卫职业技术学院,湖南 湘潭 411102;2.桂林医学院 药学院,广西 桂林 541199
鸭公树子为樟科(Lauraceae)新木姜子属(NeolitseaMerr.)植物鸭公树N.chuiiMerr.的干燥成熟种子,被收载于《中华本草》[1]。鸭公树,又名沙樟、假桂皮、青胶木、榄味新木姜等,为常绿乔木,广泛分布于福建、江西、湖南、广东、广西、贵州、云南等地的山谷疏林中[2]。传统医学认为鸭公树子的功效为行气止痛、利水消肿。前期已从鸭公树子乙酸乙酯部位和正丁醇部位分离出14 个化合物,主要是二苯乙烯类、黄酮类、小分子脂肪族类等成分[3-4]。为了进一步阐明鸭公树子药材作用的物质基础,更好地利用鸭公树子植物资源,本研究以干燥处理后的鸭公树子药材为材料,经过95%乙醇提取、三氯甲烷萃取,结合薄层色谱法(TLC)、Sephadex LH-20 柱色谱法及高效液相制备色谱法,对其中的生物碱类成分进行了分离及结构鉴定,从中共分离鉴定出9 个生物碱类化合物,分别为樟苍碱(1)、N-甲基樟苍碱(2)、乌药碱(3)、波尔定碱(4)、新木姜子碱(5)、杏黄罂粟碱(6)、异紫堇定碱(7)、烟酰胺(8)、N-反式阿魏酰酪胺(9)。并对其进行了抗炎镇痛活性评价。
1 材料
1.1 仪器
Photolysis-TOF MS 型高质量质谱仪(英国Kore公司);AVANCE-500 型核磁共振仪(瑞典Bruker公司);LC-8A 型高压制备液相色谱仪(日本岛津仪器公司);X6 型熔点测定仪(深圳科联仪器有限公司);RE-2000A 型旋转蒸发仪(上海亚荣生化仪器有限公司);BPG-9030BH 型电热恒温鼓风干燥箱(上海和呈仪器制造有限公司);SHZ-D(Ⅲ)型循环式水真空泵(郑州科达机械仪器设备有限公司);HH-2型数显恒温水浴锅(上海新诺仪器集团有限公司);OVP-60 型无油真空泵[陆冠森生物科技(上海)有限公司];BSA224S 型电子天平(德国赛多利斯仪器公司)。
1.2 试药
鸭公树子采自湖南省邵阳市隆回县、湖南省邵阳市洞口县,经湖南中医药大学刘塔斯教授鉴定为樟科新木姜子属植物鸭公树Neolitsea chuiiMerr.的成熟种子,其标本(编号:YGSZ-2019-1216)保存于湘潭医卫职业技术学院中药标本馆。
制备型薄层硅胶F254(德国Merck 公司);薄层色谱硅胶G(10~40 μm,青岛海洋化工厂);Sephadex LH-20 柱色谱(瑞典Amersham Pharmacia Biotech AB 公司);阿司匹林片[批号:20210524,远大医药(中国)有限公司];甲醇、乙醇、三氯甲烷均为分析纯(天津四友精细化学品有限公司);水为自制双蒸水。
1.3 实验动物
清洁级昆明种小鼠240 只,雌雄各半,体质量(170±15)g,由湖南省实验动物中心提供,实验动物生产许可证号:SCXK(湘)2016-0001。实验经中南大学湘雅医学院伦理委员会审批,批准号:伦审(科)2021-2-1024。
2 提取与分离
取鸭公树子10.0 kg压碎后,以95%乙醇加热回流提取3 次,每次1 h。滤过,弃去药材残渣,合并乙醇提取液,减压浓缩至无醇味,得乙醇提取物浸膏763.6 g。将此浸膏以蒸馏水10 L 分散后,加入0.1 mol·L–1硫酸溶液,调节pH 为2~3,用三氯甲烷8 L 萃取4 次,加入0.1 mol·L–1氢氧化钠溶液调节pH 为9~10,再用三氯甲烷8 L 萃取3 次,合并萃取液,减压浓缩后得到鸭公树子总生物碱粗提物(28.0 g)。
取总生物碱粗提物20.0 g,采用三氯甲烷-甲醇(90∶10→0∶100)梯度洗脱,以TLC 检测洗脱液,合并相同部分,得到4个流分(Fr.1~Fr.4)。其中,Fr.1 经Sephadex LH-20 柱色谱分离,以甲醇洗脱,得到化合物8[40 mg,tR=12.4 min)、9(26 mg,tR=21.6 min)。Fr.2 经半制备液相色谱(甲醇-水,35∶65,流速为2.0 mL·min–1)分离,得到化合物1(65 mg,tR=15.5 min)、5(28 mg,tR=26.8 min)。Fr.3 经半制备液相色谱(甲醇-水,45∶55,流速为2.0 mL·min–1)分离,得到化合物3(24 mg,tR=19.7 min)、4(43 mg,tR=26.2 min)。Fr.4经Sephadex LH-20柱色谱分离,以甲醇洗脱,再经半制备型液相色谱(甲醇-水,60∶40,流速为2.0 mL·min–1)分离得到化合物2(48 mg,tR=12.2 min)、6(19 mg,tR=18.4 min)、7(31 mg,tR=29.5 min)。
3 结构鉴定
化合物1:棕黄色固体,mp 102.4~103.1 ℃。ESI-MSm/z327.4 [M+H]+。1H-NMR (500 MHz,CD3OD)δ:7.96(1H,s,H-11),6.77(1H,s,H-3),6.70(1H,s,H-8),4.19 (1H,dd,J=13.5,4.5 Hz,H-6a),3.83 (3H,s,2-OCH3),3.82 (3H,s,10-OCH3),3.66(1H,dd,J=13.0,6.0 Hz,H-5),3.62 (3H,s,1-OCH3),2.98 (1H,dd,J=17.0,4.5 Hz,H-4),2.87 (1H,dd,J=14.0,4.5 Hz,H-7)。13C-NMR (125 MHz,CD3OD)δ:155.4 (C-2),148.6 (C-10),148.2 (C-9),146.7 (C-1),128.5 (C-7a),127.9 (C-3a),127.7(C-1b),124.3(C-1a),122.2 (C-11a),116.2 (C-8),113.3 (C-3),112.1(C-11),60.8(1-OCH3),56.9(2-OCH3),56.7(10-OCH3),54.8(C-6a),42.8(C-5),34.4(C-7),26.6(C-4)。以上数据与文献报道基本一致[5],故鉴定化合物1 为樟苍碱。
化合物2:棕黄色固体。ESI-MSm/z342.1[M+H]+。1H-NMR (500 MHz,CD3OD)δ:7.94 (1H,s,H-11),6.81 (1H,s,H-3),6.77 (1H,s,H-8),4.07 (1H,dd,J=13.5,4.5 Hz,H-6a),3.84 (3H,s,2-OCH3),3.82 (3H,s,10-OCH3),3.62 (1H,dd,J=13.0,4.5 Hz,H-5),3.61 (3H,s,1-OCH3),3.29 (1H,dd,J=17.0,6.0 Hz,H-4),3.25 (1H,dd,J=14.0,4.5 Hz,H-7),3.12 (3H,s,N-CH3)。13C-NMR (125 MHz,CD3OD)δ:155.6 (C-2),148.7 (C-10),148.3 (C-9),146.8 (C-1),128.9 (C-7a),127.9 (C-1b),127.8 (C-3a),124.1 (C-1a),122.1 (C-11a),116.4 (C-8),113.5 (C-3),111.9(C-11),64.3 (C-6a),60.8 (1-OCH3),56.9 (10-OCH3),56.7 (2-OCH3),54.1 (C-5),42.5 (N-CH3),32.6 (C-7),27.5 (C-4)。以上数据与文献报道基本一致[6],故鉴定化合物2为N-甲基樟苍碱。
化合物3:白色粉末。1H-NMR (500 MHz,CD3OD)δ:7.08 (2H,d,J=8.4 Hz,H-2′,6′),6.72(2H,d,J=8.4 Hz,H-3′,5′),6.64 (1H,s,H-8),6.61(1H,s,H-5),3.79(3H,s,-OCH3),3.16~2.68(4H,m,H-3,4)。13C-NMR (125 MHz,CD3OD)δ:156.4 (C-4′),147.3 (C-6),146.1 (C-7),130.0 (C-2′,6′),125.1(C-1′),123.4(C-8a),122.1(C-4a),116.1(C-3′,5′),112.5(C-8),109.8(C-5),56.1(C-1),54.6(-OCH3),39.1 (C-7′),38.2 (C-3),24.2 (C-4)。以上数据与文献报道基本一致[7],故鉴定化合物3为乌药碱。
化合物4:无定形粉末,与碘化铋钾试剂反应呈阳性。ESI-MSm/z360.1[M+Na]+。1H-NMR(500 MHz,CD3OD)δ:7.84(1H,s,H-11),6.70(1H,s,H-8),6.48(1H,s,H-3),3.77 (3H,s,10-OCH3),3.56 (3H,s,1-OCH3),2.92(1H,s,H-7),2.88(1H,s,H-4),2.86(1H,m,H-5),2.75 (1H,dd,J=12.0,2.0 Hz,H-6a),2.38(3H,s,N-CH3)。13C-NMR (125 MHz,CD3OD)δ:149.5 (C-2),146.5 (C-10),146.3 (C-9),143.0 (C-1),130.1 (C-7a),129.2 (C-3a),126.6 (C-1a),125.9 (C-1b),123.2 (C-11a),115.7 (C-8),114.7 (C-3),112.4(C-11),62.7 (C-6a),59.7 (1-OCH3),56.2 (10-OCH3),53.3 (C-5),44.2 (N-CH3),34.2 (C-7),29.0 (C-4)。以上数据与文献报道基本一致[8],故鉴定化合物4 为波尔定碱。
化合物5:结晶性粉末,与碘化铋钾试剂反应呈阳性。ESI-MSm/z346.2[M+Na]+。1H-NMR(500 MHz,DMSO-d6)δ:7.84 (1H,s,H-11),6.77 (1H,s,H-8),6.53 (1H,s,H-3),3.82 (3H,s,10-OCH3),3.74 (1H,dd,J=13.2,3.6 Hz,H-6a),3.64(3H,s,1-OCH3)。13CNMR (125 MHz,DMSO-d6)δ:150.9 (C-2),147.8 (C-9),147.2(C-1),144.5(C-10),130.1(C-7a),129.8(C-3a),127.6(C-1b),126.2(C-1a),124.7(C-11a),115.8(C-8),115.5 (C-11),112.9 (C-3),60.4 (C-6a),56.6(1-OCH3),54.7 (10-OCH3),43.5 (C-5),36.5 (C-7),28.8 (C-4)。以上数据与文献报道基本一致[9],故鉴定化合物5为新木姜子碱。
化合物6:无色细棱柱状结晶(丙酮),与改良碘化铋钾试剂反应显橘红色。1H-NMR (500 MHz,CDCl3)δ:6.94(2H,d,J=8.4 Hz,H-2′,6′),6.66(2H,d,J=8.4 Hz,H-3′,5′),3.83 (3H,s,6-OCH3),3.74(1H,dd,J=6.5,12.0 Hz,H-1),3.57 (3H,s,7-OCH3),3.14~2.58 (6H,m,H-3,4,9),2.53 (3H,s,N-CH3)。13C-NMR (125 MHz,CDCl3)δ:154.9 (C-4′),147.4(C-6),146.4(C-7),131.1(C-1′),130.9(C-2′),130.3(C-6′),128.8 (C-8a),125.3 (C-4a),115.6 (C-3′),115.5 (C-5′),111.3 (C-5),111.1 (C-8),65.1 (C-1),55.9 (6-OCH3),55.7 (7-OCH3),46.2 (C-3),42.3 (NCH3),40.7(C-9a),24.8(C-4)。以上数据与文献报道基本一致[10],故鉴定化合物6为杏黄罂粟碱。
化合物7:棕黄色固体。ESI-MSm/z341.8[M+H]+。1H-NMR (500 MHz,CDCl3)δ:6.94 (1H,d,J=8.0 Hz,H-8),6.90 (1H,d,J=8.0 Hz,H-9),6.74 (1H,s,H-3),4.02 (1H,dd,J=13.5,4.5 Hz,H-6a),3.89(3H,s,10-OCH3),3.82 (3H,s,2-OCH3),3.74 (1H,dd,J=13.0,6.0 Hz,H-5a),3.66 (3H,s,1-OCH3),3.45(1H,ddd,J=13.0,12.5,4.5 Hz,H-5b),3.27 (1H,ddd,J=17.0,12.5,6.0 Hz,H-4a),3.23 (1H,dd,J=14.0,4.5 Hz,H-7a),3.13 (3H,s,N-CH3),3.08 (1H,dd,J=17.0,4.5 Hz,H-4b),2.66 (1H,dd,J=14.0,13.5 Hz,H-7b)。13C-NMR (125 MHz,CDCl3)δ:155.0(C-2),151.3(C-10),145.6(C-11),144.2(C-1),128.1 (C-7a),127.9 (C-3a),127.2 (C-1b),126.4 (C-1a),121.1 (C-8),120.7 (C-11a),113.4(C-9),112.8(C-3),64.6 (C-6a),60.8 (1-OCH3),57.0 (2-OCH3),56.9 (10-OCH3),53.8 (C-5),42.3 (N-CH3),34.1 (C-7),27.4(C-4)。以上数据与文献报道基本一致[11],故鉴定化合物7为异紫堇定碱。
化合物8:白色粉末,易溶于甲醇、丙酮。ESI-MSm/z121.2 [M–H]–。1H-NMR (500 MHz,CDCl3)δ:9.07(1H,d,J=1.5 Hz,H-2),8.79(1H,d,J=5.0 Hz,H-6),8.25 (1H,d,J=8.0 Hz,H-4),7.56 (1H,dd,J=8.0,5.0 Hz,H-5)。13C-NMR (125 MHz,CDCl3)δ:152.9(C-6),149.7(C-2),135.8(C-4),124.1(C-5)。以上数据与文献报道基本一致[12],故鉴定化合物8 为烟酰胺。
化合物9:白色晶体(丙酮),易溶于甲醇。ESIMSm/z313.2 [M+H]+。1H-NMR (500 MHz,CD3OD)δ:7.06(1H,d,J=1.7 Hz,H-2),6.99(1H,d,J=8.5 Hz,H-2′),6.96 (1H,dd,J=8.1,1.7 Hz,H-6),6.73 (1H,d,J=8.1 Hz,H-5),6.69 (1H,d,J=8.5 Hz,H-6′),6.62(1H,d,J=8.5 Hz,H-3′),6.34(1H,d,J=15.5 Hz,H-8),3.83(3H,s,3-OCH3),3.74(1H,d,J=15.5 Hz,H-7),3.43(1H,d,J=8.5 Hz,H-8′)。13C-NMR(125 MHz,CD3OD)δ:166.3 (C-9),156.5 (C-4′),149.2 (C-3),148.9(C-4),140.1(C-7),131.2(C-1′),130.8(C-2′),130.2 (C-6′),128.2 (C-1),122.2 (C-6),119.1 (C-8),115.8(C-5),115.7(C-3′),115.5(C-5′),111.3(C-2),55.8 (3-OCH3),42.2 (C-8′),36.1 (C-7′)。以上数据与文献报道基本一致[13],故鉴定化合物9 为的N-反式阿魏酰酪胺。
4 活性评价
4.1 抗炎作用
取清洁级昆明种小鼠120 只,称体质量,随机分为对照组、模型组、阳性对照组、实验组(化合物1~9),每组10 只,雌雄各半。采用灌胃给药方式,对照组和模型组给予生理盐水,阳性对照组给予阿司匹林(0.26 g·kg–1),实验组分别给予相应化合物(0.26 g·kg–1,均以0.3%羧甲基纤维素钠溶液为溶剂)。连续灌胃给药3 d,灌胃体积均为20 mL·kg–1。末次给药30 min 后,对照组小鼠用移液枪在右耳两面涂生理盐水20 μL,模型组和实验组小鼠右耳涂以二甲苯溶液20 μL 致炎,左耳不做处理。30 min后脱颈处死小鼠,用直径7 mm的打孔器在左右两耳相同部位取下耳片,采用电子天平分别称取两耳片的湿质量,以两耳质量之差作为炎症肿胀度观察指标,按照公式(1)和(2)计算耳肿胀率和耳肿胀抑制率[14-17]。

抗炎活性结果表明,与对照组比较,模型组小鼠耳肿胀率显著提高(P<0.01),证明模型制备成功。与模型组比较,阳性对照阿司匹林能显著抑制二甲苯所致的小鼠耳肿胀(P<0.01),抗炎作用显著;鸭公树子中新木姜子碱表现出明显的抗炎活性(P<0.01),其余生物碱类成分组差异无统计学意义。各组小鼠肿胀率和肿胀抑制率见表1。
表1 鸭公树子中生物碱化学成分对二甲苯致小鼠耳廓肿胀率和肿胀抑制率的影响(,n=10)%

表1 鸭公树子中生物碱化学成分对二甲苯致小鼠耳廓肿胀率和肿胀抑制率的影响(,n=10)%
注:除对照组和模型组外,其余各组给药剂量均为0.26 g·kg–1;与对照组比较,***P<0.001;与模型组比较,△P<0.05,△△P<0.01;表2同。
4.2 镇痛作用
取清洁级昆明种小鼠120 只,动物分组、给药剂量同4.1 项下。末次给药1 h 后,对照组小鼠腹腔注射生理盐水0.01 mL·g–1,其余各组小鼠腹腔注射1%冰醋酸溶液0.01 mL·g–1。注射后,立即放入观察笼中,观察并记录小鼠扭体潜伏期和20 min 内小鼠的扭体次数。扭体的观察标准:腹腔内凹、伸展后肢、臀部抬高[18-20]。按照公式(3)计算药物镇痛率。

镇痛活性结果表明,与对照组比较,模型组小鼠扭体次数显著增加(P<0.001),证明模型制备成功。与模型组比较,阳性对照阿司匹林组能抑制醋酸引起的小鼠疼痛反应,减少小鼠扭体次数(P<0.01);鸭公树子中新木姜子碱明显延迟初次疼痛时间,具有镇痛作用(P<0.01),其余生物碱成分则均不能延迟初次疼痛时间,没有表现出镇痛作用。各组小鼠扭体次数和扭体抑制率见表2。
表2 鸭公树子中生物碱化学成分对醋酸致小鼠扭体次数和扭体抑制率的影响(,n=10)
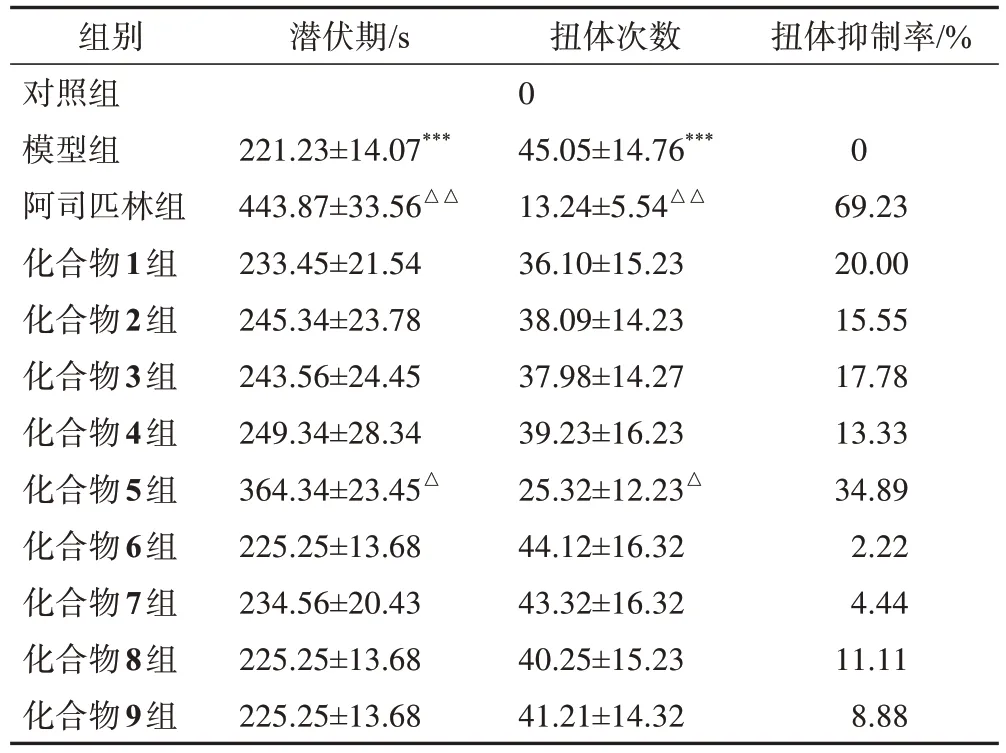
表2 鸭公树子中生物碱化学成分对醋酸致小鼠扭体次数和扭体抑制率的影响(,n=10)
5 讨论
本研究从鸭公树子提取物中分离得到9 个生物碱类化合物,其中7个为四氢异喹啉类化合物、1个为哌啶类化合物、1 个为酰胺类化合物。目前已从樟科新木姜子属植物中分离得到的生物碱有多种类型,按生物碱的化学结构可分为四氢异喹啉类生物碱、吡啶类生物碱、有机胺类生物碱、苄基异喹啉类生物碱、阿扑芬型生物碱。研究中所分离鉴定的鸭公树子中的化学成分与该属植物化学成分的基本特征相符[21-27],这些生物碱成分均为首次从鸭公树子中分离获得。
在抗炎镇痛的活性实验中,分别采用二甲苯所致小鼠耳廓肿胀法研究鸭公树子中生物碱成分的消炎作用,小鼠醋酸扭体法研究鸭公树子中生物碱成分的镇痛作用。二甲苯涂在小鼠耳廓上面导致毛细血管通透性增大、组织液渗透增多,产生红肿现象。在小鼠扭体实验中,对小鼠腹腔注射醋酸引起急性腹膜炎。药理活性实验结果显示,鸭公树子中新木姜子碱表现出明显的抗炎镇痛活性,与以往网络药理学研究推测新木姜子碱作用于多巴胺能和5-羟色胺能突触通路的蛋白靶点发挥行气止痛一致[28-29]。本研究结果发现,鸭公树子具有良好的抗炎镇痛作用,可结合传统行气止痛的功效开发单一制剂,用于疼痛症状的治疗。
