百令胶囊辅助治疗高龄早期糖尿病肾病患者的效果及对微炎症因子、氧化应激因子的影响
2022-06-14徐海涛王永宁
徐海涛,王永宁
(洛阳市中医院 老年病科,河南 洛阳 471000)
糖尿病肾病为糖尿病患者较常见的慢性并发症。据统计,糖尿病肾病已成为终末期肾衰竭的首要病因[1]。据估计,全球糖尿病患者约有1.7亿,我国糖尿病患者占23%左右,而其中30%的患者发展为糖尿病肾病[2]。目前治疗主要以控制血糖、血压和保护肾脏功能为主,以达到阻止病情恶化,延长患者生存时间的目的[3]。中医乃我国特色,中西结合治疗已被广泛应用于多种疾病,且治疗效果满意[4]。糖尿病肾病患者多有肾气亏虚,而百令胶囊具有补益肺肾的功效,推测其辅助治疗糖尿病肾病可能有较好的效果[5]。本研究通过观察百令片辅助治疗高龄早期糖尿病肾病患者临床症状的改变及治疗前后微炎症因子、氧化应激因子水平的变化,综合评定其治疗效果,为临床百令胶囊辅助治疗高龄早期糖尿病肾病提供新的依据。
1 对象和方法
1.1 研究对象将2018年7月至2021年7月在洛阳市中医院接受治疗的100例高龄早期糖尿病肾病患者,按照随机数字表法分观察组(50例)和对照组(50例)。观察组中男24例,女26例;年龄80~93岁,平均(85.19±4.07)岁;病程5~18 a,平均(11.24±3.26)a;体质量指数20~24 kg·m-2,平均体重指数(22.48±1.43)kg·m-2;腰围70~95 cm,平均(82.79±8.02)cm;糖尿病肾病分期(依据Mogensen分期法)为Ⅱ期29例,Ⅲ期21例。对照组中,男23例,女27例;年龄80~94岁,平均(85.21±4.03)岁;病程6~17 a,平均(11.43±3.14)a;体质量指数20~24 kg·m-2,平均(22.54±1.39)kg·m-2;腰围71~96 cm,平均(83.01±8.12)cm;糖尿病肾病分期(依据Mogensen分期法):Ⅱ期30例,Ⅲ期20例。纳入标准:(1)符合我国2型糖尿病肾病诊断标准[参考《中国成人糖尿病肾脏病临床诊断的专家共识》[6]的相关诊断标准];(2)年龄≥80岁。排除标准:(1)合并严重心肺疾病;(2)合并糖尿病各种急性并发症:(3)有严重胃肠功能疾病,胃肠功能极差;(4)长期使用糖皮质激素或抗氧化剂药物剂;(5)入院前进食过含冬虫夏草菌粉成分的食品和药物;(6)过敏体质。
1.2 治疗方法两组患者均接受西医常规治疗(包括饮食调整、运动锻炼,根据患者的实际情况,选择使用二甲双胍、格列齐特等降糖药物或胰岛素注射保持血糖的稳定,使用利尿剂、血管紧张素转换酶抑制剂等控制血压)。观察组在常规治疗基础上加用百令胶囊(杭州中美华东制药有限公司,国药准字Z10910036),每次2 g,每日3次,8周为1个疗程,连续治疗12周。
1.3 观察指标(1)临床效果。①明显改善:患者临床症状完全消退,肾功能受损状况缓解60% ~90%;②改善:患者临床症状基本消退,肾功能受损状况缓解20%~59%;③无效:临床症状及肾功能未见明显好转,甚至病情有恶化的趋势[6]。(2)肾功能指标。患者均在入院时及治疗期结束后,于晨起空腹采集外周静脉血5 mL,送至检验科离心取得血清,采用博科BIOBASE全自动生化分析仪检测血尿素氮(blood urea nitrogen,BUN)、血肌酐(serum creatinine,Scr)。嘱患者于治疗前和治疗结束后留取5 mL晨尿,送至检验科离心取得上层清液,采用免疫透射比浊法测定尿微量清蛋白(urinary mi-croalbuminuria,U-mAlb),试剂盒由上海优选生物科技有限公司提供。(3)炎症、氧化应激指标。采用瑞士帝肯公司生产的全自动酶免分析仪(型号TECAN150-8)检测血清肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)、白细胞介素-6(interleukin-6,IL-6)、白细胞介素-1(interleukin-1,IL-1)、谷胱甘肽过氧化物酶(glutathione peroxidase,GSH-Px)、超氧化物歧化酶(superoxide dismutase,SOD)、丙二醛(malondialdehyde,MDA)水平;采用免疫透射比浊法检测超敏-C反应蛋白(high sensitivity C-reactive protein,hs-CRP)水平,试剂盒由上海优选生物科技有限公司提供。(4)不良反应。
1.4 统计学分析采用SPSS 19.0软件进行统计分析。计量资料以均数±标准差(±s)表示,行t检验,计数资料以例数和百分数(%)表示,组间比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 治疗后临床效果经过治疗,观察组患者总体有效率(94.00%)高于对照组(80.00%)(P<0.05)。见表1。

表1 两组患者疗效比较[n(%)]
2.2 BUN、U-mAlb、Scr水平治疗前,两组患者BUN、U-mAlb、Scr水平比较,差异无统计学意义(P>0.05);治疗后,两组患者BUN、U-mAlb、Scr水平均下降,观察组降低幅度优于对照组(P<0.05)。见表2。
表2 两组患者治疗前后BUN、U-mAlb、Scr水平比较(±s)
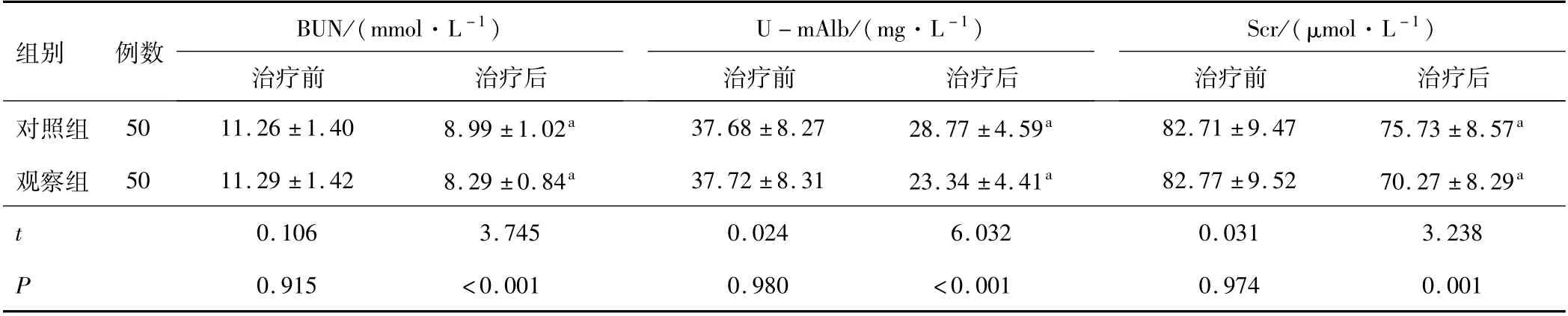
表2 两组患者治疗前后BUN、U-mAlb、Scr水平比较(±s)
注:与同组治疗前比较,a P<0.05;BUN为血尿素氮;U-mAlb为尿微量清蛋白;Scr为血肌酐。
组别 例数 BUN/(mmol·L-1)U-mAlb/(mg·L-1)Scr/(μmol·L-1)治疗前 治疗后对照组 50 11.26±1.40 8.99±1.02a 37.68±8.27 28.77±4.59a 82.71±9.47 75.73±8.57治疗前 治疗后治疗前 治疗后a观察组 50 11.29±1.42 8.29±0.84a 37.72±8.31 23.34±4.41a 82.77±9.52 70.27±8.29a t 0.106 3.745 0.024 6.032 0.031 3.238 P 0.915 <0.001 0.980 <0.001 0.974 0.001
2.3 hs-CRP、IL-6、IL-1、TNF-α水平治疗前,两组患者hs-CRP、IL-6、IL-1、TNF-α水平比较,差异无统计学意义(P>0.05);治疗后,两组患者hs-CRP、IL-6、IL-1、TNF-α水平均下降,观察组降低幅度优于对照组(P<0.05)。见表3。
表3 两组患者治疗前后hs-CRP、IL-6、IL-1、TNF-α水平比较(±s,ng·L-1)
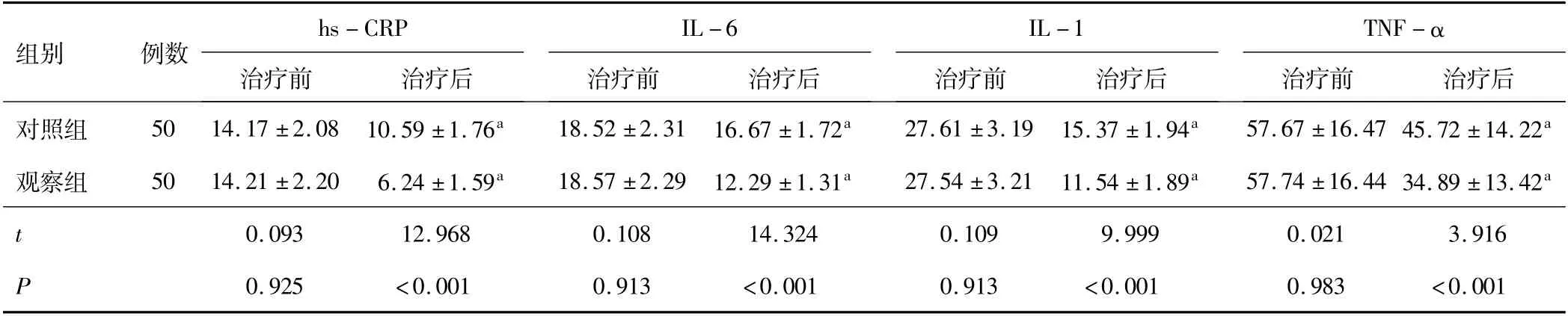
表3 两组患者治疗前后hs-CRP、IL-6、IL-1、TNF-α水平比较(±s,ng·L-1)
注:与同组治疗前比较,a P<0.05;hs-CRP为超敏-C反应蛋白;IL-6为白细胞介素-6;IL-1为白细胞介素-1;TNF-α为肿瘤坏死因子-α。
hs-CRP IL-6 IL-1 TNF-组别 例数α治疗前 治疗后对照组 50 14.17±2.08 10.59±1.76a 18.52±2.31 16.67±1.72a 27.61±3.19 15.37±1.94a 57.67±16.47 45.72±14.22治疗前 治疗后治疗前 治疗后治疗前 治疗后a观察组 50 14.21±2.20 6.24±1.59a 18.57±2.29 12.29±1.31a 27.54±3.21 11.54±1.89a 57.74±16.44 34.89±13.42a t 0.093 12.968 0.108 14.324 0.109 9.999 0.021 3.916 P 0.925 <0.001 0.913 <0.001 0.913 <0.001 0.983 <0.001
2.4 GSH-Px、MDA、SOD水平治疗前,两组患者GSH-Px、MDA、SOD水平比较,差异无统计学意义(P>0.05);治疗后,两组患者GSH-Px、SOD水平均上升,MDA水平均下降,观察组上升和下降幅度均优于对照组(P<0.05)。见表4。

表4 两组患儿不良反应发生情况比较[n(%)]
表4 两组患者治疗前后GSH-Px、MDA、SOD水平比较(±s)
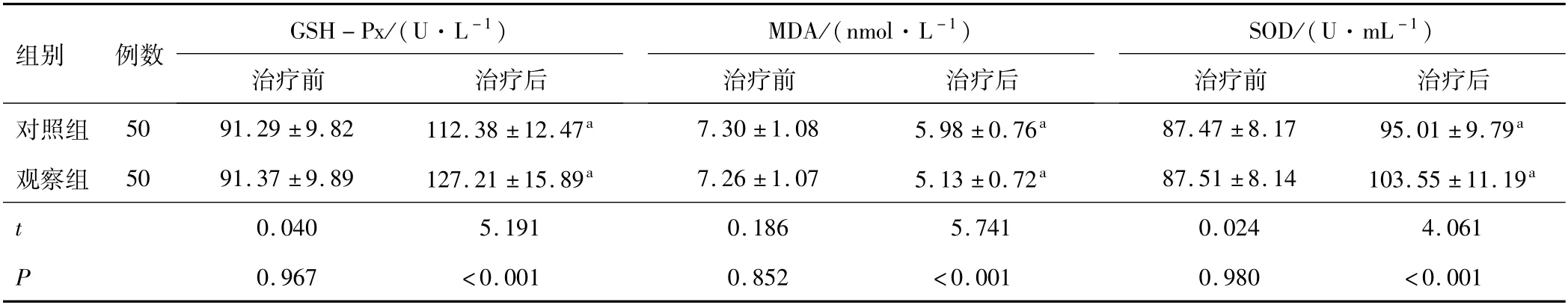
表4 两组患者治疗前后GSH-Px、MDA、SOD水平比较(±s)
注:与同组治疗前比较,a P<0.05;GSH-Px为谷胱甘肽过氧化物酶;MDA为丙二醛;SOD为超氧化物歧化酶。
组别 例数 GSH-Px/(U·L-1)MDA/(nmol·L-1)SOD/(U·mL-1)治疗前 治疗后对照组 50 91.29±9.82 112.38±12.47a 7.30±1.08 5.98±0.76a 87.47±8.17 95.01±9.79治疗前 治疗后治疗前 治疗后a观察组 50 91.37±9.89 127.21±15.89a 7.26±1.07 5.13±0.72a 87.51±8.14 103.55±11.19a t 0.040 5.191 0.186 5.741 0.024 4.061 P 0.967 <0.001 0.852 <0.001 0.980 <0.001
2.5 不良反应观察组患者不良反应发生6例,个别患者服用百令胶囊后出现咽部不适感,对照组不良反应发生4例,血压的波动、电解质紊乱可能与基础用药中降压药的使用有关,两组患者不良反应症状轻微,均无患者因对药物不耐受而终止治疗。观察组不良反应总体发生率(12.00%)与对照组(8.00%)比较,差异无统计学意义(P>0.05)。
3 讨论
早期的高滤过和蛋白尿是糖尿病肾病患者的特征性表现,然后肾功能持续性下降,直至发展为终末期肾衰,依靠血液透析来维持生命[7]。调查资料显示,糖尿病肾病占尿毒症原发病的1/3,相比无肾损害的糖尿病患者其病死率高30倍左右[8],糖尿病肾病是一项全球性健康挑战。有研究表明,机体正常氧化-还原动态平衡被打破及持续性低水平炎症状态是促进糖尿病肾病发生发展的重要因素[9]。血糖控制是关键,此外积极控制机体炎症反应、氧化应激反应对改善糖尿病患者肾功能及防止其恶性进展都有重大意义。临床实践表明,百令胶囊对于辅助治疗慢性炎症性疾病效果较好,如慢性肾小球肾炎、慢性支气管炎等[10]。
本研究结果显示,经过治疗观察组患者总体有效率(94.00%)高于对照组(80.00%);两组患者BUN、U-mAlb、Scr水平均下降,观察组降低幅度优于对照组。这表明百令胶囊辅助治疗糖尿病肾病能显著提高治疗效果,改善肾脏功能。百令胶囊的主要成分为发酵冬虫夏草菌粉。研究表明,百令胶囊中虫草多糖可以参与调节机体免疫功能,对损伤的肾小管上皮细胞有较好的修复作用,且能阻止肾小球基底膜增厚,从而起到改善肾功能的作用[11]。张鹏等[12]研究中以150例慢性肾脏病分期为Ⅲ~Ⅳ的患者为研究对象,对照组按照常规治疗,观察组加用百令胶囊治疗,结果观察组BUN、Scr下降水平优于对照组,得出百令胶囊能较好地改善肾脏功能,与本研究结果一致。本研究结果显示,两组患者hs-CRP、IL-6、IL-1、TNF-α水平均下降,观察组降低幅度优于对照组,结果表明百令胶囊对改善机体炎症状态有较明显的效果。研究表明,百令胶囊具有抗炎作用,主要机制为抑制IL-6等前炎症因子使血清可溶性细胞间黏附分子1表达上调,使淋巴细胞增殖受到抑制,从而发挥抗炎作用[13]。杨亚娜等[14]研究中以140例早期糖尿病肾病患者为研究对象,对照组接受常规西医治疗,观察组在常规西医治疗基础上加用百令胶囊,结果治疗后观察组TNF-α、IL-1等炎症因子水平低于对照组,得出百令胶囊对机体炎症反应有抑制作用,与本研究结果相符。经研究证实,早期糖尿病肾病患者机体氧化应激水平较高,导致肾小球基底膜足细胞脱落,肾小球滤过膜损伤,出现蛋白尿[15]。GSH-Px、SOD、MDA参与和调节机体氧化应激反应,且可用于评价抗氧化应激的治疗效果[16]。本研究结果显示,治疗后两组患者GSHPx、SOD水平均上升,MDA水平均下降,观察组上升和下降幅度均优于对照组。结果表明百令胶囊可有效改善早期糖尿病肾病患者的高应激水平状态。研究表明,百令胶囊中丛草多糖可参与调节抗氧化物酶的活性,使机体自由基产生减少,降低了氧化应激反应对肾小球的损伤,从而减轻蛋白尿,改善和保护肾功能[17]。本研究结果显示,治疗期间观察组不良反应总体发生率(12.00%)与对照组(8.00%)相比差异无统计学意义,结果表明常规治疗基础上加用百令胶囊未增加患者毒副反应的发生风险,药物安全性值得肯定。
综上所述,百令胶囊辅助治疗高龄早期糖尿病肾病,能显著提升治疗效果,保护和改善肾脏功能,减轻机体炎症反应,降低患者氧化应激水平,且药物安全可靠,值得临床推广应用。
