口服抗栓药物患者门诊拔牙围手术期管理的专家共识
2022-06-09潘剑薛洋赵吉宏周青邹多宏陈松龄韩冰崔念晖刘显王了胡开进
潘剑 薛洋 赵吉宏 周青 邹多宏 陈松龄韩冰 崔念晖 刘显 王了 胡开进
1.口腔疾病研究国家重点实验室 国家口腔疾病临床医学研究中心四川大学华西口腔医院口腔外科,成都 610041;2.军事口腔医学国家重点实验室,国家口腔疾病临床医学研究中心,陕西省口腔疾病临床医学研究中心,第四军医大学口腔医院颌面外科,西安 710032;3.武汉大学口腔医院口腔外科,口腔生物医学教育部重点实验室,武汉 430079;4.中国医科大学口腔医学院·附属口腔医院口腔颌面外科,辽宁省口腔疾病重点实验室,沈阳 110001;5.上海交通大学医学院附属第九人民医院口腔外科,国家口腔疾病临床医学研究中心,上海市口腔医学重点实验室,上海市口腔医学研究所,上海 200011;6.中山大学附属第一医院口腔颌面外科,广州 510080;7.吉林大学口腔医院口腔颌面外科,长春 130021;8.北京大学口腔医学院·口腔医院口腔颌面外科,国家口腔医学中心,国家口腔疾病临床医学研究中心,口腔数字化医疗技术和材料国家工程实验室,口腔数字医学北京市重点实验室,国家卫生健康委员会口腔医学计算机应用工程技术研究中心,国家药品监督管理局口腔生物材料重点实验室,北京 100081
血栓栓塞性疾病是由于血栓形成和血栓栓塞导致的疾病总称,主要涵盖两个方面:1)静脉血栓栓塞性疾病,包括深静脉血栓形成和肺血栓栓塞症;2)动脉血栓栓塞性疾病,原因包括冠状动脉粥样硬化性心脏病、脑卒中、心房颤动、心脏瓣膜置换等[1]。血栓栓塞性疾病患病人数多,且往往伴随致死、致残等严重并发症,极大地威胁人类健康[2]。这些患者中,有很大一部分需要长期口服抗栓药物对血栓形成进行防治,在降低血栓事件发生的同时也带来了出血风险的增加。拔牙手术是口腔外科门诊最常见的手术,研究[3-4]表明服用抗栓药物患者拔牙术后出血的风险较普通患者高,这使得众多口腔外科医师对这类患者拔牙围手术期的管理感到困惑。此外,种类繁多的抗栓药物,各个患者不同的基础疾病和全身情况等因素加剧了这种困惑,使医生们陷入“不停药有出血风险,停药又有血栓形成风险”的两难境地。为了加强对该类患者拔牙围手术期管理的理解,在保障患者安全的情况下及时解决患者拔牙诉求,相关专家起草本共识,希望能为广大口腔外科医师提供临床参考。
1 术前管理
1.1 不建议术前停药
口腔外科医师对出血风险的担忧在于患者脱离临床监护后可能发生一些重要解剖部位的出血水肿,从而有导致窒息的风险;为了“避免”上述风险,临床实践中依然有较多医生嘱患者拔牙前停抗栓药。但拔牙前不需停药已成为基本共识,主要有以下3 点原因:1)停用药物导致血栓风险升高,可导致死亡。Wahl 等[5]回顾了2 673 例停用抗凝药物的拔牙患者,其中有22 例(0.8%)发生血栓事件,6 例死亡;而在5 431 例不停药的患者中,仅有31 例(0.6%)需要局部止血措施以外的治疗方式,无死亡病例。2)术前停药和不停药,拔牙后出血事件的发生率差异无统计学意义[6-7]。3)大样本研究和系统性综述都表明口服抗栓药物的患者拔牙前无需停用药物[4-5,7-11],因为不停药进行拔牙手术是安全可控的,术后出血通过局部止血措施就能处理[4,8];部分研究[5]中有报道需要局部措施以外的止血措施,但不引起死亡。相比于关注是否停药,更应该注意不要在围手术期引入新的出血危险因素,这些危险因素将在后面的讨论中提到。
1.1.1 口服抗血小板药物对拔牙的影响 从临床适应证来说,服用抗血小板药物主要是预防动脉粥样硬化性心血管疾病、静脉血栓栓塞症、缺血性脑卒中、下肢动脉硬化闭塞外科手术干预后等疾病的血栓事件的发生[1,12];从用药目的来说,分为一级预防和二级预防。以阿司匹林为例,对于一级预防来说,相比于对照组或安慰剂,预防性服用阿司匹林能减少严重心血管事件的发生率(阿司匹林组0.51%/年,对照组0.57%/年),但同时也带来了更高的大出血风险(阿司匹林组0.1%/年,对照组0.07%/年)[13]。由于以一级预防为目的的患者血栓风险低,有学者[12]认为作为一级预防服用时,手术前可以停服抗血小板药物。当作为二级预防使用时,其减少严重心血管事件发生率的效果更确切(阿司匹林组6.7%/年,对照组8.2%/年),能减少约1/5 的卒中[13];因此,中国血栓性疾病防治指南明确指出,应用阿司匹林进行心血管病二级预防者,建议在接受牙科手术时继续应用[1]。对于口服抗血小板药物的拔牙患者来说,不停药行拔牙手术的出血风险较低(1.7%[14],1.4%[15]和1.8%[3]),与健康对照组相近(1.1%[14]);应用双联疗法的患者拔牙术后出血率较单一药物高[4]。因此,在临床实践中,对于服用抗血小板药物的患者,拔牙前无需停药。
1.1.2 口服抗凝药物对拔牙的影响 临床常见的口服抗凝药可分为维生素K 拮抗剂类抗凝药(vitamin K antagonist,VKAs),以华法林为代表,以及非维生素K 拮抗剂类抗凝药(non-vitamin K antagonist oral anticoagulants,NOACs)[16],主要包括达比加群酯、阿哌沙班、利伐沙班等,也有文献将其描述为直接口服抗凝药(direct oral anticoagulants,DOACs)[17]。本文中按作用机制选择NOACs的命名。
对于服用抗凝药物的患者来说,其发生术后出血的风险较服用抗血小板药物患者高[3,15],出血事件严重的往往是服用抗凝药物的患者[5]。应用华法林期间尽量避免同时使用抗血小板药物,研究[18]表明抗凝药物联用抗血小板药物可导致出血风险增加;除非在机械瓣膜置换、急性冠脉综合征或是近期行过冠状动脉支架植入或冠状动脉旁路移植术等,联合应用收益明确或收益大于出血风险时可联用抗血小板药物[1]。服用华法林的患者应密切监控其国际标准化比值(international normalized ratio,INR),只有INR 保持在目标范围内才能控制血栓风险,达到治疗效果,常见疾病的目标INR 值见表1[1]。对于口腔外科医师来说,INR可以直观反映术后出血风险,较高的INR值对应着更高的拔牙术后出血风险[18-20]。围绕拔牙术的INR安全范围,学者们进行了大量探索,但由于抗栓药物种类繁多、适应证涵盖范围广、患者自身条件差异大等因素影响,目前没有普遍适用的推荐范围,使得这一标准在不同的研究中有较大差异,拔牙手术的安全INR 为:小于2.5[21],2.0~3.0[22],小于3.5[23],小于4[3]都有相关报道。从表1数据可知,INR目标值也在诸多拔牙安全INR范围内,指南也建议接受VKAs治疗的患者,接受牙科手术时继续应用[1]。
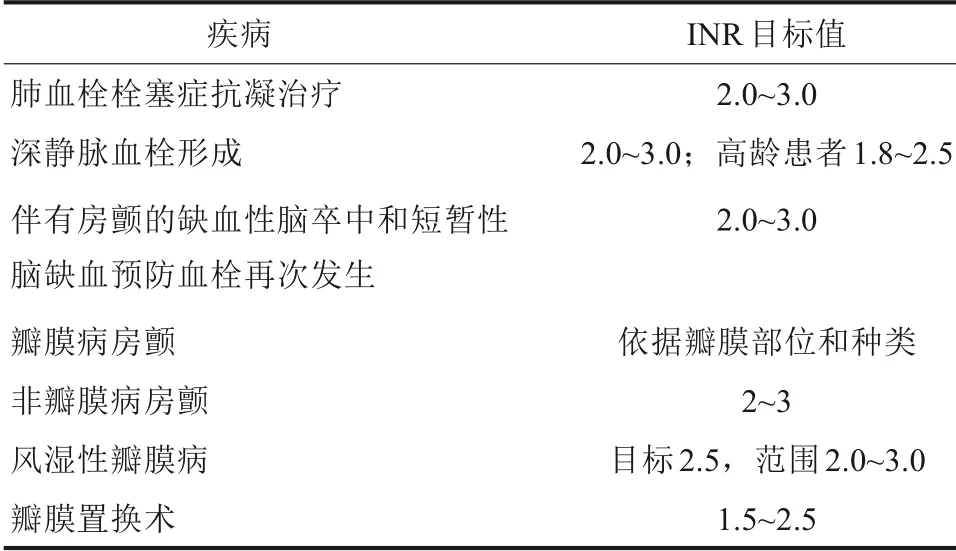
表1 常见疾病的目标INRTab 1 Target INR for common diseases
另一类常见口服抗凝药物为NOACs,临床上主要用于预防非瓣膜病房颤患者的血栓形成和防治肺血栓栓塞症和深静脉血栓形成[24],因其在特定疾病中更高的安全性和有效性,以及无需频繁检测INR 值而应用日渐广泛[24-25]。学者们针对服用两种药物拔牙术后出血风险的差异作出了探索,由于研究方法的不同,不同文献中出血率差异较大,但整体上服用NOACs 的患者较服用华法林的患者拔牙术后出血率更低(NOACs 3.1%,华法林8.8%[8];NOACs 1.5%,华法林3%[22];NOACs 17.8%,华法林20%[26];NOACs 10.5%,华法林15.3%[27]),但这些差异无统计学意义。对口服达比加群酯的患者,活化部分凝血活酶时间(acti-veated partial thromboplasting time,APTT)的比值(患者APTT/正常APTT)>1.8,出血风险高[26]。针对口服NOACs 类抗凝药患者行牙科手术的围手术期管理的高质量研究还很欠缺,尚存在争议,多数研究[17]认为口服NOACs 类抗凝药患者接受拔牙手术时无需停药,出血事件通过加压止血、缝合、生物止血材料应用和伤口再处理都能解决;也有研究表明由于NOACs 类药物半衰期较短,且维持时间不如VKAs长[22],手术时间距离上次服药时间长短与术后出血相关[26],可把手术时间安排在药物浓度低谷期[24]或选择术后服药[9],有学者在实践中把手术时间安排在服药6 h 后[8],出血率较低,有一定参考价值。文献中报道常见NOACs 用法及半衰期见表2[22,24]。

表2 NOACs服用方式和半衰期Tab 2 Administration mode and half-life of NOACs
1.2 拔牙手术出血风险评估
不同的侵入性手术有不同的出血风险,对拔牙手术来说,欧洲心率协会认为拔除1~3颗牙齿是极低出血风险的手术[9]。Verma 等[24]认为1~3 颗牙齿出血风险为低风险,而拔除大于3颗牙齿或口腔软组织切取活检为中高风险。较多的拔牙数目意味着更大的创伤,对应更高的出血风险[18,28]。除了拔牙数目外,一些复杂牙如死髓牙、阻生智牙、埋伏牙的拔除过程需要翻瓣,也会带来更大的创伤,导致出血风险的增加[29]。综上,口腔外科医师可以从手术本身出发去考虑如何规避风险,即制定手术计划时控制一次拔牙的数目,当患牙拔除难度大,需要翻瓣、去骨时可选择单颗、多次拔除所有患牙。
1.3 其他出血风险的术前管理
在临床实践中,当拔牙手术操作难度大、患者全身健康状况差、口腔内炎症较重的时候往往选择预防性使用抗生素[30]。系统性综述结果表明预防性使用抗生素能减轻患者拔牙后感染和干槽症的风险,虽然相关证据强度较低[31]。然而,术前使用抗生素可能导致口服抗栓药物患者拔牙术后出血的风险升高[18];曾有病案报道口服抗栓药物患者联用阿莫西林[32]拔牙后严重出血,或联用克拉霉素、红霉素或甲硝唑时出现其他部位的出血事件[33-34],其具体机制不明,或许与抗生素干扰肠道菌群从而影响了维生素K摄入相关[32]。
除了抗生素之外,一些合并其他系统性疾病的患者需要同时服用其他药物,一些心血管用药如胺碘酮(抗心律失常药物)、阿托伐他汀和辛伐他汀(降血脂药)、比索洛尔和氨氯地平(抗高血压药);抗癫痫药物如丙戊酸钠、氟西汀;抗真菌药物如氟康唑等可与抗凝药物相互作用增加出血风险[33]。但这些多数是散在病案报道,且不是针对拔牙后的研究,是否会增加拔牙术后出血的风险需要进一步研究,但值得引起临床注意。
如前所述,口腔内炎症是临床上部分医生拔牙前预防性使用抗生素的原因之一。炎症也与口服抗栓药物患者拔牙术后出血风险升高相关:研究表明患牙牙周炎[28],拔牙术区急性感染史[20]以及拔牙同期的急性炎症[29]是该类患者拔牙术后出血的危险因素。此外,高龄(>75岁)是术后出血的危险因素[28,35],当伴有一些全身疾病如恶性肿瘤、肝脏疾病、糖尿病、肾功能不全时,其发生拔牙术后的出血概率提高[21,35-36]。针对上述因素,在拔牙前应首先改善口腔卫生和控制炎症,既可以减少抗生素使用需求,也可以避免炎症带来的出血风险。对于伴发的系统疾病,应当首先予以积极处理,待其控制良好之后再行拔牙手术,最大程度地减轻系统性疾病带来的出血和其他并发症风险。而抗生素的使用需综合判断,当出血风险因素大时则优先避免出血风险,避免术前抗生素的使用,从术中无菌操作、减少操作时间、术前术后加强口腔卫生维护等角度降低感染风险;而如果仅仅只是口服抗栓药物而其他出血危险因素少时则可按临床常规习惯使用抗生素,从术后加强止血措施方面减少出血风险。
1.4 完善术前检查
任何患者在拔牙前都应完善术前检查,口服抗栓药物的患者在排除其他手术禁忌之外,还需关注其凝血功能。使用特定药物(华法林)的患者一般会定期复查INR,但少数患者服药依从性较差[37-38],就诊时自述指标正常,但术后即刻检查往往与口述不符[39],因此术前检查INR十分必要。在临床实践中,如果缺乏获得即刻数据的检测条件,可以对该类患者采取预约就诊制,要求患者携带术前2 周内的凝血功能报告,以便准确评估出血风险。
2 术中管理
2.1 心电监护拔牙
口服抗栓药物的患者往往是全身情况复杂的老年患者,拔牙可能诱发一些心血管疾病如高血压、冠心病等的急性发作,从而威胁患者安全。心电监护指采用心电监护仪对患者的生命指征(心率、脉搏、呼吸频率、血压、血氧饱和度)和心电图实时监测,以便对生命体征改变迅速采取对应措施,可以提高治疗的安全性[40]。
2.2 麻醉方式选择
有研究[20,28]报道下牙槽神经阻滞麻醉是服用抗栓药物患者拔牙术后出血的危险因素,笔者分析认为一方面是因为神经阻滞麻醉往往对应着复杂牙的拔除,因此这实际上也是高难度的拔牙手术过程中更大的创伤导致的;另一方面是对于手术难度不大,范围小的拔牙手术,临床上一般采用含肾上腺素的阿替卡因进行局部浸润麻醉,其中的肾上腺素含有缩血管的作用,或许可以一定程度上减少出血。在临床实践中,一般优先选择浸润麻醉,因阻滞麻醉组织间穿行路径比较长,有刺破组织和血管引发血肿的风险;如无法避免,则应熟练掌握解剖位置,避免带来额外的出血风险。
2.3 手术时机的选择
将手术安排在早上可以更好地对口服抗栓药物患者进行监测,延长留观时间,以便及时处理出血并发症。此外,由于抗血小板药物和VKAs类药物效果持续时间较长;而NOACs 半衰期较短,起效迅速,若要考虑从手术时机这一方面控制出血风险主要是针对NOACs 类药物。有文献[24]建议可把手术安排在药物浓度低谷期,即延长手术时机与服药时间之间的间隔,有研究[8]将这一时间控制在大于6 h;2018年欧洲心率协会指南中提出出血风险高的患者可省略达比加群酯或阿哌沙班的前半天用药,在术后6 h之后再服药,如表3所示,可作为参考。笔者的经验是不干预NOACs 类药物的使用,而加强术后观察和止血措施,如辅助使用明胶海绵等预防出血,尚未见严重出血事件。
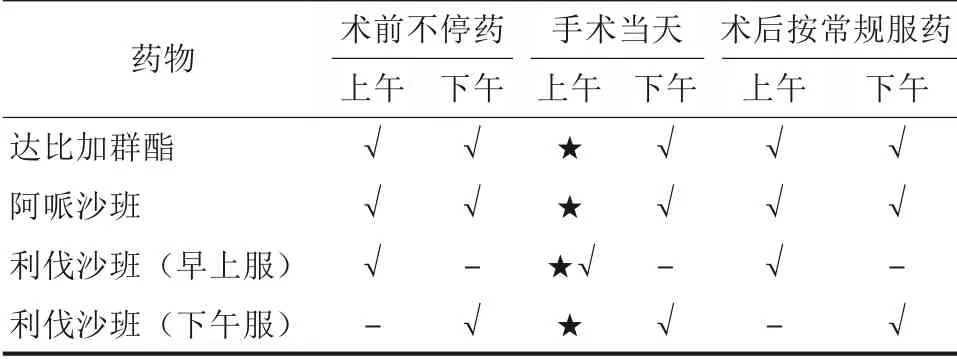
表3 服用NOACs患者拔牙时机和药物管理Tab 3 Timing of tooth extraction and drug manage‐ment in patients taking NOACs
2.4 手术技巧的把握
微创拔牙就是在拔牙过程中,通过使用标准的拔牙器械,应用微创的手术技巧,使拔牙过程对患者产生的身心创伤和影响最小化,具有手术时间短,术中、术后并发症少,患者心理畏惧程度低等优点[41]。如前所述,较大的创伤会带来出血风险的升高,因此临床医生应当提高手术技巧,将微创拔牙的理念贯穿拔牙的整个流程中。
3 术后管理
3.1 术后止血的措施
临床上,拔牙术后常规嘱患者咬棉球有效压迫止血30 min。对于是否对伤口进行缝合,笔者的考虑主要依据术后软组织瓣是否有动度,如在拔除一些前磨牙时,没有翻瓣,并不会采取缝合的措施;而对一些埋伏阻生牙,需要翻瓣暴露视野,术后软组织瓣动度较大,则会进行缝合。对口服抗栓药物的患者来说,其凝血功能受到不同程度的抑制,可以延长术后留观时间,并嘱患者延长有效压迫的时间。研究[22]表明这类患者发生术后出血(拔牙后压迫30 min 伤口仍有活动性出血)时,通过延长30 min 压迫时间就能解决超过60%的出血事件。进一步的止血措施包括止血材料填塞、缝合、伤口再处理、会诊住院治疗等[42-43],超过99%的患者通过专科局部止血措施即可达到止血,仅有极少数患者需要住院治疗[5]。常见的止血材料有明胶类、氧化纤维素类、纤维蛋白类、自体血液制品等[27,44],国内文献报道的产品主要有胶原蛋白海绵、新型牙周塞治剂、口腔创护贴、纳米贴以及复合水凝胶等[43];氨甲环酸主要以漱口液的形式使用,在国外研究中应用较多[45]。此外,一些新型的止血材料如再生氧化纤维素[42]、Hemcon Dental Dressing(以壳聚糖为基质的生物止血材料)[46]、Feracrylum Gel(一种新型凝胶)[47]也在不断地被研究和运用,术者可根据自己的临床经验选择相应止血材料辅助止血。
3.2 加强术后护理
一方面要加强健康教育,告知其发生术后出血的风险相较于其他拔牙患者更高,要引起重视,并告知其术后渗血的现象和出血后的简单处理措施,避免引起不必要的恐惧;另一方面要向患者本人和陪护家属都强调术后注意事项,包括避免吸吮、吐痰、用力鼓漱等动作,进温凉饮食,术后冰敷,避免剧烈运动和减少说话频率等。
3.3 止痛药的合理应用
非甾体类抗炎药(nonsteroidal anti-inflammatory drugs,NSAIDs)、选择性5-羟色胺抑制剂(selective serotonin inhibitors,SSRIs)和5-羟色胺-去甲肾上腺素抑制剂(serotonin-norepinephrine reuptake inhibitors,SNRIs)由于影响血小板活性,与抗凝药物合用时会增加出血风险[33]。口腔拔牙术后常用的止痛药布洛芬和双氯芬酸钠属于NSAIDs 类药物,按前述观点与抗凝药物合用会增加出血风险;而利伐沙班被报道与阿片类药物合用会增加术后出血风险[48]。因此,在术后开具处方时应谨慎,可用其他类型止痛药代替。口服华法林患者避免应用NSAIDs,包括环氧化物酶-2-选择性非甾体类抗炎药物[1]。
3.4 术后随访
患者术后止血离开临床监护后,常因术后护理不当发生出血,因此建立术后随访机制可以及时了解患者情况,指导患者进行正确的处理;患者如出现任何问题,也可在第一时间和医护人员取得联系,缓解患者的紧张和焦虑心情。
4 结语
随着人口老龄化和社会经济水平的提高,心血管患病人数逐渐增加并趋向低龄化,因此口服抗栓药物患者会越来越多,这类患者的拔牙围手术期管理相对于其他患者更加复杂。本共识从术前、术中、术后三方面总结了该类患者拔牙时应该注意的问题,希望能对广大口腔外科医师的工作起到一定的帮助。目前已经发表的研究纳入标准比较宽泛,缺乏针对特定疾病背景患者的高质量研究,未来还需要更细致地探索,才能有证可循地按疾病背景对这些患者做个性化管理。
致谢:感谢刘济远副教授和黄金霞医师对本文文献资料收集所做出的贡献。
利益冲突声明:作者声明本文无利益冲突。
