噻托溴铵联合马来酸茚达特罗在稳定期慢性阻塞性肺疾病患者中的应用效果及安全性
2022-06-06赵守焱尚建欣褚春红
赵守焱,尚建欣,褚春红
慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)是一种严重威胁人们健康的慢性病[1-2]。吸入性糖皮质激素与支气管扩张剂是慢性阻塞性肺疾病全球倡议推荐的一线治疗方案[3],但其有诱发肺部感染的风险,且停用糖皮质激素会增加COPD急性加重次数。支气管扩张剂在COPD稳定期患者的维持治疗中发挥着不可替代的作用[4]。噻托溴铵属于胆碱能受体抑制剂,其在扩张支气管和抑制乙酰胆碱生成方面具有明显效果。马来酸茚达特罗为新型长效β2-肾上腺素受体激动剂,也是目前COPD稳定期患者维持治疗的常用药物。既往研究证实,长效支气管扩张剂和长效β2-肾上腺素受体激动剂的作用机制能形成互补,进而发挥双重支气管舒张效果[5-6]。目前,噻托溴铵联合马来酸茚达特罗治疗稳定期COPD患者临床疗效的研究报道较少。鉴于此,本研究以炎症因子、细胞免疫功能为切入点,探讨了噻托溴铵联合马来酸茚达特罗在稳定期COPD患者中的应用效果及安全性,现报道如下。
1 对象与方法
1.1 研究对象 前瞻性选取2018年7月至2019年12月中国人民解放军联勤保障部队第962医院收治的稳定期COPD患者120例为研究对象。纳入标准:(1)符合《慢性阻塞性肺疾病诊治指南(2013年修订版)》[7]中COPD的诊断标准;(2)病情处于稳定期。排除标准:(1)伴有其他类型呼吸系统疾病者;(2)对本研究所用药物过敏者;(3)中途退出本研究者。按照随机数字表法将所有患者分为A、B、C组,每组40例。其中A组中途退出3例,B组中途退出2例,C组中途退出1例。三组患者性别、年龄、病程及呼吸困难分级比较,差异无统计学意义(P>0.05),见表1。本研究经中国人民解放军联勤保障部队第962医院伦理委员会审核批准(2021-001),所有患者或家属签署知情同意书。
1.2 治疗方法 所有患者给予祛痰、平喘、抗感染等常规治疗,同时根据患者需要给予硫酸沙丁胺醇(上海信谊金朱药业有限公司生产,规格2.5 ml∶2.5 mg)雾化吸入,0.1~0.2 mg/次,1~2次/d。在此基础上,A组患者给予噻托溴铵粉吸入剂(德国Boehringer Ingelheim Pharma GmbH & Co.KG,规格:18 μg)吸入治疗,18 μg/吸,1吸/d,连续治疗24周。B组患者给予马来酸茚达特罗吸入粉雾剂(瑞士Novartis Pharma Stein AG,规格:150 μg)吸入治疗,150 μg/吸,1吸/d,连续治疗24周。C组患者给予噻托溴铵粉吸入剂联合马来酸茚达特罗吸入粉雾剂吸入治疗,治疗方法同A、B组,连续治疗24周。
1.3 观察指标及方法 (1)炎症因子:治疗前及治疗24周末,采集患者空腹静脉血4 ml,3 000 r/min(离心半径10 cm)离心10 min,留取血清,采用日立7600全自动生化分析仪检测血清白介素6(interleukin- 6,IL-6)、C反应蛋白(C-reactive protein,CRP)、肿瘤坏死因子α(tumor necrosis factor-α,TNF-α)水平,其中IL-6、TNF-α采用酶联免疫吸附试验检测,CRP采用免疫比浊法检测,试剂盒均购自深圳晶美生物工程有限公司。(2)细胞免疫功能指标:治疗前及治疗24周末,采集患者空腹静脉血4 ml,抗凝后采用流式细胞仪分析CD3+T淋巴细胞分数、CD4+T淋巴细胞分数、CD8+T淋巴细胞分数,并计算T淋巴细胞比值。(3)肺功能指标:治疗前及治疗24周末,采用日本美能AS-507肺功能仪检测患者用力肺活量(forced vital capacity,FVC)、第1秒用力呼气容积(forced expiratory volume in the first second,FEV1)及呼气峰流速(peak expiratory velocity,PEF),并计算PEF占预计值的百分比(percentage of PEF to the expected value,PEFpred%)及FEV1/FVC。(4)不良反应:统计三组患者治疗期间不良反应发生情况,包括头痛、口干、咽炎、心悸等。
1.4 统计学方法 应用SPSS 20.0统计学软件进行数据处理。符合正态分布的计量资料以(±s)表示,多组间比较采用单因素方差分析,组间两两比较采用LSD-t检验;计数资料以相对数表示,组间比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 血清炎症因子水平 治疗前,三组患者血清IL-6、TNF-α、CRP水平比较,差异无统计学意义(P>0.05)。治疗24周末,三组患者血清IL-6、TNF-α、CRP水平比较,差异有统计学意义(P<0.05);其中C组患者血清IL-6、TNF-α、CRP水平低于A、B组,差异有统计学意义(P<0.05),见表2。

表1 三组患者基线资料比较Table 1 Comparison of baseline data among the three groups
表2 三组患者治疗前后血清炎症因子水平比较(±s)Table 2 Comparison of serum inflammatory factor levels among the three groups before and after treatment
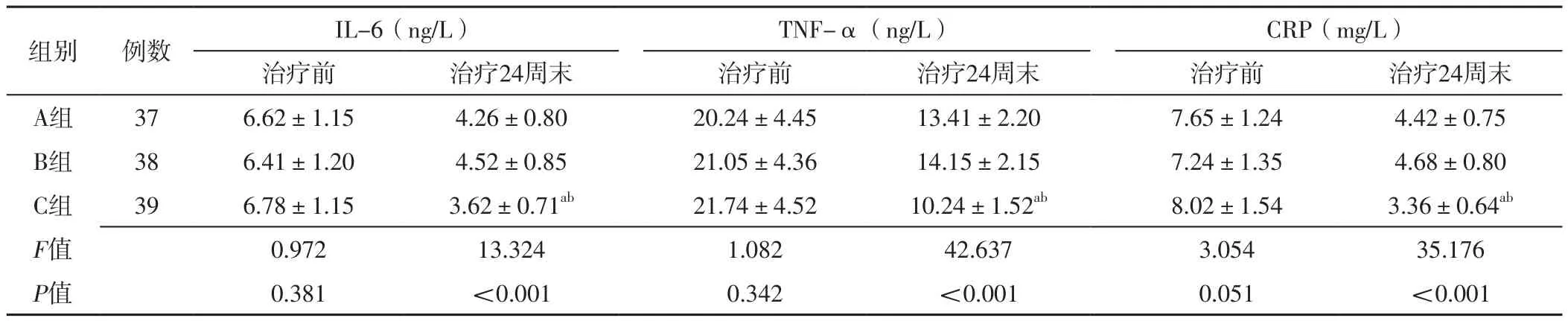
表2 三组患者治疗前后血清炎症因子水平比较(±s)Table 2 Comparison of serum inflammatory factor levels among the three groups before and after treatment
注:IL-6=白介素6,TNF-α=肿瘤坏死因子α,CRP=C反应蛋白;a表示与A组比较,P<0.05;b表示与B组比较,P<0.05
组别 例数 IL-6(ng/L) TNF-α(ng/L) CRP(mg/L)治疗前 治疗24周末 治疗前 治疗24周末 治疗前 治疗24周末A组 37 6.62±1.15 4.26±0.80 20.24±4.45 13.41±2.20 7.65±1.24 4.42±0.75 B组 38 6.41±1.20 4.52±0.85 21.05±4.36 14.15±2.15 7.24±1.35 4.68±0.80 C组 39 6.78±1.15 3.62±0.71ab 21.74±4.52 10.24±1.52ab 8.02±1.54 3.36±0.64ab F值 0.972 13.324 1.082 42.637 3.054 35.176 P值 0.381 <0.001 0.342 <0.001 0.051 <0.001
表3 三组患者治疗前后T淋巴细胞亚群比较(±s)Table 3 Comparison of T lymphocyte subsets among the three groups before and after treatment

表3 三组患者治疗前后T淋巴细胞亚群比较(±s)Table 3 Comparison of T lymphocyte subsets among the three groups before and after treatment
注:a表示与A组比较,P<0.05;b表示与B组比较,P<0.05
+ T淋巴细胞比值治疗前 治疗24周末 治疗前 治疗24周末 治疗前 治疗24周末 治疗前 治疗24周末A组 37 52.36±5.20 58.72±4.54 33.45±5.12 37.20±4.65 33.21±5.23 28.45±4.12 1.01±0.34 1.31±0.23 B组 38 53.12±4.65 57.24±5.15 34.12±5.25 36.41±5.32 32.73±5.36 27.15±4.33 1.04±0.24 1.34±0.25 C组 39 52.75±5.12 65.15±4.36ab 32.30±5.36 40.15±5.41ab 33.65±4.62 25.72±4.25ab 0.96±0.28 1.59±0.32ab F值 0.217 30.947 1.187 5.662 0.316 3.951 0.754 12.430 P值 0.805 <0.001 0.309 0.005 0.730 0.022 0.473 <0.001组别 例数 CD3+ T淋巴细胞分数(%) CD4+ T淋巴细胞分数(%) CD4+/CD8+ T淋巴细胞分数(%) CD8
2.3 肺功能指标 治疗前,三组患者FVC、FEV1、PEFpred%及FEV1/FVC比较,差异无统计学意义(P>0.05)。治疗24周末,三组患者FVC、FEV1、PEFpred%及FEV1/FVC比较,差异有统计学意义(P<0.05);其中C组患者FVC、FEV1大于A、B组,PEFpred%、FEV1/FVC高于A、B组,差异有统计学意义(P<0.05),见表4。
表4 三组患者治疗前后肺功能指标比较(±s)Table 4 Comparison of pulmonary function indexes among the three groups before and after treatment
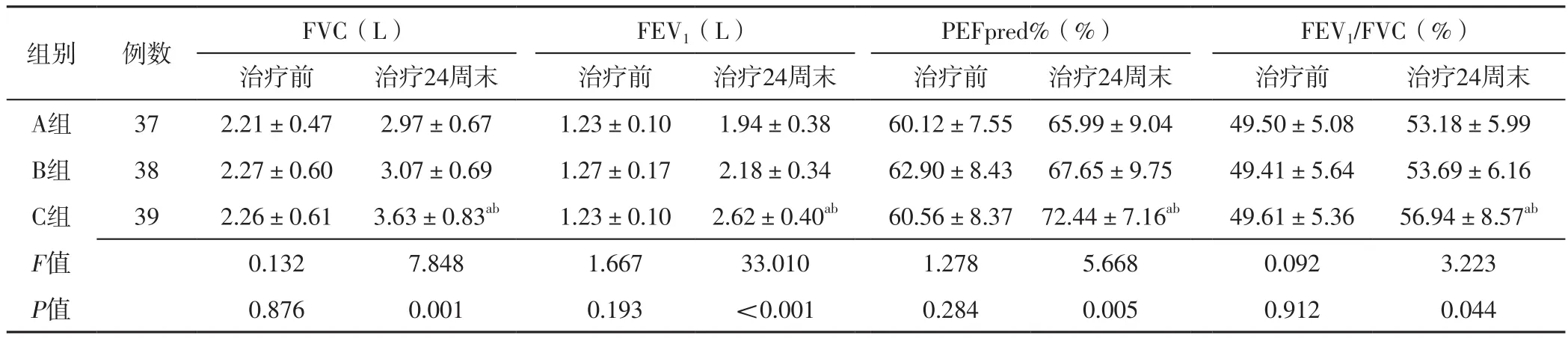
表4 三组患者治疗前后肺功能指标比较(±s)Table 4 Comparison of pulmonary function indexes among the three groups before and after treatment
注:FVC=用力肺活量,FEV1=第1秒用力呼气容积,PEFpred%=呼气峰流速占预计值的百分比;a表示与A组比较,P<0.05;b表示与B组比较,P<0.05
组别 例数 FVC(L) FEV1(L) PEFpred%(%) FEV1/FVC(%)治疗前 治疗24周末 治疗前 治疗24周末 治疗前 治疗24周末 治疗前 治疗24周末A组 37 2.21±0.47 2.97±0.67 1.23±0.10 1.94±0.38 60.12±7.55 65.99±9.04 49.50±5.08 53.18±5.99 B组 38 2.27±0.60 3.07±0.69 1.27±0.17 2.18±0.34 62.90±8.43 67.65±9.75 49.41±5.64 53.69±6.16 C组 39 2.26±0.61 3.63±0.83ab 1.23±0.10 2.62±0.40ab 60.56±8.37 72.44±7.16ab 49.61±5.36 56.94±8.57ab F值 0.132 7.848 1.667 33.010 1.278 5.668 0.092 3.223 P值 0.876 0.001 0.193 <0.001 0.284 0.005 0.912 0.044
2.4 不良反应 A组患者发生头痛1例,咽炎1例,不良反应发生率为5.4%(2/37);B组患者发生口干1例,心悸1例,不良反应发生率为5.3%(2/38);C组患者发生口干1例,心悸1例,不良反应发生率为5.1%(2/39)。三组患者不良反应均轻微,无需治疗。三组患者治疗期间不良反应发生率比较,差异无统计学意义(χ2=0.006,P=0.957)。
3 讨论
相关调查显示,我国COPD患病人数高达1亿,其中40岁以上人群患病率为13.7%[8]。且我国较欧美国家COPD患者症状更为严重,防护意识更薄弱,就诊时绝大多数患者肺功能已减退30%~50%[9]。支气管舒张剂是治疗COPD的基石,但不同患者对支气管舒张剂的反应存在差异,而不同作用机制及反应时间的支气管舒张剂联合应用能更好地控制COPD患者的临床症状[10]。研究表明,长期使用长效β2-肾上腺素受体激动剂容易激活M3受体,产生β2-肾上腺素受体减敏作用,而联合长效胆碱能受体抑制剂能够阻断M受体激活通路,抑制β2-肾上腺素受体脱敏[11]。此外,长效胆碱能受体抑制剂还可以通过拮抗气道平滑肌M2受体而缓解其对β2-受体激动剂诱导的环磷酸腺苷释放的抑制作用,进而达到“1+1>2”的支气管舒张效应[12]。
噻托溴铵是长效胆碱能受体抑制剂的代表药物,其可以选择性地结合M3受体,抑制M3受体所致的气道平滑肌松驰。马来酸茚达特罗是长效β2-肾上腺素受体激动剂的代表药物,具有扩张血管、松驰气道平滑肌、促进纤毛运动等多重作用,与其他同类药物相比,其在气道黏膜清除方面作用更为突出,且可缓解呼吸肌的疲劳程度,是目前最常用的COPD缓解期维持治疗药物。既往研究表明,噻托溴铵粉吸入剂的绝对生物利用度为19.5%,而马来酸茚达特罗则高达42%~45%,且可呈剂量依赖性地持续(24 h)扩张血管[13-14]。噻托溴铵、马来酸茚达特罗的作用路径、活化机制不同,可形成互补,发挥协同效应,能够在较低剂量的基础上达成最大化扩张支气管的效果[15-17]。MALTAIS等[18]进行的一项纳入2 425例COPD患者的随机对照研究结果显示,噻托溴铵+马来酸茚达罗吸入剂在改善COPD患者肺功能方面明显优于噻托溴铵。DONOHUE等[19]研究报道,与马来酸茚达特罗相比,噻托溴铵+马来酸茚达特罗可有效提高患者的FEV1及生活质量。本研究结果显示,治疗24周末,C组患者FVC、FEV1大于A、B组,PEFpred%、FEV1/FVC高于A、B组,且三组患者治疗期间不良反应发生率比较差异无统计学意义,提示噻托溴铵联合马来酸茚达罗吸入剂能有效改善稳定期COPD患者的肺功能,且未增加药物相关不良反应。
COPD是一种慢性炎症浸润性疾病,各种中性粒细胞、淋巴细胞、巨噬细胞等均能促进气道炎症进展[20]。β2-肾上腺素受体激动剂具有促进黏液细胞分泌、抑制炎症递质释放等多重生物学效应[21]。胆碱能受体抑制剂可通过调节迷走神经活性、抑制乙酰胆碱活性等多条途径发挥抗炎效果[22]。噻托溴铵联合马来酸茚达特罗为一种胆碱能受体抑制剂、β2-肾上腺素受体激动剂组合的“双长效气管扩张剂”,可分别作用于大、小气道,且药物颗粒可迅速送达并富集于肺部,进而达到“双箭并举”的效果[23]。相关研究表明,噻托溴铵联合马来酸茚达特罗能有效拮抗COPD患者的炎症反应,改善患者肺功能[24]。本研究结果显示,治疗24周末,C组患者血清IL-6、TNF-α、CRP水平及CD8+T淋巴细胞分数低于A、B组,T淋巴细胞分数、T淋巴细胞分数、T淋巴细胞比值高于A、B组,提示噻托溴铵联合马来酸茚达特罗可有效抑制稳定期COPD患者的炎症反应、调节细胞免疫功能。
综上所述,噻托溴铵联合马来酸茚达特罗能有效抑制COPD患者炎症反应,调节细胞免疫功能,进而促进患者肺功能恢复,且未增加药物相关不良反应。但本研究仅分析了噻托溴铵联合马来酸茚达特罗影响炎症因子、细胞免疫功能的表象,其内在机制尚不明确,仍需后续扩大样本量、开展多中心随机对照研究进一步证实。
作者贡献:赵守焱进行文章的构思与设计、研究的实施与可行性分析,撰写、修订论文,负责文章的质量控制及审校,对文章整体负责、监督管理;尚建欣、褚春红进行数据收集、整理、分析,结果分析与解释。
本文无利益冲突。
