金刚烷-手性方酰胺催化剂的合成
2022-06-01高艳蓉唐文强仝红娟
高艳蓉,唐文强*,刘 斌,仝红娟
(1.陕西国际商贸学院医药学院,陕西 西安712046;2.陕西省中药绿色制造技术协同创新中心,陕西 西安712046)
手性方酰胺作为一类结构特殊的手性催化剂,具有优良的氢键供体活性及刚性结构,在不对称催化反应中的重要作用得到了人们的重视[1-2]。鉴于手性方酰胺催化剂在不对称催化反应中优异的催化活性及立体选择性,目前,手性方酰胺被广泛应用于各种不对称催化体系中,如硝基烯与查尔酮的不对称加成反应体系[3]、硝基烯与异丁醛的不对称Michael加成反应体系[4]、不对称Mannich反应体系[5]、氮杂二烯与氮内酯的[4+2]环化反应体系[6]、Michael/Aldol串联反应[7]等,越来越多的基于手性方酰胺催化的体系被开发出来。金刚烷是一种具有高度对称结构的笼状化合物,其骨架是由3个具有椅式构像特征的环己烷构成的环状四面体,类似于金刚石的一个晶格单元[8]。金刚烷以其独特的物理和化学性质得到了广泛的应用,尤其是在不对称催化领域,大位阻金刚烷基可以起到较好的空间位阻作用,从而诱导反应物在空间上以某种特定的方向发生反应,得到单一构型的产物[9-12]。
为了开发结构新颖的手性方酰胺催化剂,作者以方酸二乙酯(Ⅱ)为原料,经两步氨解反应,分别引入大位阻的金刚烷基团和手性基团,得到两种金刚烷-手性方酰胺催化剂(Ⅰa和Ⅰb,合成路线见图1),为手性方酰胺催化剂在不对称催化反应中的应用提供支持。
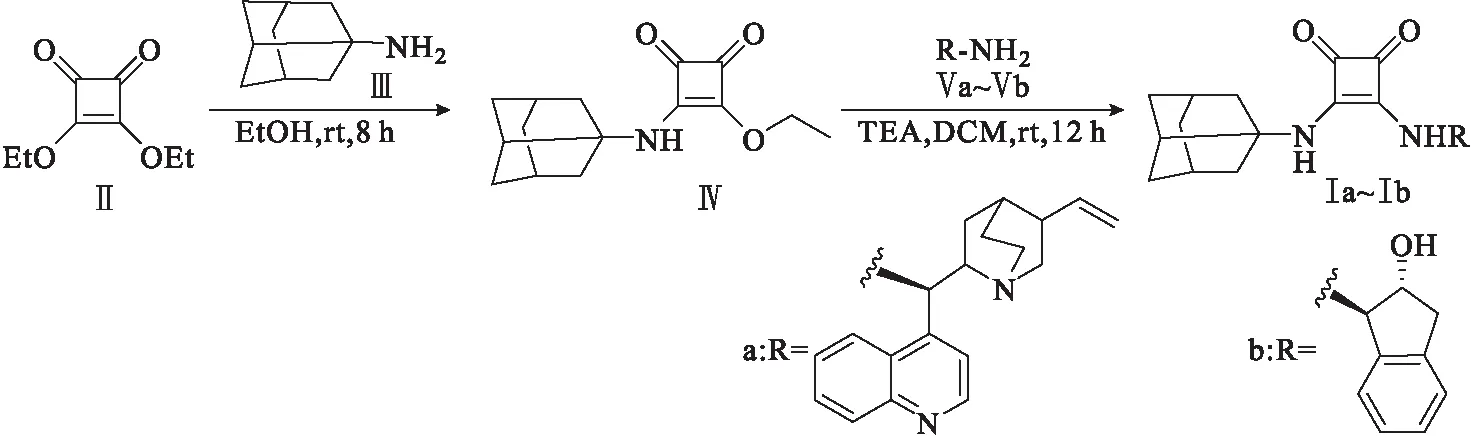
图1 金刚烷-手性方酰胺催化剂的合成路线
1 实验
1.1 试剂与仪器
方酸二乙酯(Ⅱ)、金刚烷胺(Ⅲ)、9-氨基-(9-脱氧)表辛可宁三盐酸盐(Ⅴa)、(1R,2R)-(-)-1-氨基-2-茚醇(Ⅴb),泰坦科技股份有限公司;柱层析硅胶(300~400目),青岛海洋化工厂;其它试剂均为市售分析纯。
AV400型核磁共振波谱仪(CDCl3或DMSO-d6为溶剂,TMS为内标),德国Bruker公司;Ultima Global Spectrometer型质谱仪(ESI源),美国Waters公司;RE-52AA型旋转蒸发仪,上海亚荣生化仪器厂;SHB-Ⅲ型循环水式多用真空泵,郑州长城科工贸有限公司。
1.2 合成方法
1.2.1 金刚烷-方酰胺单乙酯(Ⅳ)的合成
将方酸二乙酯(Ⅱ)3.4 g(20.0 mmol)加入到无水乙醇(30 mL)中,搅拌均匀后加入金刚烷胺(Ⅲ)3.0 g(22.0 mmol),室温反应8 h,析出大量固体,减压抽滤,得到3.6 g淡黄色固体中间体Ⅳ,收率68.0%。1HNMR(400 MHz,CDCl3),δ:6.06(brs,1H),4.91~4.77(m,2H),2.20~2.11(m,3H),1.98~1.90(m,5H),1.73~1.65(m,5H),1.48(t,J=7.0 Hz,3H);ESI-MS,m/z:262.2[M+H]+。
1.2.2 金刚烷-手性方酰胺(Ⅰ)的合成
将中间体Ⅳ1.3 g(5.0 mmol)、三乙胺1.5 g(15.0 mmol)分别加入二氯甲烷(80 mL)中,搅拌均匀后,加入手性胺(Ⅴ)(6.0 mmol),室温反应12 h,析出大量固体,减压抽滤,得到金刚烷-手性方酰胺(Ⅰ)。
金刚烷-手性方酰胺(Ⅰa):白色固体,收率68.2%。1HNMR(400 MHz,DMSO-d6),δ:8.97(d,J=4.5 Hz,1H),8.43(d,J=8.4 Hz,1H),8.14(d,J=8.8 Hz,1H),8.08(d,J=8.3 Hz,1H),7.80(t,J=7.2 Hz,1H),7.71(t,J=7.5 Hz,1H),7.66(d,J=4.4 Hz,1H),7.61(s,1H),6.12(s,1H),5.87~5.78(m,1H),5.21~5.17(m,1H),5.10~5.08(m,1H),3.22~3.10(m,1H),2.95~2.77(m,3H),2.24~2.22(m,1H),2.05~2.00(m,3H),1.91~1.86(m,5H),1.63~1.55(m,6H),1.24(t,J=7.2 Hz,2H),1.18(t,J=7.1 Hz,1H),1.07~0.96(m,1H),0.87~0.81(m,1H);13CNMR(100 MHz,DMSO-d6),δ:167.36,150.66,147.96,140.57,127.10,122.96,114.75,109.47,80.64,80.19,59.17,52.14,48.64,42.25,35.16,28.54,27.19,25.07;ESI-MS,m/z:509.4[M+H]+。
金刚烷-手性方酰胺(Ⅰb):白色固体,收率65.8%。1HNMR(400 MHz,DMSO-d6),δ:8.01~7.98(m,1H),7.32~7.14(m,3H),5.46~5.42(m,1H),5.34(s,1H),4.51(s,1H),3.40~3.35(m,4H),3.11~3.06(m,1H),2.88~2.84(m,1H),2.13~2.06(m,2H),2.02~1.91(m,4H),1.25~1.22(m,5H);13CNMR(100 MHz,DMSO-d6),δ:168.27,167.82,141.72,140.51,127.83,126.59,125.02,124.29,72.49,62.61,60.93,52.04,42.62,35.34,28.90;ESI-MS,m/z:365.3[M+H]+。
2 结果与讨论
2.1 物料比对金刚烷-方酰胺单乙酯(Ⅳ)收率的影响
方酸二乙酯(Ⅱ)与金刚烷胺(Ⅲ)发生氨解反应合成中间体Ⅳ,考察物料比n(Ⅲ)∶n(Ⅱ)对中间体Ⅳ收率的影响,结果见表1。

表1 物料比对中间体Ⅳ收率的影响
考虑到原料成本,为了尽可能将化合物Ⅱ反应完全,选择化合物Ⅲ过量。由表1可知,当n(Ⅲ)∶n(Ⅱ)=1.0∶1时,中间体Ⅳ收率为61.4%;增加化合物Ⅲ的用量为n(Ⅲ)∶n(Ⅱ)=1.1∶1,中间体Ⅳ收率达到68.0%;继续增加化合物Ⅲ的用量,中间体Ⅳ收率反而降低。主要是因为,化合物Ⅲ过量较多,则化合物Ⅱ结构中两个酯基均会发生氨解反应,生成双氨解反应副产物;TLC监测也显示副产物点明显。因此,选择适宜的物料比n(Ⅲ)∶n(Ⅱ)=1.1∶1。
2.2 金刚烷-手性方酰胺(Ⅰ)的合成条件优化
以Ⅰa的合成作为模型反应,考察反应溶剂、物料比n(Ⅴ)∶n(Ⅳ)、反应时间等因素对目标化合物Ⅰa收率的影响,结果见表 2。
由表2可知,固定物料比n(Ⅴ)∶n(Ⅳ)=1.0∶1、反应时间为12 h,考察4种反应溶剂(甲醇、乙醇、四氢呋喃、二氯甲烷)对目标化合物Ⅰa收率的影响,发现:该氨解反应在4种溶剂中均可进行,其中,在二氯甲烷中Ⅰa收率最高,为57.1%;在其它3种溶剂中收率较低。因此,选择反应溶剂为二氯甲烷。固定反应溶剂为二氯甲烷、反应时间为12 h,考察n(Ⅴ)∶n(Ⅳ)对目标化合物Ⅰa收率的影响,发现:n(Ⅴ)∶n(Ⅳ)=1.2∶1时,目标化合物Ⅰa收率最高,为68.2%;继续增大n(Ⅴ)∶n(Ⅳ)=1.3∶1时,Ⅰa收率并没有明显提高。因此,选择n(Ⅴ)∶n(Ⅳ)=1.2∶1。固定反应溶剂为二氯甲烷、n(Ⅴ)∶n(Ⅳ)=1.2∶1,考察反应时间对目标化合物Ⅰa收率的影响,发现:缩短反应时间为10 h时,Ⅰa收率明显降低;而延长反应时间为14 h时,Ⅰa收率没有明显变化。因此,确定适宜反应时间为12 h。
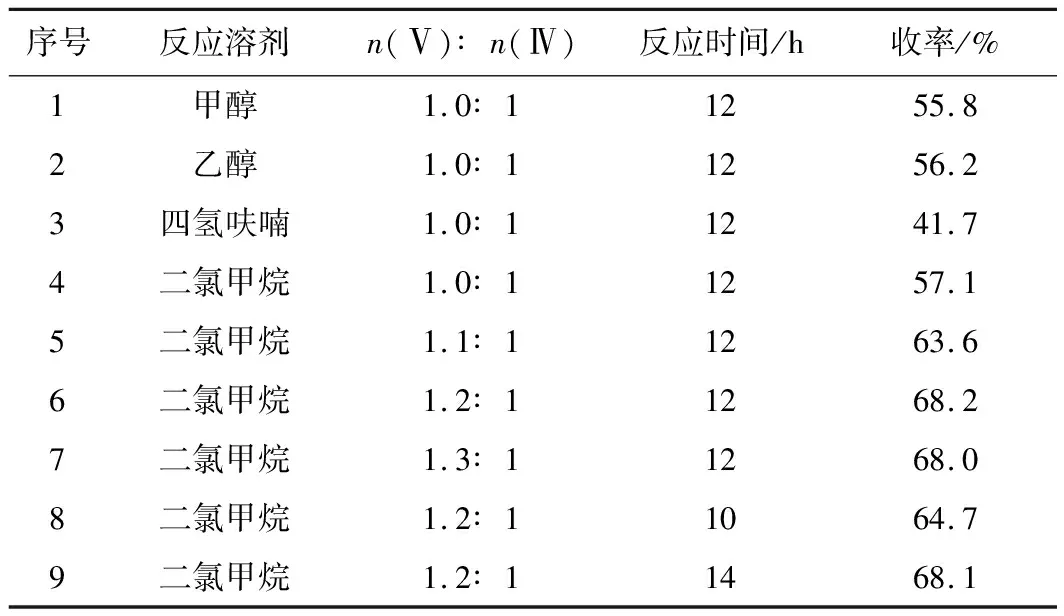
表2 反应条件对目标化合物Ⅰa收率的影响
2.3 中间体及目标化合物的1HNMR分析(图2、图3)
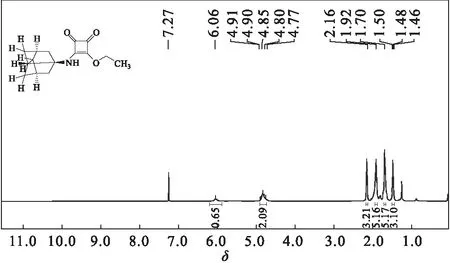
图2 中间体Ⅳ的核磁共振氢谱
由图2可知:δ6.06处的宽峰,归属为-NH-信号峰;δ4.91~4.77处的多重峰,归属为乙氧基上的亚甲基;δ2.20~2.11处的多重峰、δ1.98~1.90处的多重峰、δ1.73~1.65处的多重峰,均为金刚烷结构的亚甲基及次甲基;δ1.48处的三重峰,归属为乙氧基上的甲基。结合质谱结果,确定中间体Ⅳ结构正确。
由图3a可知:对照图2,发现乙氧基信号峰消失,同时金鸡纳碱结构中的烯烃(δ5.87~5.78、δ5.21~5.17、δ5.10~5.08处的多重峰)及芳香烃信号峰出现,说明目标化合物Ⅰa形成。由图3b可知:对照图2,发现乙氧基信号峰消失,同时茚醇结构中的芳香烃(δ8.01~7.98、δ7.32~7.14处的多重峰)信号峰出现,说明目标化合物Ⅰb形成。结合13CNMR和质谱分析,确定目标化合物结构正确。

图3 目标化合物Ⅰa(a)和Ⅰb(b)的核磁共振氢谱
3 结论
以方酸二乙酯(Ⅱ)和金刚烷胺(Ⅲ)为原料,经氨解反应得到金刚烷-方酰胺单乙酯中间体(Ⅳ),再分别与9-氨基-(9-脱氧)表辛可宁三盐酸盐(Ⅴa)和(1R,2R)-(-)-1-氨基-2-茚醇(Ⅴb)发生氨解反应得到两种金刚烷-手性方酰胺衍生物Ⅰa和Ⅰb,中间体及目标化合物结构经1HNMR、13CNMR和MS表征。分别对两步反应的主要影响因素进行讨论,确定合成金刚烷-方酰胺单乙酯(Ⅳ)的最佳物料比n(Ⅲ)∶n(Ⅱ)=1.1∶1;合成目标化合物Ⅰ的最佳反应条件为:反应溶剂为二氯甲烷、物料比n(Ⅴ)∶n(Ⅳ)=1.2∶1、反应时间12 h。该研究提供了两种结构新颖的手性方酰胺催化剂,可用于各种不对称催化体系的筛选,具有一定的应用价值,有望在不对称催化反应中取得较高的对映选择性和收率。
