脑电信号传感检测芯片系统综述*
2022-05-30王梓斌刘国柱孙建辉
王梓斌,刘国柱,孙建辉
(1.山东师范大学物理与电子科学学院,济南 250358;2.中科芯集成电路有限公司,江苏无锡 214072)
1 引言
脑电(Electroencephalogram, EEG)信号与生物体的生命状态密切相关,其具有非线性、幅值低、频率范围低、噪声强、随机性强等特点。随着医学、神经科学、认知心理学、微电子技术、人工智能研究等学科与技术的迅速发展,EEG 信号的检测发挥着越来越重要的作用。EEG 信号是脑神经细胞电生理活动在大脑皮层或头皮表面的总体反映,作为人体体征信号中的一种典型信号,其包含了大量的神经电生理信息。对EEG信号进行采集与分析,一方面,对于临床医学尤其在抑郁症、癫痫、脑肿瘤、痴呆等诸多神经系统疾病的临床诊断中发挥着重要作用;另一方面,在脑科学研究与工程应用方面,EEG 信号检测设备与人工智能(Artificial Intelligence,AI)技术相互融合促进,例如研究人员正在尝试通过提取EEG 信号有关特征以实现脑机接口(Brain Computer Interface, BCI)通讯闭环控制。然而EEG 信号是低频率低幅值的非平稳随机信号,很容易受到头皮与传感器之间接触状态的影响以及来自环境噪声等各类背景噪声的干扰[1],因此这些微弱的EEG 信号需要被放大并进行一系列抗噪声处理。
EEG 检测包括基于传感器/电极的信号采集以及采集后的调理芯片处理,传统的EEG 检测流程包括:将湿电极制成的EEG 检测帽戴到使用者头上,将导电胶涂抹到电极与头皮的接触处,接上引线进行采集;采集的信号通过放大器进行微弱EEG 小信号放大处理,以及随后的滤波等预处理操作;经过通信模块将信号传输到计算机等上位机进行算法处理[2]。近十几年来,具备体积小、使用安全方便、佩戴舒适等特点的便携式EEG 检测微型设备开始获得广泛的实际应用,这种微型化装置可以对癫痫等慢性疾病进行长期监测,也将大大提高用户对脑机接口系统的接受度。因此基于EEG 传感检测芯片构成的便携可穿戴EEG 信号检测微系统有着良好的研发和应用前景,具有广泛的医学意义[3]。本文主要介绍了EEG 信号检测微传感器芯片,主要包括EEG 电极、EEG 信号传感后调理芯片2 部分,对EEG 检测传感器与传感后调理芯片的国内外研究工作以及发展趋势进行了综述。
2 EEG 检测芯片系统传感器模块
电极能够从头皮表面获取EEG 信号,在EEG 信号检测过程中发挥着重要的作用,其主要分为湿电极和干电极。传统的EEG 信号采集方法通常使用湿接触电极,湿电极多年来一直是记录头皮表面EEG 信号的最常用设备,然而这需要操作员花费时间将导电凝胶涂抹到每个测试位置,使用后凝胶的清理过程对于受试者来说也比较痛苦。因此,湿接触电极的使用过程非常繁琐,不方便神经系统疾病的诊断,特别是在需要长时间记录EEG 信号的情况下(长时间使用的情况下导电凝胶会脱水凝固),所以传统湿电极不适合可穿戴EEG 检测设备或系统。
为了克服传统湿电极的缺点,各类的新型干电极被研发出来,这些设计在消除电极对电解凝胶依赖的同时保证了低接触阻抗和良好的信噪比。根据电极与头皮的接触方式与程度进行分类,干电极主要分为两大类:(1)干接触电极,可以进一步被分为有创干接触电极与无创干接触电极;(2)无接触电极,通过“电容耦合”效应来感知头皮的生物电位信号,而无需直接与头皮接触,但是这种传感方法对于神经信号记录来说不够准确、可靠和灵敏[4]。干接触电极大多需要穿过头发,通过直接接触头皮去感知EEG 信号,但是由于不使用导电凝胶,直接贴在头皮上,电极与头皮之间的阻抗会非常大,这对传感后放大器模块的电路设计提出了挑战,需要优化匹配传感器与头皮之间的电气接口。同时如何最大可能地降低EEG 检测过程中各类噪声引发的感知EEG 信号污染,这也给电极的设计带来了困难。
此外,也可以依据不同的研究技术或制作工艺路线对干电极进行分类:(1)使用微机电系统(Micro Electro Mechanical System, MEMS)工艺制造的EEG干电极;(2)适合微型可穿戴设备或系统的EEG 有源电极,该设计将干接触电极和传感后电路集成在一起;(3)电容AC 耦合(Alternating Current Coupling,AC Coupling)的无接触干电极;(4)半干电极;(5)DC 耦合(Direct Current Coupling,DC Coupling)的干接触电极;(6)通过指状、梳状等类似结构穿过头皮解决“头发障碍”的干电极;(7)通过3D 打印机制备的干电极;(8)其余类型的干电极。同时,这些报道的干电极存在不同技术路线或制作工艺路线的互相融合。
2.1 有创的干接触电极
由于头皮上的角质层会带来高阻抗,因此,一些研究主要集中在借助MEMS 工艺技术制作微针或者纳米针穿透头皮的角质层[5],以此大幅度降低头皮与电极之间的阻抗,相比于无创直接贴合头皮获取EEG信号的平板干接触电极,通过微针电极获取的信号质量更好,然而其具备一定的刺穿性,存在感染的风险,同时电极制作的成本也很高。当然,如果电极微针的长度合适,使用者不会感到任何疼痛。为了避免疼痛,微针的长度最好不超过200 μm,在理想情况下,穿透长度应减少至70 μm,医学文献中报告的表皮层厚度仅为70 μm[6]。2002 年斯德哥尔摩皇家理工学院课题组使用微针MEMS 干电极成功采集前额EEG 信号,并提出微针的尺寸与涂层材料和电极的接触阻抗有着密切的联系,干电极上的微针阵列如图1 所示,该电极底层载体为一块圆形双面电路板,涂有Ag/AgCl 涂层材料的微针附着在底层载体上,该MEMS 干电极技术以侵入性的方式获取EEG 信号[7]。

图1 干电极上的微针阵列[7]
2008 年巴塞罗那大学神经病学实验室报告了使用多壁碳纳米管(Multi Walled Carbon Nano Tube,MWCNT)材料的新型微针阵列电极[8],并提供了一系列人体试验结果,MWCNT 电极如图2 所示,该电极呈现微针形状。微针状电极以导电的多掺杂硅作为衬底,然后在多掺杂硅衬底上面附着碳纳米管材料,其设计目标是微针状电极能够穿透头皮角质层并改善接触阻抗。测试表明其性能与当时研究的主流方向湿电极相当,并且试验六个月后未观察到受试者身上有任何副作用,受试者在使用电极时也未报告任何疼痛或异常感觉。
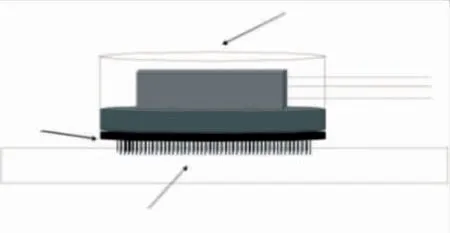
图2 MWCNT 电极设计原型图[8]
2013 年上海交通大学采用切割、刻蚀和溅射等一系列MEMS 工艺制备了一种可用于长期脑电图测量的金字塔形微针电极。通过穿刺测试和舒适度调查,优化了电极的刺穿力度和深度,金字塔形电极如图3所示,刺穿深度为200 μm,使用舒适、安全、无疼痛[9]。
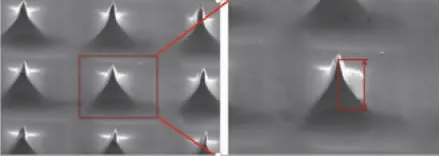
图3 金字塔形电极及其微针在显微镜下呈现的图像[9]
2.2 无创的干接触电极
常见的干接触电极还有无创干接触电极,与使用微针穿透头皮角质层的具有刺穿性的有创电极不同,无创干接触电极与头皮的接触面上不会有微针,接触面通常为基于柔性材料制作的平板结构,以此保证头皮与电极保持持续的紧密接触。由于电极与头皮的接触面没有涂抹导电膏,电极也没有穿透角质层感知EEG 信号,因此电极的接触阻抗很大,这就要求后端放大器的输入阻抗足够大,以此匹配前端电极的阻抗。此外,电极与头皮面的接触状况会受到电极和头发之间摩擦的影响,所以突破“头发障碍”也是需要克服的困难。通常传感器的整体结构被设计为“指状”或者“梳状”,以保证电极穿越“头发障碍”,达到电极阵列更好地与头皮可靠接触的目的。最早在1994 年,加利福尼亚大学提出了一种用于EEG 信号记录的干电极[10],传感器的整体结构如图4 所示。设计的电极避免了使用前涂抹导电膏,并且与传统湿电极进行对比,发现EEG 信号输出完全符合当时的评估标准,然而其设计的电极仍然存在着一些需要解决的问题。由于在采集EEG 信号的过程中需要保持电极与头皮的良好接触,而在当时,由于集成电路技术并不是很发达,干电极的表面积较大(通常直径为6~15 mm),因此电极和头发的接触运动可能会导致头皮与电极分离。同时,由于运动伪影,在干电极的使用中经常观察到低频闪烁噪声(1/f)以及近似直流的电极失调噪声,这些噪声会降低所得到的EEG 图像的质量。

图4 实验性干电极(所有组件均封装在屏蔽铜盒中)[10]
2011 年台湾交通大学提出了一种新型的干泡沫电极以用于长期脑电图检测[11],这种电极改善了以往干电极不能很好地透过“头发障碍”接触头皮的问题,同时它不同于其他大多数使用MEMS 工艺刺穿头皮的干电极,也不同于当时一些具有无创特点的织物电极,这些织物电极通常用于心电图(Electrocardiograph,ECG)的检测,不适合测量毛发部位的生物电位,因为毛发会减少皮肤和电极的接触面积。这种新型干泡沫电极在解决这些“头发障碍”问题的同时,还进一步保持了织物电极无创、舒适的特点。其设计将一种由聚氨酯材料制成的导电聚合物泡沫压缩变形,干泡沫EEG 检测电极如图5 所示,给出了设计传感器的每层组成结构与每层的几何尺寸。经过实验评估,发现在电极与皮肤接触面积相同的情况下,一方面,该新型干泡沫电极的接触阻抗远低于织物电极的接触阻抗;另一方面,新型干泡沫电极的性能表现与湿电极相近,并且有毛发处的阻抗和无毛发处的阻抗几乎相等,说明它能够适应不规则头皮表面,甚至毛发部位。由于该电极良好的柔软性和头皮附着力,在长时间的步行运动下,该电极运动伪影明显小于传统湿电极。尽管电极使用材料的生物相容性仍需进一步验证,但这展现了该电极在EEG 信号检测上的潜力,它为临床和研究应用提供了一种新型的干电极原型。

图5 干泡沫EEG 检测电极[11]
2.3 半干接触电极
传统湿电极通过涂抹导电凝胶,填充头皮与电极之间的缝隙,构成导通电路,降低电极与头皮之间的接触阻抗,使用湿电极构成的EEG 信号检测系统采集到的EEG 信号质量最好,湿接触电极可以作为其他电极系统的标准。然而使用湿电极采集EEG 信号存在电极使用前准备工作复杂繁琐以及使用后清理困难等问题,难以在日常生活中广泛使用;干电极不需要使用导电凝胶,但是也有信号质量差、噪声严重的问题。部分研究结合了“湿”(低阻抗)和“干”(无凝胶)电极系统的优点,研制了可以自动往电极-头皮接触面传输少量电解液的“半干电极”,以克服常规干接触电极和湿电极(Ag/AgCl)用于EEG 信号记录的局限性,“半干电极”展现了EEG 信号测试和应用开发的前景,是一种有使用前途的中间替代品。
2016 年葡萄牙波尔图大学神经心理生理学实验室提出了一种基于聚碳酸酯芯和润湿剂(电解液)的新型聚合物电极[12-13],这种新型电极的设计类似于毛笔的原理,电极尖端通过少量放置在皮肤和电极接触处的润湿剂保持毛笔笔尖持续湿润,润湿剂是通过由重力和来自内置储液器的毛细力驱动至电极尖端的;信号传导则是通过内置储液器内的氯化物银丝。研究人员在相同条件下比较了使用聚合物电极系统和传统Ag/AgCl 电极系统在听觉怪球范式实验中的性能表现,结果表明,其性能表现与传统的Ag/AgCl 电极类似。2017 年中国科学院半导体研究所集成光电子学国家重点实验室开发了一种兼具干电极高便捷性和湿电极低接触阻抗的新型微渗漏电极[14],其结构如图6(a)所示,其中i 为圆柱状的树脂外壳,ii 为氯化过的银丝,iii 为灵活柔软的电极尖端,iv 为聚合物海绵,v 为标准商用湿电极EEG 引线。图6(b)展示了电极的实物形状,其灵活柔软的电极尖端类似于中国毛笔的尖端,它的锥形尖端可以穿过头发,很容易接触头皮。图6(c)给出了电极在头皮的检测位点。电极在与头皮接触后,其尖端只需较小的压力便可以改变形状,从而扩大头皮与电极的接触面积,进而获得更好的接触阻抗。使用前,将电极浸入电解液中,海绵将持续吸收电解液直至饱和,使用中,存储了电解液的海绵将通过尖端向头皮连续提供少量电解液,持续保持头皮与电极尖端的接触处湿润。同时,研究人员比较了该新型微渗漏电极与其他几款半干电极,结果表明,与其他半干电极相比,采用弹性柔软接触材料的微渗漏电极使用时间最长,接触阻抗最低;同时,随着对电极材料和电解液的逐步研究,半干电极将会在兼具便捷性的同时性能更加强大,为便携式EEG 信号检测装置所使用。图6(d)是以该电极为基础制作的EEG 检测帽。
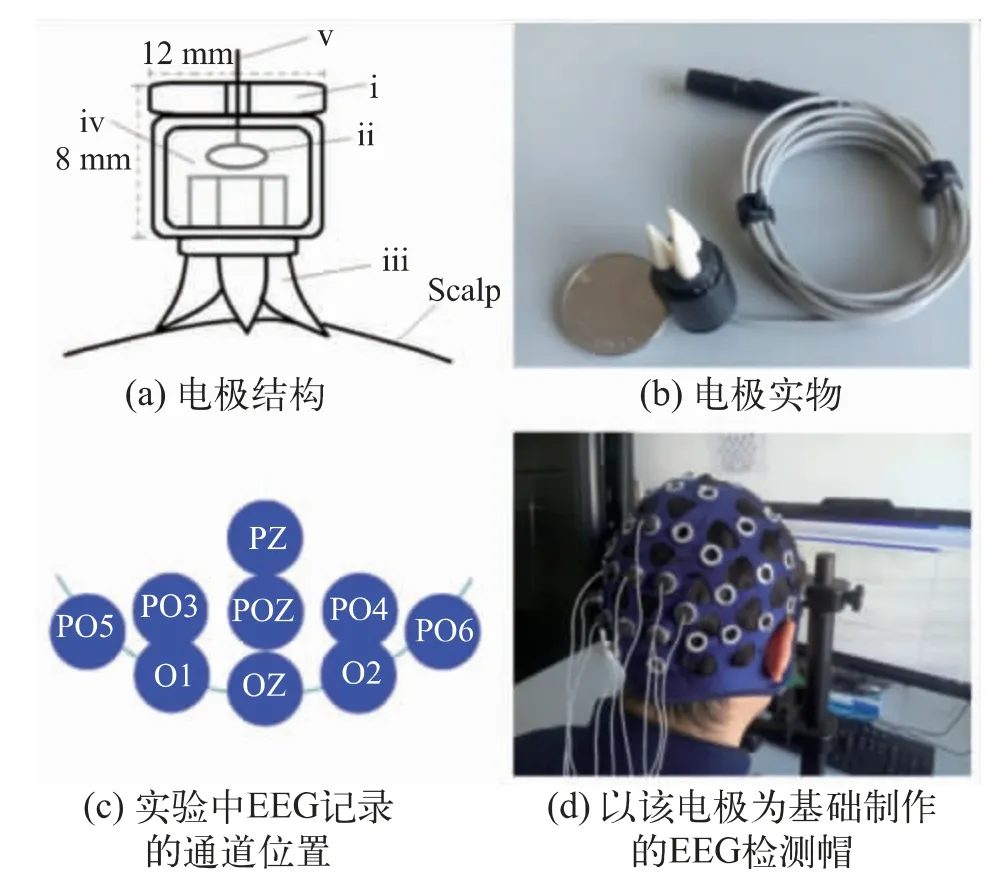
图6 新型微渗漏电极[14]
2.4 无接触电极
无接触电容电极通过测量头皮表面和置于头发上的电极之间的电容来记录EEG 信号,它依赖于检测位移电流,位移电流与EEG 信号源相关的电场变化成正比。尽管有很多人认为无接触电极不适用于医疗级别的场景,对干接触电极的改善才是研究的主流,但也有很多科研人员仍然在研究无接触电极。湿电极和干接触电极都需要直接接触皮肤才能顺利工作,而无接触电极可以隔着衣服,头发等绝缘层工作,理论上更加方便、安全,也可以带给使用者更好的舒适感。最早在1973 年日本东北大学提出了一种基于钛酸钡陶瓷材料的无接触电容型电极,该电极可以用于EEG、ECG 等微弱生物信号的检测[15]。1994 年英国萨塞克斯大学描述了一个ECG 阵列系统,其由25 个超高阻抗传感器(属于无接触电极)组成,不需要与身体进行欧姆电接触[16]。进一步的,即便使用无接触电容型电极,借助传感后电路结构的改善,仍然可以弥补无接触电极感知信号不够准确的缺点。例如,2010 年加利福尼亚大学电气与计算机工程系课题组开发了一种无线生物信号检测系统,其使用了无接触电极,实物图如图7 所示,其给出了电容传感器的组成结构:接头、放大器、中间介质层和处于底层的感应板。该系统展示了无接触电极同样可以产生与临床级Ag/AgCl 电极涂导电膏的湿电极质量相当的信号,可以应用于准确检测ECG 和EEG 信号,非常适合未来的移动医疗设备,同时作者也提出,电容式无接触传感器的一个主要缺点是易受运动伪影的影响[17]。

图7 无接触电容电极实物图[17]
针对无接触电极的运动伪影问题,也有论文进行了分析与解决,例如,2017 年弗林德斯大学提出了一种新的无接触电极结构设计,其无接触电极结构设计图如图8 所示,通过构建一个分段共面环形电容电极,增加环形分离,增加了EEG 的通信率并改善了伪影问题,最终获得可靠的信号[18]。
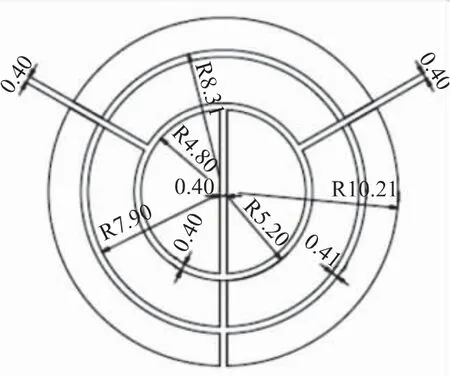
图8 无接触电极结构设计图[18](单位:mm)
2013 年韩国首尔大学引入了一种可以用于EEG信号记录的电容电极[19],基于聚合物泡沫材料的EEG电容电极如图9 所示,该电极材料基于导电聚合物泡沫制成,从而提高了电极性能,和其他电容电极一样,它不需要皮肤与电极直接接触。
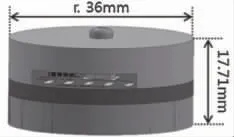
图9 基于聚合物泡沫材料的EEG 电容电极[19]
同年,首尔大学还开发了一种基于聚二甲基硅氧烷(Polydimethylsiloxane,PDMS)材料的通过粘合剂贴在头皮上的小尺寸生物电容电极[20],用于长期脑电图监测。该EEG 电极与皮肤之间的粘附力相对较强,因此电极可以在无任何附加装置的情况下附着在头皮上,该电极相对于以往的电容电极尺寸小得多,同时保持着优良的电气特性,其直径仅为6 mm,高度为4 mm,可以被头发遮住,其结构如图10 所示。基于皮肤和细胞的试验表明,该电极具有足够的生物相容性,可长期使用。
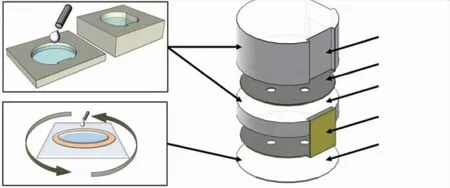
图10 基于PDMS 材料的EEG 电极以及组装示意图[20]
2016 年首尔大学制备了一种基于碳纳米管(Carbon Nano-Tube, CNT)/ 粘合剂聚二甲基硅氧烷(adhesive Polydimethylsiloxane,aPDMS)复合材料的无接触电容电极[21],用于EEG 信号的测量,电极结构如图11 所示。CNT/aPDMS 复合材料合成电极具有弹性好、导电性强、易粘着的特点,能够在多毛发处与头皮进行自适应的接触和附着。通过记录脑电图来评估电极的性能,结果表明该电极具有较高的信噪比,可以产生与使用传统湿电极获得的信号相当的高质量信号。
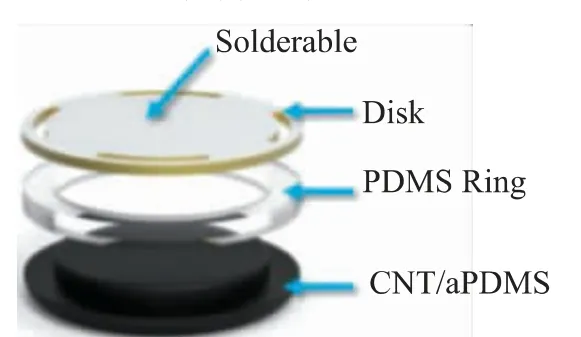
图11 电极的结构图(包括焊盘、CNT/aPDMS 层和PDMS 环)[21]
此外,由于电容电极中的电极阻抗比传统湿电极高得多,电容电极已经有逐步发展成为有源电极的趋势,电极内部被嵌入了高输入阻抗前置放大器。
2.5 适合可穿戴设备的有源干电极
近几年,面向便携可穿戴设备的EEG 信号采集有源电极系统也被报道了,有源电极系统集成了电极部分与传感后电路部分。这些有源电极系统充分考虑了头皮与传感器之间的接口阻抗模型,通过传感后电路结构改进去匹配实际的头皮与传感器之间的接口阻抗,以达到方便、准确、可靠、安全地优化EEG 的感知。常见的满足EEG 可穿戴设备的体表电极可分为以下几类[22]:适合长期佩戴的金属板电极、低成本的一次性泡沫垫电极、可吸附在头皮的金属电极(不需要束带固定)、浮动电极(需要尽量减少运动伪影噪声)、柔性电极(佩戴舒适)和微针电极(皮下)。其中,可以滑动穿过头发的柔性金属/聚合物有源电极是进行高质量电极-头皮接触最常见的形式。2015 年台湾图像与生物医学光电研究所提出了一种新型的梳状有源干电极[23],其原理图如图12 所示,该电极适合测量毛发部位的脑电图。与其他梳状电极不同,通过集成有源电路,该电极表现出更优异的性能,避免了信号衰减、相位失真并降低了共模抑制比。即使在运动状态下,它也能有效地获取头皮的EEG 信号。

图12 梳状有源干电极原理图[23]
韩国光州技术科学院课题组于2019 年在Sensors期刊发表论文,其设计了一种二线制有源干接触电极系统,该系统将手指状弹簧机械形态的干接触电极和传感后有源缓冲电路相结合,用于EEG 信号检测[24],系统基于可伸缩的干接触电极,能够调节电极与头皮的接触程度。同时,电极部分和传感后缓冲电路进行了可靠的电耦合,并能适应不均匀、多毛发的头皮并提供具有低输入电容的有效输入阻抗转换。该报道提出的有源干接触电极示意图及实物图如图13 所示,其系统包括有源电极电路和辅助电源电路两个独立的部分。电极模块为圆柱形,直径为11 mm,高度为17 mm。该有源电极将放大器、极低泄漏二极管以及12 个弹簧形状的电极集成在单个印刷电路板(Printed Circuit Board,PCB)上。实验表明,该有源干接触电极具有优良的电气特性,即较低(1.131 μVRMS)的放大器输入等效噪声、较小的输入电容等。
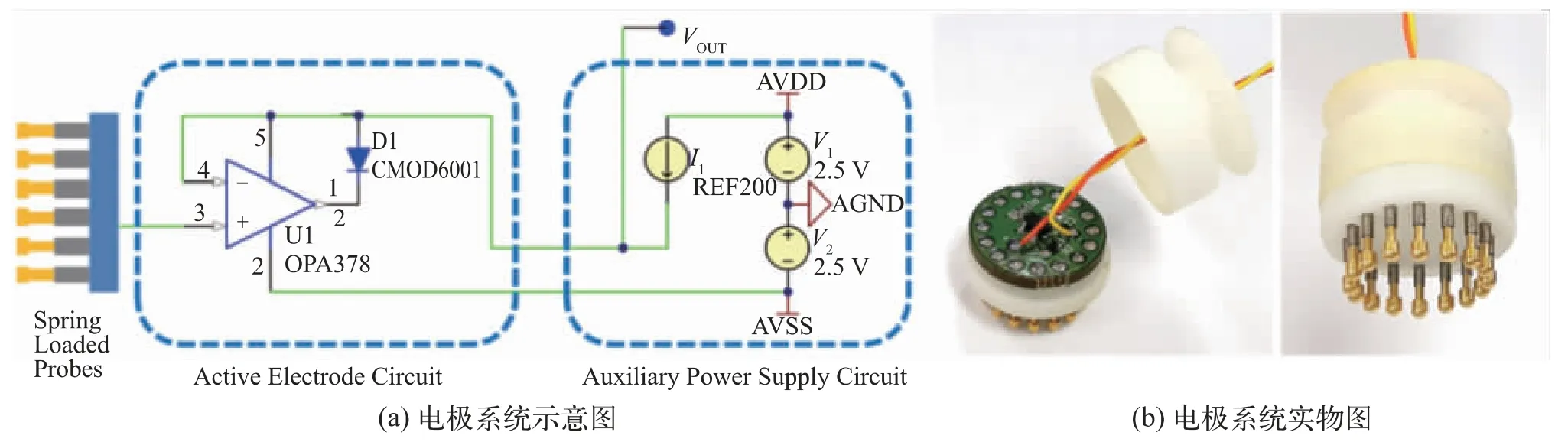
图13 有源干电极系统[24]
2021 年复旦大学基于银薄片/PDMS 导电复合材料(Electrically Conductive Composite, ECC)开发了可用于EEG 传感的柔性可伸缩有源干电极[25]。基于ECC材料的柔性可伸缩有源干电极系统如图14 所示,该课题组提出的有源干电极由柔软的衬底、电极和缓冲电路(由运算放大器和电容器组成)构成。基底采用硅树脂材料经过成型工艺制成,电极的制造则是通过在衬底上涂覆ECC 实现。此外,电路互连、元件的焊接以及与柔性印刷电路板(Flexible Printed Circuit,FPC)的连接都直接通过ECC 实现,简化了制造过程。与传统的Ag/AgCl 无源湿电极相比,该有源干电极的背景噪声与其相当,并且对电源线干扰和运动伪影的敏感性更低。该电极系统在长时间佩戴时能够提供更好的舒适性,并且能够满足高质量EEG 传感的要求。

图14 基于ECC 材料的柔性可伸缩有源干电极系统[25]
3 EEG 信号传感后调理集成芯片
通过EEG 传感器(电极)感知的EEG 信号属于低电压低频的微弱生物小信号,这些微弱的生物信号需要被放大,因此对于低噪声放大增益的要求比一般非生物信号的放大器高得多,并且它们非常容易受到环境干扰和电路输入端口与内部噪声的破坏。影响EEG质量的噪声主要包括差分输入失调电压、1/f低频闪烁噪声、非理想MOS 开关电荷注入效应引起的毛刺噪声、电路内部高斯白噪声以及其他噪声等,这些噪声需要尽可能地消除或抑制。为了得到高质量的EEG 信号,用于处理低频微电压EEG 生物放大器的芯片设计面临以下挑战:设计EEG 信号放大滤波电路时,由于EEG 信号容易受到50 Hz/60 Hz 的工频交流室电的共模噪声以及差分放大器输入共模噪声干扰,因此应采用高共模抑制比(Common Mode Rejection Ratio,CMRR)的电路设计方法予以抑制;对EEG 的带内噪声(尤其是低频闪烁1/f噪声以及近似直流的电极失调噪声),应进行消除或抑制;此外,生物放大器的输入阻抗需要与传感器输出阻抗匹配设计,以容忍电极输出阻抗失配,这要求放大器的输入阻抗足够高;同时生物放大器芯片的功耗应尽可能低,以适用于便携式微型集成设备或系统。除了EEG 信号放大器对采集的信号进行放大滤波等操作外,EEG 信号传感后调理芯片通常还包括将EEG 模拟信号到数字信号量化转换处理的生物模/ 数转换器(Biological Analog/Digital Converter,bioADC)和负责数字EEG 无线传输的无线射频发送电路。随着AI 技术的快速发展,包含特征提取、特征分类等模式识别/人工智能硬件引擎的EEG智能电路逐步被嵌入到EEG 信号检测芯片中。
3.1 传感器与头皮之间的电气模型
电极与头皮的接触方式以及使用的电极材料决定了电极与头皮之间的阻抗网络、电极极化电压以及固定在头皮上的使用舒适度。传感器与头皮之间的阻抗网络包括电阻与电容,电极偏移电压是电极之间的极化电压差,其取决于两个电极的电化学不平衡,Ag/AgCl 电极因其较低的电极极化电压得到了广泛应用。几种EEG 电极与头皮之间的电气模型如图15 所示,分别给出了湿电极、干接触电极与无接触电极的电气接口模型[26]。对于传感后调理芯片的设计,一方面需要考虑所使用的电极类型以及建立对应的电极与头皮之间的电气模型,并且进行接口模型与传感后调理芯片的阻抗匹配、极化电压特征控制与噪声消除/抑制等传感器与传感后电路的接口设计;另一方面需要借助传感后电路结构的创新进一步改善EEG 信号的检测性能。
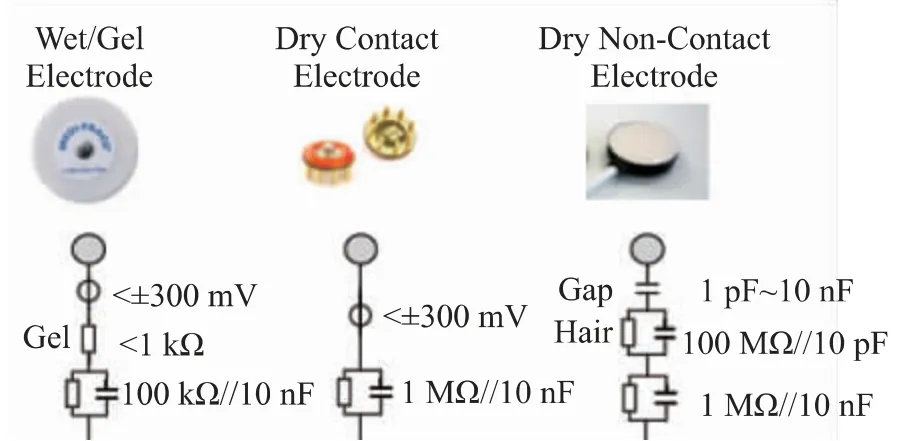
图15 几种EEG 电极与头皮之间的电气模型[26]
3.2 交流耦合的反相放大器
由于系统对噪声和元件面积的限制,带有电阻反馈的生物放大器很少使用,而带电容反馈的交流耦合反相放大器解决了这两个问题[27],并且交流耦合反相放大器表现出多设计指标平衡的模拟性能,因此被广泛应用于可穿戴EEG 和植入式EEG 医疗芯片仪器[28-29]。交流耦合反相放大器基本结构[30]如图16 所示。通过优化交流核心放大器[31-33],可以进一步降低交流电容耦合反相放大器的能耗。2015 年爱因霍芬理工大学报道的基于0.18 μm CMOS 工艺的生物放大器实现了0.34 μVRMS的等效输入噪声(带宽范围0.7~182 Hz),1.74 的噪声效率因子(Noise Efficiency Factor,NEF),通过多供电电源管理电路与电流复用技术达到1.56 μW 的能耗[34],交流电容耦合放大器的一个挑战是其输入阻抗和噪声之间的参数权衡。2007 年Medtronic Neuro Technology 公司、麻省理工学院与ADI 公司报道了基于0.8 μm CMOS 工艺、带多个环路的交流耦合放大器结构[35],其结构如图17 所示。该交流耦合放大器与输入耦合电容Ci有关,报道的低噪声斩波放大器实现了低频闪烁1/f噪声与爆米花噪声的消除(此外,电极偏移电压可通过高通滤波器进行消除),达到0.98 μVRMS的等效输入噪声(带宽范围0.05~100 Hz),能耗是2.0 μW(1.8 V 供电电压)。

图16 交流耦合反相放大器结构[30]
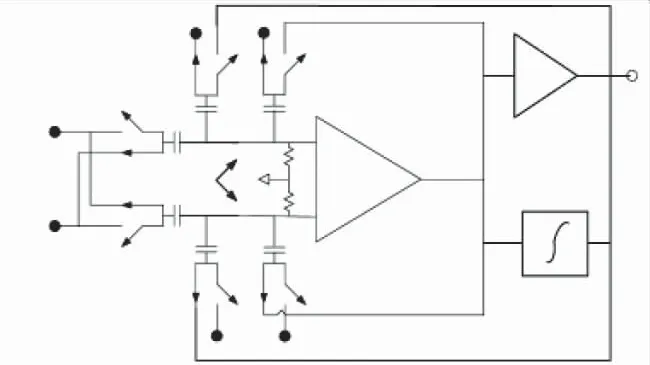
图17 交流耦合神经电放大器结构[35]
3.3 电容反馈的非反相放大器
电容反馈的非反相放大器可以利用电容反馈而不是电阻反馈来减轻电阻器噪声,基于电容反馈的非反相放大器结构如图18 所示[27]。2014 年欧洲微电子中心(IMEC)联合代尔夫特理工大学与松下电器公司报道了基于0.18 μm CMOS 工艺、电容反馈的非反相放大器结构。电容反馈的非反相放大器电路结构如图19 所示,其展示了带输出纹波抑制的斩波去噪电容反馈放大器电路结构。该电路实现了1.75 μVRMS等效输入噪声(带宽范围0.5~100Hz),84dB 的CMRR,700μW的能耗(1.8 V 供电电压),借助直流伺服回路DSL(DC Servo-Loop)可以消除±250 mV 的电极偏移电压[36]。
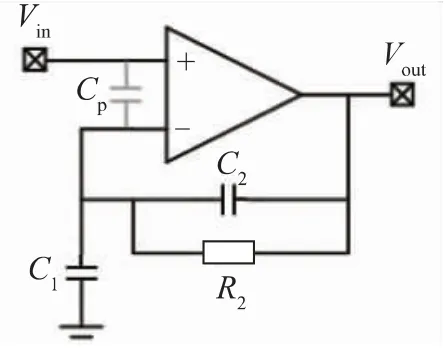
图18 电容反馈非反相放大器[27]
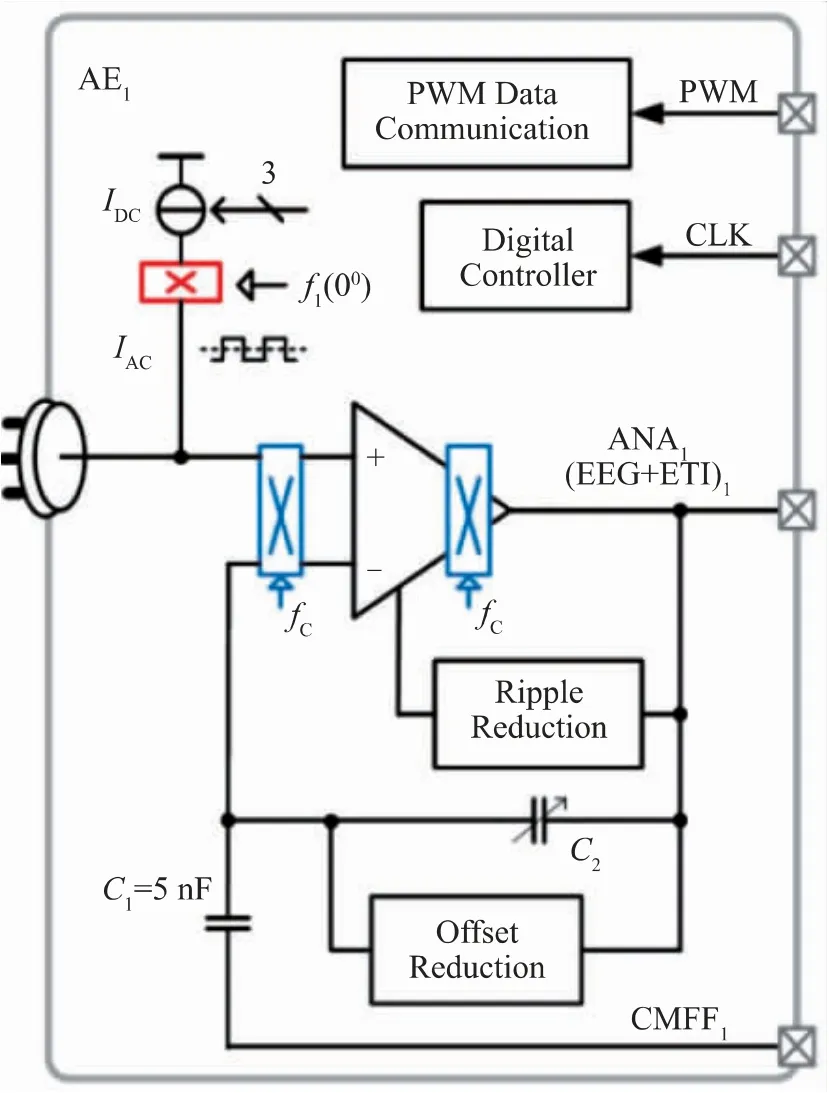
图19 电容反馈的非反相放大器电路结构[36]
3.4 直流耦合的放大器
交流耦合放大器在对电极偏移电压进行抑制的同时,也阻断了极低频EEG 信号,从而引起EEG 信号失真。由于极低频(小于1 Hz)EEG 信号可能被用于监测各种认知任务(比如语言)和感觉运动任务(比如运动准备和期望)[37],因此交流耦合放大器不适用于测量非常慢的EEG 信号检测应用场景[38]。图20 展示了直流耦合放大器基本结构[26],与交流耦合放大器相比,直流耦合放大器能保留极低频信号,但其增益将受到由电极偏移电压和微伏级EEG 信号确定的大动态范围(大于90 dB)的限制。此外,通常需要采用高分辨率ADC(大于16 位)来满足噪声规范,从而导致多通道EEG 信号检测芯片系统的功耗显著增加。直流耦合放大器可以借助多种不同的结构实现,比如电流平衡放大器[39-40]、电流反馈放大器[41-42]、3 个运算放大器和电容耦合斩波放大器[35,43]。
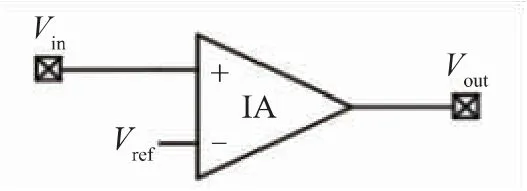
图20 直流耦合放大器基本结构[26]
2010 年代尔夫特理工大学基于65 nm CMOS 工艺,报道了带多种反馈环路的直流电容耦合斩波放大器[43],直流耦合斩波放大器结构如图21 所示。该设计基于正反馈环路以提高放大器输入阻抗,使用纹波抑制环路以消除放大器输出端的纹波噪声。放大器实现了1 μV 的电极偏移电压,134 dB 的CMRR,120 dB 的电源抑制比(Power Supply Rejection Ratio, PSRR),0.16%的增益精度以及3.1 的NEF。
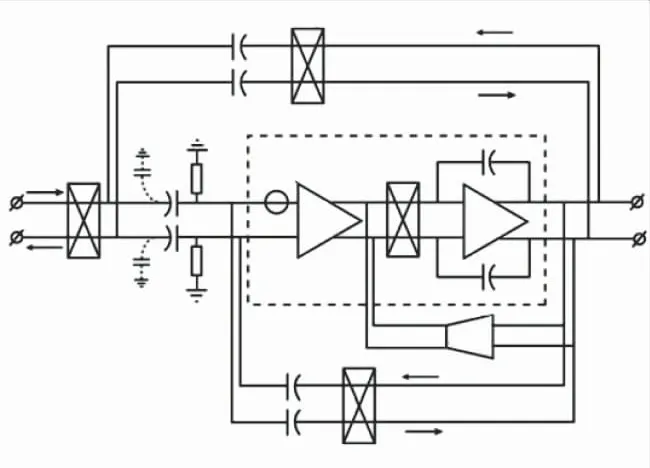
图21 直流耦合斩波放大器结构[43]
另一种直流耦合放大器即“功能上”的直流耦合放大器[44-45],可以结合交流耦合和直流耦合放大器的优点,即在低能耗(小于1 μW)下具有非常大的电极偏移容忍度(±350 mV),同时仍然保持直流耦合的特点。借助DSL 反馈的直流耦合放大器如图22 所示,通过基于电压-电压反馈的直流伺服回路DSL 来跟踪放大器输出处的偏移,并通过驱动放大器的反相输入来消除电极偏移电压。因此,交流耦合EEG 在放大器的输出端可用,而直流和极低频EEG 信号在具有单位增益的直流伺服回路的输出端也可用,即“功能性”的直流耦合电路可以通过组合交流和直流输出来实现。

图22 借助DSL 反馈的直流耦合放大器[26]
3.5 斩波技术消除噪声
除了高斯热噪声外,低频1/f闪烁噪声通常是几千或几百赫兹以下的低频生物放大器的主要噪声源,该1/f噪声消除对于EEG 的有效检测非常关键。传统上,可以通过增大输入晶体管的尺寸来降低低频闪烁1/f噪声,但是使用较大晶体管会使芯片物理版图面积增大,而且还需要依赖寄生电容来降低输入阻抗。动态电路去噪技术能以能耗和面积效率较高的方式消除或抑制放大器的低频闪烁1/f噪声和固有电极偏移电压。2 种著名的动态电路去噪声技术包括自动调零(Auto-Zero,AZ)去噪技术和斩波去噪技术[46]。AZ 技术分2 个阶段运行,噪声和偏移量在第一阶段进行采样和存储,因此它们将在第二阶段进行补偿。AZ 技术的缺点是高频噪声会被折叠回来并分布在原来的信号带宽上,因此AZ 技术不适合微伏级的EEG 信号低噪声放大器使用。而斩波技术通过周期性地交换放大器的输入,斩波开关连续工作,把低频闪烁1/f噪声调制到斩波频率位置,而有用的EEG 信号经过两次斩波调制又被解调回到原来信息带宽,并且斩波技术不存在AZ 技术的噪声折叠回原来信号带宽的问题,因此,对于检测微伏级的EEG 信号,斩波技术对于EEG 低噪声放大器设计更有效(如图23 所示)。
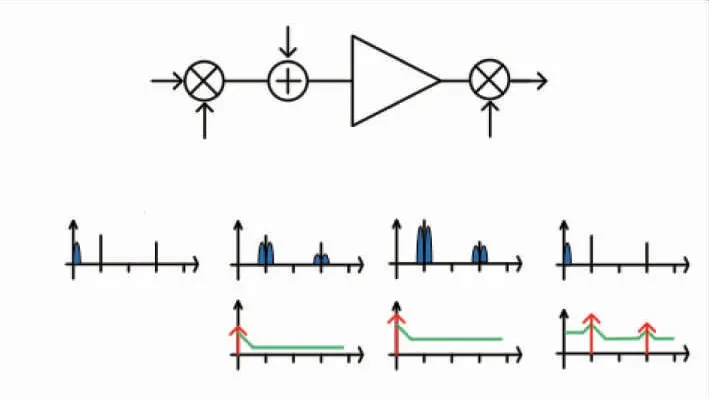
图23 斩波Chopping 调制/解调实现有用EEG 信号与低频闪烁1/f 噪声在频域的分离[46]
3.6 斩波稳定交流电容耦合放大器
2016 年丹麦奥胡斯大学集成电路与器件课题组基于180 nm CMOS 工艺,报道了一种用于EEG 信号采集的低功耗放大器设计[47],该报道关注于实现放大器的高输入阻抗和低功耗的设计指标。放大器结构图如图24 所示,该报道提出的EEG 信号放大器由2 部分构成,分别为有源电极和读出电路,其中读出电路主要由斩波稳定放大器(Chopping Stabilization Amplifier,CSA)、低通滤波器(Low Pass Filter,LPF)以及可编程增益放大器(Programmable Gain Amplifier,PGA)电路模块构成,同时使用了输入阻抗提升回路以增加CSA 的输入阻抗。经过测试,该报道的放大器的输入阻抗分别增大到163 GΩ(1 Hz 时)与16.3 GΩ(10 Hz 时)。同时,该报道的设计通过降低电压电源等技术降低了能耗开销,测试结果表明该低功耗放大器设计能耗为0.92 μW(0.8 V 供电电压时),等效输入噪声为1.7 μVRMS(带宽范围0.5~100 Hz)等。2017 年山东师范大学基于180 nm CMOS 工艺,报道了一款低频微弱EEG 信号低噪声斩波稳定放大芯片[48],该斩波放大器应用了斩波消除噪声技术、输入阻抗增大环路技术、单级放大核的中频稳定增益环路技术、放大器的输出纹波电压抑制环路技术、非理想斩波开关注入引起的毛刺噪声消除技术等,以消除低频1/f噪声、差分放大器输入失调电压以及非理想斩波开关切换引起的毛刺等噪声,测试结果表明该芯片能够满足V 级EEG 信号的有效放大,实现4216~11220 倍的EEG 电压放大增益,0.8 μVRMS等效输入噪声(带宽范围100 Hz以内),单通道放大器能耗是8.1 μW(1.8 V 供电电压)。
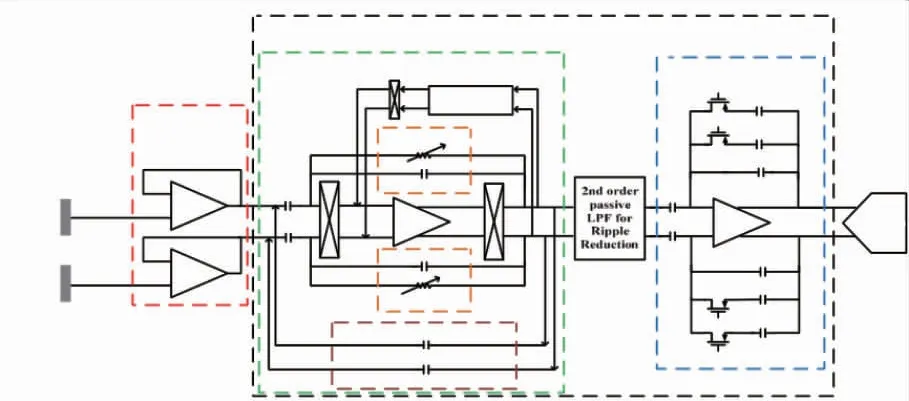
图24 放大器结构图[47]
3.7 自带前置低噪声放大器的EEG 数字化ADC 芯片
2016 年约翰·霍普金斯大学医学院课题组基于180 nm CMOS 工艺,报道了一种具有4 通道bioADC的植入式双向神经接口芯片[49]。bioADC 双向神经接口IC 设计结构如图25 所示。相比于传统的生物信号检测芯片系统,该bioADC 能够直接将毫伏级的神经电压转换为数字信号,达到9.4 bit 等效量化位数(Effective Number Of Bit,ENOB),信噪失真比(Signal Noise Distortion Ratio,SNDR)为58.5 dB,无杂散动态范围(Spurious Free Dynamic Range,SFDR)为74 dB,等效输入噪声1.0 μVRMS(带宽范围0.25~200 Hz),能耗是5.5 μW,CMRR 是97 dB,NEF 是4.67。

图25 bioADC 双向神经接口IC 设计结构[49]
2019 年丹麦奥胡斯大学基于180 nm CMOS 工艺,报道了一种低功耗高输入阻抗模拟前端专用ASIC集成电路,该电路结构包括生物放大器和神经信号专用ADC,用于连续采集EEG 信号[50]。低功耗高输入阻抗模拟前端专用ASIC 芯片如图26 所示,其展示了模拟前端电路组成结构,包括生物放大器、可编程增益放大器PGA 与神经信号专用ADC 模块。其设计的放大器利用DC 直流耦合的单位增益有源电极来增加放大器的输入阻抗,通过使用高开环增益的缓冲器,降低了信号电极和参考电极之间的不匹配度,生物放大器使用跨导右腿驱动技术,CMRR 可达到108 dB,并且使用MOS 晶体管工作于亚阈值区,可以降低电源电压以达到低压低功耗设计,测试结果表明该电路能耗降低到3.7 μW(ADC 转换速率是20 kS/s),等效输入噪声为1.5 μVRMS(带宽范围0.5~1.2 kHz)。
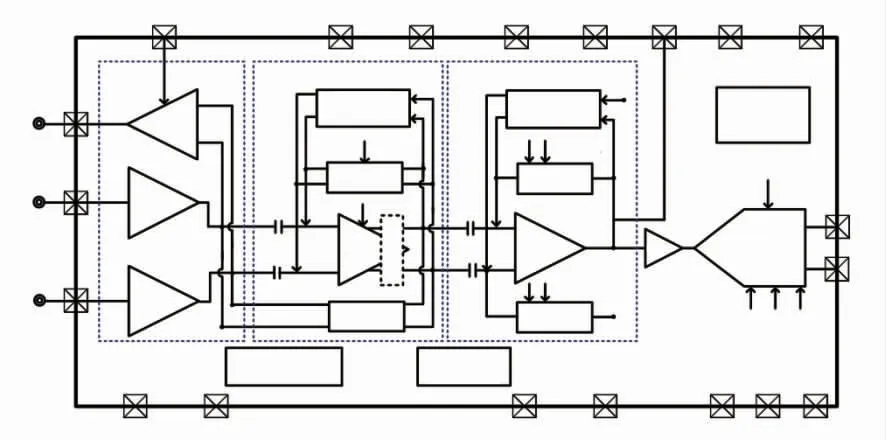
图26 低功耗高输入阻抗模拟前端专用ASIC 芯片[50]
3.8 带无线通信功能的EEG 调理芯片
在EEG 信号通过电极传感后,调理芯片除了对信号进行一系列处理外,还要对信号进行传输。在过去对EEG 检测设备的研究中,为了更好的便携性和舒适性,人们对小型可穿戴医疗设备进行了设计研究,其中EEG 信号无线射频技术给人们使用这些设备带来了便利。比如,2017 年约克大学设计了基于超带宽(Ultra Wide Bandwidth,UWB)(3.1~10.6 GHz)技术的神经电信号低功耗蓝牙(Bluetooth Low Energy,BLE)无线发射器[51]。2019 年加拿大约克大学电气工程与计算机科学系课题组基于BLE 5.0 Transceiver 射频收发芯片等第三方元器件,构建了无线神经电收发系统[52]。2020 年IMEC 报道了一种用于多模式生命体征监测的769 μW 电池供电片上芯片系统(System on Chip,SoC)芯片[53],一体式电池供电低功耗SoC 的架构如图27 所示,其展示了提出的片上集成SoC 系统架构,包括专用读数、电源管理电路、数字信号处理和无线通信都集成在一个芯片中。这种高集成度可以实现系统微型化,尽量减少芯片外的部件数量,从而降低设计成本,提高穿戴舒适性和整体设计的信号完整性。测试结果表明该报道的放大器通道能耗为19.2 μW,放大器增益为40/80/160 倍等[53]。
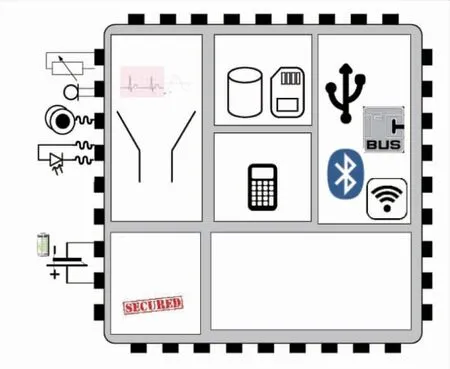
图27 一体式电池供电低功耗SoC 架构[53]
3.9 具有特征识别与归类功能的AI-EEG 芯片
2013 年IMEC 联合麻省理工学院基于180 nm 1P6M CMOS 工艺,报道了一种EEG 连续检测和记录患者特定癫痫病发作的检测SoC 芯片[54],EEG 信号检测、特征识别电路如图28 所示,该芯片集成了8 通道高动态模拟前端(Analog Front End,AFE)、具备特征向量识别功能的分类处理器和一个64 kB 的静态随机存取存储器(SRAM)。每个通道由斩波稳定电容耦合放大器和模拟信号处理单元组成,并且斩波稳定电容耦合放大器和模拟信号处理单元使用的所有电容都集成在该SoC 上。测试结果表明,该SoC 芯片等效输入噪声0.91 μVRMS(带宽范围0.5~100 Hz),NEF 是5.1。

图28 EEG 检测、特征识别电路[54]
4 结论
本文针对EEG 传感器与传感后调理芯片进行了综述。除了传统的湿电极外,传感器还包括干电极、MEMS 电极、柔性材料电极、梳妆结构电极、集成了传感后调理电路的有源电极等。电极未来的发展趋势是不同技术路线的互相融合,比如适合可穿戴设备的有源电极可以是不同材料、工艺与结构制作的干电极,并且可能采用与头皮接触性能更好的梳妆结构。对于EEG 信号检测电极,其检测安全性、灵敏度、可靠度、电极与头皮的接触阻抗网络、电极极化电压需要根据EEG 具体应用场景进行折中选择与优化。传感后调理电路主要包括微伏级EEG 信号低噪声放大器、模/数转换电路ADC 和无线射频电路。最为关键的放大器结构主要有直流耦合放大器结构,比如基于斩波稳定技术的直流耦合放大器,以及交流耦合放大器等结构。放大器通过电路结构的创新与电路具体指标的改善,实现低噪声生物放大器与前置传感器的联合优化设计,以改善放大器与传感器之间的接口阻抗匹配,降低放大器的等效输入噪声,消除或抑制电极失调电压,降低CMRR、PSRR 和功耗,抑制输出纹波,调节低频带宽等关键参数。随着未来人工智能技术的发展,针对EEG 具体应用场景的具有特征识别与归类功能的智能EEG 信号检测芯片也在不断涌现。
