接受皮下特异性免疫治疗的变应性鼻炎患者新型冠状病毒疫苗接种管理—复旦EENT 医院经验△
2022-05-29刘娟冯仙顾瑜蓉李厚勇余洪猛王德辉李华斌
刘娟 冯仙 顾瑜蓉 李厚勇 余洪猛 王德辉 李华斌
(复旦大学附属眼耳鼻喉科医院耳鼻喉科 上海 200031)
新型冠状病毒(SARS-CoV-2,简称新冠病毒;又称2019-nCoV)引发的疾病称为新型冠状病毒肺炎(corona-virus disease 2019,COVID-19;简称新冠肺炎),会引起严重急性呼吸综合征(severe acute respiratory syndrome,SARS), 威 胁 人 类 健 康 和公共安全[1]。尽管我国的疫情整体趋于平稳,但COVID-19 仍在全球高位流行,且病毒变异加快,我国外防输入的压力持续增大,国内疫情也时有多点扩散,疫情传播链不断延长,因此,我国的疫情防控形势依然严峻复杂。人类对该病毒普遍易感,且感染后缺乏有效的治疗手段,接种新冠病毒疫苗(简称新冠疫苗)可以有效预防新冠病毒感染,减少重症感染的概率,降低死亡率,是主动构建群体免疫、控制疫情的重要策略。
变应性鼻炎(allergic rhinitis,AR)是耳鼻喉科的常见病和慢性病之一,我国大陆地区的人口患病率为4%~38%[2],且近年来其患病率仍在明显上升[3]。临床主要表现为鼻痒、喷嚏、流清涕、鼻塞等症状,严重者可并发鼻窦炎、中耳炎、哮喘等多种疾病,严重影响人们的生活质量。AR强调防治结合、四位一体的原则,即环境控制、药物治疗、免疫治疗和健康教育。其中免疫治疗即变应原特异性免疫治疗(allergen-specific immunotherapy,AIT),是目前唯一可能影响疾病自然进程的治疗措施,其发展已有100多年历史[4-7]。有研究[3]证实,免疫治疗对AR同时具有近期和远期疗效,是AR的一线治疗方式。皮下特异性免疫治疗(subcutaneous immunotherapy,SCIT)是经典的治疗方式,分为起始治疗阶段(剂量累加阶段)和维持治疗阶段(剂量维持阶段)。世界卫生组织推荐免疫治疗维持3~5年,临床推荐用药至少2年以上。
由于AR免疫治疗的疗程较长,而新冠疫苗也需及时接种,这2种疫苗的接种需要妥善处理。此外,很多AR患者和少部分医务人员对AR患者接种新冠疫苗也有所顾虑。因此,当前亟需对接受SCIT的AR患者接种新冠疫苗给予具体的临床操作建议。本文通过统计正在我科接受SCIT的AR患者接种新冠疫苗情况及接种后对SCIT的影响,总结接受SCIT的AR患者接种新冠疫苗的管理经验,现报告如下。
1 资料与方法
1.1 临床资料 截止2021年11月30日,共计421例AR患者正在我科接受SCIT,其中最早开始治疗的时间是2017年4月7日。所有患者均符合文献[3]的诊断标准,均为中重度AR。患者皮肤点刺试验或血清特异性免疫球蛋白E(immunoglobulin E,IgE)检测明确诊断变应原主要为尘螨。患者有特异性免疫治疗的需求,符合免疫治疗的适应证,无免疫治疗的禁忌证。
1.2 免疫治疗方案 遵循《变应性鼻炎皮下免疫治疗的临床操作规范》,使用丹麦ALK-Abello公司生产的安脱达即屋尘螨变应原制剂进行常规SCIT。起始治疗阶段:于上臂远端三分之一的外侧皮下注射,一般每1~2周注射1次,左右手交替注射,通常需要15次。从最低浓度、最低剂量开始,1号瓶(浓度100 SQ-U/mL)、2号瓶(浓度1 000 SQ-U/mL)、3号瓶(浓度10 000 SQ-U/mL)的治疗剂量依次按0.2、0.4、0.8 mL递增。4号瓶(浓度100 000 SQ-U/mL)治疗剂量依次为0.1、0.2、0.4、0.6、0.8、1.0 mL。维持治疗阶段:起始治疗阶段达到的最大耐受剂量即维持剂量,一般为4号瓶1.0 mL。达到维持剂量后,先隔2周注射1次,再隔4周注射1次,最后间隔4~8周维持注射治疗,治疗时间持续至少2年以上。如果超过2次注射之间的时间间隔,按照以下方案调整注射剂量(表1、2)。

表1 SCIT起始阶段剂量调整方案
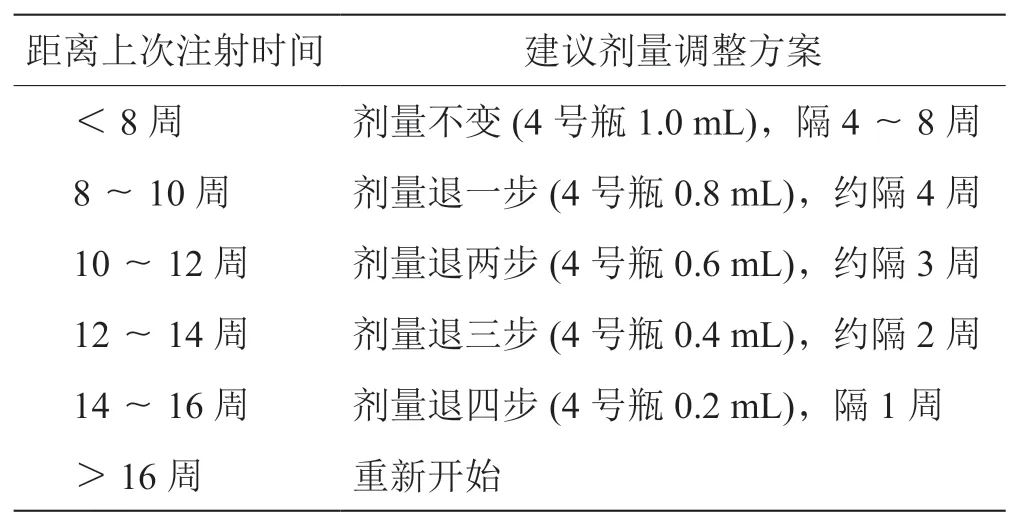
表2 SCIT维持阶段剂量调整方案
1.3 新冠疫苗接种情况调查 电话询问和(或)在进行免疫治疗时当面询问患者,记录是否接种新冠疫苗、接种新冠疫苗时的免疫治疗阶段、接种后免疫治疗剂量是否调整、接种后是否有不良反应、接种后鼻炎是否加重等。若患者未接种新冠疫苗,询问未接种的原因。
1.4 统计学处理 应用SPSS 22.0统计软件对数据进行统计学处理,采用χ2检验进行统计学分析,以P<0.05为差异有统计学意义。
2 结果
2.1 患者基本资料 421例AR患者的基本资料详见表3。本文中的全程接种是指接种2针灭活疫苗或1针腺病毒载体疫苗,不包含加强针。本文统计时加强针接种刚开始开展,本研究中接种加强针的患者极少,因此未统计加强针的接种情况。

表3 421例AR患者的基本资料[n(%), N=421]
2.2 接种新冠疫苗患者的资料分析 排除6例新冠疫苗接种情况不详的患者,将其余415例按性别、是否伴有哮喘和免疫治疗所处的阶段进行分组,分别进行卡方检验。结果显示:新冠疫苗接种率在性别和患者免疫治疗所处的阶段分组之间差异均无统计学意义(P值均>0.05);而伴有哮喘的患者其新冠疫苗接种率明显低于不伴哮喘的患者(P<0.05,表4)。由于统计资料时,新冠疫苗的接种还未广泛在儿童患者中推广,此文暂未对年龄进行分组统计学分析。
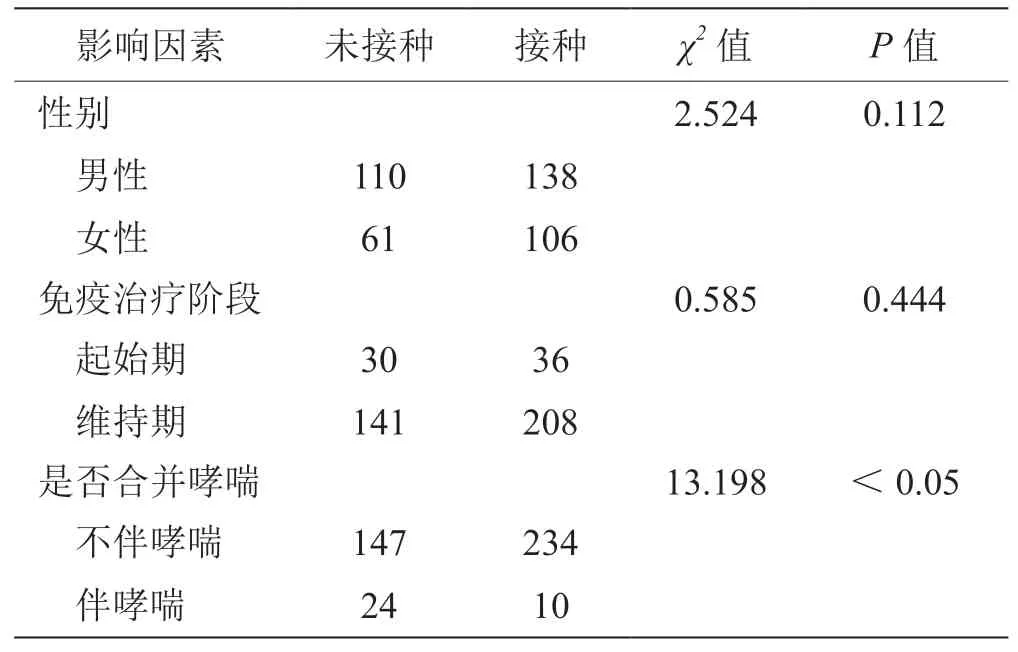
表4 接种新冠疫苗的影响因素(N=415)
244例患者共接种4种类型的新冠疫苗(图1)。北京科兴中维生物技术有限公司的新冠病毒灭活疫苗(商品名:克尔来福)117例(48%)、国药集团中国生物所属北京生物制品研究所(BIBP)新冠灭活疫苗112例(46%)、武汉生物制品研究所(WIBP)新冠灭活疫苗6例(2%)、康希诺生物股份公司/军事医学研究院研发的腺病毒载体疫苗(商品名:克威莎TM)10例(4%),其中有1例患者第1针接种克尔来福,接种第2针时该疫苗暂时缺货,采用了WIBP同类型疫苗混合接种。

图1 244例患者新冠疫苗接种种类及占比
244例接种新冠疫苗的患者中,40例在免疫治疗前完成接种,5例在免疫治疗起始阶段接种,199例在免疫治疗维持阶段接种。
2.3 接种新冠疫苗患者出现鼻炎加重和不良反应情况分析 209例全程接种新冠疫苗的患者中,共有7例认为接种新冠疫苗后鼻炎加重。将这些患者按性别、年龄、是否伴哮喘和患者免疫治疗所处阶段进行分组,统计学分析显示各分组间差异均无统计学意义(P值均>0.05),详见表5。

表5 完成新冠疫苗全程接种后鼻炎加重的影响因素(N=209)
209例全程接种新冠疫苗的患者中,23例出现不良反应,发生率为11%。全身不良反应20例,主要表现为低热、头痛、乏力、犯困等,其中5例鼻炎加重;局部不良反应9例,主要表现为注射部位疼痛、肿块或注射部位以外的湿疹。将这些患者按性别、年龄、是否伴哮喘和患者免疫治疗所处阶段进行分组,统计学分析显示各分组间差异均无统计学意义(P值均>0.05),详见表6。
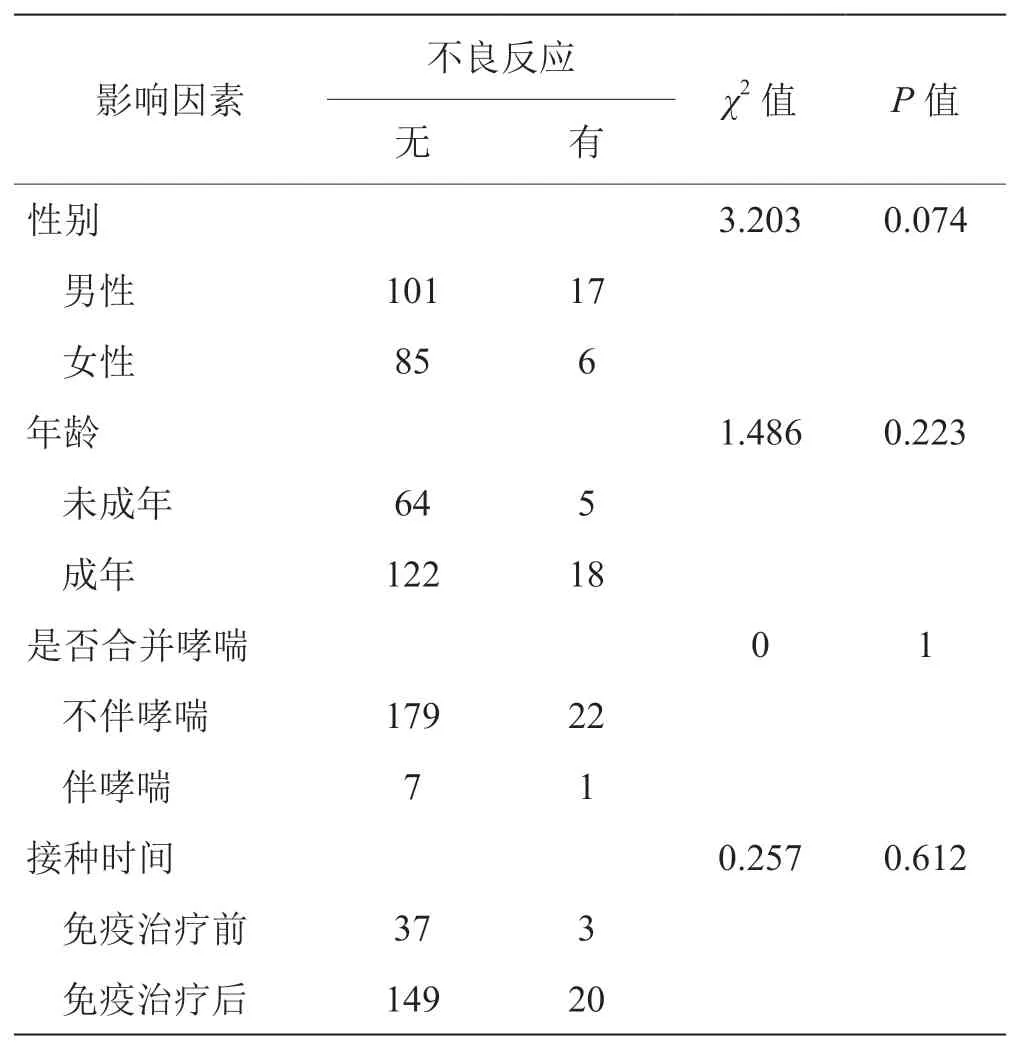
表6 完成新冠疫苗全程接种后不良反应的影响因素(N=209)
2.4 接种新冠疫苗对SCIT的影响及调整策略 完成新冠疫苗全程接种的患者共209例,其中29例由于接种新冠疫苗后要求间隔2周以上才能接种其他疫苗,导致免疫治疗的间隔时间延长,需要调整免疫剂量或重新开始SCIT。5例在起始治疗阶段接种新冠疫苗的患者均需要重新开始SCIT。24例在维持治疗阶段接种新冠疫苗的患者中,12例维持剂量从1.0 mL降至0.8 mL,并在随后的4周时恢复到最高剂量1.0mL;9例维持剂量从1.0 mL降至0.6 mL,在随后的7周时恢复到最高剂量1.0 mL;其余3例在接种新冠疫苗前因其他原因维持剂量不到1.0 mL,且由于接种新冠疫苗后间隔时间延长,SCIT的剂量有较大幅度退步(2例调整到0.4 mL,1例调整到0.1 mL),目前仍在治疗中,剂量均未达到最高维持剂量1.0 mL。
按性别、是否伴哮喘和接种时患者免疫治疗所处阶段进行分组,统计学分析显示:需要进行免疫剂量调整的患者比例在性别和是否伴哮喘分组之间差异均无统计学意义(P值均>0.05);而在年龄分组和患者免疫治疗所处阶段分组之间差异均有统计学意义(P值均<0.05),未成年患者接种新冠疫苗后需要调整免疫剂量的比例明显高于成年患者,免疫治疗阶段完成新冠疫苗接种的患者需要调整免疫剂量的比例明显高于免疫治疗前(表8)。
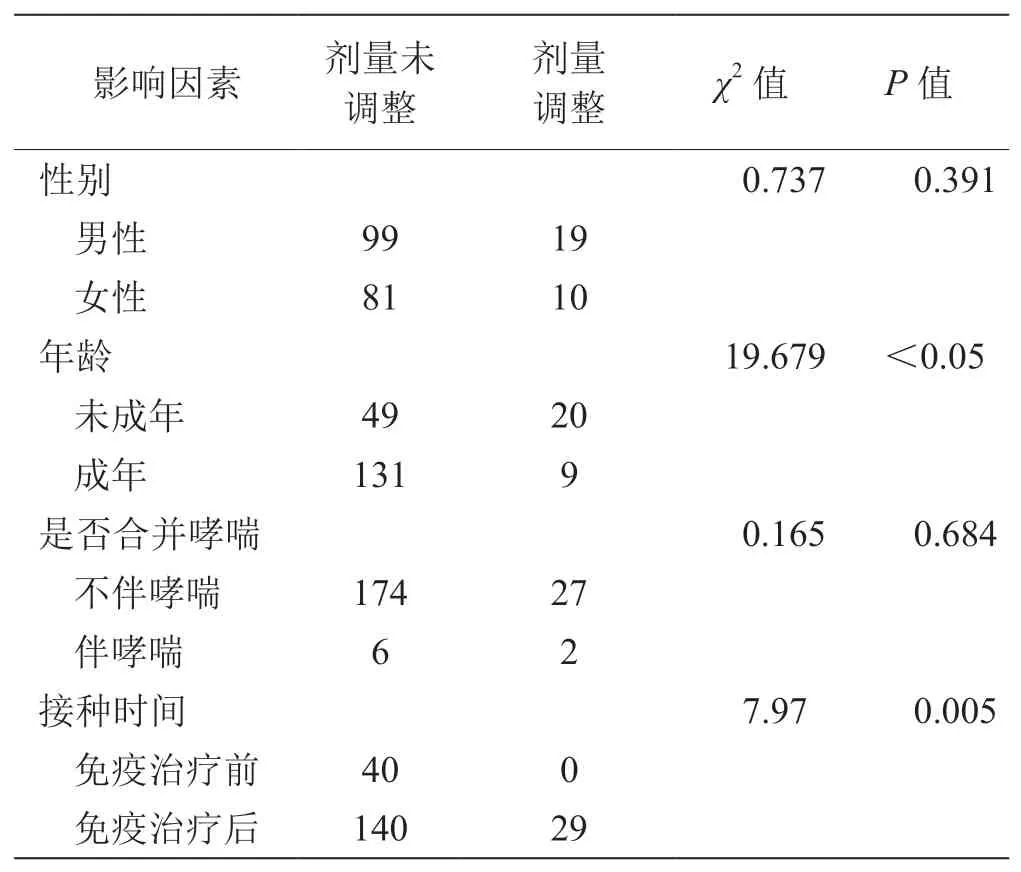
表8 完成新冠疫苗全程接种后免疫治疗剂量调整的影响因素(N=209)
按接种新冠疫苗后患者是否出现不良反应进行分组,统计学分析显示:接种新冠疫苗后发生不良反应的患者出现鼻炎加重的比例明显高于无不良反应的患者,详见表7。进一步将处于治疗阶段接种新冠疫苗的169例患者按起始和维持阶段分组,卡方检验显示,起始阶段接种新冠疫苗需要调整免疫治疗剂量的比例为100%,明显高于维持阶段需要调整免疫治疗剂量的比例,差异具有统计学意义(表9)。

表7 接种新冠疫苗后是否出现不良反应与鼻炎加重之间的关系(N=209)
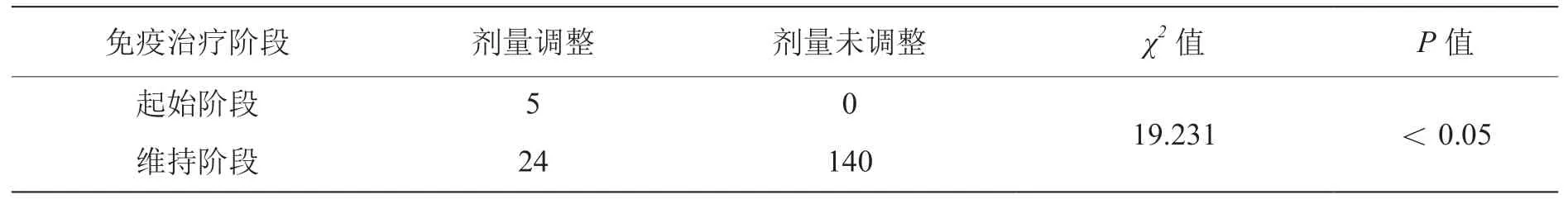
表9 剂量调整和接种新冠疫苗时的免疫治疗阶段之间的关系(N=169)
2.5 患者未接种新冠疫苗的原因 171例未接种新冠疫苗的患者,原因按比例从高到低依次为:欲择期接种、不愿意接种、没有强制接种、迟疑不决、自认为过敏体质不适合接种、自认为合并哮喘不适合接种、自认为身体虚弱不宜接种、认为新冠疫苗不安全、怀孕、接种点医师认为不适合接种和自认为做好防护不会被传染(图2)。

图2 未接种新冠疫苗的原因
3 讨论
AR是特异性个体接触了环境中的过敏原后,由过敏原特异性IgE介导的Th2型鼻黏膜慢性非感染性炎症。SARS-CoV-2感染导致新冠肺炎重症患者的免疫学特征是免疫过度激化引发“细胞因子风暴”[8-9]。目前仅有少量数据显示AR和新冠病毒感染风险之间的关系,而且这些数据大多间接来源于变应性哮喘和新冠病毒感染风险之间的研究。而部分研究[10-14]认为变应性疾病不是新冠病毒感染或发展为重症新冠肺炎的危险因素。有研究显示,变应性疾病患者可以抵抗重症新冠肺炎,其可能机制包括:降低了病毒侵入人体的受体表达水平;慢性2型炎症;AR患者较年轻或者无全身性疾病,对治疗有较高的依从性,以及长期使用喷鼻或吸入激素[15]。血管紧张素转换酶2(angiotensin-converting enzyme 2,ACE2)是新冠病毒入侵人体的受体。美国威斯康星大学医学与公共卫生学院的研究发现,AR与支气管哮喘患者气道上皮细胞中ACE2表达水平下降,这项研究从侧面验证了AR与支气管哮喘患者不易感染新冠肺炎[13-14,16]。但是韩国的一项大样本数据研究却得出了相反的结论,他们认为呼吸道变应性疾病是新冠病毒感染或发展为重症新冠肺炎的危险因素,这些患者感染新冠病毒后的致死率、重症监护室(ICU)入住率、无创通气使用率和住院天数均会增加[17]。此外,美国疾病控制与预防中心也认为中重度哮喘可能是感染新冠肺炎的高危因素。新冠病毒会严重影响患者的呼吸系统,可能诱发哮喘的急性发作,甚至诱发肺炎和急性呼吸道疾病;因此,目前还需要更多的研究来探讨变应性疾病与新冠病毒感染风险之间的相关性。我们认为,无论变应性疾病是否是新冠病毒感染的保护因素,鉴于其传染性强、传播速度快、感染后疾病严重和病死率高的特征,建议变应性疾病患者要始终做好防护,在症状控制良好时接种新冠疫苗。在2021年底,我国国务院联防联控机制已将疫苗接种目标人群由12岁以上调整为3岁以上。为了更好地指导AR患儿接种新冠疫苗,李华斌等[18]制订了儿童AR患者接种新冠疫苗的专家共识。在我科进行SCIT的AR患者,在症状控制良好的状况下,我们都建议尽早接种新冠疫苗。本研究中,正在进行SCIT的AR患者其新冠疫苗接种率为58%,远低于同期上海市人群新冠疫苗的接种率87.7%[19]。统计结果显示,患者性别和SCIT所处阶段与新冠疫苗的接种率之间没有明显关系,仅伴有哮喘的患者接种率明显低于不伴哮喘的患者(P<0.05)。不接种新冠疫苗的原因中,有接近一半的患者表示欲择期接种,20%表示不愿意接种,18%认为自己的体质不适合接种(自认为过敏体质不适合接种、自认为合并哮喘不适合接种、自认为身体虚弱不宜接种),11%表示没有被强制要求接种,仅有极少数患者认为疫苗不安全或没有接种的必要。诚然,AR患者不接种新冠疫苗的原因可能不止一种,本文仅列出患者提供的最主要原因,其中18%的患者明确表示因为体质因素不接种新冠疫苗,其他患者给出的原因或许与过敏有间接关系。
AR并非新冠疫苗接种的禁忌证。AR的常见变应原是吸入性的,包括常年性变应原(尘螨、蟑螂、动物皮屑等)和季节性变应原(花粉和部分真菌等)。《新冠病毒疫苗接种技术指南(第一版)》[20]中提到2条与“过敏”有关的禁忌证:①对疫苗的活性成分、非活性成分、生产工艺中使用的物质过敏者,或以前接种同类疫苗时出现过敏者;②既往发生过疫苗严重过敏反应者(如急性过敏反应、血管神经性水肿、呼吸困难等)。AR的变应原和疫苗成分没有直接相关性,若患者既往疫苗接种未发生过严重过敏反应,则所谓的过敏体质不是接种新冠疫苗的禁忌证。但AR患者在接种疫苗时需要保持良好的健康状况,建议避开患者过敏症状的发作期;如果在发作期,可以使用药物控制症状,待症状缓解后再进行疫苗接种[21]。
本研究中,绝大多数患者接种的疫苗种类是BIBP灭活疫苗和克尔来福,这和上海地区主要供应的疫苗种类是一致的。本研究中正在接受SCIT的患者全程接种新冠疫苗后的不良反应发生率为11%,低于系统评价[22]接种新冠疫苗后28 d内的不良反应发生率。该分析显示,6项研究的不良反应发生率低于30%,2项为30%~50%,2项高于50%。本研究中的不良反应主要为轻度,全身表现主要为头痛、低热和乏力等,局部表现主要为注射部位疼痛和肿块。这些不良反应与新冠疫苗接种说明书中普通人群接种新冠疫苗的不良反应是一致的。仅1例患者接种后低热1周,经治疗后好转。未发现严重不良反应。将患者按性别、年龄、是否伴有哮喘和SCIT所处阶段进行分组统计分析不良反应发生率,结果显示这些分组之间差异均无统计学意义(P值均>0.05)。因此,本研究认为,正在进行SCIT的AR患者在症状控制良好的状态下可以正常接种新冠疫苗。希望本研究能为AR患者和医务人员提供接种新冠疫苗的专业建议,进而提高新冠疫苗的接种率。
本研究还显示,正在接受SCIT的AR患者中有3%(7/209)在接种新冠疫苗后鼻炎症状加重,而且接种后出现不良反应的患者其鼻炎加重的比例高于接种后无不良反应的患者。这提示鼻炎加重可能与接种新冠疫苗后的不良反应类似,因为新冠疫苗的接种说明书中确有一项不良反应为鼻炎。但本研究中的鼻炎加重比例略高,可能是由于接种新冠疫苗延长了SCIT的间隔时间,最终可能导致AR的症状反复。
本研究还发现,在SCIT开始前接种新冠疫苗的患者对SCIT没有影响;在维持治疗阶段接种新冠疫苗的患者,绝大多数(141/165,89.1%)也没有影响SCIT;而在起始治疗阶段开始接种新冠疫苗的患者均需要重新开始SCIT。24例在维持治疗阶段开始接种新冠疫苗的患者中,大多(21/24,87.5%)可以在4周或7周恢复到原先的维持剂量。因此,我们建议AR患者若有SCIT的需求,应在未开始起始治疗时,先使用药物控制好AR症状,待新冠疫苗接种结束2周后开始SCIT。若AR患者已经开始免疫治疗,且处于免疫治疗的起始阶段,建议待免疫治疗起始阶段结束,在维持阶段每4~8周注射一次期间开始新冠疫苗接种。该建议的提出基于二点:①很多患者的鼻炎症状在SCIT维持阶段已基本得到控制;②在维持阶段接种新冠疫苗对免疫治疗的剂量维持影响最小。若在维持阶段因接种新冠疫苗而需要调整治疗剂量,一般也只需后退1~2步后即可恢复到维持剂量,避免重新开始SCIT,降低因此给患者带来的额外医疗和时间成本。本研究结果也支持该建议。
本研究还发现,未成年患者接种新冠疫苗后SCIT剂量需要调整的比例明显高于成年患者。该结果可能是由于未成年患者接种的疫苗均为灭活疫苗,且接种时间常由学校统一安排,2针的间隔时间常>3周,最终导致免疫治疗的间隔时间超出8周而需要进行剂量调整,因此建议患者为了不影响SCIT,可以按照时间规定自行预约新冠疫苗的接种时间(即在SCIT后的2周预约新冠疫苗第二针注射,并在完成第一针新冠疫苗接种后立即预约3周后的第二针新冠疫苗,这样全程接种结束后的2周可以正常进行SCIT)。详见图3,建议在绿色时间段内控制好鼻炎症状后进行新冠疫苗接种。

图3 新冠疫苗接种的时机
综上所述,全球新冠肺炎疫情仍然严峻,接种新冠疫苗,主动构建免疫屏障仍是控制疫情的重要措施。接受SCIT的AR患者接种新冠疫苗的反应与普通人群类似,对鼻炎的影响也很小。我们建议,AR患者在过敏症状控制良好的健康状态下应选择SCIT前或SCIT维持阶段接种新冠疫苗,这样能最大限度降低接种新冠疫苗对SCIT的影响。
