高原人群CYP2C9和VKORC1基因多态性及其与华法林用药剂量的相关性研究
2022-05-20胡建鹏李云熊倩李宏伟陈坤前高连灏陈一非李秀萍王俊玲
胡建鹏,李云,熊倩,李宏伟,陈坤前,高连灏,陈一非,李秀萍,王俊玲
(曲靖市第一人民医院1.检验中心,2.麻醉科,3.心脏血管外科,4.神经介入科,云南曲靖 655000)
华法林是一种双香豆素衍生物[1],通过抑制维生素K 及其环氧化物的相互转化而发挥抗凝作用。主要适用于预防和治疗血栓栓塞性疾病(深静脉血栓、肺动脉栓塞、脑梗死、心房颤动、瓣膜病),心脏瓣膜置换术,以及心腔内血栓形成等抗凝治疗。但由于华法林治疗窗口窄,剂量变异性大,与其他药物和食物相互作用,需要实验室监测,血药浓度过高或敏感性增加可导致严重出血事件等,因此在中国的使用率较低[2-3]。
高原地区的特征为低压、低氧、高寒及强辐射,在此环境下长期生活会导致患者机体各系统特别是血液、呼吸、心血管、内分泌等产生一系列病理和生理变化,进而影响药物的体内代谢过程。高原环境主要影响高血浆蛋白结合药物的药代动力学(PK)[4]。华法林与血浆蛋白(主要是白蛋白)结合率高达98%~99%,但只有游离华法林能发挥抗凝作用,因此,影响华法林与血浆蛋白结合的因素都可能直接影响华法林的抗凝疗效。
在临床实践中,如何综合考虑遗传与环境因素,使华法林抗凝治疗剂量更加准确,从而降低治疗过程中的风险,使患者最大程度受益,是临床医师面临的共同问题。目前,为了实现华法林精准用药,国内外已建立了多种华法林给药剂量预测模型,这些模型大多基于CYP2C9 和VKORCl基因多态性,部分模型还将CYP4F2、EPHX1及GGCX基因纳入考虑,综合患者种族、性别、年龄、体重、疾病、是否合用肝酶诱导剂、胺碘酮等因素进行多因素回归分析。所建模型对华法林个体剂量差异的解释程度为20%~70%不等[5-12]。曲靖地处云贵高原中部,平均海拔2 000 m。本研究旨在分析高原地区基因组给药模型预测剂量的准确性及临床应用价值,供临床医师参考。
1 资料与方法
1.1 仪器与试剂
1.1.1 主要仪器生物安全柜(美国Thermo 公司);高速离心机(德国Sigma 公司);伯乐CFX96 实时荧光定量PCR 仪(美国Bio-Rad 公司);MK-20 振荡恒温加热器、OneDrop 紫外分光光度计、立式压力蒸汽灭菌器(日本Yamato 公司);净化工作台(SWCJ-2FD 苏州安泰公司);Eppendorf 可调移液器。
1.1.2 主要试剂天根血液基因组DNA 提取试剂盒(TIANamp Blood DNA Kit DP318)、人类CYP2C9& VKORC1 基因多态性检测试剂盒购自武汉友芝友公司。
1.2 标本收集
收集曲靖地区2016年10月—2020年1月375 例行华法林代谢基因多态性检测的患者。主要包括深静脉血栓、肺栓塞、脑梗死、冠状动脉粥样硬化、慢性阻塞性肺疾病,经及心脏瓣膜置换术后等心脑血管疾病患者。采集EDTA-K2抗凝全血2 mL,2~8℃保存不超过1 个月,检测后DNA 和全血标本-80℃保存2年以备复查。记录患者性别、年龄、身高、体重、吸烟史、合并房颤、置换主动脉瓣膜等基本信息,以及临床合并用药情况。本研究经医院医学伦理委员会批准(C2018013),患者签署知情同意书。
1.3 试验方法
使用离心柱吸附法提取人外周血细胞中基因组DNA,所提取DNA 用OneDrop 紫外分光光度计测定浓度及纯度,要求DNA 的A260/280 在1.8~2.0。使 用 qRT-PCR 法 检 测 CYP2C9*3 (A1075C,rs1057910)和VKORC1(G-1639A,rs9923231)基因多态性。
1.4 基于药物基因组学的华法林剂量预测公式
使用国家卫生健康委员会(National Health Commission,PRC)2015年发布的《药物代谢酶和药物作用靶点基因检测技术指南(试行)》推荐的基于中国人群华法林用药剂量计算公式和国际华法林遗传药理学协会(The International Warfarin Pharmacogenetics Consortium, IWPC)推荐的亚裔人群华法林剂量预测公式计算华法林预测剂量(见表1)。按照中国医生华法林用药习惯,3 mg/片规格片剂最常用,每次调整剂量1/4 片,因此,当维持剂量与预测剂量相差≤0.75 mg 时,判定为在预测范围内。

表1 两种华法林剂量预测公式
1.5 统计学方法
数据分析采用Excel 和IBM SPSS Statistics 23 统计软件。符合正态分布的计量资料以均数±标准差(±s)表示,比较用t检验;计数资料以例(%)表示,比较用χ2检验;华法林预测与实际维持剂量的相关性分析采用Pearson 法,并用χ2检验验证CYP2C9*3 和VKORC1 基因型检测结果是否符合Hardy-Weinberg 遗传平衡定律。P<0.05 为差异有统计学意义。
2 结果
2.1 患者基本信息
行基因检测的375 例患者中,182 例未服用华法林,193 例服用了华法林。服用华法林患者收集到初始剂量,其中174 例收集到维持剂量相关数据。将服用华法林者、未服用华法林者及收集到华法林维持剂量者的基本信息进行比较,可知患者实际治疗过程中是否选择服用华法林进行抗凝,通常与患者的性别构成、身高、吸烟史、是否合并房颤、是否注射低分子肝素钙无关(P>0.05),而与患者年龄、体重、体表面积(BSA)、初始国际标准化比值(INR)、是否置换主动脉瓣膜,以及是否服用阿司匹林、利伐沙班或氯吡格雷相关(P<0.05)。
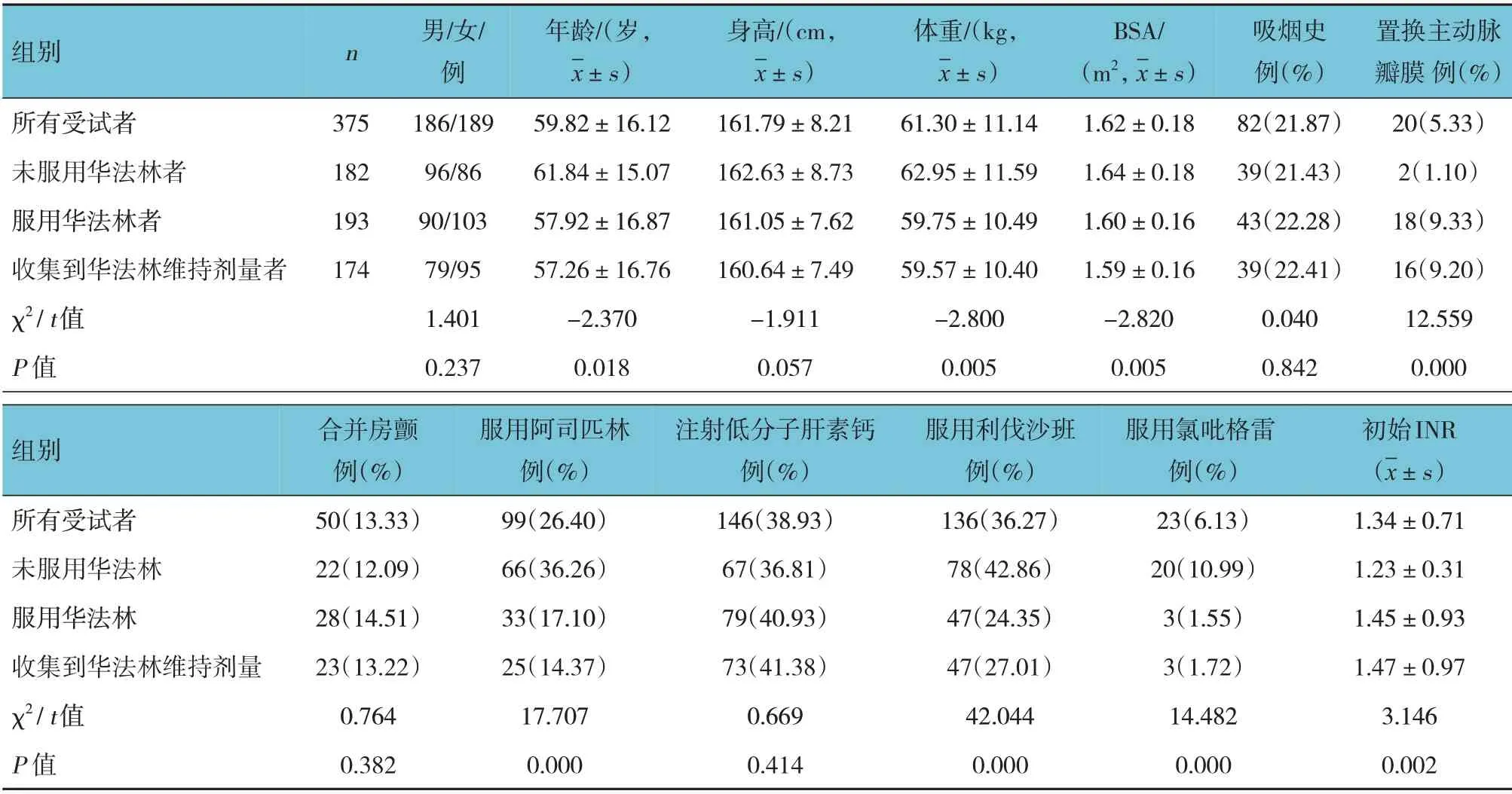
表2 受试者基本特征
2.2 所有患者基因分型分布情况
行基因检测的375 例患者中,CYP2C9基因*1/*1(AA)、*1/*3(AC)及*3/*3(CC)基因型频率分别为93.07%(349/375)、6.93%(26/375)和0.00%(0/375)。VKORC1-1639基因AA、AG 及GG 基因型频率分别为82.66%(310/375)、16.27%(61/375)和1.07%(4/375)。因此,CYP2C9*1 等位基因频率为96.54%,CYP2C9*3 等位基因频率为3.46%。VKORC1-1639 A等位基因频率为90.79%,VKORC1-1639 G 等位基因频率为9.21%。χ2检验结果表明,CYP2C9*3A>C 和VKORC1-1639G>A 基因频率均符合Hardy-Weinberg遗传平衡定律(χ2=0.021 和0.177,P=0.885 和0.915)。所有患者的基因型分布和预测剂量见表3。
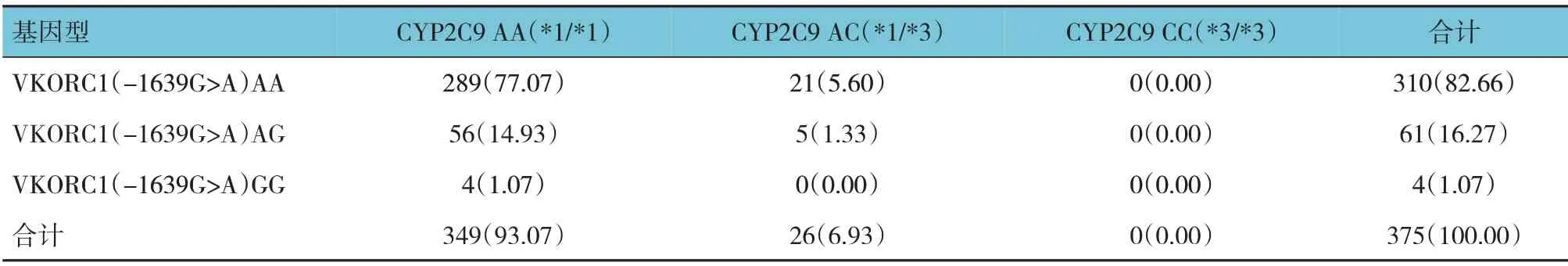
表3 375例患者CYP2C9*3和VKORC1(-1639 G>A)基因型分布频率 例(%)
2.3 所有患者两种模型预测剂量情况
行基因检测的375 例患者根据检测结果并结合患者基本信息,用两种模型预测华法林剂量。结果发现,所有基因型组合PRC 和IWPC 模型预测剂量差异均无统计学意义(P>0.05)。因携带CYP2C9*1/*1 & VKORC1 AA 基因型患者最多,占77.07%(289/375),以其为对照组。统计结果显示,无论是使用PRC 还是IWPC 模型,CYP2C9*1/*1 & VKORC1 AG组、CYP2C9*1/*1 & VKORC1 GG 组和CYP2C9*1/*3& VKORC1 AA 组预测剂量与对照组比较,差异有统计学意义(P<0.05),而CYP2C9*1/*3 & VKORC1 AG组预测剂量与对照组比较,差异无统计学意义(P>0.05)。经多重比较发现,其他所有基因型组合预测剂量两两比较,差异有统计学意义(P<0.05)。见表4。
表4 375例患者不同基因型组合预测剂量情况 (mg/d,±s)
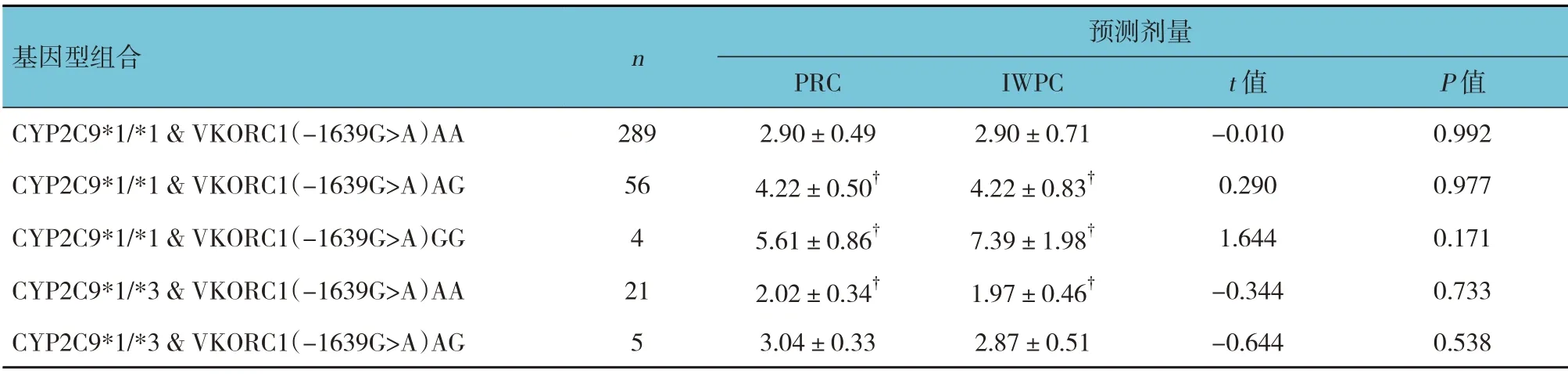
表4 375例患者不同基因型组合预测剂量情况 (mg/d,±s)
注:†与CYP2C9(*1/*1)&VKORC1(-1639G>A)AA比较,P <0.05。
基因型组合n 预测剂量CYP2C9*1/*1&VKORC1(-1639G>A)AA CYP2C9*1/*1&VKORC1(-1639G>A)AG CYP2C9*1/*1&VKORC1(-1639G>A)GG CYP2C9*1/*3&VKORC1(-1639G>A)AA CYP2C9*1/*3&VKORC1(-1639G>A)AG P 值0.992 0.977 0.171 0.733 0.538 289 56 4 21 5 PRC 2.90±0.49 4.22±0.50†5.61±0.86†2.02±0.34†3.04±0.33 IWPC 2.90±0.71 4.22±0.83†7.39±1.98†1.97±0.46†2.87±0.51 t 值-0.010 0.290 1.644-0.344-0.644
2.4 不同CYP2C9&VKORC1 基因型组合的华法林剂量
对CYP2C9 & VKORC1 不同基因型组合PRC 和IWPC 模型预测剂量和维持剂量分析发现,除CYP2C9*1/*3 & VKORC1 AA 组的PRC 模型预测剂量低于维持剂量以外,其他所有基因型组合的IWPC 和PRC 模型的预测剂量均高于维持剂量,尤其是CYP2C9*1/*1 & VKORC1 AA 和CYP2C9*1/*1 &VKORC1 AG 基因型患者预测剂量均高于维持剂量(P<0.05),其他基因型比较,差异无统计学意义(P>0.05)。各基因型两种模型预测剂量比较,差异无统计学意义(P>0.05)。因携带CYP2C9*1/*1& VKORC1 AA 基因型患者最多,占78.16%(136/174),以其为对照组。统计结果显示,CYP2C9*1/*1& VKORC1 AG 和CYP2C9*1/*1 & VKORC1 GG 组维持剂量分别为(3.41±1.01)mg 和(4.75±0.35)mg,均高于CYP2C9*1/*1 & VKORC1 AA 组(2.59±0.73)mg(P<0.05);CYP2C9*1/*3 & VKORC1 AA 组维持剂量为(2.00±0.53)mg,低于所有其他基因型组合(P<0.05);CYP2C9*1/*3 & VKORC1 AG 基因型仅1 例患者收集到维持剂量,不纳入比较。本研究中携带CYP2C9*3 等位基因的患者预测准确性最高,IWPC和PRC 模型分别为100%(6/6)和83.33%(5/6)。PRC 模型预测准确性为72.99%(127/174),其中CYP2C9*1/*1 & VKORC1 AA 基因型患者136 例,有106 例在预测范围内,预测准确性为77.94%(106/136)。IWPC 模型预测的准确性为62.64%(109/174),其中CYP2C9*1/*1 & VKORC1 AA 基因型患者136 例,有91 例在预测范围内,预测准确性为66.91%(91/136)。见表5和图1。
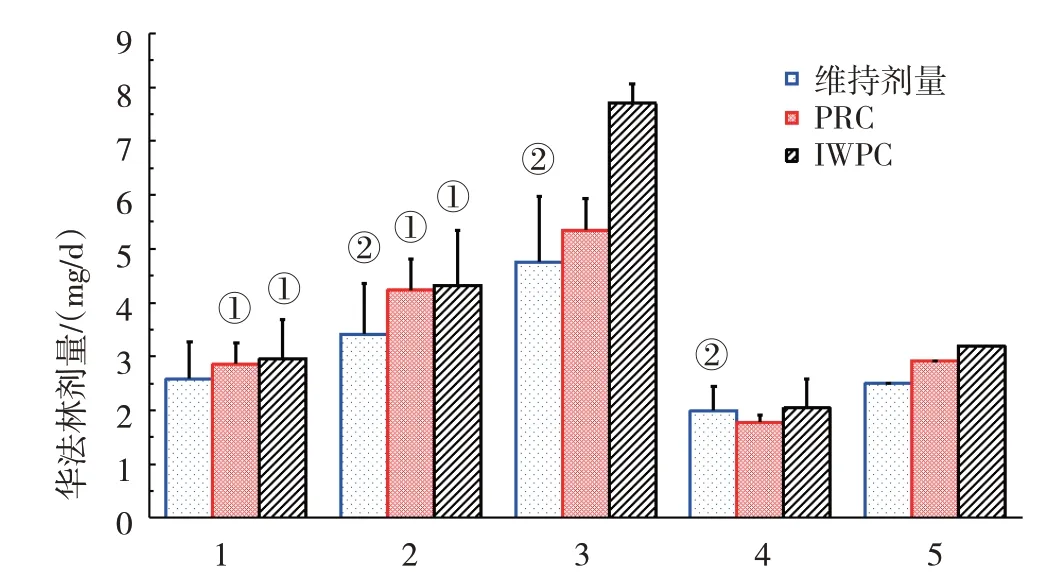
图1 不同基因型华法林预测剂量与维持剂量比较(±s)
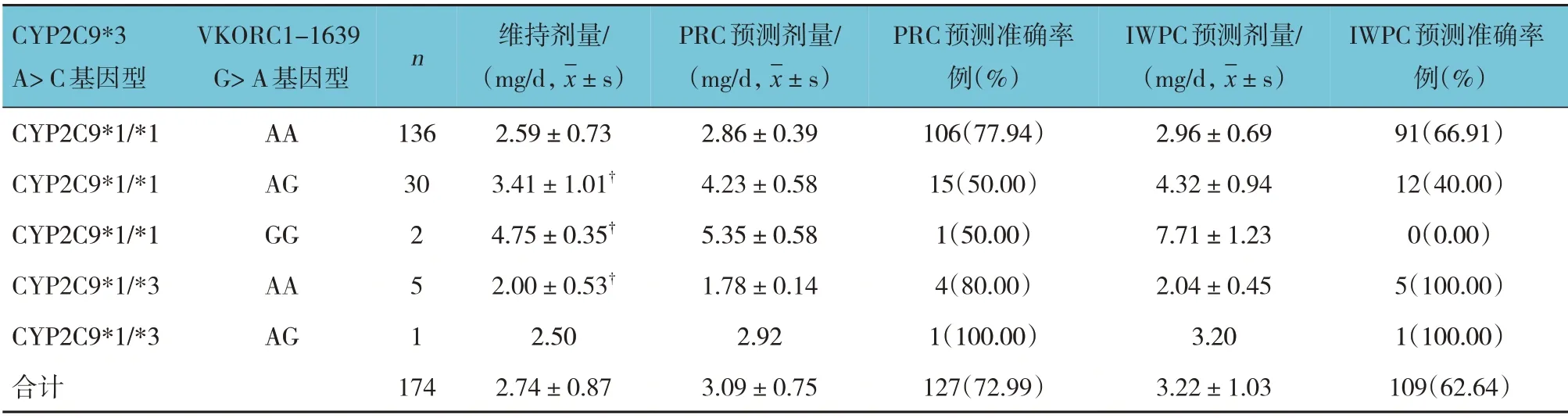
表5 不同CYP2C9&VKORC1基因型患者华法林剂量情况
2.5 IWPC 和PRC 模型预测剂量与维持剂量相关性分析
将收集到维持剂量的174 例患者维持剂量设置为横坐标,预测剂量分别设置为纵坐标,绘制散点图,并添加趋势线,对两个模型的预测剂量与维持剂量进行相关性分析,得到PRC 模型Pearson 相关系数r1=0.546,决定系数R12=0.298;IWPC 模型Pearson相关系数r1=0.567,决定系数R22=0.322。如图2所示,图中虚线为理想预测剂量(预测剂量=维持剂量),实线为两个模型华法林预测剂量趋势线。
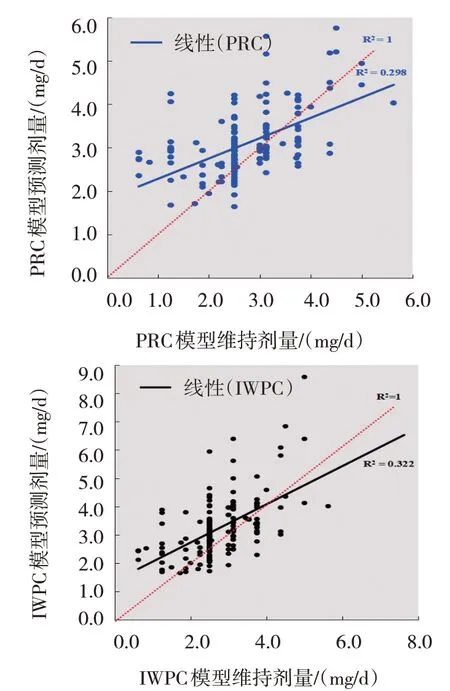
图2 华法林两种预测模型预测剂量与维持剂量的相关性
3 讨论
自周宏灏院士在国际上首次发现和阐明了遗传因素引起药物种族和个体差异的若干现象和机制及其规律,建立了有国家和民族特色的遗传药理学理论体系,开拓了我国药物基因组学研究领域,率先提出和推动“量体裁衣”个体化药物精准治疗以来,国内外大量研究将基因型与其他相关影响因素联合进行统计分析,建立基于基因组学的华法林剂量预测模型,并对所建模型进行回顾性和前瞻性验证。
本研究通过回顾性分析,利用权威报道的PRC和IWPC 模型,对高原人群基于基因组学的华法林剂量预测模型进行有效性验证。通过检测CYP2C9*3(A1075C, rs1057910) 和 VKORC1 (G-1639A,rs9923231)基因多态性,综合患者的性别、年龄、身高、体重、合并用药、房颤和置换主动脉瓣膜与否,以及合并用药等因素,发现PRC 和IWPC 模型分别可解释29.8%和32.2%的给药剂量个体差异,且预测剂量与实际维持剂量呈正相关(r1=0.546,r2=0.567),与已有文献报道符合[13]。但总体上华法林预测剂量与实际维持剂量存在偏差,CYP2C9*1/*1 & VKORC1 AA 和CYP2C9*1/*1 & VKORC1 AG 基因型患者预测剂量均显著高于维持剂量。经分析,导致预测剂量高于实际维持剂量的原因主要有以下几个方面:①建立模型时病例来源人群与该研究纳入人群的基本特征背景存在差异。②建立模型时未将高原特殊环境影响因素纳入考虑,高原地区因其低压、低氧、高寒、强辐射及血氧饱和度较低等特点,影响华法林与血浆蛋白(主要是白蛋白)结合,血液中游离华法林含量增加,对华法林的需求量降低。③样本量较小,实验结果存在一定局限性。④我国机械瓣膜置换术后的抗凝强度标准低于指南推荐范围[14]。⑤华法林治疗窗口窄,起效缓慢,医生在使用过程中极为谨慎。
预测模型的解释性低也提示可能还存在其他遗传和非遗传因素的影响[15]。已有文献报道,华法林的剂量还受APOE、EPHX1、CYP4F2、GGCX、CYP3A4、CYP1A2、UGT1A1、CYP2C19、NQO1等基因的影响[16-17]。另外,生活方式、饮食习惯、联合用药、病理生理状态等非遗传因素对华法林抗凝疗效也有显著影响。如胺碘酮、甲硝唑、环丙沙星、吡罗昔康、奥美拉唑、龟苓膏等药物可增强华法林抗凝作用,而利福平、利巴韦林、灰黄霉素、奈夫西林、消胆胺、美沙拉嗪、巴比妥类、卡马西平、维生素K 等药物可抑制华法林抗凝作用[3]。吸烟、发热、饮酒、腹泻等也可抑制华法林抗凝作用[18]。
本研究置换了主动脉瓣膜的20 例患者中18 例选择服用华法林进行抗凝,占90%,说明临床医师在选择抗凝药物时,患者是否置换主动脉瓣膜是一个极其重要的决定指标。此外,服用华法林组患者体重、BSA 及年龄均低于未服用华法林组,说明临床医生可能对预测剂量偏低且年龄较小的患者更偏向选择华法林,而对于预测剂量较高、年龄偏大的患者使用华法林时会更为谨慎。同时,使用氯吡格雷的患者主要来自于神经介入科,通常不合并使用华法林。而使用利伐沙班和低分子肝素钙的患者主要来自于心脏血管外科,因华法林达到有效血药浓度需要72 h 左右,因此通常需要先用低分子肝素钙重叠3 d。对于未服用华法林的患者,通常会选择利伐沙班、阿司匹林或氯吡格雷进行治疗。
本研究目前仍在继续对不同病历资料和临床终点事件进行收集,虽然可解释性有限,但获取遗传和非遗传信息可以为临床医生在使用和调整药物剂量时提供参考,对于携带VKORC1-1639 G等位基因的患者可从更高剂量开始,调整剂量时也可更加大胆,缩短达到目标INR 值所需时间。而对于携带CYP2C9*3 等位基因的患者,则需更加谨慎,从更小剂量开始服用以降低出血风险。研究结果已经提示使用华法林前先对患者进行相关基因检测可对临床抗凝治疗的有效性和安全性产生积极影响。鉴于已有报道不同海拔健康人群凝血功能随着海拔高度的升高而发生改变[凝血酶原时间(PT)、部分凝血活酶时间(APTT)、凝血酶时间(TT)逐渐延长,而纤维蛋白原(Fib)含量逐渐下降][19-20],在进一步的研究中,本课题组将构建更大的样本数据库,纳入患者长期居住地海拔、血氧饱和度、凝血指标、民族、同型半胱氨酸(Hcy)、联合使用氯吡格雷、低分子肝素钙或利伐沙班等遗传和非遗传信息,以建立适合于高原民族地区的华法林剂量预测模型,同时为发掘新的适合中国人的华法林剂量预测公式奠定基础,使研究成果惠及更多患者。
