(Na, K)基地质聚合物原位合成沸石及其钝化土壤Cu2+、Zn2+污染性能研究
2022-05-19邓梓萱
黄 毅,吴 迪,姚 霞,李 煊,邓梓萱,谭 睿
(湖南城市学院 材料与化学工程学院,湖南 益阳 413000)
随着工业经济的高速发展,废弃物进入土壤生态系统,土壤重金属污染态势日趋严峻.2014年我国环境保护部和国土资源部联合发布的《全国土壤污染状况调查公报》显示:我国土壤各种污染物总超标率为16.1%,其中耕地土壤点位超标率高达19.4%,且其主要污染物为镉、镍、铜、砷、汞、铅、滴滴涕和多环芳烃.湖南是“有色金属之乡”,其土壤重金属污染问题更为严重.Hu等[1]对2008—2018 年的1 203 份有关我国土壤重金属污染的研究报告进行了总结分析,结果表明湖南省为土壤重金属污染最严重的省份之一.化学钝化法是重金属污染土壤最常用的修复方法之一,其通过向土壤中加入钝化剂,使重金属发生氧化还原、沉淀、吸附、螯合等一系列反应,降低其在土壤环境中的生物有效性和可迁移性,从而减少重金属元素的毒性.天然黏土类矿物是最为常见的化学钝化剂之一,因其成本低、使用简便、效果好,且对土壤环境的长期影响小,无二次污染,在重金属污染土壤的治理领域中具有较大潜力.蒙脱石、凹凸棒、沸石、海泡石和蛭石等天然黏土类矿物均表现出一定的重金属污染修复效果,其中沸石由于具有很大的比表面积和优良的离子交换性能,其修复效果更加明显[2].沸石施用于土壤,还具有保肥、调节土壤pH 值等功能,特别是钾基沸石还能充当缓释钾肥[3-4].
地质聚合物是一类新型的无机胶凝材料,由于其具有类沸石结构,被视为沸石的前驱体.近年来,基于地质聚合物反应原位合成沸石或沸石制品的研究受到了广泛关注.相比于传统水热合成法,地质聚合物反应原位合成沸石的方法具有工艺简单、成本低、溶剂需求量小等优点[5-6].以地质聚合物为前驱体合成A 型沸石、八面沸石和方钠石等钠基沸石已有较多的研究报道,并已应用于废水处理和相分离领域[7-10],而用于土壤污染修复的却鲜见报道.
基于此,本文以NaOH 和KOH 混合碱液作激发剂,以偏高岭土为固体原料,基于地质聚合物反应合成沸石,并探讨所合成的沸石材料钝化土壤Cu2+、Zn2+污染及其调节土壤pH 值,提高土壤中有效钾含量的性能,以期为土壤重金属污染的治理提供一种低成本、高效率、对土壤扰动小,同时还能提供缓释钾肥的钝化材料.
1 实验部分
1.1 (Na, K)基地质聚合物原位合成沸石及其表征
1.1.1 地质聚合物原位合成沸石工艺
将偏高岭土(购于山西金洋高岭土有限公司)经X 射线荧光光谱仪(XRF),测定其化学成分(见表1).将NaOH、KOH(均为分析纯)和水按一定质量比例混合均匀形成浆液,并倒入模具中,在温度80 ℃和湿度95±5%的条件下,养护24 h 后取出,研磨至200 目以下,获得所需样品.为进行修复效果对比,本研究制备了3 种不同原料组成的样品,如表2 所示.

表1 偏高岭土的化学组成 %
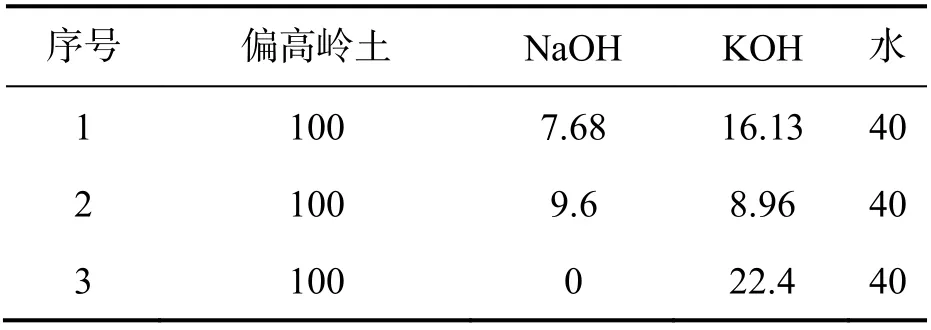
表2 地质聚合物原位合成沸石的原料组成 g
1.1.2 样品表征分析
使用德国布鲁克AXS 公司D8 Advance X 型X 射线粉末衍射仪(XRD)对样品的物相进行表征,其实验条件为40 kV,22.5 mA,Cu-Kα,扫描速率为2°/min;使用日本日立公司SU8010 型场发射电子扫描显微镜(FESEM)对样品微观形貌进行表征;样品比表面积和孔径分布用N2吸附-脱附进行测试(美国麦克公司ASAP 2020 型比表面积及孔径分析仪),其中比表面积数据由BET 法获得,微孔(孔径<2 nm)孔容用T-PLOT 法获得,中孔(2 nm<孔径<50 nm)孔容用BJH(Barrett-Joyner-Halenda)法获得.
1.2 (Na, K)基地质聚合物原位合成沸石钝化土壤中Cu2+、Zn2+实验过程
1.2.1 模拟污染土样的获得和制备
从益阳市郊区某稻田中取得若干质量的土样,风干后研磨至直径2 mm 以下;分别称取一定量Cu(NO3)2和ZnSO4溶于水中制成溶液,与研磨后的土壤充分混合,使土壤样品中外源Cu2+、Zn2+含量分别达到500 和2 000 mg/kg;向土壤样品中补充水分,使土壤含水量保持在70%左右,密封放置20 d,获得模拟污染土壤样品.
1.2.2 Cu2+、Zn2+污染土样的钝化实验
在模拟污染土样中加入一定质量比例的地质聚合物原位合成沸石样品,充分混合均匀;在室温条件下培养(土壤含水量保持在70%左右)若干天后,将土样风干;根据国家标准《土壤 8 种有效态元素的测定 二乙烯三胺五乙酸浸提-电感耦合等离子体发射光谱法》(HJ 804-2016)测定风干土样中的有效态Cu、Zn 含量(土壤元素有效态指的是能被植物吸收利用的元素);用钝化效率表征该合成沸石样品钝化土壤Cu2+、Zn2+污染的效果,钝化效率按式(1)[11]进行计算.
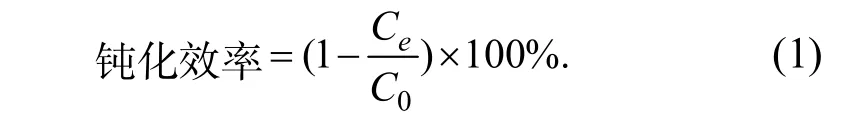
其中,Ce为污染土壤钝化后单一金属元素浸出浓度,mg/kg;C0为污染土壤钝化前单一金属元素有效态含量,mg/kg.
土壤速效K 含量根据农业行业标准《土壤速效钾和缓效钾含量的测定》(NY/T 889-2004)中规定的方法进行测定;土壤pH 值根据环境保护标准《土壤 pH 值的测定 电位法》(HJ 962-2018)用pH 计(上海雷磁PHS-3C 型)测定.以上测试均做3 次平行实验,结果取其平均值.
2 结果与讨论
2.1 (Na, K)基地质聚合物原位合成沸石表征结果分析
2.1.1 XRD 分析
偏高岭土和地质聚合物样品的XRD 图谱如图1 所示.由图1 可知,偏高岭土原料主要以无定形相为主,还含有少量在高温煅烧过程中所形成的石英,无定形相产生的“馒头”峰的位置在2θ=23°左右[12].样品1 和样品2 出现了不同类型沸石晶体的衍射峰,其中,样品1 以I 型和F 型钾沸石为主;样品2 以碱沸石和方钠石为主;样品3 未生成沸石晶体,“馒头”峰的位置移到了2θ=28°左右,这代表着无定形态地质聚合物的生成[13].由此可以看出,改变激发剂中的NaOH/KOH 比例,可以获得不同类型产物.当只用KOH 作为激发剂时(样品3),K+在地质聚合物形成过程中有利于长链硅铝聚合物的形成,这些长链聚合物移动和重构阻力较大,因此K 基地质聚合物不易转化为沸石[14];当使用NaOH/KOH 混合碱液时,Na+在地质聚合物向沸石转化过程中可起到结构导向作用,有利于沸石形成.
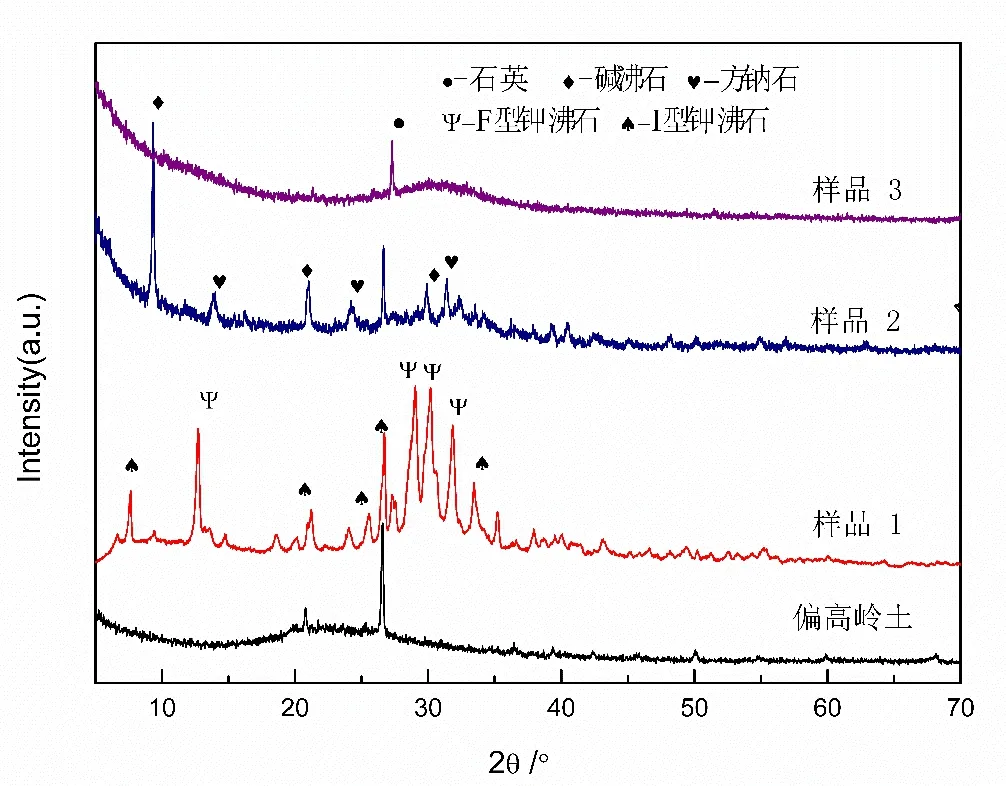
图1 偏高岭土及地质聚合物样品的XRD 图谱
2.1.2 SEM 分析
样品1~样品3 的扫描电镜照片分别如图2(a)~图2(c)所示.由图2(a)可知,样品1 中的F 型钾沸石为粒径0.1 μm 左右的立方状颗粒,I 型沸石为粒径0.5 μm 左右的片状;图2(b)显示样品2 中的碱沸石颗粒粒径为3 μm 左右,呈近立方状或球状形貌;图2(c)表明样品3 中未出现明显结晶相.由此可知,其主要为无定形态地质聚合物.

图2 各样品的SEM 图
2.1.3 比表面积和孔容分析
3 个样品的比表面积和孔容数据如表3 所示.
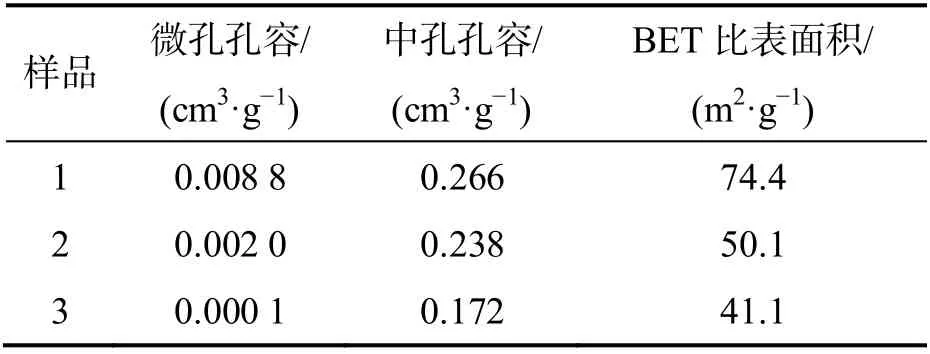
表3 各样品比表面积和孔容
由表3 可知,样品1 具有最大的比表面积和孔容;样品2 次之;未发现沸石生成的样品3 比表面积最小,几乎不存在微孔孔容.这说明地质聚合物不含微孔分布,而沸石属于微孔材料,具有更大的比表面积.
2.2 地质聚合物原位合成沸石钝化土壤Cu2+、Zn2+污染性能分析
2.2.1 地质聚合物原位合成沸石钝化土壤Cu2+、Zn2+污染效率
3 个地质聚合物原位合成沸石样品对土壤中Cu2+、Zn2+污染钝化效率如图3 所示.
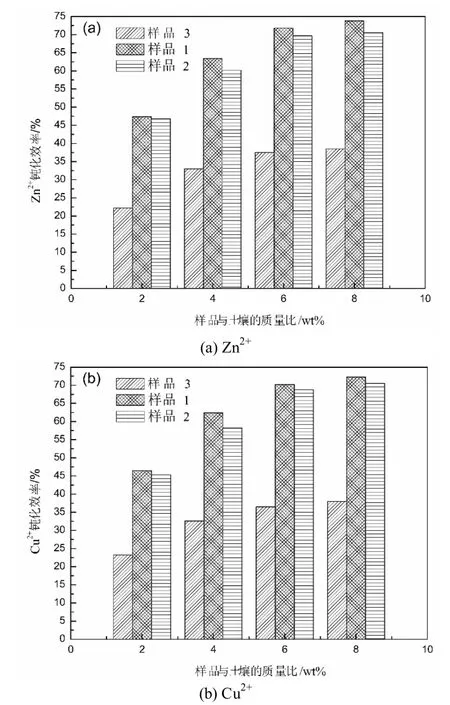
图3 沸石对土壤样品的污染钝化效率
由图3 可知,未生成沸石的样品3 对土壤的钝化效率明显小于以沸石为主要物相的样品1 和样品2.这是因为,与地质聚合物相比,沸石比表面积更大,对重金属的吸附能力更强.样品2的钝化效率略高于样品1,这同样归因于样品2比样品1 具有更大的比表面积.3 个样品的钝化效率均随样品加入量的增加而增加,但当样品与土壤质量比超过4 wt%以后,钝化效率的增长幅度明显减弱.这可能是因为,钝化剂样品的过量增加会向土壤中引入大量的Na+、K+离子,从而影响土壤胶体本身对重金属离子的吸附能力[15],部分抵消了样品施用量增加所带来的钝化效率增长.当样品与土壤质量比达6 wt%以上时,样品1 和样品2 对土壤Cu2+、Zn2+污染的钝化效率均达70%左右.
2.2.2 施用地质聚合物原位合成沸石对土壤pH值的影响
不同的地质聚合物原位合成沸石添加量对土壤pH 值的影响如图4 所示.
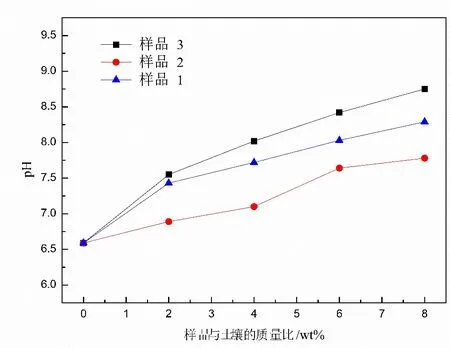
图4 样品施用对土壤pH 值的影响
由图4 可知,土壤pH 值随样品添加量的增加呈近似线性增加.这是因为,地质聚合物本身是一种碱性材料,含有未反应完全的NaOH 或KOH.样品3 施用后,土壤pH 值的增长更为明显,这主要是因为KOH 的碱性强于NaOH.土壤pH 值的增加有利于土壤中重金属的钝化,因为土壤呈碱性,重金属会形成沉淀,不易被植物所吸收,这也是地质聚合物原位合成沸石钝化重金属土壤的机理之一[16].常见作物的适宜土壤pH 值为5.5~7.5,因此地质聚合物原位合成沸石的施用量不宜超过6 wt%,避免影响作物生长.
2.2.3 施用地质聚合物原位合成沸石对土壤有效钾含量的影响
不同的地质聚合物原位合成沸石添加量对土壤有效钾含量的影响如图5 所示.
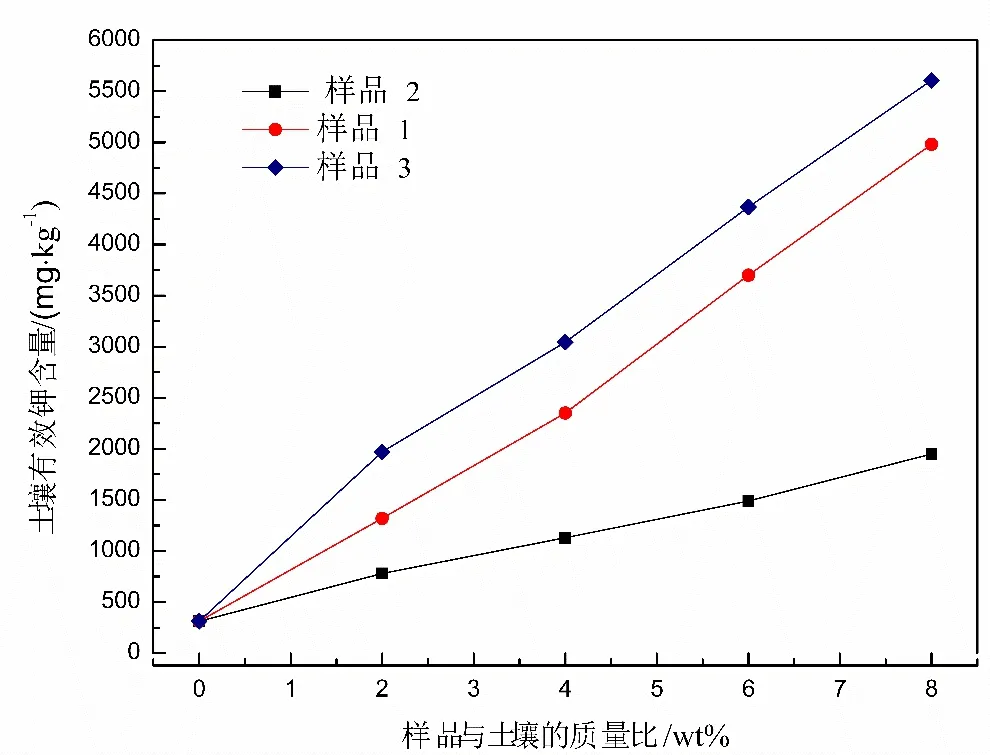
图5 样品施用对土壤有效钾含量的影响
由图5 可知,土壤中有效钾含量随样品施用量的增加也呈近似线性增加.3 种样品对土壤有效钾含量的不同影响主要归因于3 种样品制备原料中KOH 的质量比例不同.样品3 全部使用KOH 作为激发剂,因此使土壤中有效钾含量增加更为明显.
3 结论
1)通过改变NaOH 和KOH 的质量比例,地质聚合物可原位转化为碱沸石、方钠石、F 型钾沸石、I 型钾沸石等多种类型沸石.
2)地质聚合物转化为沸石后,比表面积和孔容明显增加,因此对Cu2+、Zn2+污染土壤具有更高的修复效率.当地质聚合物原位合成沸石样品的施用量达6 wt%时,对Cu2+、Zn2+污染土壤的钝化效率为70%左右;此后继续提高施用量,钝化效率增加不明显,且会造成土壤pH 值超过常见农作物适宜生长的pH 值范围,因此施用量不宜超过6 wt%.
3)施用地质聚合物或其原位合成沸石样品可明显提高土壤的有效钾含量.当施用量达6 wt%时,土壤中有效钾含量可从未施加钝化材料时的312 mg/kg 提升至1 000 mg/kg 以上.
