山东省市售龙胆泻肝丸(水丸)质量分析
2022-05-16李俊卿王金凤李占芳宋建建崔洋洋路公静
李俊卿,王金凤,李占芳,宋建建,崔洋洋,路公静
(1. 山东省东营市食品药品检验研究院,山东 东营 257091; 2. 北京中医药大学,北京 100029)
龙胆泻肝丸处方源自《医方集解》,由龙胆、炙甘草、栀子(炒)、黄芩、泽泻、木通、盐车前子、柴胡、酒当归、地黄10 味中药材组方,具有清肝胆、利湿热功效[1],广泛用于慢性胆囊炎、急性带状疱疹、慢性前列腺炎等疾病的治疗[2-3]。为加强药品质量监督管理,客观评价和提高山东省龙胆泻肝丸的质量,保障广大人民群众的用药安全[4-8],根据《山东省药品监督管理局关于印发2020年山东省药品质量风险监测工作方案的通知》(局函〔2020〕76 号)及《2020年山东省药品质量风险监测工作方案》(鲁食药检业〔2020〕36 号)要求,开展龙胆泻肝丸(水丸)质量风险研究。本研究中采用2015年版《中国药典(一部)》标准检验与探索性研究相结合的方法,对从山东省12 个地市抽取的30 批龙胆泻肝丸(水丸)进行质量评价,并提出合理化建议,以进一步加强龙胆泻肝丸(水丸)的监督管理。现报道如下。
1 样品信息及检验依据
龙胆泻肝丸(水丸)来源于山东省的12 个地市,涉及药品生产企业14 家,共30 批样品,样品信息见表1。所有样品生产日期均为2020年12月31日前,故按照2015年版《中国药典(一部)》进行检验,检验项目包括性状、鉴别、水分、装量差异、溶散时限、微生物限度和含量测定。

表1 龙胆泻肝丸(水丸)样品信息Tab.1 Information of Longdan Xiegan Pills(Water-Bindered Pills)samples
2 方法与结果
2.1 法定标准检验
性状:依据法定检验标准,应为暗黄色水丸,味苦。结果30 批样品均为暗黄色,味苦,颜色略有差异,但均符合标准规定。
鉴别:依据法定检验标准,包括显微鉴别1 项和薄层色谱鉴别3 项。结果30 批样品均显示其显微特征,薄层色谱图中均有相应特征斑点出现,均符合规定。
水分:依据法法定检验标准,水分应不得过9.0%。结果30批样品的水分为2.7%~7.6%,均符合规定。
装量差异:依据法定检验标准,超出装量差异限度的不得多于2袋(瓶),并不得有1袋(瓶)超出限度1倍。结果30批样品均符合规定。
溶散时限:依据法定检验标准,应在1 h 内完全溶散。结果30 批样品的溶散时限为31~59 min,均符合规定。
微生物限度:依据法定检验标准,结果30批样品均符合规定。
含量测定:依据法定检验标准,本品每1 g 含龙胆以龙胆苦苷(C16H20O9)计,不得少于0.80 mg;含栀子以栀子苷(C17H24O10)计,不得少于1.30 mg;含黄芩以黄芩苷(C21H18O11)计,不得少于3.80 mg。结果龙胆苦苷、栀子苷、黄芩苷的含量分别为1.36~6.31 mg/ g、2.24~3.77 mg/g、4.53~9.49 mg/g,均符合规定。可见,30批样品含量有一定差异,可能与生产工艺、投料量和饮片质量有关。
2.2 探索性研究
2.2.1 仪器与试药
仪器:岛津LC - 20AT 型高效液相色谱仪(日本岛津公司);7900 型电感耦合等离子体质谱仪(安捷伦科技有限公司);MARS6240/50 型微波消解仪(美国CEM公司);BT224S 型分析天平(赛多利斯科学仪器有限公司,精度为万分之一)。
试药:龙胆泻肝丸(样品信息见表1);硝酸(分析纯,太仓沪试试剂有限公司,批号为20191219);乙腈(色谱纯,国药集团化学试剂有限公司,批号为20201203);水为超纯水;23-乙酰泽泻醇B 对照品(中国食品药品检定研究院,批号为111846-201504,纯度为100%);砷(As)、镉(Cd)、铬、铅(Pb)多元素标准溶液[GNM-M041940-2013,批号为20D3577,质量浓度为1000 μg/mL],金单元素标准溶液[GNM-SAU-003-2013,批号为19D6574,质量浓度为1.0 μg/ mL],锗、铟、铋多元素标准溶液(GNM - M033030 - 2013,批号为2D3605,质量浓度为10.0 μg/mL),均购自国家有色金属及电子材料分析测试中心;汞(Hg)单元素标准溶液[GBW(E)080124,批号为19052],铜(Cu)单元素标准溶液[GBW(E)080122,批号为19101],质量浓度均为100 μg/mL,均购自中国计量科学研究院。
2.2.2 高效液相色谱法测定23 - 乙酰泽泻醇B 含量
1)色谱条件
色谱柱:Agilent C18柱(250 mm × 4.6 mm,5 μm);流动相:乙腈-水(75∶25,V/V);流速:1.0 mL/min;检测波长:208 nm;柱温:30 ℃;进样量:10 μL。
2)溶液制备
取23 - 乙酰泽泻醇B 对照品10 mg,精密称定,加乙腈制成质量浓度为100 μg/ mL 的对照品贮备液。取样品适量,研细,取2 g,精密称定,置具塞平底烧瓶中,加入乙腈20 mL,密塞,称定质量,超声(功率为300 W,频率为50 kHz)45 min,放冷,再称定质量,用乙腈补足减失的质量,摇匀,滤过,取续滤液,即得供试品溶液。
3)方法学考察
线性关系考察:吸取溶液制备项下对照品贮备液0.2,0.4,0.8,1.0,2.0,3.0,5.0 mL,置10 mL 容量瓶中,加乙腈稀释并定容,制成质量浓度分别为2.086,4.172,8.344,10.430,20.860,31.290,52.150 μg/ mL的系列对照品溶液。按拟订色谱条件进样测定,以对照品溶液质量浓度(X,μg/mL)为横坐标、峰面积积分值(Y)为纵坐标进行线性回归,得回归方程Y= 8118.5X-3873.3(R2=1.0000,n=7)。结果表明,23-乙酰泽泻醇B 质量浓度在2.086~52.150 μg/mL 范围内与峰面积线性关系良好。
精密度试验:吸取溶液制备项下对照品贮备液适量,按拟订色谱条件连续重复进样测定6 次,记录峰面积。结果23-乙酰泽泻醇B峰面积的平均值为179743,RSD为0.72%(n=6),表明仪器精密度良好。
稳定性试验:吸取溶液制备项下供试品溶液适量,分别于室温下放置0,2,4,8,12,16,24 h 时进样测定,记录峰面积。结果23 - 乙酰泽泻醇B 峰面积的平均值为181911,RSD为0.56%(n=7),表明供试品溶液在室温下放置24 h内稳定性良好。
重复性试验:取同一批(批号为2005015)样品,依法制备供试品溶液6 份,按拟订色谱条件进样测定,记录峰面积,并计算含量。结果23-乙酰泽泻醇B 的平均含量为0.23 mg/g,RSD为0.63%(n=6),表明方法重复性良好。
加样回收试验:取样品(批号为2005015)适量,共9 份,精密称定,置100 mL 锥形瓶中,分别加入23 - 乙酰泽泻醇B对照品0.1669,0.2086,0.2503 mg,各3份,依法制备供试品溶液,按拟订色谱条件进样测定,记录峰面积,并计算回收率。结果平均回收率为99.41%,RSD为0.86%(n=9)。
4)样品含量测定
取30批样品各适量,精密称定,依法制备供试品溶液,各平行2份,按拟订色谱条件进样测定,按外标法计算样品中23-乙酰泽泻醇B 的含量。结果见表2。可见,样品中23-乙酰泽泻醇B的含量为0.028~0.388 mg/g;H 生产企业的样品含量为0.127~0.388 mg / g,批间含量差异较大;G 生产企业的样品含量为0.143~0.162 mg/g,批间含量差异较小,均匀性较好;K生产企业的2 批样品中的23-乙酰泽泻醇B 的含量远低于其他生产企业的样品,可能存在投料不足或原料药质量不佳的情况。本研究中仅有2批样品,代表性不强,还需收集更多样品进行研究。
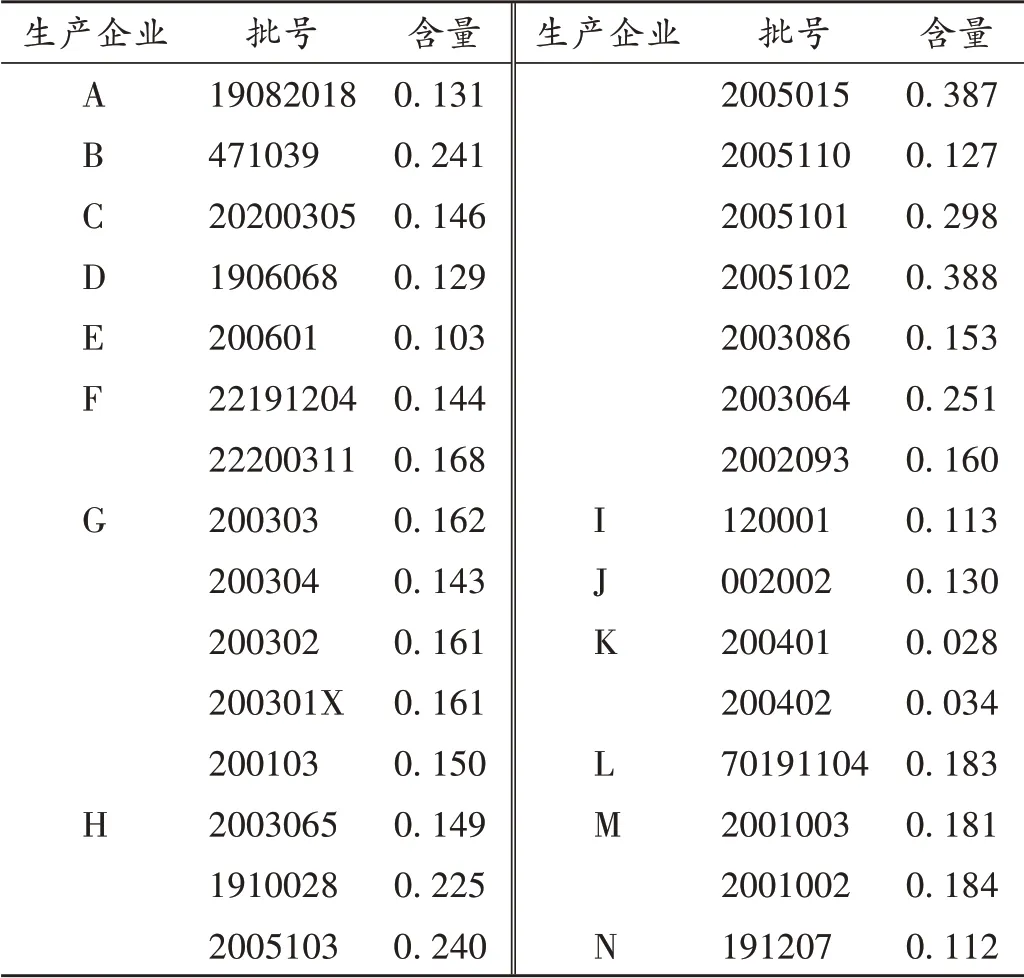
表2 样品中23-乙酰泽泻醇B含量测定结果(mg/g,n=2)Tab.2 Results of content determination of 23 - acetyl alisol B in samples(mg/g,n=2)
2.2.3 电感耦合等离子体质谱(ICP-MS)法测定样品中重金属及有害元素含量
《中国药典(四部)》[9]中方法,采用电感耦合等离子体质谱仪检测样品中重金属及有害元素Pb,As,Cd,Hg,Cu的含量。结果见表3。
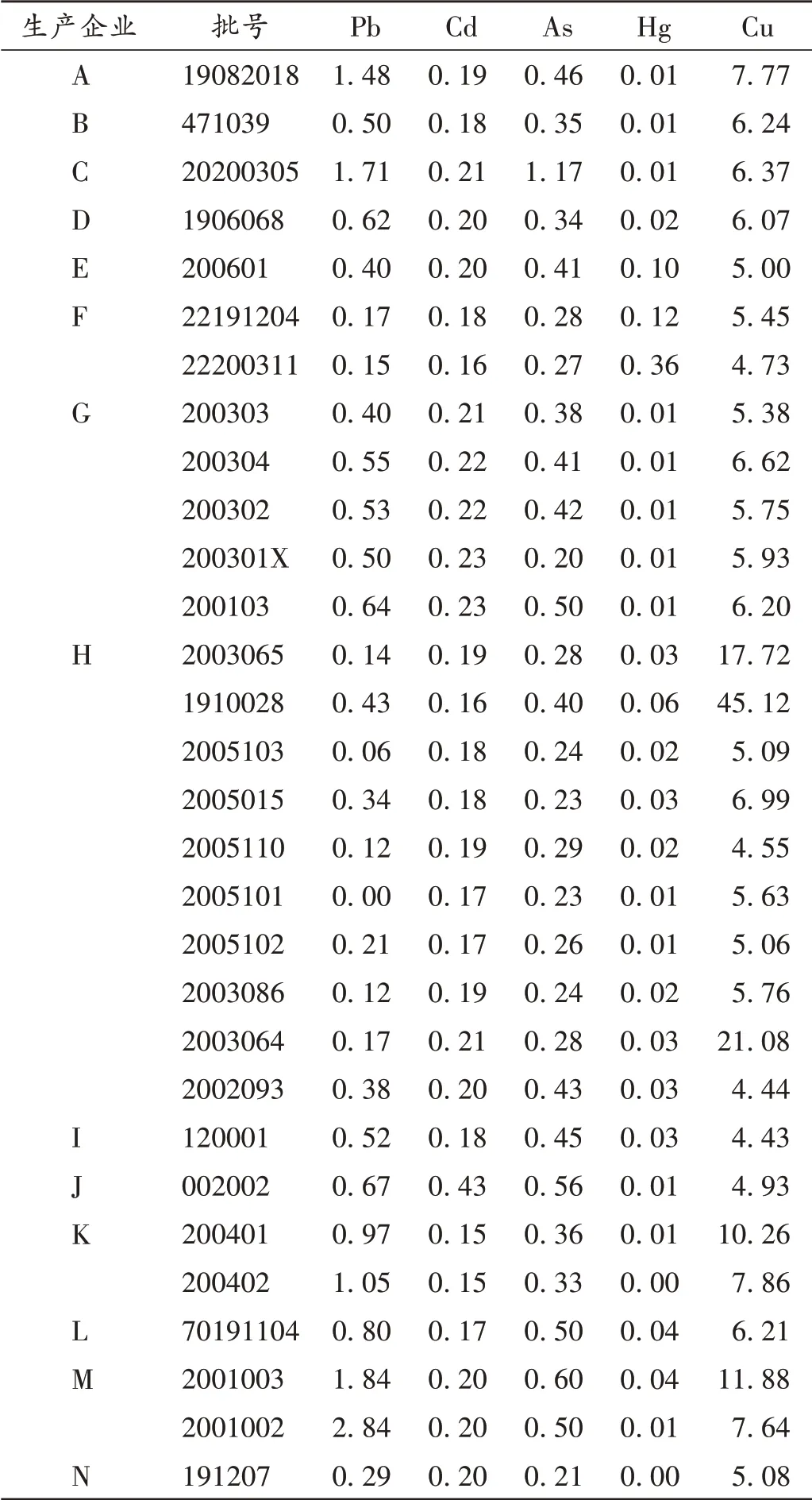
表3 样品中重金属及有害元素含量测定结果(μg/g)Tab.3 Results of content determination of heavy metals and harmful elements in samples(μg/g)
参考2020年版《中国药典(四部)》中植物类中药材重金属及有害元素限度规定,即Cu ≤20 mg/ kg,As ≤2 mg/kg,Cd ≤1 mg/kg,Pb ≤5 mg/kg,Hg ≤0.2 mg/kg。30 批样品中,有2 个生产企业Cu 超标,有1 个生产企业Hg 超标。相较于中药材,中成药服用量及疗程确切,故通过计算每周的重金属摄入量,并与每周耐受摄入量(Pb=0.025 mg/kg,Cd=0.007 mg/kg,As=0.015 mg/kg,Hg=1.6 μg/kg,Cu=0.5 mg/kg)[10]进行比较,以评价样品的安全风险。公式为Xi'=Xi×I/W[10-11],式中,Xi'为样品中某种重金属每千克体质量的每周摄入量;Xi为样品中某种重金属含量;I为样品的每周最大服用量;W为正常成年人的平均体质量,取60 kg。样品每日服用量取12 g,按上述公式计算,结果各重金属及有害元素每周摄入量均低于每周耐受摄入量,表明风险较低,但长期服用是否存在安全隐患尚需进一步评估。
3 讨论
3.1 含量测定指标性成分选择
泽泻为方中臣药,其药理活性成分主要为泽泻醇类[12-13]。其中,23-乙酰泽泻醇B 为主要成分,故以泽泻中的23 - 乙酰泽泻醇B 为特征指标,建立了考察龙胆泻肝丸中泽泻质量的高效液相色谱法。
3.2 现行法定标准存在的问题
龙胆为方中君药,清肝胆实火,清下焦湿热;黄芩、栀子为臣药,助龙胆清泻肝火之功;泽泻、木通、车前子清下焦湿热;地黄、当归为佐药,补阴血;柴胡有疏肝之功效。本次抽检样品的执行标准为2015年版《中国药典(一部)》,其中仅对龙胆、栀子和黄芩进行质量控制,未控制其余药味。故本研究中进一步对泽泻进行探索性研究,建立了龙胆泻肝丸(水丸)中泽泻的含量测定方法。结合法定检验标准及探索性研究发现,不同生产企业及相同生产企业不同批次间药品的质量存在一定差异,原因可能与生产工艺、投料量和原料药质量有关。建议生产企业落实主体责任,加强原料药的质量控制,保证产品质量。
3.3 样品中重金属含量偏高
龙胆泻肝丸(水丸)方中大部分药材的药用部位为根茎,故原料药材的重金属含量可能导致成药中重金属及有害元素含量偏高。通过探索性研究发现,30 批样品中均不同程度检出了Pb,As,Cu,Cd,Hg 元素,参考2020年版《中国药典(四部)》中植物类中药材重金属及有害元素限度规定,样品存在重金属Hg和Cu含量超标问题。进一步以各元素每周摄入量评价其风险,结果各元素每周摄入量均低于每周耐受摄入量,表明风险较低,但长期服用是否存在安全隐患尚需进一步评估。
3.4 建议
中药材的质量问题与中成药的重金属污染情况密切相关,中药材的重金属污染是一个长期且复杂的问题,与中药材产地、品种、入药部位、生长环境等诸多因素密切相关。建议药品监督管理部门增强对部分生产企业的监管力度,持续强化日常监督检查与专项检查工作,警示药品生产企业加强对原料药的质量控制,消除安全隐患,从源头控制药品质量,保障临床用药安全、有效。
