肝豆状核变性动物模型的研究进展
2022-05-14杨玉龙魏涛华杨文明郝文杰钱南南江海林
杨玉龙, 魏涛华, 杨文明,3, 郝文杰, 杨 悦, 钱南南, 李 祥, 江海林
1 安徽中医药大学 研究生院, 合肥 230000; 2 安徽中医药大学第一附属医院 脑病中心,合肥 230000; 3 新安医学教育部重点实验室, 合肥 230000
肝豆状核变性又称Wilson病(Wilson’s disease, WD),是一种与铜代谢障碍有关的以铜的病理性蓄积为特征的常染色体隐性遗传病[1]。系定位于13q14.3的ATP7B基因突变引起肝细胞铜转运障碍,导致铜稳态受损,肝、脑、肾等器官铜沉积,进而产生一系列临床症状,Czonkowska等[2]通过研究发现,肝损伤是WD最早和最常见的表现。
细胞内铜稳态的调控主要有赖于两个铜转运ATP酶,ATP7A和ATP7B。在低铜环境中ATP7B将细胞质内的铜转运至囊泡进行生物学合成。当细胞内铜含量增,ATP7B则由反面高尔基体管网状结构转移至细胞质胞膜旁,以利于将多余的铜转运到细胞外[3]。随着对WD遗传基础和病理生理学认识的不断深入,寻找理想的WD动物模型已成为WD基础研究中的核心内容。目前针对WD模型方面的研究主要有离体细胞模型和动物模型。离体细胞模型主要包括皮肤成纤维细胞模型及肝细胞模型[4]。但由于离体细胞模型主要用于进行细胞水平及分子水平的研究,无法进行个体整体水平的动态研究及评估,近年来逐渐被动物模型取代。动物模型具有WD的整体特性,可以按研究需要及时采集或分批采集各种标本样品以了解疾病的发病过程及其机制;亦可严格控制实验条件,排除干扰因素,从而提高实验结果的可比性和重复性,使所得到的成果更准确[4],近年来成为Wilson病研究的热点。目前WD的动物模型主要为:(1)小鼠,如毒乳(toxic milk,TX)小鼠、Jackson毒乳(the Jackson laboratory toxic milk,TX-J)小鼠、ATP7B基因敲除(ATP7B-/-)小鼠;(2)大鼠,如Long-Evans cinnamon(LEC)大鼠、PINA和ATP7B基因有缺陷(LPP)大鼠;(3)大型哺乳动物,如Bedlington犬、拉布拉多寻回犬及北罗纳德赛羊。这些模型对研究铜的分布和代谢,肝、脑等器官病理生理表现以及疾病治疗等方面具有重要价值[5]。现将以上动物模型的国内外相关研究进展综述如下。
1 小鼠模型
小鼠与人类在基因水平上高度同源,是复制人类疾病的常用动物[6]。目前WD的小鼠主要有模型TX小鼠、TX-J小鼠及ATP7B-/-小鼠。
1.1 TX小鼠
TX小鼠是由DL品系小鼠自然突变产生,由Rauch教授[7]于1983年首次提出。其表型特征为:色素沉着减少、生长发育不良、震颤、行为运动异常。由于母鼠母乳喂养的致命影响,Rauch将这种新的突变品系命名为毒奶小鼠。
1.1.1 病理生理改变 TX小鼠约在2月龄开始出现铜的沉积,首先是肝脏和脑,以肝脏为重,至第4个月沉积最为显著,可达对照组的60~80倍[8]。到6个月大时,肝脏出现结节状纤维化、胆管增生和炎性细胞浸润。在>6月龄的小鼠肝脏中发现肝实质在形态学、超微结构及完整性方面均与正常肝细胞存在巨大差异[9]。对这些小鼠肝脏病理生理的进一步研究显示,TX小鼠和WD患者的肝脏在大体形态、组织学和超微结构异常方面有许多相似之处。除肝脏外小鼠的脑部也出现不同程度的损伤,Howell等[10]通过研究发现TX小鼠在3月龄时脑内的铜含量开始升高,尤其是大脑皮层、纹状体、丘脑、下丘脑、小脑和脑干。然而TX小鼠不同时期的脑损伤程度不同:疾病早期(3月龄)脑内有铜沉积但无明显病理损伤;疾病中期(6月龄)脑内铜、铁水平均升高,TX小鼠脑内可见明显脱髓鞘和轴突损伤,但无明显神经元坏死;在疾病的晚期(12月龄)TX小鼠脑内可观察到明显的神经细胞坏死迹象[11]。此外,与月龄相当的对照组相比,TX小鼠所有脑功能区的金属硫蛋白水平均明显更高,这可用于解释为何有些小鼠脑遭受铜毒性而症状缺乏[12]。
肾损伤也是WD常见的临床特征之一,损伤可以发生在WD的任何时期[13]。WD患者的肾脏铜沉积损伤以近端肾小管上皮细胞最明显, 远端肾小管及肾小囊也可受损[14]。由于过量的铜沉积于肾脏,引起肾小管上皮细胞扁平、基底膜增厚, 随着铜沉积的进一步加重可引起肾脏再吸收障碍而出现氨基酸尿、高钙尿症、高磷酸盐尿和蛋白尿等[15]。
1.1.2 应用研究 Chen等[16]在用200 mg/kg剂量的青霉胺治疗4月龄TX小鼠3 d后发现,小鼠血清和大脑中游离铜浓度升高而大脑中蛋白质结合铜浓度降低,持续给药10和14 d,总铜水平随之下降。游离铜的增加与皮质和基底神经节中氧化应激的增加有关,这揭示了在开始螯合治疗后WD患者神经系统症状有时出现恶化的原因。唐露露等[17]通过研究发现,与模型组比较,肝豆扶木汤高、中剂量组和青霉胺组血清ALT、AST明显降低,Alb升高,表明肝豆扶木汤具有保护肝细胞损伤的作用,并且能有效地改善肝纤维化TX小鼠的肝组织病理。Zhang等[18]研究结果表明有丝分裂与WD小鼠的神经损伤也有关,并发现肝豆灵可能通过调节pink1/parkin通路抑制海马的有丝分裂,从而对TX小鼠脑神经保护起重要作用。在另一个应用TX小鼠模型的实验中,Buck等[19]对TX小鼠进行了骨髓干细胞移植,并证明了5个月后铜代谢紊乱被部分纠正。然而,这种最初的反应并没有长期保持下去,9个月后未再观察到铜代谢和肝组织学的显著改善。由于TX小鼠与WD患者突变基因相同且肝损伤表现突出,目前已广泛应用于WD研究。
1.2 TX-J小鼠
TX-J小鼠,又被称为Jackson毒乳小鼠,是在1987年缅因州巴尔港杰克逊实验室的C3H/HeJ动物资源群体中发现的一种新的常染色体隐性突变体,其遗传缺陷源于Atp7b基因外显子8中2135位的一个自发隐性点突变,导致G712D错义,这与TX小鼠稍有差异。马萨诸塞州大学Harold Rauch教授通过等位基因测试表明,TX-J突变与原始的TX突变是等位基因[20]。
1.2.1 病理生理改变 肝脏病理表现与TX-J小鼠月龄有密切关联,纯合子TX-J小鼠在3周龄时肝脏铜水平开始升高,在3~5月龄时达到对照组的100倍。3月龄时TX-J小鼠线粒体嵴顶端发生囊性扩张,这WD患者的病理表现相同。5月龄时,线粒体复合物检测显示复合物IV活性降低25%。6月龄TX-J小鼠线粒体中可见多形性变化、基质密度增加和电子致密包体,此时肝脏细胞的细胞核也发生变化,出现核增大和核内包涵体。肝脏结节在8~12个月时形成,此时肝脏大体形态相对正常,铜含量高而金属硫蛋白含量低。Jończy等[21]用罗丹宁染色肝脏切片发现TX-J中的铜不仅在肝实质细胞中积累,也可沉积在非实质细胞中。
与TX小鼠相同,在TX-J小鼠的神经系统中也发现了铜的沉积。相关研究发现TX-J小鼠在3个月大的时候就表现出丘脑和豆状核的铜过载。在小鼠12月龄时,其大脑纹状体、海马体和小脑中的铜浓度增加,但此时大脑皮层中的铜浓度没有变化[22]。随着铜的不断沉积,大脑皮层中的铜浓度也有所升高[23]。当对其行为进行分析时发现,TX-J小鼠的行为也有轻微异常,其中包括偏好使用前肢及动作笨拙等。
1.2.2 应用研究 尽管TX-J小鼠发现较晚,但一些重要的WD干预和治疗研究已经广泛使用该模型并取得了很好的效果。如一项描述铜螯合剂青霉胺对脑铜代谢影响的研究就是在TX-J小鼠中进行的,该研究使用青霉胺对TX-J小鼠灌胃14 d后发现小鼠体内游离铜的含量增加而蛋白质结合铜浓度的含量降低。另外,Mordaunt等[24]发现与野生型小鼠相比,TX-J小鼠的胚胎肝脏中Txn1基因的表达显著更高,在对母体补充四周的胆碱饮食后,表达可恢复到野生型水平。综上所述,TX-J小鼠是一种较理想的WD模型,由于铜沉积出现较早,因此较适合进行铜代谢等方面研究。
1.3 ATP7B-/-小鼠
近年来随着基因工程的快速发展,利用同源重组技术敲除ATP7B基因第2外显子的转基因小鼠也越来越多的被用于WD研究。
1.3.1 病理生理改变 ATP7B-/-小鼠主要表现有低铜蓝蛋白血症、尿铜增加及肝脏铜沉积,与其他模型相比发病较早且肝损伤更严重。ATP7B-/-小鼠的肝脏病理损伤程度取决于铜暴露的时间和细胞内铜的分布。肝损伤包括早期超微结构改变、脂肪变性和轻度炎症(1.5月龄时),随后出现肝炎、发育不良和晚期坏死性炎症(3~5月龄时)。这些变化伴随的是胆管增生、纤维化的发展,甚至是后期(9月龄)的肿瘤增生。然而,大多数小鼠在严重肝炎中存活下来,并在肝脏的大部分区域表现出显著的再生。因此,ATP7B-/-小鼠不仅是研究铜中毒病理的有效模型,而且为研究铜中毒的代偿机制和防御机制提供了途径。此外,有关研究[25]表明在小鼠11月龄时脑实质中的铜积累增加了2倍。目前对于ATP7B-/-小鼠神经系统表现的研究还相对较少,有学者推测ATP7B-/-小鼠明显缺乏神经系统异常表现可能是由ATP7A的功能代偿所致,有关机制有待进一步研究探索。
1.3.2 应用研究 肝脏中的铜含量较高使ATP7B-/-小鼠成为有价值的疗效评估模型。Roybal等[26]在另一份报告中指出,妊娠早期肝细胞移植可显著改善ATP7B-/-小鼠的铜浓度并降低肝脏病理损伤。同时,此研究也为WD子宫内基因治疗的有效性提供了依据。目前ATP7B基因敲除小鼠的研究重点是针对小鼠铜和脂质代谢受损的药物治疗,但其制备复杂导致目前应用尚不广泛。但随着分子生物学和基因工程技术的进一步发展, ATP7B-/-小鼠将成为WD动物模型研究的新方向。
2 大鼠模型
2.1 LEC大鼠
LEC大鼠是从Long-Evans大鼠群体中分离出来的突变大鼠的自交系,其与人类基因同源性达80%以上。LEC大鼠主要表现出自发性肝铜异常积聚伴随低血清铜和低铜蓝蛋白,由于此与WD的表现类似,因而被应用于WD的研究。LEC大鼠约4月龄时出现暴发性肝炎或暴发性肝衰竭、转氨酶和胆红素升高及部分或大量肝细胞坏死,病死率>30%~40%,存活下来的大鼠多在12月龄时发生纤维化并伴有肝细胞癌和胆管癌。
2.1.1 病理生理改变 LEC大鼠的肝脏病理变化突出最早被应用于肝炎和肝癌的研究,后发现其具有与WD相似的生化特征和临床表现而广泛应用于WD的研究[4]。在大鼠6周龄时,肝组织学显示细胞核大小发生改变,肝细胞膨胀,核分裂象增多;在黄疸出现之前的疾病早期阶段,可出现细胞凋亡、Kupffer细胞和多形核白细胞数量增加;严重黄疸和胆红素升高时,肝脏病理表现出胆汁淤积、肝细胞坏死和红细胞吞噬。微阵列分析[27]表明,LEC大鼠肝疾病的进展和肝铜积累与细胞色素P450相关的基因转录水平上调、氧化应激、DNA损伤和凋亡相关。其中氧化应激机制主要包括:超氧化物歧化酶活性增加,谷胱甘肽比(GSH/GSSG)降低,以及肝脏硫代巴比妥酸活性物质水平显著升高[28]。Sternlieb等[29]发现电镜下大鼠线粒体基质密度明显变化,嵴出现延伸、扩张、堆积或消失,基质内含物有电子致密沉积。蛋白质组学分析也证实了线粒体基质蛋白表达水平的升高[30]。线粒体是铜中毒的主要靶点,铜中毒导致线粒体膜交联和解体,最终导致肝细胞死亡[31];12周龄时LEC大鼠表现出甘油三酯、游离胆固醇和胆固醇酯升高,有研究[32]显示肝脏病理和肝铜积累与脂代谢的改变也有关联。
与肝脏病理学相比,LEC大鼠的神经系统表现和脑病理学研究较少。Hayashi等[33]发现大脑中的脱氧核糖核酸单链在24周时出现断裂,铜在LEC大鼠的所有大脑区域积累,并在大约24周龄达到峰值。
2.1.2 应用研究 LEC大鼠模型目前在国内外已经得到了广泛应用。有学者通过实验[34]证实灌胃青霉胺12周可以改善LEC大鼠的肝转氨酶和组织学,从而预防肝炎的发生。早期应用曲恩汀螯合铜可预防肝炎的发生,显著改善肝组织学,并在长期内减少肝细胞癌和胆管纤维化的发生。急性肝炎发作后早期给予大鼠四硫钼酸盐可以减轻肝损伤[35]。与空白对照组相比,锌可以预防LEC大鼠肝炎的发展,并提高其存活率,有学者猜测其潜在机制可能与金属硫蛋白的肝转录水平增加和氧化应激降低有关。
近些年在LEC大鼠上进行的研究阐明了基于肝细胞和干细胞移植以及基因技术治疗WD的可能性。临床上许多WD患者需要进行肝移植,但由于供体器官短缺限制了此治疗手段的应用,因此通过细胞或基因治疗来永久治愈患者就成为WD治疗的一大突破。Jaber等[36]研究发现细胞治疗是可行的,移植的肝细胞可整合到肝实质并能恢复缺乏的功能。有关研究[37]表明,通过门静脉向LEC大鼠肝脏注入ATP7B转导的骨髓间充质干细胞与ATP7B表达增加、铜蓝蛋白水平升高、肝脏铜浓度降低、AST和ALT水平降低相关,且在门静脉输注干细胞前进行放疗预处理和缺血再灌注,可获得最佳的肝移植和再增殖效果。综上所述,LEC大鼠是一种铜快速积累模型,在4月龄时由于严重肝炎和之后的肝细胞癌导致病死率很高。由于其肝病进展迅速,因此特别适合用于进行干预研究。
2.2 LPP大鼠
为了消除非ATP7B突变对表型的影响,Ahmed等[38]将LEC大鼠与PVG大鼠杂交,后者为野生型,具有NAT(N-乙酰基转移酶)、ATP7B基因和正常毛色,这一过程产生了具有野生型大鼠NAT和毛色但ATP7B发生突变的新鼠种,称为LPP大鼠。LPP大鼠自出生后肝铜逐渐积累,并在90天左右出现肝生化异常,一旦肝疾病迅速进展,未经治疗的LPP大鼠可在30天内死亡[39]。
2.2.1 病理生理改变 与LEC大鼠相似,LPP大鼠的主要特征是肝硬化、严重黄疸,并经常在4月龄死亡[38]。Lichtmannegger等[40]研究发现LPP肝脏的显微外观与WD患者相似,表现出进行性肝纤维化和线粒体异常。
2.2.2 应用研究 有研究[40]表明甲烷氧化菌素作为一种长期螯合剂在治疗LPP大鼠急性肝衰竭方面有效,通过每天注射两次持续1周可恢复肝脏铜水平、肝功能和肝质量,并可防止大鼠死亡。
3 其他大型哺乳动物模型
一些大型哺乳动物在铜代谢方面也存在遗传缺陷,均表现出铜在肝脏中积累和铜毒性,例如犬(杜宾犬、拉布拉多寻回犬、Bedlington犬)和北罗纳德赛羊等。然而其潜在的遗传缺陷与WD不同,故作为WD模型的作用是有限的。下面以Bedlington犬、拉布拉多寻回犬及北罗纳德赛羊进行举例。
3.1 Bedlington犬 Bedlington犬最早也曾被当作Wilson病的动物模型。由于肝铜的聚集引起肝损伤和继发性溶血并表现出与Wilson病患者相似的肝纤维化和肝硬化的肝铜中毒迹象而曾被用作Wilson病动物模型进行铜负荷的相关研究[41]。然而,其潜在的遗传缺陷是在COMMD1基因中发现的而非ATP7B基因[42]。虽然其肝脏铜的积聚和肝脏病理与WD相似,但与啮齿动物模型一样,不存在明显的神经系统缺陷且铜蓝蛋白浓度正常,故目前该模型较少被使用。
3.2 拉布拉多寻回犬 2016年,一项关于拉布拉多寻回犬铜中毒的全基因组关联(GWAS)研究[43]表明,C端ATP7B的精氨酸至谷氨酰胺突变与肝脏铜含量增加有关联,从而将其确立为进一步的Wilson病动物模型。
3.3 北罗纳德赛羊 北罗纳德赛羊是另一个有趣的哺乳动物肝脏和神经系统铜积累模型。然而,与犬类模型一样,其在临床上和遗传学上与WD不同[44]。其潜在的基因缺陷目前仍然未知。然而,该模型对于研究铜在大脑中的积累等方面有一定的重要性[42]。此外,这种动物模型可能有助于识别能够抑制肝星状细胞激活和增殖的药物,这已被认为是治疗肝纤维化的潜在靶点[45]。
以上几种大型哺乳动物对于WD的研究有一定价值,为WD的潜在模型,有待进一步探索发掘。
每种动物模型都有其特定的属性。一方面,大多数WD动物模型表现出肝脏和脑组织铜含量增加、脂质代谢异常、铜蓝蛋白水平低、金属硫蛋白水平增加,这些表型与WD患者相同或相似。但另一方面,有些表型与WD患者也有差异。现将一些常见动物模型的特点进行总结(表1)。
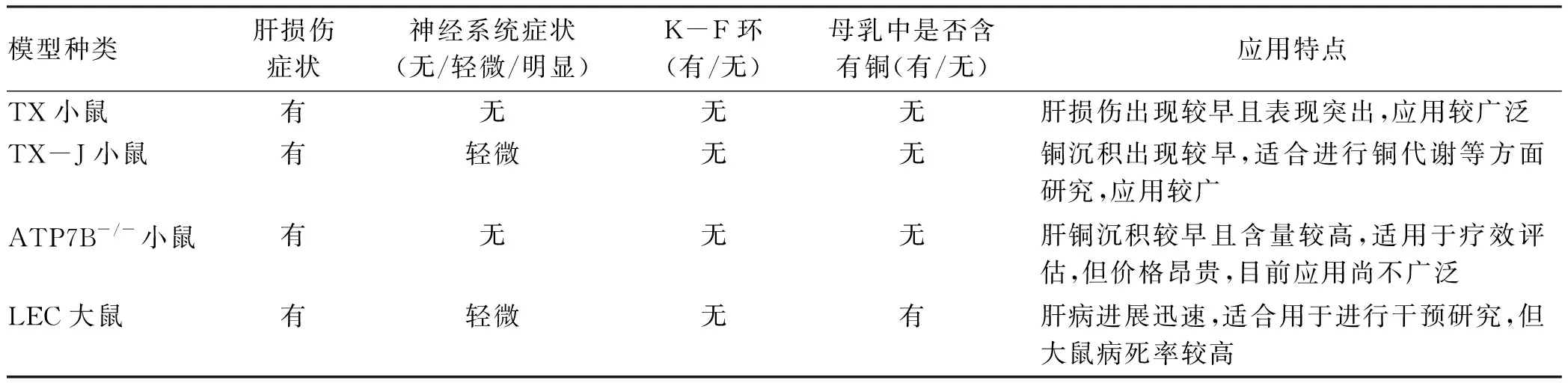
表1 常见WD动物模型特点
4 结语
一种理想的疾病动物模型对疾病的基础和临床研究意义重大,上述列举的动物模型各有优劣,其大多显示出与人类肝脏很好的相似性。从TX小鼠的轻度肝病到ATP7B-/-小鼠更明显的病理,再到LEC大鼠的暴发性肝衰竭和死亡, 为学者们提供了一系列肝病模型,有助于提高对WD肝脏病理生理的认识,但其与WD患者的表现也有明显的差异,如大多缺乏令人信服的神经症状、特定的大脑病理以及K-F环。由于神经系统病变在许多WD患者均能观察到,显然需要在这个领域进行更多的研究,需要更为理想的动物模型来用于WD相关研究。一个稳定可靠、易于复制、经济易得且能够准确反映WD患者的所有临床表型特征动物模型,将为WD的深入研究提供强力支持。
利益冲突声明:所有作者均声明不存在利益冲突。
作者贡献声明:杨玉龙、魏涛华负责课题设计,撰写论文;郝文杰、杨悦、钱南南、李祥、江海林参与收集数据,修改论文;杨文明负责拟定写作思路,指导撰写文章并最后定稿。
