重症急性胰腺炎继发区域性门脉高压致乳糜腹水1 例
2022-05-10张明君郭晓娟刘金哲任渝棠
张明君 黄 勍 郭晓娟 刘金哲 任渝棠 姜 泊
重症急性胰腺炎(SAP)的常见局部并发症包括胰腺及周围组织坏死、胰腺及胰周脓肿、胰腺假性囊肿等,SAP 还可能发生器官功能衰竭、胰性脑病、腹腔间室隔综合征等全身并发症。乳糜腹水是SAP 的罕见并发症,治疗较为困难,近20 年内鲜见文献报道。SAP 引起门脉高压并发乳糜腹水更为罕见,目前仅见国外文献报道3 例,现将清华大学附属北京清华长庚医院收治的1 例患者报道如下。
1 临床资料
患者,女性,68 岁,因“间断性上腹痛1 年,腹胀、纳差3 个月”于2020 年6 月4 日收治入院。患者入院前1 年(2019 年6 月)患SAP,在外院经保守治疗后好转出院。患者入院前10 个月(2019年8 月)复查CT 示胰腺假性囊肿形成(80×53×119 mm),门脉系统受压,显示不清(图1)。患者入院前3 个月(2020 年3 月)因腹胀、纳差在外院就诊,实验室检查示血红蛋白(Hb)99 g/L,白蛋白(ALB)29 g/L,其余血常规指标、生物化学指标、淀粉酶、脂肪酶均未见异常,腹部CT 示腹腔、盆腔大量积液,肝内、外胆管扩张,利尿效果欠佳。其后患者腹胀逐渐加重,2020 年4 月在本院急诊行腹腔穿刺引流腹水,腹水外观浑浊,呈乳黄色(图2),比重1.013,李凡他试验阳性,有核细胞108 个/μL,单核细胞占87.4%,白细胞(WBC)103 个/μL,红细胞(RBC)0 个/μL,总蛋白(TP)<20 g/L,乳酸脱氢酶(LDH)61 U/L,ALB<10 U/L,腺苷脱氨酶(ADA)2.3 U/L,三酰甘油(TG)4.32 mmol/L。同期血液生物化学指标ALB 28.2 g/L,TG 0.65 mmol/L。发病1 年期间,无腹泻、皮疹、关节痛、口腔溃疡、雷诺现象,纳差,大便正常,体质量下降25 kg,利尿后尿量1 000 mL/d。既往无特殊用药史,无脂肪肝、病毒性肝炎病史,无吸烟、饮酒史,无糖尿病、冠心病、高血压病史。入院查体:贫血貌,腹膨隆,腹壁静脉显露,脐上静脉血流向上,脐下静脉血流向下,腹软,无压痛、反跳痛及肌紧张,肝、脾触诊不满意,Murphy 征阴性,全腹叩诊浊音,液波震颤阳性,肝区、脾区叩痛阴性,肠鸣音较弱1 次/min,心、肺查体无异常。
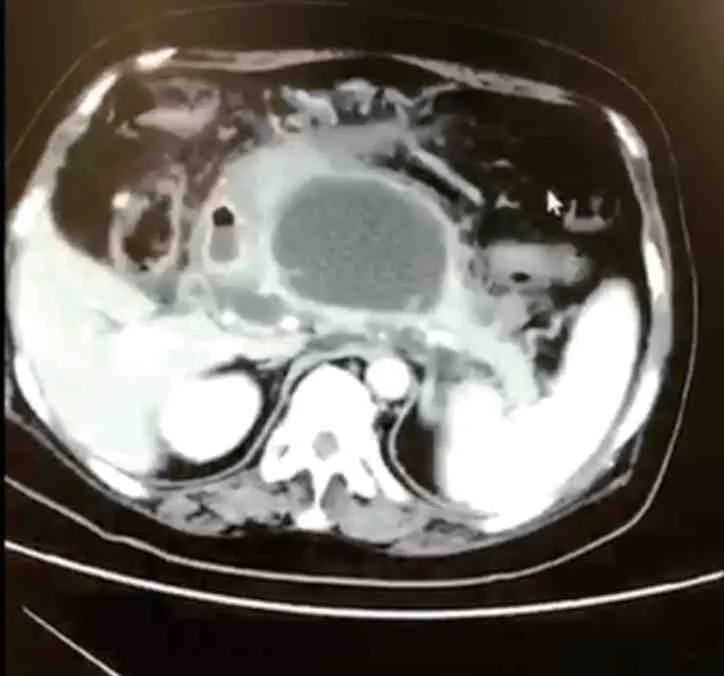
图1 2019 年8 月腹部CT 图像
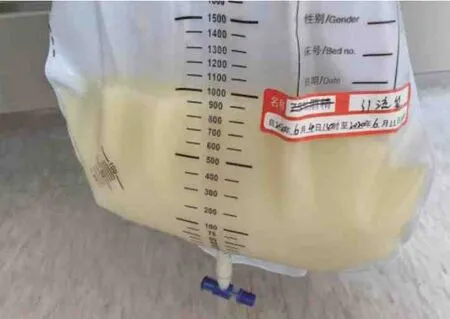
图2 腹水外观浑浊,呈乳黄色
患者入院后多次腹水检测均显示血清腹水白蛋白梯度(SAAG)>11 g/L,自身免疫性肝病抗体谱、抗可溶性抗原(ENA)抗体谱、抗中性粒细胞胞浆抗体(ANCA)、抗心磷脂抗体(ACA)、狼疮抗凝物、补体、免疫球蛋白、蛋白C、蛋白S 均未见明显异常,HBV、丙型肝炎病毒(HCV)、EB 病毒(EBV)、巨细胞病毒(CMV)等肝脏病毒学指标均阴性,血清铜蓝蛋白阴性。腹部CT(2020 年6 月)示肝脏形态正常,脾脏不大,胰腺头颈部显示不清,无胰腺实质钙化、胰管扩张等,胆总管末端变窄,继发上游肝内、外胆管扩张,门脉海绵样变性,腹腔、盆腔大量积液(图3)。胃镜(2020 年6 月)可见食道下段轻度静脉曲张,胃窦后壁静脉曲张(图4)。血管超声示门静脉主干及肝内分支管腔纤细,闭塞可能,周围侧枝形成。肺动脉CT示左肺上叶、右肺下叶肺动脉栓塞。予禁食、肠外营养、生长抑素、利尿、腹腔引流治疗,并予低分子肝素、利伐沙班抗凝。

图3 2020 年6 月腹部CT 图像 A 肝脏形态正常,大量腹水,胃壁静脉曲张 B 脾脏不大,脾静脉不宽,门脉主干显示不清,侧枝循环形成 C 胰头结构不清,未见假性囊肿 D 大量腹水,门脉海绵样变性
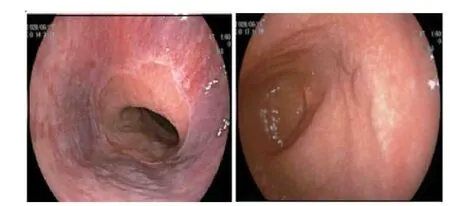
图4 2020 年6 月胃镜图像 A 食管下段静脉曲张B 胃窦后壁静脉曲张
分析腹水的病因:患者住院期间多次腹水检测均显示SAAG>11 g/L,故考虑为门脉高压性腹水。门脉高压性腹水的病因主要包括:(1)肝前性门脉或脾静脉血栓、肿瘤、囊肿压迫等;(2)肝性各种原因所致的肝硬化;(3)肝后性 布加综合征、缩窄性心包炎、右心功能不全等。患者无脂肪肝、病毒性肝炎等肝病病史,无特殊用药史,无饮酒史,入院后肝脏病毒学检测、自身免疫性肝病抗体谱等检查均为阴性、多次影像学检查均提示肝脏形态正常,可排除肝性因素。患者无肝脏体积增大、门脉增宽等肝淤血征象,可以排除肝后性因素。患者的影像学检查结果提示门脉主干及肝内分支管腔纤细、闭塞可能,周围侧枝形成,符合门脉海绵样变。因此,考虑患者门脉高压的原因为肝前性因素。
分析门脉闭塞的病因:患者既往体健,患SAP后CT 示并发巨大胰腺假性囊肿,门脉系统受压,可导致局部血流缓慢,加之SAP 患者血液呈高凝状态,这些均是血栓形成的危险因素,因此本课题组推测患者的门脉系统曾有血栓形成。患者存在肺动脉血栓也证明了患者有易栓体质。入院后的检查未见门脉血栓,猜测血栓可能已自溶,而门脉海绵样变性提示门脉曾有血栓形成。此外,胰腺炎可引起肠道功能障碍,包括肠道屏障损伤和动力障碍,导致肠道菌群失调等,肠道微生态改变可能也参与了血栓形成过程。门脉闭塞的常见原因还包括肿瘤、寄生虫、医源性因素、自身免疫性疾病相关性血管炎等,患者均无相关病史及影像学证据,故可排除。由此可见,胰腺假性囊肿及门脉血栓形成是导致患者门脉闭塞的病因。
鉴别乳糜腹水的病因十分困难,患者同时存在胰腺炎及区域性门脉高压,两者均可引起乳糜腹水。2020 年9 月对患者行门静脉造影,结果提示门静脉远端和肠系膜上静脉交汇处可见4 cm 长的闭塞,遂行门静脉支架置入术(图5)。术后患者门脉高压得到缓解,逐渐恢复正常饮食,继续予利尿、引流腹水,患者腹围逐渐缩小,病情好转,于2020 年10 月出院。2021 年2 月随访患者,患者已过渡为正常饮食,体质量升高5 kg,2021 年2 月复查CT示腹腔、盆腔仅有少量积液。结合随访结果,考虑该患者乳糜腹水的病因为SAP 所致的区域性门脉高压。
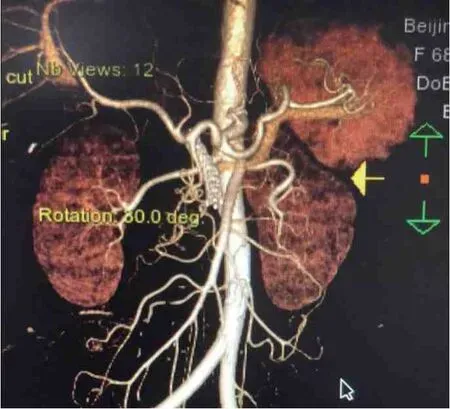
图5 2020 年9 月门静脉支架置入后的门静脉造影图像
2 讨论
乳糜腹水是由各种原因引起的胸导管、腹腔淋巴管及其分支损伤、破裂或阻塞导致淋巴液回流障碍,使来自肠道的淋巴液进入腹腔而形成[1]。腹水中TG>1.25 mmol/L、淋巴管核素显像或直接淋巴管造影示造影剂进入腹腔,三者均可诊断乳糜腹水。引起乳糜腹水的主要病因包括肝硬化门脉高压症、恶性肿瘤、结核及丝虫病等感染性疾病、外伤及手术创伤、先天性疾病、自身免疫性疾病等,急性和慢性胰腺炎是引起乳糜腹水的罕见病因[1-2]。
胰腺炎引起乳糜腹水的机制主要是胰腺位于乳糜池前方,位置毗邻,发生胰腺炎时,水肿的胰腺、胰腺假性囊肿、胰周脓肿可直接压迫淋巴管导致淋巴管破裂或阻塞,同时渗出的炎性物质、胰酶等可腐蚀淋巴管。引起乳糜腹水的多为SAP,也有文献报道有单纯水肿型胰腺炎病史的患者在胆囊切除术中偶然发现少量乳糜腹水[3]。因此,推测急性胰腺炎引起乳糜腹水的患者并不罕见,少量乳糜腹水难以诊断,且对病情影响较小,可自行吸收。
门脉高压也可引起乳糜腹水,门脉高压使得肝脏及胃肠淋巴液回流增多,淋巴管压力升高,引起胸导管内回流受限,导致淋巴管渗出或破裂,使得乳糜液进入腹腔形成乳糜腹水,门脉高压所致腹水多为漏出液,其中0.5%~1%为乳糜性[4]。刘揆亮等[5]报道了34 例肝硬化门脉高压所致乳糜腹水病例。
除了积极治疗原发疾病外,乳糜腹水的治疗以保守治疗为主,包括:(1)无脂、低脂饮食 中链脂肪酸经肠道吸收后,不经过淋巴管,直接弥散入门脉系统,可减少淋巴液形成,在SAP 患者疾病早期给予肠内营养有利于抑制肠道菌群移位,减少感染相关并发症的发生和降低病死率[6]。徐晓帆等[7]采用无脂肠内营养治疗SAP 后乳糜腹水患者取得了满意效果。(2)全肠外营养 可抑制胃液和肠液的分泌、减少淋巴液的形成和流动。(3)生长抑素及其类似物 可抑制胃肠道激素的释放,减少胃肠液、胰液的分泌,降低门脉压力,减少肠道淋巴液的生成[8]。(4)腹腔引流 对经4~6 周保守治疗无效的患者可考虑手术治疗(如解除病因的手术、缝扎乳糜漏孔、分流手术等)。
目前国外仅报道了3 例SAP 导致门脉高压并发乳糜腹水的患者,其中2 例经门静脉支架置入术以缓解门脉高压而治愈[9-10],1 例经保守治疗(全肠外营养+生长抑素)治愈[11]。本病例是SAP 导致区域性门脉高压并发乳糜腹水患者,经保守治疗效果不佳,遂行门静脉支架置入术以缓解门脉高压,术后腹水逐渐消退,因此考虑引起该患者发生乳糜腹水的原因为胰源性区域性门脉高压。
