壳寡糖纳米硒的工艺优化研究
2022-05-09叶大天任祥雨夏磊林昌宇肖云玉闻正顺
叶大天 任祥雨 夏磊 林昌宇 肖云玉 闻正顺

摘要 [目的]优化壳寡糖納米硒的合成工艺。[方法]采用单因素探究壳寡糖与亚硒酸钠的比例、乙酸质量浓度和反应时间对纳米粒子粒径、PDI和电位的影响,并以PDI为主要判断依据,电位为次要判断依据,进行正交试验,优化反应的条件。[结果]最优工艺条件为壳寡糖与亚硒酸钠的比例为16∶1,乙酸质量浓度为3%,反应时间为2.5 d,得到壳寡糖纳米硒的PDI为0.238,电位为50.36 mV。通过方差分析可知,反应条件对PDI影响由大到小依次为壳寡糖与亚硒酸钠的比例>反应时间>乙酸质量浓度,反应条件对电位影响由大到小依次为反应时间>壳寡糖与亚硒酸钠的比例>乙酸质量浓度。[结论]该研究优化了壳寡糖纳米硒的合成条件,为壳寡糖纳米硒的进一步开发利用提供了支持。
关键词 壳寡糖;纳米硒;合成工艺;优化;正交试验
中图分类号 TB 383.1 文献标识码 A 文章编号 0517-6611(2022)08-0156-04
doi:10.3969/j.issn.0517-6611.2022.08.043
开放科学(资源服务)标识码(OSID):
Study on Process Optimization of Chitooligosaccharides-Selenium Nanoparticles
YE Da-tian 1, REN Xiang-yu 1, XIA Lei 2 et al
(1.School of Food Science and Pharmaceutics, Zhejiang Ocean University,Zhoushan,Zhejiang 316022;2.Zhoushan Center of Agricultural Products Quality and Safety Supervision and Management, Zhoushan, Zhejiang 316021)
Abstract [Objective]To optimize the synthesis process of chitooligosaccharides-selenium nanoparticles.[Method] The single factor was used to explore the influence of the ratio of chitooligosaccharide to sodium selenite, the mass concentration of acetic acid and the reaction time on the particle size, PDI and potential of nanoparticles. Using PDI as the main judgment basis and potential as the secondary judgment basis, an orthogonal experiment was carried out to optimize the reaction conditions.[Result]The best process conditions for synthesizing chitooligosaccharides-selenium nanoparticles were the ratio of chitooligosaccharides to sodium selenite 16∶1, 3% acetic acid mass concentration, and the reaction time 2.5 days. Under this condition, the PDI of the chitooligosaccharides-selenium nanoparticles was 0.238 and the potential was 50.36 mV.The variance analysis of the experimental factors showed that the effect of reaction conditions on PDI was in the order of the ratio of chitooligosaccharide to sodium selenite > reaction time > acetic acid mass concentration, and the effect of reaction conditions on potential is in the order of reaction time > the ratio of chitooligosaccharide to sodium selenite > acetic acid mass concentration.[Conclusion] The synthesis conditions of chitooligosaccharides-selenium nanoparticles are optimized, which provides support for the further development and utilization of chitooligosaccharides-selenium nanoparticles.
Key words Chitooligosaccharides;Nano-selenium;Synthesis process;Optimization;Orthogonal experiment
硒是人体和动物体内许多抗氧化酶如谷胱甘肽过氧化物酶和硒蛋白P的必需微量元素和组成部分。硒缺乏会导致各种临床后果,包括癌症、心血管疾病、2型糖尿病和肺部疾病 [1]。因此,补充硒非常重要,而膳食硒的有效剂量和毒性剂量之间的差距很小,其生物利用度和生物活性受到很大限制 [2]。研究表明,零氧化态的红色硒纳米粒子具有优异的生物利用度和低毒性 [3]。由于红色硒纳米粒子容易转化为热力学稳定的灰色类似物,而这种类似物生物学上是惰性的,因此为了稳定红色的纳米硒,人们会用多糖、蛋白、多酚等作为稳定剂 [4-6]。壳寡糖又叫壳聚寡糖、低聚壳聚糖,是将壳聚糖经特殊的生物酶技术(或化学降解、微波降解技术)降解得到的一种聚合度在2~20的寡糖。壳寡糖是带正电荷阳离子碱性氨基低聚糖,其阳离子性质相当特殊,因为大多数多糖在酸性环境中通常呈中性或带负电荷。这种特性使其能够与其他带负电荷的合成或天然聚合物形成静电复合物或多层结构 [7]。有研究表明,使用壳聚糖可以作为还原剂和稳定剂合成硒纳米粒子(SeNPs),通过控制温度,简单的一锅反应合成了83~208 nm的分散良好的CS-Se纳米复合材料 [8]。该试验采用单因素研究壳寡糖与亚硒酸钠的比例、乙酸质量浓度和反应时间对纳米粒子粒径、聚合物分散性指数(polydispersity index,PDI)和电位的影响,并以PDI为主要判断依据,电位为次要判断依据,进行了正交试验,对壳寡糖纳米硒的合成工艺进行优化,以期为硒纳米粒子的开发提供理论依据。
1 材料与方法
1.1 試验材料与试剂
壳寡糖(浙江金壳药业股份有限公司);亚硒酸钠(长沙哈林化工有限公司);乙酸(分析纯AR,国药)。
1.2 试验仪器
LG10-2.4Axx高速离心机(北京京立离心机有限公司);AREC.T加热磁力搅拌器(意大利VELP公司);JM-B1003电子天平(上海数宜电子衡器有限公司);Zetasizer_Nano_ZS_90激光粒度仪(英国马尔文公司)。
1.3 试验方法
1.3.1 壳寡糖纳米硒粒子的制备。
将一定量的壳寡糖放入锥形瓶中,加入一定质量浓度的乙酸溶液30 mL,室温下搅拌1 h使壳寡糖充分溶解。另称量100 mg的亚硒酸钠溶于10 mL 纯水中,然后将亚硒酸钠加入壳寡糖溶液中,并在47 ℃的水浴中以1 000 r/min避光反应一定时间。将反应完成的溶液在10 000 r/min下离心取沉淀,并水洗沉淀3次,将残留的亚硒酸根除去,然后将沉淀溶于10 mL的水中备用。将0.1 g的壳寡糖放入锥形瓶中,加入3%的乙酸溶液10 mL,搅拌使壳寡糖溶解,加入先前的沉淀水溶液,室温下避光搅拌1 h后,10 000 r/min离心取沉淀,再10 000 r/min离心水洗沉淀1次,生成的橙红色溶液即为壳寡糖纳米硒待测样品。
1.3.2 粒子的粒径和PDI分析。
取少量待测样品于石英皿中,加纯水稀释到一定的浓度后,放进Zetasizer_Nano_ZS_90激光粒度仪的槽中进行粒径和PDI分析。
1.3.3 粒子的电位分析。
将待测样品吸入电解槽中,放进Zetasizer_Nano_ZS_90激光粒度仪的槽中进行电位分析。
1.3.4 单因素试验设计。
固定乙酸质量浓度为3%,反应时间为2.5 d,探究不同的壳寡糖与亚硒酸钠的比例(8∶1、10∶1、12∶1、14∶1、16∶1、18∶1,g∶g)对粒径、PDI和电位的影响。固定壳寡糖与亚硒酸钠的比例为10∶1,反应时间为2.5 d,探究不同的乙酸质量浓度(1%、2%、3%、4%、5%)对粒径、PDI和电位的影响。固定壳寡糖与亚硒酸钠的比例为10∶1,乙酸质量浓度为3%,探究不同的反应时间(1.5、2.0、2.5、3.0、3.5 d)对粒径、PDI和电位的影响。
1.3.5 正交试验设计。
由单因素的试验结果来确定各因素适宜的合成条件,通过试验的因素个数和水平数来选取正确的正交试验表,该试验选取正交表L9(3 4)进行试验(表1),确定最佳的工艺条件。
1.3.6 正交试验评判标准。
选取PDI值和电位作为壳寡糖纳米硒粒子的评判依据。PDI为主要的判断依据,电位为次要的判断依据。PDI值代表粒子的分散程度,其值越小代表粒子分布越均匀。电位的大小与粒子的稳定性有关,电位越大粒子的稳定性越好,一般粒子的电位需要大于30 mV说明粒子有较好的稳定性。
1.4 数据分析
利用 Excel 2007 进行试验数据的整理,利用 GraphPad Prism 8.0.1软件进行作图。
2 结果与分析
2.1 单因素试验
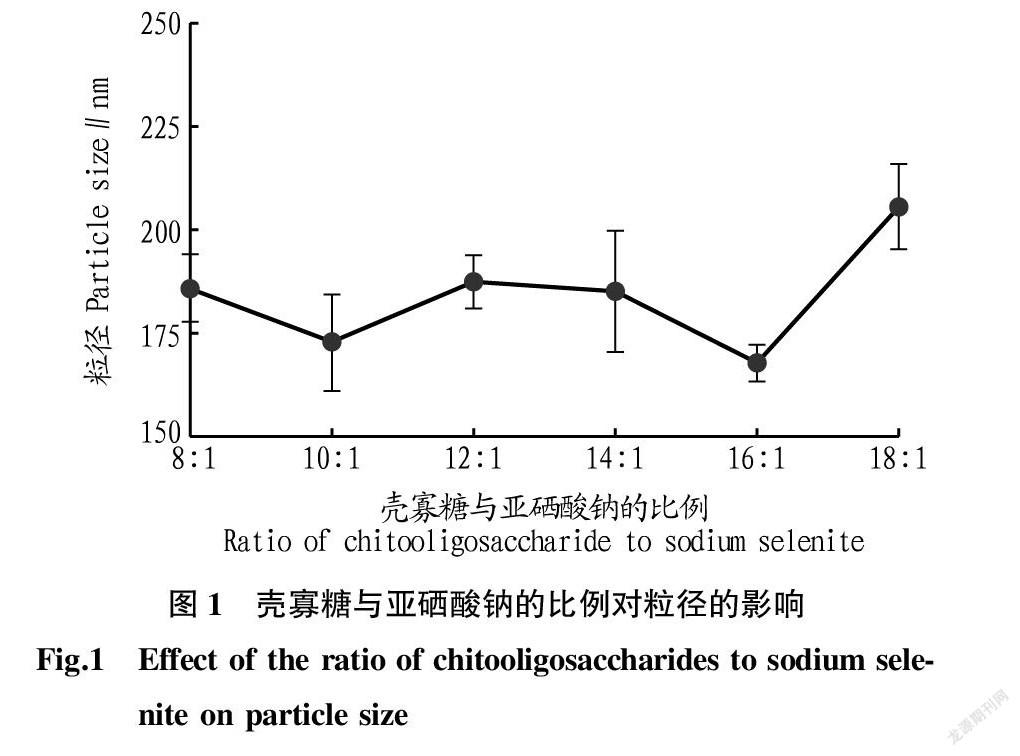
2.1.1 壳寡糖与亚硒酸钠的比例对粒径的影响。由图1可知,粒子的粒径随壳寡糖与亚硒酸钠的比例升高总体呈先平稳后增大的趋势,壳寡糖与亚硒酸钠的比例在8∶1~16∶1时,粒径在167.6~187.5 nm。而当壳寡糖与亚硒酸钠的比例从16∶1变化到18∶1时,粒径由167.6 nm上升至205.7 nm,可能是因为壳寡糖加入的量太多时,生成的纳米硒外层包裹着更多的壳寡糖。
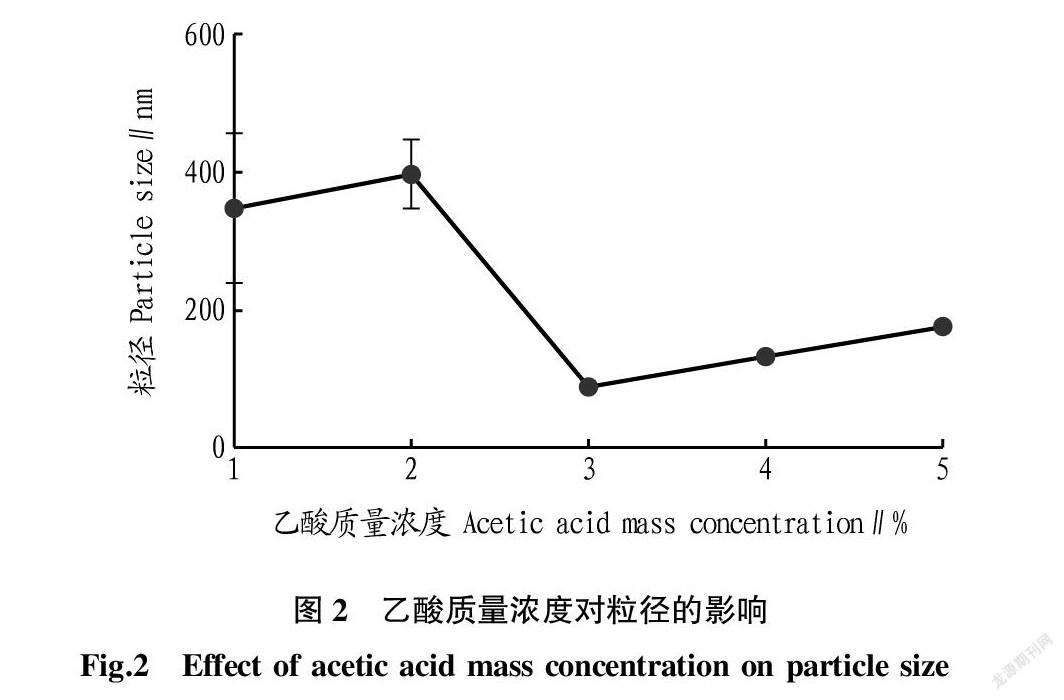
2.1.2 乙酸质量浓度对粒径的影响。由图2可知,粒子的粒径随乙酸质量浓度的上升总体呈先减小后增大的趋势,在3%的乙酸质量浓度下粒子的粒径最小,为172.7 nm。当乙酸质量浓度由2%上升至3%时,粒子的粒径由430.0 nm下降至172.7 nm,而乙酸质量浓度由3%上升至5%时,粒子的粒径由172.7 nm增加到247.0 nm。这可能是因为随着乙酸质量浓度的增大,改变了反应体系的pH,从而导致了粒径的变化。
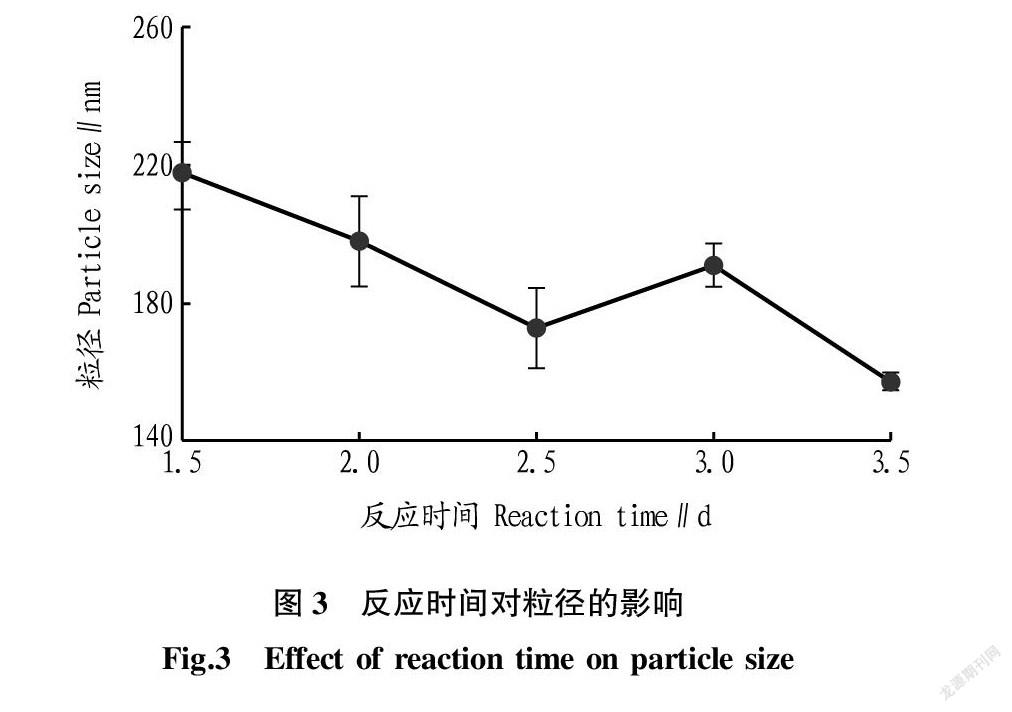
2.1.3 反应时间对粒径的影响。由图3可知,粒子的粒径随反应时间的延长总体呈下降的趋势。反应时间在1.5~3.5 d,粒径的大小由218.0 nm下降至157.2 nm。可能是因为反应时间会影响纳米粒子的产物的结晶程度,从而影响粒径的大小。
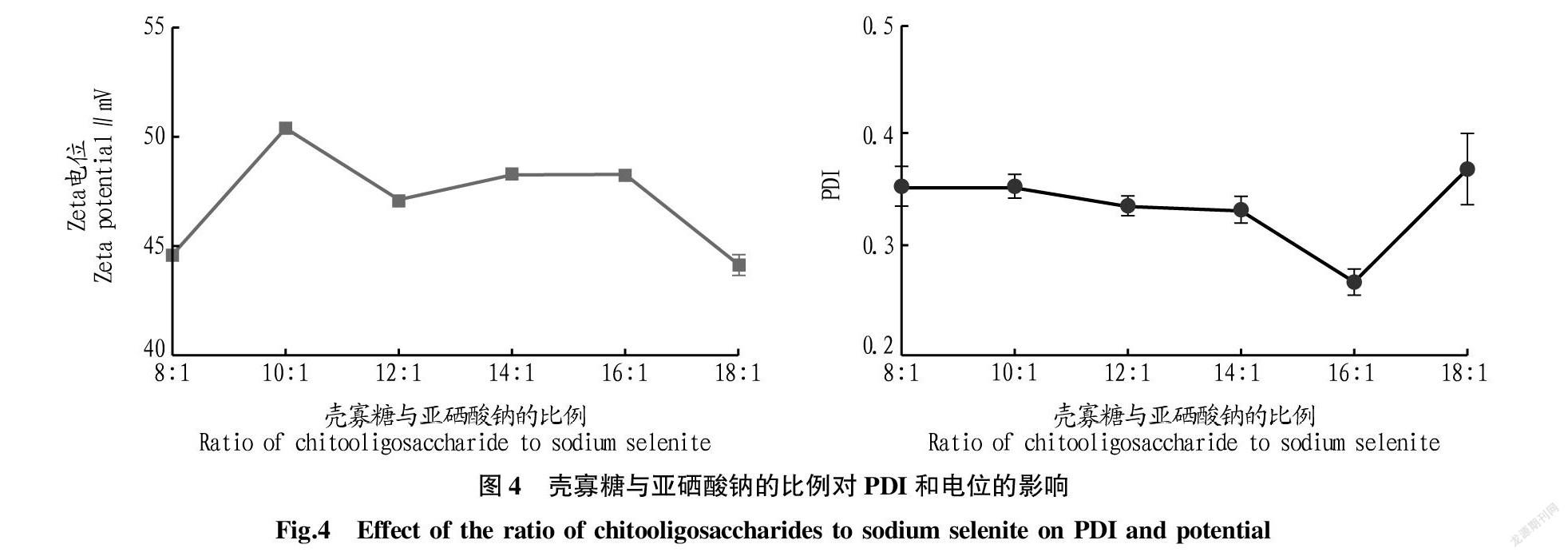
2.1.4 壳寡糖与亚硒酸钠的比例对PDI和电位的影响。由图4可知,粒子的PDI随壳寡糖与亚硒酸钠的比例升高总体呈先减小后增大的趋势,而当壳寡糖与亚硒酸钠的比例为16∶1时PDI最小,为0.269;当壳寡糖与亚硒酸钠的比例为8∶1~16∶1时,PDI缓慢减少,而壳寡糖与亚硒酸钠的比例为16∶1~18∶1时PDI增加明显。粒子的电位随壳寡糖与亚硒酸钠的比例升高总体呈先增大后平稳减小的趋势,当壳寡糖与亚硒酸钠的比例为10∶1时电位最大,为50.33 mV。综上考虑PDI为主要判断依据,兼顾电位,选择壳寡糖与亚硒酸钠的比例为14∶1、16∶1和18∶1进行正交试验。
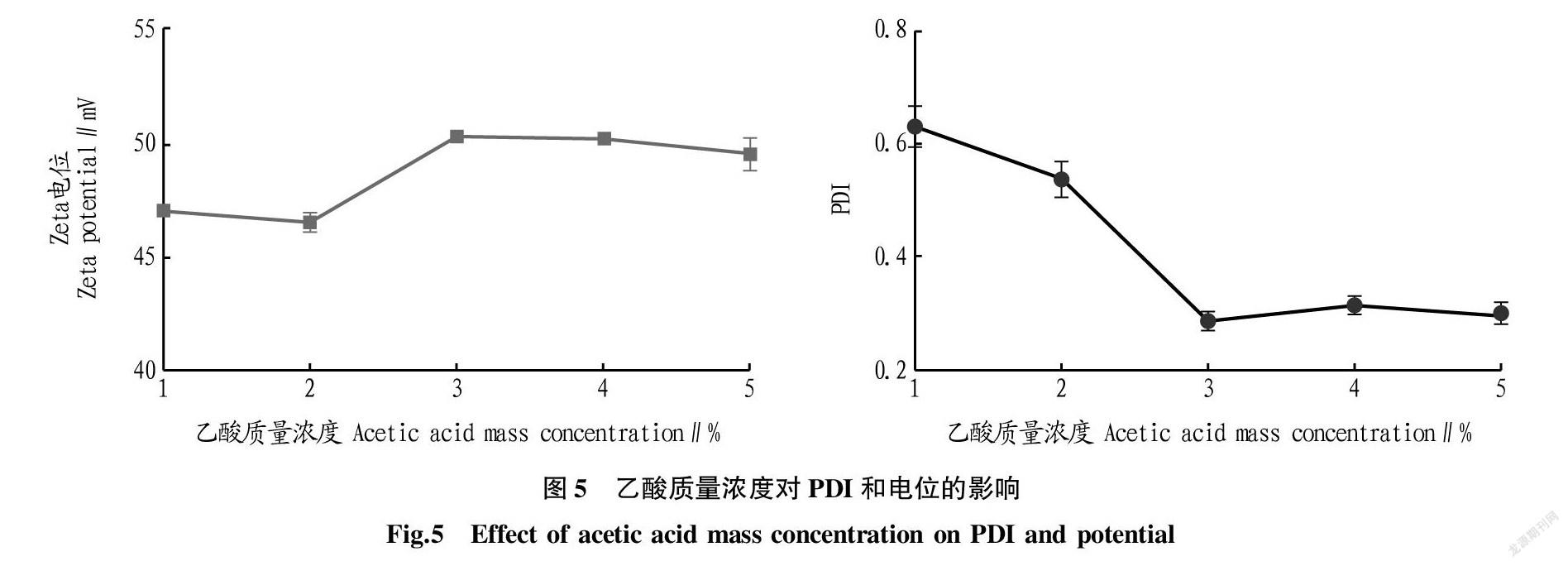
2.1.5 乙酸质量浓度对PDI和电位的影响。由图5可知,粒子的PDI随乙酸质量浓度的升高总体呈先减小后趋向平稳的趋势,而在乙酸质量浓度为3%时PDI最小,为0.286;当乙酸质量浓度在1%~3%时,PDI由0.628减少至0.286,而在3%~5%时,PDI变化不大。粒子的电位随乙酸质量浓度的升高总体呈先增大后平稳减小的趋势,当乙酸质量浓度为3%时电位最大,为50.33 mV。综上考虑PDI为主要判断依据,兼顾电位,选择乙酸质量浓度为2%、3%和4%进行正交试验。
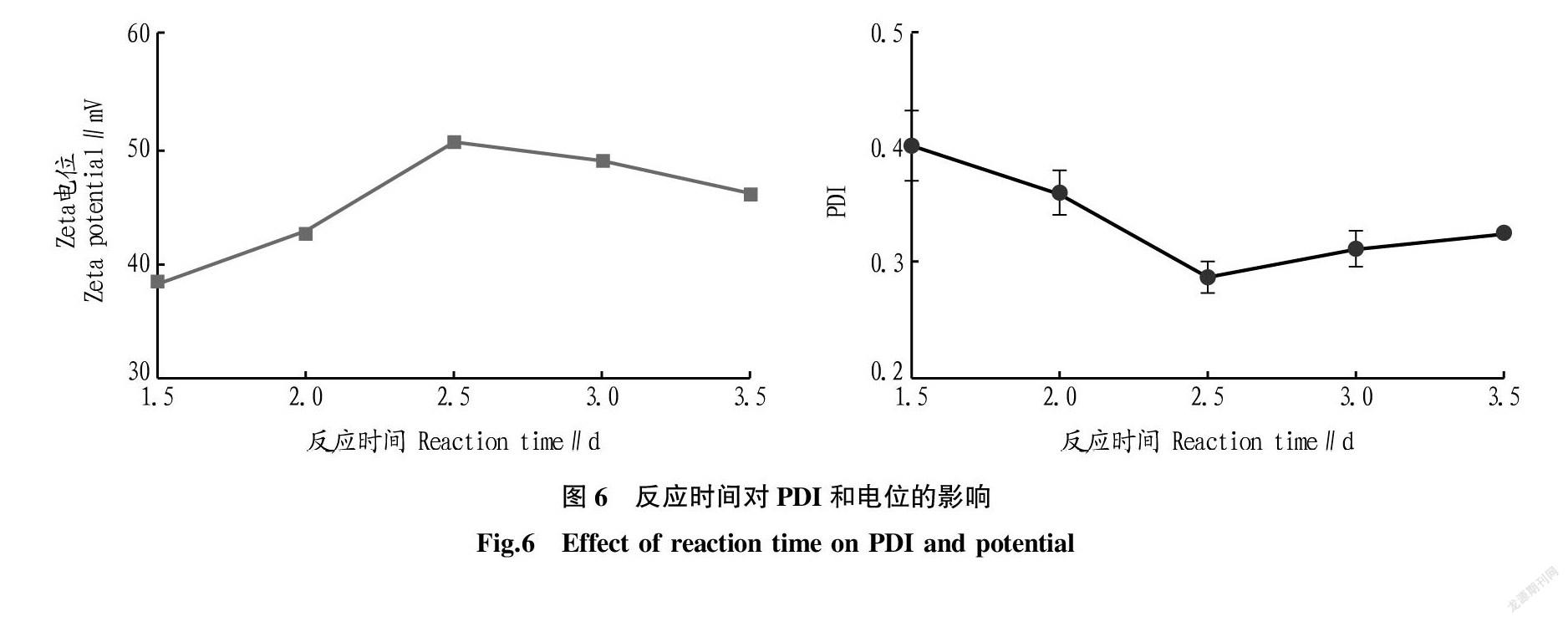
2.1.6 反应时间对PDI和电位的影响。由图6可知,粒子的PDI随反应时间的延长总体呈先减少后增大的趋势,而在反应时间为2.5 d时,PDI最小,为0.286;反应时间在1.5~2.5 d时,PDI由0.403减少至0.286,反应时间在2.5~3.5 d时,PDI由0.286增加至0.325。粒子的电位随反应时间的延长呈先增大后平稳减小的趋势,当反应时间为2.5 d时,电位最大。综上考虑PDI为主要判断依据,兼顾电位,选择2.0、2.5和3.0 d 进行正交试验。
2.2 正交试验
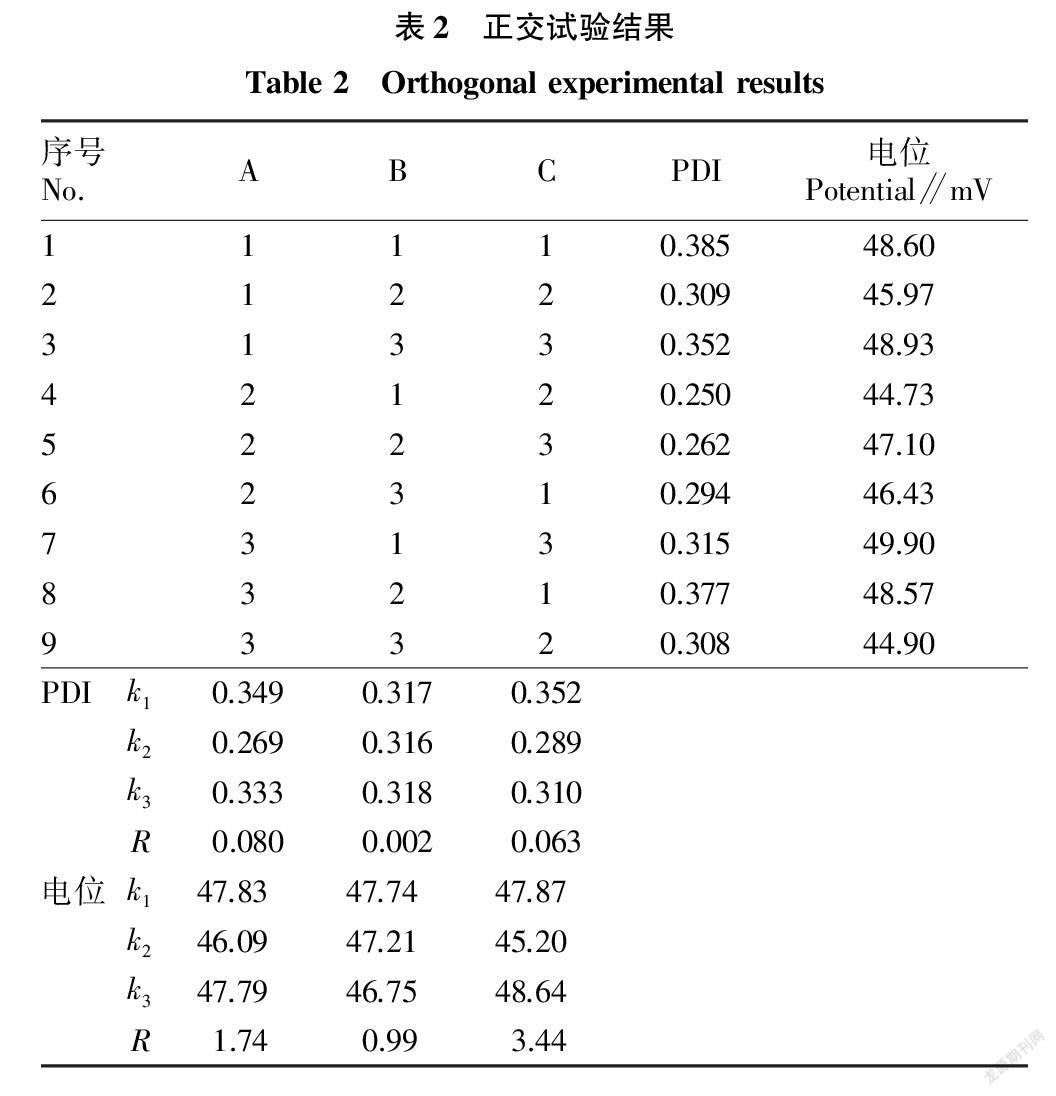
由正交试验结果(表2)可知,反应条件对PDI影响由大到小依次为壳寡糖与亚硒酸钠的比例(A)>反应时间(C)>乙酸质量浓度(B),PDI的最佳反应条件为A2B2C2;反应条件对电位影响由大到小依次为反应时间(C)>壳寡糖与亚硒酸钠的比例(A)>乙酸质量浓度(B),电位的最佳反应条件为A1B1C3,采用综合平衡法进行分析得到最优组合。对于因素A:由于PDI最佳反應条件为A2,电位最佳反应条件为A1,而A1与A2的电位相对相差不大,PDI两者相差较大,所以选择A2为最优条件。对于因素B:PDI和电位两者相差都不大,但是以PDI为主要的判断依据,因此选择B2。对于因素C:PDI最佳反应条件为C2,电位最佳反应条件为C3,两者的相对差值差不多,但是以PDI为主要的判断依据,因此选择C2。综上所述,最佳的反应条件为A2B2C2,即壳寡糖与亚硒酸钠的比例为16∶1,乙酸质量浓度为3%,反应时间为2.5 d。
按照最佳反应条件即壳寡糖与亚硒酸钠的比例为16∶1,乙酸质量浓度为3%,反应时间为2.5 d,得到壳寡糖纳米硒的PDI为0.238,电位为50.36 mV,明显优于先前在正交试验中的结果,说明该条件可行。
3 结论与讨论
纳米硒的合成方法有化学合成和生物合成 [9],化学合成采用硒盐与还原剂的还原,通常通过稳定剂防止硒原子簇生长并在胶体悬浮液中获得稳定的纳米粒子。许多方法包括物理蒸发方法、水热方法、γ-辐射还原和声化学方法被用作纳米硒合成的过程 [10-12]。水热法是常用的合成纳米硒的方法,有研究利用水热法以枸杞多糖为修饰剂和稳定剂制备枸杞多糖纳米硒 [13]。对于合成纳米硒的影响因素,pH是影响纳米粒子形成的原因之一,其主要是通过改变纳米粒子的表面化学特性而改变粒子的稳定性,因此零电位点是关键。随着pH偏离零电位点,纳米粒子的稳定性将会增大,而且pH的改变会导致纳米粒子的化学键的断裂或者合成,从而影响纳米粒子的稳定性 [14]。另外,反应时间会影响纳米粒子的结晶程度 [15]。因此,该研究采用单因素的方法研究了壳寡糖与亚硒酸钠的比例、乙酸质量浓度和反应时间对纳米粒子粒径、PDI和电位的影响,并以PDI为主要判断依据,进行了正交试验,优化了反应的条件。结果表明,反应条件对PDI影响由大到小依次为壳寡糖与亚硒酸钠的比例>反应时间>乙酸质量浓度,反应条件对电位影响由大到小依次为反应时间>壳寡糖与亚硒酸钠的比例>乙酸质量浓度,而最优工艺条件为壳寡糖与亚硒酸钠的比例为16∶1,乙酸质量浓度为3%,反应时间为2.5 d,得到壳寡糖纳米硒的PDI为0.238,电位为50.36 mV。综上所述,该研究为壳寡糖纳米硒的制备提供了科学参考。
参考文献
[1] SANTHOSH KUMAR B,PRIYADARSINI K I.Selenium nutrition:How important is it? [J].Biomedicine & preventive nutrition,2014,4(2):333-341.
[2] WANG W F,MAI K S,ZHANG W B,et al.Dietary selenium requirement and its toxicity in juvenile abalone Haliotis discus hannai Ino[J].Aquaculture,2012,330/331/332/333:42-46.
[3] TORRES S K,CAMPOS V L,LEN C G,et al.Biosynthesis of selenium nanoparticles by Pantoea agglomerans and their antioxidant activity[J].Journal of nanoparticle research,2012,14(11):1-9.
[4] ZHANG X,YAN H H,MA L,et al.Preparation and characterization of selenium nanoparticles decorated by Spirulina platensis polysaccharide[J].Journal of food biochemistry,2020,44(9):e13363.
[5] XU C L,QIAO L,GUO Y,et al.Preparation,characteristics and antioxidant activity of polysaccharides and proteins-capped selenium nanoparticles synthesized by Lactobacillus casei ATCC 393[J].Carbohydrate polymers,2018,195:576-585.
[6] MITTAL A K,KUMAR S,BANERJEE U C.Quercetin and gallic acid mediated synthesis of bimetallic(silver and selenium)nanoparticles and their antitumor and antimicrobial potential[J].Journal of colloid and interface science,2014,431:194-199.
[7] VENKATESAN J,KIM S K.Chitosan composites for bone tissue engineering-An overview[J].Marine drugs,2010,8(8):2252-2266.
[8] CHEN W W,YUE L,JIANG Q X,et al.Synthesis of varisized chitosan-selenium nanocomposites through heating treatment and evaluation of their antioxidant properties[J].International journal of biological macromolecules,2018,114:751-758.
[9] MATES I,ANTONIAC I,VASILE L,et al.Selenium nanoparticles:Production,characterization and possible applications in biomedicine and food science[J].UPB scientific bulletin,series B:Chemistry and materials science,2019,81(1):205-216.
[10] YU B,YOU P T,SONG M F,et al.A facile and fast synthetic approach to create selenium nanoparticles with diverse shapes and their antioxidation ability[J].New journal of chemistry,2016,40(2):1118-1123.
[11] ZHANG S Y,ZHANG J,WANG H Y,et al.Synthesis of selenium nanoparticles in the presence of polysaccharides[J].Materials letters,2004,58(21):2590-2594.
[12] WANG H L,ZHANG J S,YU H Q.Elemental selenium at nano size possesses lower toxicity without compromising the fundamental effect on selenoenzymes:comparison with selenomethionine in mice[J].Free radical biology and medicine,2007,42(10):1524-1533.
[13] 楊雪.枸杞多糖纳米硒体外消化吸收特性及抗疲劳活性研究[D].扬州:扬州大学,2021:20-30.
[14] 翟晓娜.壳聚糖纳米硒体系的制备及其物化特性和生物活性的研究[D].北京:中国农业大学,2017:43-58.
[15] 胡万军,李旭东,郭银贵,等.水热法反应条件对纳米硼酸盐形貌的影响研究进展[J].山东化工,2021,50(18):68-69.
