免疫联合化疗方案治疗PD-L1高表达晚期NSCLC患者的效果及对生存率的影响
2022-05-09曹丹


【摘要】 目的:研究免疫联合化疗方案治疗程序性死亡受体配体1(PD-L1)高表达晚期非小细胞肺癌(NSCLC)患者的效果及对生存率的影响。方法:将2016年2月-2018年2月铁岭市中心医院收治的65例PD-L1高表达晚期NSCLC患者纳入研究。将其按照随机数字表法分为联合组33例与单纯化疗组32例。单纯化疗组实施单纯化疗方案治疗,联合组实施免疫联合化疗方案治疗。分析两组临床疗效,治疗前后T淋巴细胞亚群变化情况,毒副反应发生情况,1、2、3年生存率等方面的差异。结果:联合组治疗总有效率为48.48%,相较于单纯化疗组的31.25%略高,但差异无统计学意义(P>0.05)。联合组治疗后CD3+、CD4+、CD8+及CD4+/CD8+均高于單纯化疗组(P<0.05)。两组恶心呕吐、腹泻、贫血及食欲下降发生率比较,差异均无统计学意义(P>0.05)。联合组2、3年生存率分别为63.64%、51.52%,均高于单纯化疗组的37.50%、25.00%,差异均有统计学意义(P<0.05)。结论:免疫联合化疗方案应用于PD-L1高表达晚期NSCLC患者的疗效较佳,可促进患者机体免疫功能的恢复,提高2、3年生存率。
【关键词】 非小细胞肺癌 程序性死亡受体配体1 免疫治疗 生存率
Effect of Immunotherapy Combined with Chemotherapy Method in the Treatment of Advanced NSCLC Patients with High PD-L1 Expression and Its Influence on Survival Rate/CAO Dan. //Medical Innovation of China, 2022, 19(09): -147
[Abstract] Objective: To analyze the effect of immunotherapy combined with chemotherapy method in the treatment of advanced NSCLC patients with high programmed death receptor ligand 1 (PD-L1) and its influence on survival rate. Method: A total of 65 patients with advanced NSCLC with high PD-L1 expression admitted to Tieling City Central Hospital from February 2016 to February 2018 were included in the study. According to the random number table method, the patients were divided into the combined group 33 cases and the chemotherapy alone group 32 cases. The chemotherapy alone group was treated with chemotherapy alone, and the combined group was treated with immune combined chemotherapy. Clinical efficacy, changes of T lymphocyte subsets before and after treatment, occurrence of toxic and side effects, and 1-year, 2-year, 3-year survival rates were analyzed between two groups. Result: The total effective rate of the combined group was 48.48%, whice was slightly higher than 31.25% of the chemotherapy alone group, but the difference was not statistically significant (P>0.05). The levels of CD3+, CD4+, CD8+ and CD4+/CD8+ in combined group were higher than those in the chemotherapy alone group (P<0.05). There were no significant differences in the incidence of nausea, vomiting, diarrhea, anemia and decreased appetite between the two groups (P>0.05). The 2-year and 3-year survival rates of the combined group were 63.64% and 51.52%, which were higher than 37.50% and 25.00% of the chemotherapy alone group, the differences were statistically significant (P<0.05). Conclusion: The combination of immunotherapy and chemotherapy has a better efficacy in advanced NSCLC patients with high PD-L1 expression, which can promote the recovery of immune function and improve the 2 and 3-year survival rate of patients.
[Key words] Non-small cell lung cancer Programmed death receptor ligand 1 Immunotherapy Survival rate
First-author’s address: Tieling City Central Hospital, Liaoning Province, Tieling 112000, China
doi:10.3969/j.issn.1674-4985.2022.09.036
晚期非小细胞肺癌(NSCLC),目前临床治疗仍以化疗为主的综合治疗作为一线治疗方案,然而部分患者会对化疗药物产生不同程度的耐药性,因此,尋求一种新型的有效治疗方案成为广大医务工作者亟待解决的重要问题[1-3]。此外,程序性死亡受体配体1(PD-L1)高表达主要是指免疫组化检查显示PD-L1表达≥50%的NSCLC患者[4]。迄今为止,临床上关于该类NSCLC患者的治疗研究并不多见,尤其是采用免疫联合化疗方案治疗该病患者的研究较为少见,具有一定的研究价值。鉴于此,本文通过研究免疫联合化疗方案治疗PD-L1高表达晚期NSCLC患者的效果及对生存率的影响,旨在为临床干预提供思路支持,现报道如下。
1 资料与方法
1.1 一般资料 将2016年2月-2018年2月铁岭市中心医院收治的65例PD-L1高表达晚期NSCLC患者纳入研究。纳入标准:(1)所有受试者均经病理检查确诊为NSCLC,且TNM分期均为Ⅲ、Ⅳ期;(2)均为成年人,性别不限;(3)均经免疫组化检查发现PD-L1表达≥50%;(4)入组前尚未接受相关抗肿瘤治疗。排除标准:(1)心、肝、肾等脏器发生严重病变;(2)合并活动性自身免疫性疾病;(3)伴有其他恶性肿瘤;(4)研究期间因故退出或失访;(5)预计生存期<3个月;(6)对本研究相关药物过敏。将其按照随机数字表法分为联合组33例与单纯化疗组32例。本研究已经医院伦理学委员会批准,患者及家属均知情同意并签署知情同意书。
1.2 方法 单纯化疗组实施单纯化疗方案治疗,即予以培美曲塞二钠(生产厂家:山西振东泰盛制药有限公司,批准文号:国药准字H20080249,规格:0.5 g)500 mg/m2+顺铂(生产厂家:齐鲁制药有限公司,批准文号:国药准字H20213819,规格:50 mL︰50 mg)75 mg/m2静滴,每3周进行1次的治疗,持续治疗18周。联合组实施免疫联合化疗方案治疗,其中化疗方案和单纯化疗组相同,同时予以Pembrolizumab(生产厂家:美国默沙东公司,批准文号:注册证号S20180019,规格:100 mg/4 mL)200 mg/次,静脉输注,每3周进行1次的治疗,持续治疗18周。
1.3 观察指标与判定标准 对所有受试者均进行为期3年的随访观察,随访方式为电话随访、上门随访及复查等,随访频率为1次/月,随访截止时间为死亡。分析两组临床疗效,治疗前后T淋巴细胞亚群变化情况,毒副反应发生情况,1、2、3年生存率等方面的差异。疗效评估主要参考实体瘤反应评价表标准完成,(1)完全缓解(CR):病灶彻底消失,且持续时间>4周;(2)部分缓解(PR):病灶相较于治疗前缩小≥30%,且持续时间>4周;(3)稳定(SD):病灶相较于治疗前无明显缩小或增大;(4)恶化(PD):病灶相较于治疗前增大>25%或出现新病灶[5]。总有效=CR+PR。分别于治疗前1 d、治疗18周后,采集两组晨起静脉血3 mL,保存至-80 ℃冰箱中待测,T淋巴细胞亚群的检测主要是通过赛默飞Attune NxT流式细胞仪完成,检测指标包括CD3+、CD4+、CD8+,并计算CD4+/CD8+。毒副反应包括恶心呕吐、腹泻、贫血及食欲下降。
1.4 统计学处理 采用SPSS 22.0软件对所得数据进行统计分析,符合正态分布的计量资料用(x±s)表示,组间比较采用独立样本t检验;计数资料以率(%)表示,比较采用字2检验。检验水准为α=0.05。以P<0.05为差异有统计学意义。
2 结果
2.1 两组一般资料比较 联合组,男18例,女15例;年龄36~81岁,平均(60.73±5.68)岁;吸烟史17例,饮酒史13例;病理类型:腺癌13例,鳞癌20例;体质量指数17~30 kg/m2,平均(21.73±2.06)kg/m2。单纯化疗组,男19例,女13例;年龄35~83岁,平均(60.77±5.70)岁;吸烟史18例,饮酒史12例;病理类型:腺癌14例,鳞癌18例;体质量指数17~29 kg/m2,平均(21.69±2.02)kg/m2。两组性别、年龄等一般资料比较,差异均无统计学意义(P>0.05),具有可比性。
2.2 两组疗效比较 联合组治疗总有效率为48.48%,相较于单纯化疗组的31.25%略高,但差异无统计学意义(字2=2.011,P=0.156)。见表1。
2.3 两组治疗前后T淋巴细胞亚群比较 两组治疗前T淋巴细胞亚群比较,差异均无统计学意义(P>0.05);联合组治疗后CD3+、CD4+、CD8+及CD4+/CD8+均高于单纯化疗组(P<0.05)。见表2。
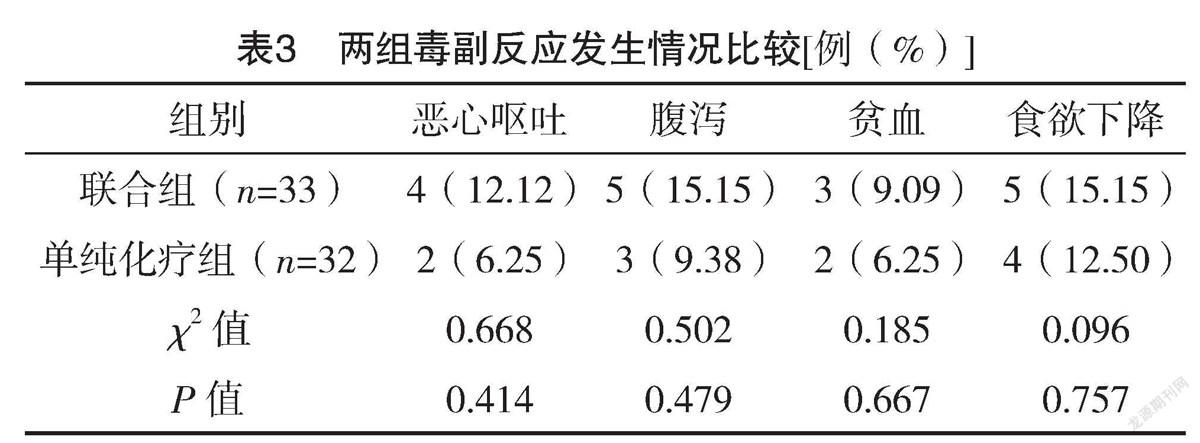
2.4 两组毒副反应发生情况比较 两组恶心呕吐、腹泻、贫血及食欲下降发生率比较,差异均无统计学意义(P>0.05),见表3。
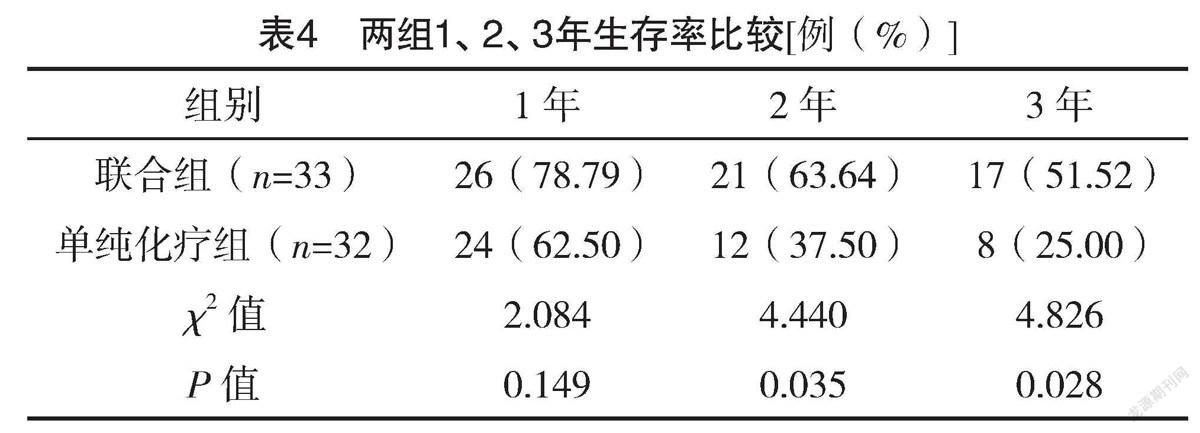
2.5 两组1、2、3年生存率比较 两组1年生存率比较,差异无统计学意义(P>0.05);联合组2、3年生存率均高于单纯化疗组,差异均有统计学意义(P<0.05)。见表4。
3 讨论
迄今为止,关于NSCLC的具体病因与发病机制尚且存在一定的争议,目前普遍认为可能和吸烟、生活方式、遗传及基因突变等密切相关[6-8]。含铂类药物化疗是目前公认的晚期NSCLC患者一线治疗方案,但化疗药物的长期使用可能会对患者器官和/或组织产生不同程度的损害,进一步导致机体免疫力与抵抗力的降低[9-11]。随着近年来相关研究的日益深入,越来越多的学者认为以免疫检查点抑制剂为代表的免疫治疗可能在极大程度上改善晚期NSCLC患者的预后,提升生存率[12-14]。
本研究结果显示,联合组治疗总有效率相较于单纯化疗组略高,但差异无统计学意义(P>0.05)。PD-1属于位于T淋巴细胞表面的重要受体之一,其在激活后可起到抑制T淋巴细胞活化的作用,而PD-1与PD-L1则是一对免疫抑制性因子,后者是前者的重要配体,两者可对CD4+与CD8+T淋巴细胞的增殖起到抑制作用,进一步对患者机体免疫应答起到负向调控作用,最终刺激肿瘤细胞增殖与转移。而免疫治疗过程中所采用的Pembrolizumab本质是针对PD-1的完全人源化免疫球蛋白G4与抗剂单克隆抗体,可通过对患者PD-1与PD-L1表达产生调控作用,进一步抑制肿瘤细胞的增殖、转移过程,最终达到灭杀肿瘤细胞的目的。此外,联合组治疗后CD3+、CD4+、CD8+及CD4+/CD8+均高于单纯化疗组(P<0.05)。提示免疫联合化疗方案应用于PD-L1高表达晚期NSCLC患者中,可有效促进细胞免疫功能的改善。究其原因,化疗会对患者的T淋巴细胞产生不同程度的损害,从而影响机体免疫功能,而Pembrolizumab的应用可有效减轻化疗对患者T淋巴细胞亚群所产生的损害,促进自然杀伤细胞活性的改善,最终实现对机体正常免疫功能有效维持的目的[15-17]。另外,两组恶心呕吐、腹泻、贫血及食欲下降发生率比较,差异均无统计学意义(P>0.05)。反映了联合组治疗方式应用于PD-L1高表达晚期NSCLC患者中,具有较好的安全性。分析原因,可能和该治疗方案可有效减轻患者因化疗而出现的免疫功能下降有关。本研究结果显示,联合组2、3年生存率均高于单纯化疗组,差异均有统计学意义(P<0.05)。说明联合组治疗方案应用于PD-L1高表达晚期NSCLC患者中,可显著提升2、3年存活率。其主要原因可能在于联合组治疗方案可发挥一定的协同互补作用,继而促进肿瘤病灶的消失,为预后改善创造了重要基础。同时,该治疗方案可通过调控PD-1/PD-L1抗体表达,从而减轻T淋巴细胞亚群出现的损伤,最终达到改善预后的目的[18-20]。
综上所述,对PD-L1高表达晚期NSCLC患者开展免疫联合化疗方案治疗的效果显著,可在一定程度上减轻患者因化疗而导致的免疫功能下降,同时不会增加毒副反应发生风险,有助于2、3年生存率的提高。
参考文献
[1]刘一,黄琳,门鹏,等.帕博利珠单抗一线治疗局部晚期/转移性非小细胞肺癌的快速卫生技术评估[J].中國新药杂志,2021,30(12):1137-1146.
[2]宋勇,张潮.Pembrolizumab与多西紫杉醇在晚期经治PD-L1阳性非小细胞肺癌患者中的疗效比较[J].循证医学,2017,17(1):50-54.
[3]郝帅,何勇.从免疫单药到多药联合——PD-1/PD-L1抑制剂治疗NSCLC的优选之路[J].重庆医学,2018,47(22):2885-2888.
[4]王钰聪,徐英辉,李宏伟,等.PD1/PD-L1免疫检查点抑制剂治疗非小细胞肺癌的研究进展[J].吉林大学学报(医学版),2019,45(4):965-970.
[5]徐赫,马爱霞.基于分区生存模型的帕博利珠单抗单药与化疗一线治疗PD-L1肿瘤比例分数不同的非小细胞肺癌的成本-效果分析[J].中国医院药学杂志,2020,40(23):2468-2473.
[6]宋鹏,尚聪聪,张力,等.PD-1/PD-L1抑制剂治疗中青年和高龄非小细胞肺癌患者有效性的Meta分析[J].山西医科大学学报,2018,49(11):1334-1340.
[7]马海玥,贾佳,郭会芹,等.肺腺癌胸水标本中PD-L1的蛋白表达与临床病理特征及分子改变的相关性研究[J].中国肺癌杂志,2020,23(3):150-155.
[8]耿茜,蒋华,李栋庆,等.PD-1抗体联合低剂量白蛋白结合紫杉醇对肺癌裸鼠移植瘤抗肿瘤作用的实验研究[J].临床肿瘤学杂志,2021,26(5):411-416.
[9]中国抗癌协会肿瘤病理专业委员会肺癌学组,中国抗癌协会肺癌专业委员会,PD-L检测共识专家组.非小细胞肺癌PD-L1免疫组织化学检测规范中国专家共识[J].中国肺癌杂志,2020,23(9):733-740.
[10]朱振宸,宋兰,隋昕,等.PD-1/PD-L1抑制剂治疗非小细胞肺癌中不典型肿瘤反应影像学评价的研究进展[J].中华放射学杂志,2021,55(1):82-86.
[11]李浩洋,秦娜,俞孟军,等.PD-L1高表达晚期非小细胞肺癌患者单纯免疫治疗与免疫联合化疗疗效比较[J].中国肺癌杂志,2021,24(3):161-166.
[12]张敬茹,赵立波,顾健,等.非小细胞肺癌一线治疗新药PD-1抑制剂pembrolizumab[J].中国新药杂志,2018,27(9):969-972.
[13]刘国强,康朔,王欣晨,等.帕博利珠单抗一线治疗PD-L1高表达的晚期非小细胞肺癌的药物经济学评价[J].中国药房,2021,32(11):1361-1356.
[14] XIA L,LIU Y,WANG Y.PD-1/PD-L1 Blockade Therapy in Advanced Non-Small-Cell Lung Cancer:Current Status and Future Directions[J].Oncologist,2019,24(1):S31-S41.
[15]王芸,王郁阳,姜曼,等.帕博利珠单抗对晚期非小细胞肺癌患者T淋巴细胞亚群的影响及疗效观测[J].中国肺癌杂志,2021,24(3):182-187.
[16] HSU P C,JABLONS D M,YANG C T,et al.Epidermal Growth Factor Receptor(EGFR) Pathway,Yes-Associated Protein(YAP) and the Regulation of Programmed Death-Ligand 1(PD-L1) in Non-Small CellLung Cancer(NSCLC)[J].Int J Mol Sci,2019,20(15):3821-3822.
[17] LIU S Y,WU Y L.Tislelizumab:an investigational anti-PD-1 antibody for the treatment of advanced non-small cell lung cancer(NSCLC)[J].Expert Opin Investig Drugs,2020,29(12):1355-1364.
[18] DATAR I,SANMAMED M F,WANG J,et al.Expression Analysis and Significance of,PD-1,LAG-3,and TIM-3 in Human,Non-Small,Cell,Lung,Cancer,Using Spatially Resolved and Multiparametric Single-Cell,Analysis[J].Clin Cancer Res,2019,25(15):4663-4673.
[19]陈淦雄,李淦清.腺苷激酶-1在非小细胞肺癌患者血清中的表达与肺癌临床病理学特点及预后的关系[J].中国医学创新,2021,18(7):142-145.
[20] KITAGAWA S,HAKOZAKI T,KITADAI R,et al.Switching administration of anti-PD-1 and anti-PD-L1 antibodies as immune checkpoint inhibitor rechallenge in individuals with advanced non-small celllung cancer:Case series and literature review[J].Thorac Cancer,2020,11(7):1927-1933.
(收稿日期:2021-08-18)
①辽宁省铁岭市中心医院 辽宁 铁岭 112000
通信作者:曹丹
