Ni/氮掺杂碳催化剂的制备及其催化甲烷干重整实验研究
2022-04-29孟俊光张居兵卜昌盛王昕晔刘长奇陈晓乐
潘 伟,孟俊光,2,3,张居兵,卜昌盛,王昕晔,4,刘长奇,谢 浩,4,陈晓乐
(1. 南京师范大学 能源与机械工程学院,江苏 南京 210042;2. 广东工业大学 广东省植物资源生物炼制重点实验室,广东 广州 510640;3. 中国科学院可再生能源重点实验室,广东 广州 510640;4. 南京师范大学 镇江创新发展研究院,江苏 镇江 212050)
温室气体的大量排放造成的全球气候变暖问题已经成为人类面临的巨大挑战之一。因此CO2的高效循环利用越来越受到世界各国的重视[1]。甲烷干重整作为CO2高效转化技术之一,因其既能同时利用两种温室气体CH4和CO2,且转化产物中n(H2)/n(CO) ≈ 1,又能够直接作为后续铁基催化剂上Fischer-Tropsch合成和合成二甲醚的原料,被认为是CO2循环利用的理想途径之一[2]。甲烷干重整反应涉及的具体反应化学式如下:

其中,反应方程式(2)、(3)和(5)均有可能造成催化剂的积炭,逆水煤气变换反应(4)的存在将会影响产气中的n(H2)/n(CO)。因此,制备同时具有高抗积炭性和高选择性的催化剂成为了甲烷干重整研究领域的热点。研究[3]表明,贵金属催化剂(Ru、Ir、Pt和Rh等)对甲烷干重整具有较好的催化活性和催化稳定性,但是其稀有性和昂贵的价格限制了进一步应用。过渡金属催化剂(Ni、Co等)[4-5]虽然具有较好的初始活性,但是在反应过程中极易因催化剂的烧结和积炭而失活。抑制催化剂烧结的方法主要是加强活性金属与载体的相互作用[6],通常可以在载体上制造缺陷位,使金属锚定在缺陷位上,从而形成更稳定的活性位(Ni—Nx)[7]。因此,载体的性质也将直接对催化活性产生影响,目前研究较多的载体有Al2O3、MgO、CeO2以及碳载体等[8-10]。相比于其他载体,碳载体因其含有众多官能团,且具有较大的比表面积而成为优良载体的候选之一[11]。但是大部分碳材料呈现化学惰性,研究表明,在碳材料中增加杂原子(比如N)能够有效增加碳材料表面缺陷位并且引入新的官能团。同时引入的杂原子能够加强与其结合的C原子周围的电子移动性以及电子云密度,从而显著增强催化活性[12-13]。研究[14]发现,氮源不同,掺杂之后N物种与碳材料的结合形式也会不同,其对催化剂产生的影响也不同。例如:吡啶-N能够通过改变其周围电子云密度从而增强碳材料的价带结构;吡啶-N和吡咯-N共用电子对所形成的Lewis酸位能够提升氧化还原反应速率。引入N物种的方式有两种,一种是直接炭化含氮的前驱体(比如葡萄糖胺、聚氨酯、大豆或者豆渣等),另外一种是利用含氮的化合物(比如三聚氰胺、氨气和尿素等)改性碳材料[15-17]。目前,在氮掺杂碳催化剂的研究中,对于上述两种方式引入的N物种对碳载体结构及对甲烷干重整反应性能的影响鲜有报道。同时,Ni/氮掺杂碳催化剂与甲烷干重整的构效关系仍有待进一步研究。
考虑到外部引入的N物种与材料本身富含的N物种可能与碳载体的作用形式不同,从而影响催化剂性能,为了明晰N物种对碳材料表面的改变以及对甲烷干重整反应性能的影响,在本研究中,采用两种不同的掺氮方式获得氮掺杂碳材料,一种是选取含氮化合物(三聚氰胺和邻二氮杂菲)改性碳材料,另一种是直接炭化富氮木质废弃物豆渣。采用浸渍法制备一系列Ni/碳、Ni/氮掺杂碳催化剂,结合元素分析、ICP、XRD、BET和XPS等催化剂表征手段考察掺氮前后以及氮源对甲烷干重整反应性能的影响。
1 实验部分
1.1 实验原料与试剂
本文中使用的实验原料和试剂如表1和表2所示。

表1 实验原料及其规格Table 1 Raw materials for experiments and their specifications
表2 实验试剂及其规格Table 2 Experimental reagents and their specifications
1.2 催化剂的制备
1.2.1 碳载体的制备与活化
将干燥后的原料(毛竹粉和豆渣)置于管式炉中,在N2气氛下以10 °C/min从室温加热到700 °C维持1 h,冷却之后得到碳载体。将上述制备好的碳载体按照m(KOH):m(碳载体) = 1:1的比例,在室温下浸渍在1 mol/L的KOH溶液中,静置10 h后置于烘箱中105 °C干燥10 h。将干燥后的样品置于管式炉中在N2气氛下以10 °C/min升至850 °C维持2 h。活化后的样品经酸洗、洗涤、过滤至滤液呈中性。所得固体在105 °C干燥10 h,研磨至60~80目备用。以毛竹粉和豆渣为原料制备的碳载体(催化剂)分别记作BC和DC。
1.2.2 氮掺杂碳载体的制备
以BC为原料,分别采用邻二氮杂菲和三聚氰胺对其掺氮,具体制备方法如下:称取一定质量的邻二氮杂菲和三聚氰胺,并将其分别溶于水和乙醇溶液中,制成N质量分数为5%的溶液。在室温下分别将BC浸入上述溶液中并超声震荡1 h,之后在烘箱中105 °C干燥24 h。干燥后的样品在管式炉N2气氛中以10 °C/min从室温升至850 °C并维持2 h。冷却后将样品研磨至100~200目,得到氮掺杂碳载体。以邻二氮杂菲和三聚氰胺为氮源制备的氮掺杂碳载体(催化剂)分别记为BCO和BCM。
1.2.3 Ni/氮掺杂碳催化剂的制备
称取一定质量的Ni(NO3)2•6H2O溶解在水溶液中,制成Ni质量分数为5%的溶液,加入上述碳载体(催化剂)或氮掺杂碳载体(催化剂)后将混合溶液超声震荡1 h,之后置于烘箱中105 °C干燥24 h。将干燥后的样品置于管式炉中,N2气氛下以10 °C/min升温至600 °C并维持6 h。所得催化剂分别标记为BC-5%、DC-5%、BCO-5%和BCM-5%。
1.3 催化剂的活性评价
催化剂的活性评价在固定床反应器中进行。将0.2 g催化剂放置在位于石英管(内径为22.5 mm,管长为1200.0 mm)中部的开孔挡板上,H2、N2、CH4和CO2由反应器上部通入,其流量由质量流量控制器(D08-2F)控制V(CH4):V(CO2):V(N2) = 1:1:8,总气体流量为200 mL/min,气体产物依次经过干燥器和过滤器,之后进入煤气分析仪(MRU-10-230V/5A)检测分析。实验开始前催化剂预先用H2体积分数为10% 的H2/N2混合气在500 °C下还原1 h,每次催化剂活性评价实验持续4 h。实验过程中通过改变总气体流量来改变空速(各气体组分比例不变)。
CH4、CO2转化率( 、 )和n(H2)/n(CO)由式(6)~式(8)计算得到。



1.4 催化剂表征
采用Elementar Vario EL型有机元素分析仪(EA)对催化剂进行元素分析。催化剂在1150 °C、纯氧氛围的氧化管中完全燃烧产生NOx,随后该混合气在还原管(850 °C、还原铜)中进一步还原为N2,经过吸附-解吸柱分离后,通过色谱柱进行分离后热导检测,得到N元素含量。
采用美国康塔NOVA 2200e N2全自动吸附分析仪表征催化剂的微观结构信息。催化剂先在300 °C下脱附3 h,去除水汽,随后在-196 °C下进行N2吸附与脱附实验,基于密度函数理论(DFT)模型计算比表面积。
采用D/max 2500/PC Cu Kα辐射X射线衍射仪(XRD)获取催化剂的晶相结构及晶体参数,仪器参数为波长λ = 0.15406 nm,管电压为40 kV,管电流为100 mA,操作条件为扫描角度2θ范围10°~80°,扫描步长0.02 (°)/s。
采用钢研纳克Plasma 3000电感耦合等离子体原子发射光谱仪(ICP-OES)检测金属Ni的负载量。测试波长范围30~800 nm,分辨率0.004 nm(200 nm),精密度相对标准偏差< 0.5%(n = 10),稳定性相对标准偏差< 1.0 %(4 h)。
采用Thermo Scientific K-Alpha型X射线光电子能谱仪(XPS)测定催化剂中C、N、O和Ni的价态信息。激发源为Al Kα,工作电压15.0 kV,以C 1s的285.0 eV为标准校正能量。
2 结果与分析
2.1 Ni/氮掺杂碳催化剂N含量分析
为了表征氮掺杂效果,对制备的催化剂进行了元素分析,其中N含量(质量分数,下同)如表3所示。未掺氮之前BC-5%催化剂中N含量仅为0.23%,掺氮之后N含量明显上升,以邻二氮杂菲为氮源的催化剂BCO-5%中N含量约为原来的7倍,以三聚氰胺为氮源的BCM-5%中N含量约为原来的14倍。相比之下,三聚氰胺的氮掺杂效果更优。原因可能是邻二氮杂菲中的N为苯环N,结构更加稳定,在掺杂过程中不容易与碳载体发生反应,而三聚氰胺中既有苯环N也有氨基N,在掺杂过程中容易与碳载体发生反应,从而更容易进入碳载体的结构中[16-17]。以豆渣为原料的DC-5%催化剂中的N含量约为竹粉为原料的BC-5%催化剂的4倍。

表3 Ni/氮掺杂碳催化剂的元素含量、Ni颗粒晶粒尺寸和比表面积Table 3 Elemental content, Ni particle size and specific surface area of Ni/nitrogen-doped carbon catalysts
2.2 Ni/氮掺杂碳催化剂Ni负载量分析
为了研究氮掺杂对催化剂中Ni负载量的影响,对催化剂中Ni含量进行了分析,如表3所示。可以看出,氮掺杂之前,BC-5%催化剂中Ni的真实负载量仅有1.22%,大部分Ni都在负载过程中流失。而氮掺杂之后BCO-5%和BCM-5%中Ni含量分别达到了3.25%和2.41%,均明显高于BC-5%,说明氮的掺入提升了Ni的负载量。然而结合BCO-5%和BCM-5%的元素分析发现,实际的Ni负载量并没有与N含量成正比,说明金属的负载不仅仅与N含量有关,也可能与N的存在形态有关。同时发现,在理论负载量相同的情况下,DC-5%中Ni的真实负载量最高,进一步表明金属的负载不仅仅与N含量成正相关。
2.3 Ni/氮掺杂碳催化剂XRD表征
为了明晰氮掺杂前后催化剂中碳和金属Ni的晶型结构,对所制备的催化剂进行了晶型结构分析,结果如图1所示。掺氮前后,催化剂的晶型变化不大。未负载金属的BC和BCO碳载体仅检测到了石墨碳的衍射峰,负载金属之后,无论是未掺氮的BC-5%,还是掺氮的BCO-5%,均只检测到了单质Ni的衍射峰。其中2θ= 44.5°处为Ni0(111)晶面,51.9°处为Ni0(200)晶面,76.4°处为Ni0(220)晶面[9,15],说明负载的Ni物种在煅烧过程中(N2气氛)被碳载体还原。根据Scherrer公式,计算出的Ni颗粒粒径尺寸列于表3中,可以看出,BC-5%的中Ni颗粒粒径为26.3 nm,采用邻二氮杂菲掺氮之后,BCO-5%的Ni颗粒粒径增大至33.4 nm,说明虽然BCO-5%中N的加入使Ni的负载量有所增加,但是Ni颗粒出现了团聚,这可能对后续的催化性能不利。但是采用三聚氰胺掺氮之后,BCM-5%中Ni颗粒粒径降低至20.3 nm,说明Ni在BCM-5%中分散地更加均匀。DC-5%中的Ni颗粒直径最小,为16.5 nm,原因可能是相比于掺氮碳载体,N在富氮碳载体中分散地更加均匀,另外,这可能与掺氮碳载体中N的存在形式有关。
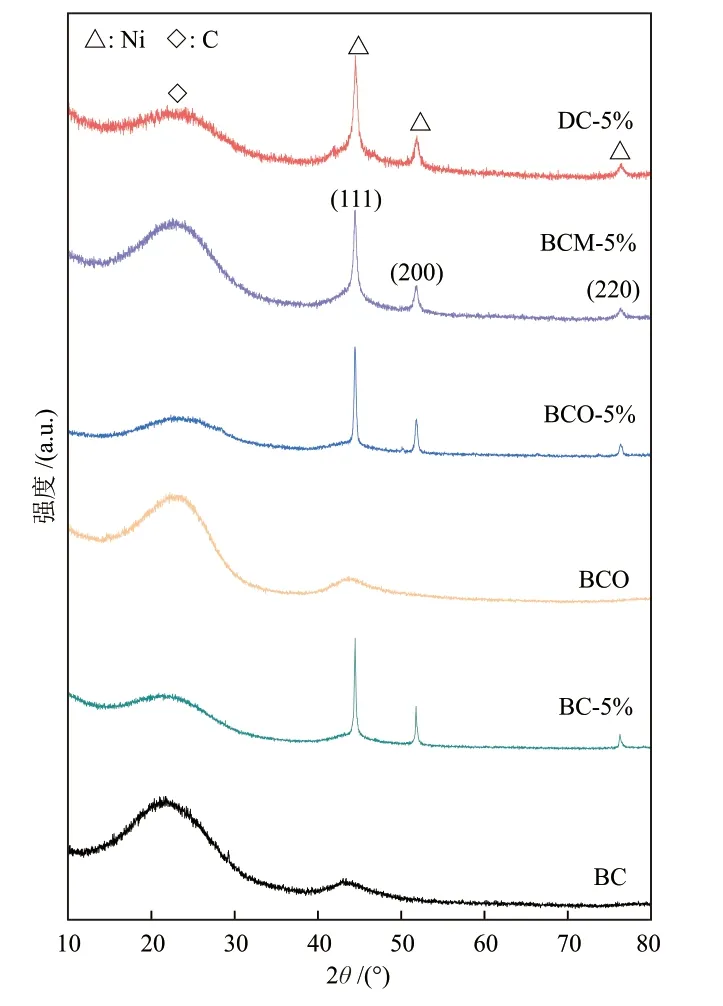
图1 Ni/氮掺杂碳催化剂的XRD谱图Fig. 1 XRD of Ni/nitrogen-doped carbon catalysts
2.4 Ni/氮掺杂碳催化剂BET表征
为了研究氮掺杂对催化剂比表面积的影响,对催化剂进行了比表面积分析,结果如表3所示。可以看出,掺氮之后BCO相比于BC比表面积出现了明显地下降,说明N的掺入破坏了碳载体的孔道结构,使得部分孔道坍塌。三聚氰胺掺氮后BCM-5%催化剂比表面积减少的最多。而对于富氮废弃物豆渣制备的催化剂DC-5%,由于其避免了掺氮这一步骤,从而避免了碳结构被大面积破坏,因此其比表面积比Ni/氮掺杂碳催化剂(BCM-5%和BCO-5%)大。较大的比表面积有利于反应气体在催化剂颗粒中吸附与扩散,对甲烷干重整反应具有促进作用。
2.5 Ni/氮掺杂碳催化剂XPS分析
为了进一步明确不同氮源制备的催化剂表面的元素价态,对新鲜催化剂进行了XPS分析,C、N、O和Ni的高分辨率光谱图和成键比例分别列于图2和表4中。
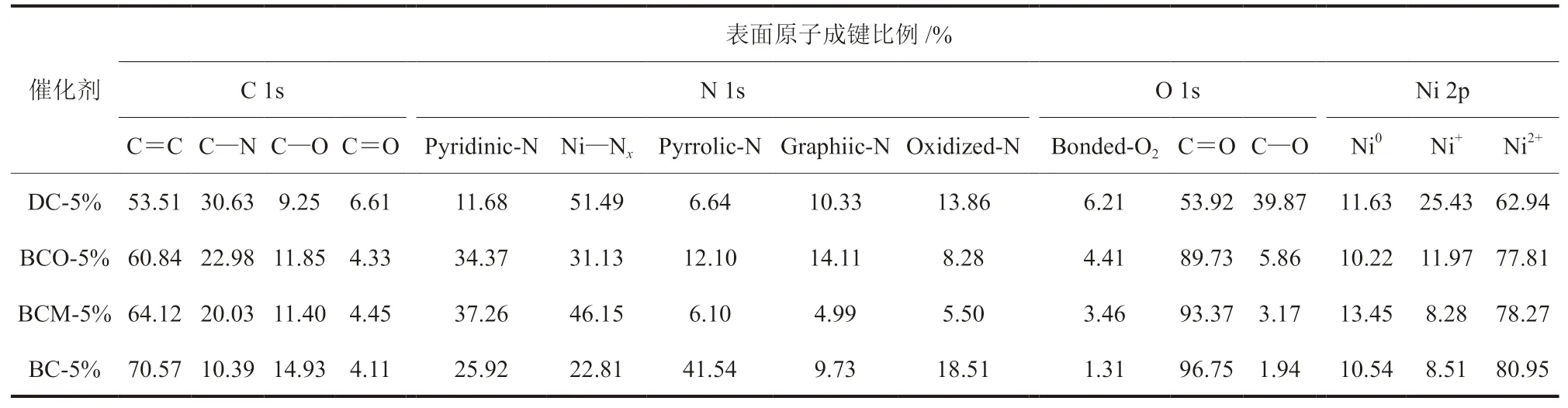
表4 Ni/氮掺杂碳催化剂的表面原子成键情况Table 4 Surface atomic bonding of Ni/nitrogen-doped carbon catalysts
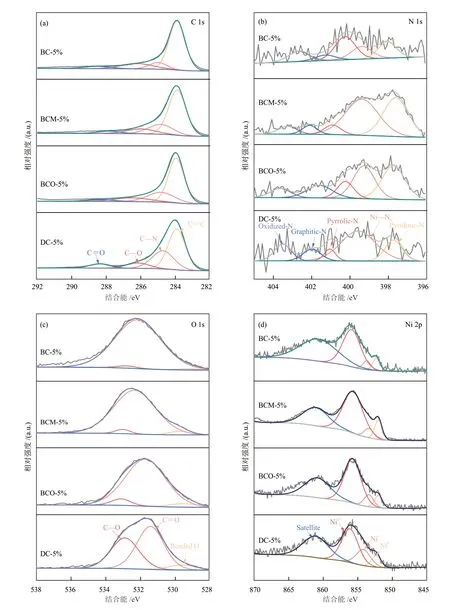
图2 Ni/氮掺杂碳催化剂的XPS谱图Fig. 2 XPS spectra for Ni/nitrogen-doped carbon catalysts
图2(a)为C 1s的高分辨光谱图,主要将表面C物种分为4种类型,284.0 eV处的sp2C(C=C键),284.9 eV处的C—N键,286.5 eV处的C—O键和288.3 eV处的C=O键[18]。C—N的增加说明N被成功掺杂进了碳载体中,N的掺入能够增强催化剂的吸附能力,从而有利于锚定和稳固负载的Ni原子[12]。从表4中可以看出,未掺氮的BC-5%催化剂中C—N的比例仅为10.39%,掺氮之后BCO-5%和BCM-5%中C—N的比例明显提升。富氮的DC-5%催化剂中C—N的比例最高,说明外部掺杂氮形成的杂化碳的数量不及天然的富氮碳材料,C—N的含量也直接影响着催化剂中真实Ni的负载量,C—N比例高的DC-5%催化剂中Ni的真实负载量也最高。
图2(b)为N 1s的高分辨光谱图,按照结合能从低到高将N依次分为吡啶-N(Pyridinic-N),Ni—Nx,吡咯-N(Pyrrolic-N),石墨-N(Graphiic-N)和氧化-N(Oxidized-N)[19-20]。Pyridinic-N和Pyrrolic-N被证明对电催化过程有着明显地促进作用[21],而金属-Nx则被证明对反应物中C—C键的氧化断裂作用影响显著[22]。4种催化剂中Ni—Nx的比例由高到底为DC-5% > BCM-5% > BCO-5% > BC-5%,这可能会对其甲烷干重整反应性能起着决定性影响。
图2(c)为O 1s的高分辨光谱图。530.0 eV处的峰被归因于表面吸附氧(Bonded-O2),这种形态的氧具有较强的活性,有利于催化剂表面积炭的消除[22]。4种催化剂中Bonded-O2比例从高到低为
DC-5% > BCO-5% > BCM-5% > BC-5%。DC-5%
中C—O键的比例明显高于其他3种催化剂,说明该催化剂中O的存在形态更加多样化。
图2(d)所示为Ni 2p的高分辨光谱图。852.2 eV处 的 峰 为Ni0,853.8 eV处 为Ni+,855.8 eV处 为Ni2+[23]。研究表明,Ni+的存在能够调节Ni物种表面电子结构,且Ni+能够促进通过形成*COOH中间物的方式来降低CO2还原的障碍,从而作为CO2还原成CO的高效的活性位点[23]。4种催化剂中DC-5%中Ni+的比例最高,达到25.43%。
2.6 催化剂的性能分析
图3为氮源对催化剂甲烷干重整反应性能的影响。实验工况为:反应温度为850 °C,空速为15000 mL/(g·h)(每小时经过每克催化剂的总气体体积)。

图3 甲烷干重整催化剂性能评价Fig. 3 Performance evaluation of dry reforming catalyst for methane
BC催化剂对CH4几乎没有催化活性,在整个反应过程中CH4转化率均在5%以下,对CO2的转化率稍高,能够达到10%左右,这可能是CO2与碳载体发生了反应,产物中n(H2)/n(CO)远高于1,说明少量转化了的CH4在BC催化剂上发生的是裂解反应。当负载了金属Ni之后,催化活性得到了显著提升,BC-5%对CH4的初始转化率达到了68.7%,对CO2的初始转化率达到了89.5%。在掺杂氮之后,虽然BCO-5%和BCM-5%催化剂的比表面积均有所下降,但是催化活性得到了进一步的提升,说明氮掺杂引起的Ni结合形态的改变相比于氮掺杂对碳结构的改变对催化活性的影响更大。
对比从外部引入氮源的催化剂,发现BCM-5%和BCO-5%催化剂具有相当的初始催化活性(15 min时CH4转化率分别为90.5%和87.6%),但是随后BCM-5%和BCO-5%的活性具有不同程度的降低。催化剂初始活性迅速降低可归因于在初始阶段,Ni以Ni0存在,具有较高的催化活性,CH4的裂解速率大于CO2的吸附解离速率,CH4裂解产生的积炭没有被完全消除,从而覆盖活性位,导致初始活性迅速降低。与BCM-5%相比,BCO-5%的催化初始活性降低得更多,结合晶粒尺寸分析,BCO-5%的晶粒尺寸更大(较大的晶粒尺寸意味着较差的金属分散性),同时Ni—Nx的比例也低于BCM-5%(Ni—Nx被认为对C—H键的断裂作用显著[24])。但是在随后的反应中,发现BCO-5%催化活性又缓慢上升,这主要得益于BCO-5%中的Bonded-O2和C—N[12,22]。Bonded-O2在氧化还原反应中具有很高的反应活性,在甲烷干重整反应中表现为对积炭有较高的反应活性,C—N形成的C缺陷则更有助于CO2的吸附,这些因素使得BCO-5%在经历了催化活性下降之后能够通过Bonded-O2和CO2的解离吸附循环持续消除催化剂表面的积炭,从而恢复反应活性。相反,BCM-5%催化剂在整个反应过程中活性均在缓慢下降,说明该催化剂中缓慢产生的积炭没有被有效消除,造成催化剂的缓慢失活,这是由于BCM-5%催化剂中Bonded-O2和C—N的比例均小于BCO-5%。
富氮废弃物豆渣制备的DC-5%在制备的催化剂中具有最高的催化活性,原因归结于以下两个方面:一方面是由于其比表面积最大;另一方面是源于其Ni负载量最高的同时晶粒尺寸又最小。比表面积高是因为没有掺氮步骤破坏其原有的孔隙结构。Ni负载量高同时晶粒尺寸小则与Ni、N、C的存在形态有关。通过元素分析可知,DC-5%的N含量仅为外部引入氮源催化剂的三分之一左右,说明Ni负载量和晶粒尺寸不仅与N含量有关,还与N的存在形态和分布情况相关。结合XPS分析,DC-5%催化剂中C—N和Ni—Nx的比例均最高,N的这两种形态被证明在氧化还原反应的催化剂中具有重要作用,C—N为金属的负载提供了更均匀的缺陷位,使金属粒径更小,负载地更加均匀,而Ni—Nx则可能更有利于C—H键和C=O键的断裂[24]。同时,DC-5%中Ni+和Bonded-O2的比例也最高,Ni+被证明是CO2还原为CO的高效活性位点,而Bonded-O2则有利于积炭的消除[21,23]。
Ni/氮掺杂碳催化剂甲烷干重整产物中n(H2)/n(CO)在0.6~1.0之间,说明在反应过程中可能发生了逆水煤气变换反应(反应(4)),或者是CO2与碳载体发生反应生成了CO。
通过上述实验发现DC-5%催化剂表现出了最优的催化活性,为了测试其稳定性,在更低的温度(800 °C)以及更高的空速条件下(60000 mL/(g·h))对其进行了连续性实验,结果如图4所示。可以看出,在空速为60000 mL/(g·h)时,催化剂初始阶段的活性稍低,自活化阶段(包括被氧化活性金属的再次还原和积炭的消除)持续了将近10 h,之后一直维持着稳定的催化活性。在100 h的连续性实验中,CH4转化率维持在83%左右,CO2转化率维持在90%左右,且未发现失活迹象。表明DC-5%催化剂具有较高的催化稳定性,在初始阶段并没有持续失活,而使依靠自身的理化特性,如Bonded-O2、Ni—Nx以及大量的Ni+,经过自活化阶段之后使得催化活性回到较高且稳定的水平。
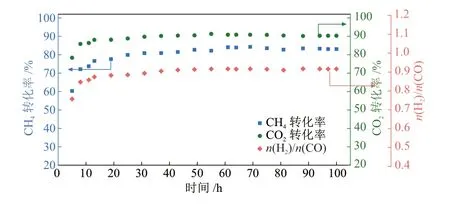
图4 DC-5%催化剂稳定性测试Fig. 4 Stability testing of DC-5% catalyst
3 结论
本文制备了一系列Ni/氮掺杂碳载体催化剂,考察了催化剂掺氮前后以及不同掺氮方式对甲烷干重整反应性能的影响,并对反应性能最优的DC-5%催化剂进行了稳定性测试,得出以下结论:
(1)N掺入碳载体之后,形成的C—N结合形态有助于增加催化剂中Ni的实际负载量,使Ni/氮掺杂碳催化剂的反应活性明显优于未掺氮催化剂。
(2)催化剂的活性不仅与N含量有关,与N的存在形态和分布状况也有关。N以C—N和Ni—Nx的形式存在时能够提高催化剂的反应活性。
(3)Bonded-O2有利于消除催化剂表面积炭从而提高催化剂的稳定性。
(4)富氮废弃物豆渣制备的DC-5%催化剂由于C—N、Ni—Nx和Bonded-O2之间的协同作用,在100 h的连续性反应中表现出了优异的催化活性和稳定性(CH4和CO2的转化率始终分别稳定在83%和90%左右)。
