胆道恶性肿瘤辅助治疗的研究现状及展望
2022-04-28吴芳芳综述郑桐森审校
吴芳芳 综述 郑桐森 审校
胆道恶性肿瘤(Biliary tract carcinoma,BTC)是一类罕见的、具有高度异质性和侵袭性的肝胆恶性肿瘤。主要包括胆囊癌(Gallbladder cancers,GBC)和胆管癌(Cholangiocarcinoma,CCA),胆管癌按部位可分为肝内胆管细胞癌(Intrahepatic cholangiocarcinoma,ICCA)和肝外胆管细胞癌(Extrahepatic cholangiocarcinoma,ECCA),而ECCA又可分为肝门周围胆管细胞癌(Perihilar cholangiocarcinoma,PCCA)和远端胆管细胞癌(Distal cholangiocarcinoma,DCCA)[1]。BTC较为少见,约占所有消化系统肿瘤的3%。其中,GBC最为常见,约占80%~95%,全球发病率位居消化道肿瘤第6位[2]。BTC绝大多数为腺癌,侵袭性强,发现时多为晚期,预后极差,5年存活率低于5%[3]。尽管部分早期诊断的患者有行根治性手术的机会,但术后复发率高达60%~70%[4]。与较高复发率和预后不良相关的因素有切缘阳性(R+)、淋巴管侵犯、血管侵犯、淋巴结阳性(N+)、较高的肿瘤分化程度等[5-6]。手术切除后辅以化疗、放疗或综合治疗可消除残留病变和微转移,是降低复发风险,提高总生存期(Overall survival,OS)的重点。但较低的发病率,早期诊断困难,加上极高的恶性程度,使得开展相关研究困难重重,多年来未能有大的突破。支持辅助治疗的证据大多来源于回顾性研究及荟萃分析[7-9]。虽然证据不足,但为了改善预后,临床上越来越多的高危因素患者接受了辅助治疗。有研究表明,近年来ICCA术后辅助化疗使用率随着时间的推移而增加(33%~41%,P<0.05),此现象在N+和T3/T4患者中尤为明显,中位OS也从32个月提高到41个月(P<0.05)[10-11]。随着诊疗技术的发展以及基因组研究和下一代测序技术的开展,BTC越来越多的被人们所熟知,辅助治疗研究领域也迈上了新的台阶。本文回顾了可切除BTC辅助治疗的相关研究和最新证据。
1 化疗
1.1 以吉西他滨为基础的治疗
以吉西他滨为基础的治疗多年来一直是局部晚期或转移性BTC治疗的一线疗法,鉴于不错的疗效及安全性,随后人们对其在辅助治疗环境中的作用进行了探索。主要方案包括吉西他滨单药、吉西他滨联合顺铂及吉西他滨联合奥沙利铂等,部分研究得出了不错的结果[12-14],但大多是Ⅰ/Ⅱ临床试验研究。近年来相继发布了两项关于吉西他滨辅助治疗的大型前瞻性研究,但结果并不理想。BCAT研究[15]纳入了225例ECCA患者,旨在探究吉西他滨对比单纯手术在辅助治疗中的疗效,中位随访时间79.4个月,主要终点OS没有统计学差异(62.3个月vs.63.8个月,P=0.964),无复发生存期(Relapse-free survival,RFS)也无明显获益(36.0个月vs.39.9个月,P=0.693)。法国多中心Ⅲ期试验PRODIGE 12-ACCORD 18[16],共纳入196例患者,随机分为吉西他滨+奥沙利铂组(95例)和单独观察组(99名),中位随访时间46.5个月,两组的中位RFS无统计学差异(30.4个月vs.18.5个月,P=0.48),中位OS也无统计学差异(75.8个月vs.50.8个月,P=0.74)。在两项研究的亚组分析中,根据切缘性质或淋巴结状况分层,两组患者的存活率依旧没有统计学差异。吉西他滨在辅助治疗环境中表现出不错的耐受性,但现有证据不能证实其在延长生存期上的获益。由于这些研究患者的数量有限,且纳入的患者组成不一,我们仍对吉西他滨的辅助作用抱有希望,相应的进一步研究也在积极进行中,我们期待ACTICCA-1研究的结果(表1)。
1.2 以氟尿嘧啶类为基础的治疗
口服氟嘧啶类药物S-1在局部晚期和转移性BTC的临床试验中显示出不错的疗效[17-18]。近期两个术后S-1辅助化疗的Ⅱ期试验结果被报道,KHBO 1208研究表明[19],在BTC肝大部切除患者中,S-1辅助治疗相较于吉西他滨有更佳的生存率,且淋巴结阳性者获益更多,但同时也显示出更高的不良反应发生率。N-SOG 09研究旨在探究S-1辅助治疗对淋巴结阳性BTC患者的疗效[20],该试验包括23例HCCA、20例DCCA和7例GBC患者。治疗完成率为64%,3年生存率和无复发生存率分别为50%和32.0%,中位OS和中位RFS分别为34.6个月和18.4个月。实验表明S-1辅助化疗对淋巴结阳性的BTC患者可能是有希望的。在此背景下,ASCOT实验(UMIN00001168)的结果令人期待[21]。近期一项关于5-FU辅助治疗在BTC中的有效性和安全性的荟萃分析发布,结果支持5-FU方案应用于切除的BTC患者[22]。此外,高危患者更有可能从中受益,例如N+或有血管侵犯。另一类氟尿嘧啶类药物——卡培他滨也随着BILCAP实验[23]结果的发布走进我们的视野,且成为了目前唯一的指南推荐用药。该研究共纳入447例患者,在按方案分析(卡培他滨组210例,观察组220例)中,得出了令人欣喜的结果,卡培他滨组对比观察组,中位OS(53个月vs.36个月,P=0.028),中位RFS(25.9个月vs.17.4个月,P=0.001)。就目前研究而言,氟尿嘧啶类药物似乎是BTC辅助治疗不错的选择,但仍需更多的大型前瞻性临床研究来证实其疗效,以及探究更佳的适用人群和剂量。
1.3 吉西他滨辅助化疗与氟嘧啶类辅助化疗的比较
吉西他滨为基础的疗法和氟尿嘧啶为基础的疗法是BTC辅助治疗领域的两大支柱,究竟孰优孰劣也引发了大量的对照研究。KHBO 1208Ⅱ期研究[19]评估了吉西他滨与S-1在辅助环境中的疗效,研究的主要终点RFS虽无统计学差异,但S-1有改善OS的趋势。近期发布的一项研究表明[24],与单纯手术相比,包括吉西他滨和5-FU为主的辅助治疗可以延长BTC患者的OS。此外,吉西他滨的疗效优于5-FU,且有利于提高无复发生存率。而另一项研究得出与吉西他滨单一辅助治疗相比,S-1单一辅助治疗可提高淋巴结阳性PCCA患者的生存率[25]。各类研究结果互不相同,存在不少争议之处,随着后续大量研究的开展,它们之间的争议也越演越烈(表1)。GEMOXCC第Ⅲ阶段试验(NCT02548195)于2015年启动,286例ICCA患者随机分为吉西他滨加奥沙利铂和卡培他滨组。主要终点是RFS,次要结果是OS和不良事件。正在进行的ACTICCA-01第Ⅲ阶段试验于2014年启动,目的是评估辅助剂吉西他滨加顺铂对比卡培他滨的疗效和安全性[26]。我们期待这些研究能够带给我们惊喜。
2 放疗与放化疗
由于缺乏大型前瞻性随机试验数据,辅助放疗对BTC的作用仍然存在争议。一项探究辅助放疗对接受根治性GBC切除术后患者生存情况影响的研究表明,辅助放疗仅与短期生存获益相关,但这种获益会随着时间的推移而消失[27]。Leng等[28]进行的一项回顾性研究表明辅助放疗并不能提高PCCA患者的生存率。一项纳入了1 465例ECCA和GBC患者的荟萃分析显示[29],术后接受辅助放疗患者的5年总生存率与单纯手术者相比有显著改善(OR=0.63,95%CI:0.5~0.81,P=0.0002),其中N+和R+患者尤为获益。此外,该研究还表明辅助放疗组局部复发率明显低于未放疗组(OR=0.54,95%CI:0.38~0.76,P=0.0004)。但在另一项辅助治疗的大型Meta分析中[24],对于R+和N+的患者,同步放化疗可延长患者OS(HR=0.69,95%CI:0.49~1.00;HR=0.22,95%CI:0.074~0.66),而单纯放疗不能提供任何生存优势。现有的回顾性研究及荟萃分析得出了矛盾的结果,且每项研究纳入的BTC亚型不一,故对于辅助放疗的作用还需进一步证实。
2015年发表的SWOG 0809第Ⅱ阶段试验是到目前为止辅助放化疗的最高水平证据[30],基于该研究结果,Ⅲ期临床试验(NCT02798510)于2016年4月启动,共纳入140例ECCA或GBC患者,患者每三周接受一次吉西他滨加卡培他滨辅助化疗,随后随机分为基于卡培他滨的放化疗组(50.4 Gy)或吉西他滨加卡培他滨继续治疗组,共6个周期。研究的主要终点是OS,但目前尚未公布结果。在相关的临床实践指南中[31],建议对术后合并R1或N+的ECCA或GBC患者行放化疗,以降低局部复发风险。仍需要进一步的研究来确定最有可能从辅助放疗中受益的患者亚群,并需要前瞻性随机试验的数据支持。
3 靶向或免疫治疗联合化疗
随着靶向和免疫治疗在多种晚期恶性肿瘤研究中取得的进展,相关药物在术后辅助治疗领域的研究也在如火如荼的进行中(表1)。酪氨酸激酶抑制剂阿帕替尼正在进行一项Ⅱ期临床试验研究(NCT03609489),该研究比较了阿帕替尼加卡培他滨和单用卡培他滨作为BTC辅助治疗的疗效,研究主要终点是无进展生存期(Progression-free survival,PFS)。同样,阿帕替尼联合替加氟-奥沙利铂(SOX方案)目前正与单一药物阿帕替尼进行单一机构Ⅱ期临床试验(NCT03702491)的比较。这项研究计划纳入138例接受BTC切除的患者,主要终点为PFS。在免疫治疗方法方面,一项Ⅰ期试验(NCT04608786)正在评估PD-L1抑制剂ZKAB001联合卡培他滨作为BTC切除患者辅助治疗的效果,另一项正在进行的Ⅱ期试验(NCT04295317)旨在评估ICAA患者接受PD-1抑制剂SHR-1210联合卡培他滨作为辅助治疗的效果。复旦大学正在进行一项Ⅰ/Ⅱ期临床试验研究(NCT04782804),拟比较在具有高危因素的ICCA术后辅助治疗中,PD-1抗体Tislelizumab联合卡培他滨和单药卡培他滨术后辅助的疗效。
4 新辅助治疗
一些回顾性研究表明,新辅助治疗可提高BTC的R0切除率,还能改善最初不能切除的局部晚期CCA患者的预后[32-34]。目前德国有一项正在进行的Ⅲ期试验(GAIN试验)(NCT03673072),以验证新辅助治疗(术前和术后各3个周期吉西他滨+顺铂治疗+手术)相对于手术(+辅助治疗)在OS方面的优越性[35]。研究对象为胆囊切除术后发现为恶性的GBC(即所谓的偶发GBC)、可切除的ECCA和ICCA。计划招募患者数量为300人,初步结果将于2024年公布。最近在日本,JCOG1920(NABICAT)研究开始招募[36]。这是一项吉西他滨+顺铂+S-1(GCS)新辅助3个疗程再切除对比直接手术治疗可切除BTC的Ⅲ期试验,目标样本量为300,主要结果是OS。
5 小结与展望
目前,BTC全球发病率呈现上升趋势,以亚洲国家最为常见。想要改善BTC患者的生存率,首先,需要先进的诊断技术,做到早诊断和早治疗。其次,围手术期辅助治疗对于增加R0切除率及延长OS至关重要,具体的治疗手段仍需进一步探索。最后,迫切需要管理晚期疾病的新战略,提高晚期BTC的化疗敏感性。现阶段,卡培他滨在众研究中崭露头角,它是否能经得住进一步的考验我们拭目以待。辅助放疗或放化疗对R+和N+的患者有一定的益处,但仍需进一步的随机对照研究来证实。免疫及靶向治疗是未来的新希望,期待有好的结果出现能够扭转BTC患者的命运。BTC异质性极强,包括ICCA、PCCA和DCCA在内的每个亚型都有不同的基因组图谱、肿瘤生物学、临床特点和预后[37],纳入患者病理亚型的差异可能是部分研究结果不理想的原因之一。今后的围手术期辅助治疗研究有必要集中在特定的胆道亚部位,并结合靶向或免疫等新疗法[38]。现阶段大量临床研究正在积极的进行中,相信它们的结果将会开启BTC辅助治疗的新篇章。
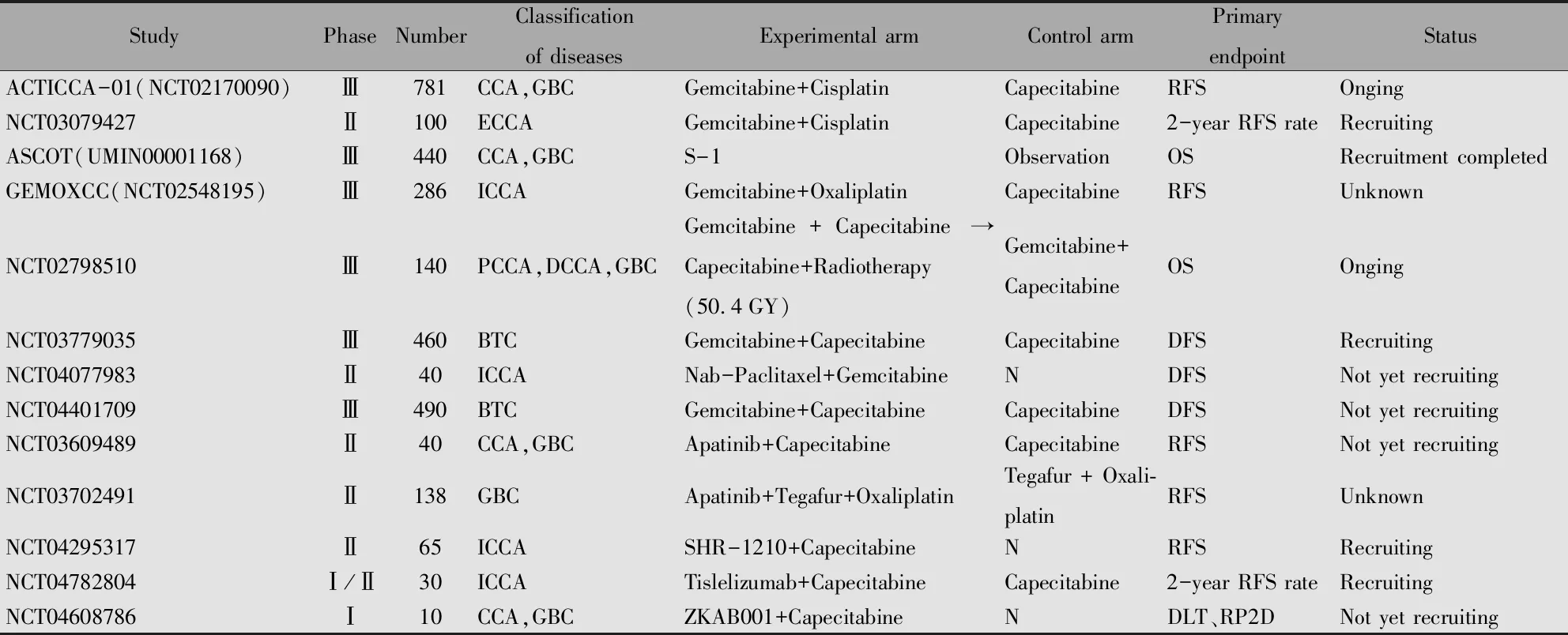
表1 胆道恶性肿瘤辅助治疗的临床试验
