复合水凝胶敷料的制备及其性能研究
2022-04-28程静静翟胜娜马春阳张洪亮司永飞刘秋华侯伟娜
程静静,翟胜娜,马春阳,张洪亮,司永飞,刘秋华,侯伟娜
(河南驼人贝斯特医疗器械有限公司,河南 长垣 453400)
皮肤组织由于致伤因子的作用出现离断或缺损后,保护层丢失,极易造成细菌感染并引起并发症,因此,具有防污染、防二次创伤、对创面进行全方位保护且具有促进创面愈合功能的新型敷料已成为研究的热点。本文选用性能优异且无毒副作用的原材料,采用清洁高效的电子束辐照交联技术,制备复合型水凝胶敷料,旨在提高水凝胶敷料的粘附性、溶胀度、韧性和抗菌性等性能,使其在医疗领域的应用更具竞争力。
羧甲基壳聚糖有良好的抗菌性、水溶性。单独的PEO和PVA水凝胶强度很低,不能满足临床应用的需求。在PVAPEO/CMCS共混的同时,加入适量的甘油,会得到一种具有抑菌性、韧性较好的新型水凝胶敷料。
1 实验材料和方法
1.1 材料与仪器
聚乙烯醇(PVA),粘度25~31 mPa·s(阿拉丁P139534);
羧甲基壳聚糖(CMCS),粘度为10~100 mPa·s(青岛弘海);
聚氧化乙烯(PEO),分子量为20万(巴斯夫);甘油(分析纯,国药集团化学试剂有限公司);
电子天平,电热恒温鼓风干燥箱,傅立叶红外光谱仪,扫描电子显微镜,真空搅拌机。
1.2 水凝胶敷料的制备
配制5%的羧甲基壳聚糖水溶液、15%聚乙烯醇溶液、10%聚氧化乙烯溶液;称取上述配制好的羧甲基壳聚糖水溶液、聚乙烯醇溶液、聚氧化乙烯溶液,以合适的比例在抽真空的搅拌釜中混合,然后加入一定量的甘油。在压片模具中铺好无纺布/聚氨酯膜,将配置好的混合液倒在无纺布/聚氨酯膜上,上面附上离型纸,挤压成所需要的形状后,经电子束辐射交联,辐射剂量为20~40 kGy,产品如图1所示。
图1 水凝胶敷料
1.3 性能分析和测试
1.3.1 凝胶质量分数
裁取样品在30℃电热鼓风干燥箱中干燥,直至重量不再变化,记录为m1,在50℃的去离子水中萃取24 h,水浴比为50∶1,继续在干燥箱中干燥,直至重量不再变化,记录为m2。
计算凝胶质量分数=(m2/m1)×100%
1.3.2 力学性能
(1)将水凝胶样品切出宽为2.5 cm的样条,若从离型纸上取下样品,松弛360 s。
(2)样条上做两个间隔约为5 cm的平行标记,测量两个标记间隔的长度,记为C1。
(3)以标记处为分界线,将条状样品的两端夹在拉力机的夹头中,并以500 mm/min的拉伸速度移动。记录样条断裂时最大的力M。
(4)断裂时的标距记为C2。
1.3.3 溶胀度
取本品3片,精密称量每片的质量M1,再将每片浸入盛有50 ml室温去离子水的烧杯中,待其充分溶胀后,立即精密称量每片的质量M2,按式(1)计算溶胀度,取其平均值,应符合上述要求。
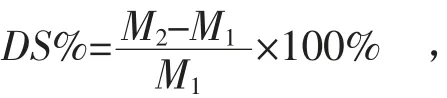
式中:DS%为溶胀度;M1为样品吸水溶胀前质量,单位为g;M2为样品吸水溶胀后质量,单位为g。
1.3.4 阻水性
打开LFY-244D医用材料阻水性性能测试仪电源开关,再分别打开加压阀和卸压阀,并向有机玻璃管顶端加纯化水,直至气泡排泄完毕。关闭卸压阀,向有机玻璃管顶端加纯化水直至液面与试样盘顶端持平。关闭加压阀,继续加水至300 mm刻度线。添加裁好的样片,将试样铺平,O型圈放入试样盘上凹槽内,缓慢放上一块不透水试样且无气泡产生,样品上表面放一张滤纸,压上上压盘,拧紧螺杆。点击开始,并打开加压阀,继续向有机玻璃管顶端加水不少于500 mm。300 s蜂鸣器响,可观察试样测试状态。按下停止旋钮,分别打开加压阀、卸压阀,排水,然后拧松螺杆,拿出样品。
1.3.5 阻菌性
依据YY/T 0471.5-2017接触性创面敷料试验方法进行试验。
(1)分别将已活化好的金黄色葡萄球菌、大肠杆菌进行菌种稀释,用无菌PBS液体对菌落进行梯度稀释到6*106 cfu/ml。
(2)将已辐照灭菌的水凝胶样品进行裁剪,规格为5 cm*5 cm,在洁净工作台中将其用镊子轻轻放在固体培养基上,然后吸取50μl菌悬液,分为5滴滴在样品上。
(3)调节生化培养箱温度为25℃,湿度为40%,将培养皿(含样品、培养基、菌液)正向放置在上述培养箱中培养48 h。
(4)在洁净工作台中去除样片,然后将培养皿(含培养基)倒置、培养。
1.3.6 红外光谱
将水凝胶敷料用Thermo Fisher公司的傅里叶变换红外光谱仪,在400~4 000 cm-1处扫描测定。
1.3.7 细胞毒性
浸提液制备:按照最新国标16886.5-2017和16886.12-2017,在无菌条件下,制备浸提液,准备细胞,进行MMT反应试验,计算细胞存活率。
2 结果与讨论
2.1 凝胶质量分数
凝胶质量分数与辐射剂量的趋势图,如图2所示,图2中a表示CMCS/PEO/PVA溶液质量比=2∶4∶8;b表示CMCS/PEO/PVA溶液质量比=1∶4∶8;c表示CMCS/PEO/PVA溶液质量比=1∶4∶6。从图1中可以看出,当辐射剂量相同时,随着PVA含量的增加,凝胶分数会增大;随着羧甲基壳聚糖的增加,凝胶分数会减少,而抑菌性能会提升;当羧甲基壳聚糖、聚乙烯醇溶液、聚氧化乙烯溶液质量比为1∶8∶4时,凝胶分数达到最大。当辐射剂量40 kGy、50 kGy、60 kGy时,凝胶质量分数趋于平缓,考虑到工业化生产时,在保证质量的前提下,节省成本,采用辐射剂量40 kGy即可满足要求。

图2 凝胶质量分数与辐射剂量的趋势图
2.2 力学性能
剂量聚乙烯醇/聚氧化乙烯/羧甲基壳聚糖(PVA/PEO/CMCS)复合水凝胶敷料的拉伸强度图、断裂伸长率,如图3所示,结果显示PVA/PEO/CMCS(PPC)3种材料复合的综合力学性能优于PVA(P)、PVA/PEO(PP)和PVA/CMCS(PC),且在30 kGy时PPC的断裂伸长率最优,在40 kGy剂量时PPC样品的拉伸强度最佳,3种材料复合水凝胶具有良好的力学性能。当PVA/PEO/CMCS以质量比为1∶8∶4复合时,加入适量的甘油,随着辐射剂量的增加,水凝胶敷料的断裂伸长率先增大后降低,拉伸强度先降低后增大。
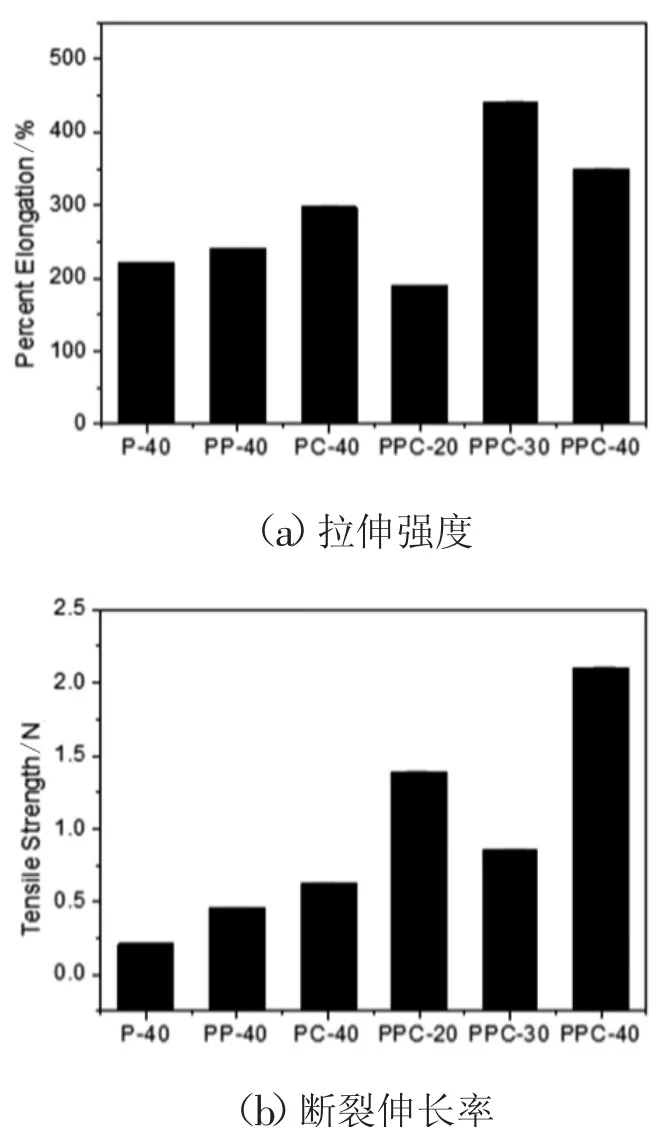
图3 力学性能实验
2.3 溶胀度
当PVA/PEO/CMCS以质量比为1∶8∶4复合时,水凝胶敷料吸水溶胀,随着浸泡时间的延长,溶胀度先增大后保持平衡,最终溶胀度大于200%;结果如图4所示。
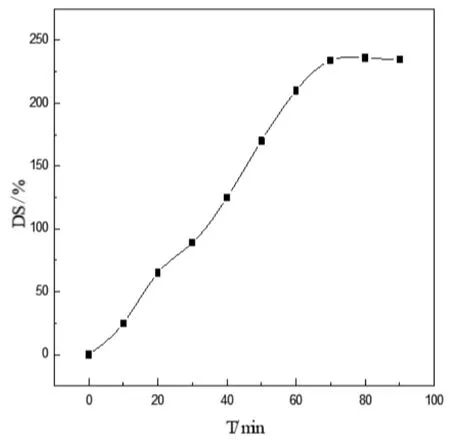
图4 溶胀度实验
2.4 阻水性
样品有良好的阻水性,能承受500 mm静水压300 s的能力,阻水性实验如图5所示。

图5 阻水性实验
2.5 阻菌性
水凝胶敷料的阻菌性测试图如图6所示,结果显示水凝胶敷料覆盖的地方无微生物生长,说明聚乙烯醇/聚氧化乙烯/羧甲基壳聚糖复合水凝胶具有一定的阻菌性。
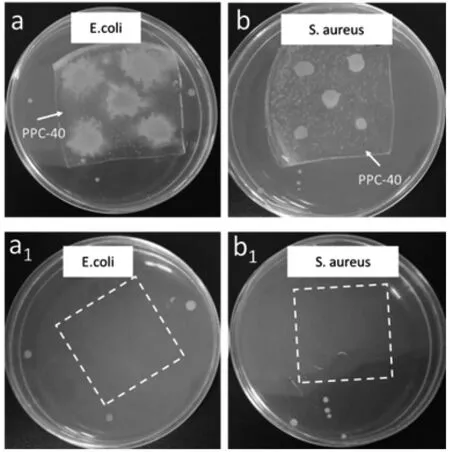
图6 阻菌性测试图
2.6 红外光谱分析
PVA/PEO/CMCS复合水凝胶材料的FT-IR图,如图7所示。在复合水凝胶中出现了新峰,说明在电子束辐射下,聚乙烯醇、聚氧化乙烯、羧甲基壳聚糖发生了交联反应。氨基官能团的出峰位置1 600 cm-1没有发生改变,所以经过辐射交联后,还具有良好的抑菌性。
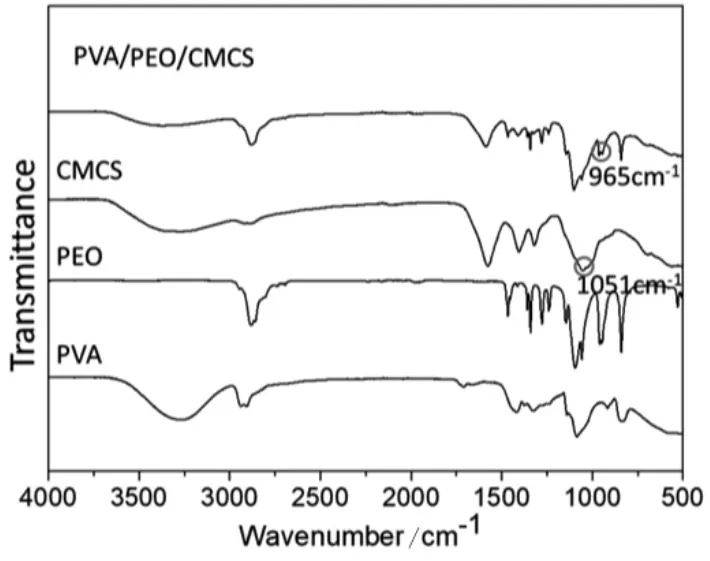
图7 红外光谱图
2.7 细胞毒性分析
通过MTT法测试水凝胶样品对小鼠成纤维细胞(L929)增值率的影响,结果显示细胞毒性不大于2级,如图8所示,满足临床使用要求。

图8 水凝胶细胞毒性
3 结论
水凝胶敷料色泽均一,呈浅白色、半透明状,表面均匀且粘度适中,溶胀度大于200%,为伤口提供湿润的愈合环境,适用于肉芽生长过程不理想的急性、慢性伤口的护理,如下肢溃疡、褥疮,还可用于二度烧伤,凝胶冰凉舒适的作用可减轻伤口的疼痛。高含水量的亲水性高分子凝结可持续的往伤口释放水分,创造伤口愈合理想的水分环境,自动调节伤口的湿润程度,可在创面停留长达7 d。水凝胶敷料的细胞毒性小于二级,且具有良好的阻菌性、阻水性和水蒸气透过率。当辐射剂量相同时,随着PVA含量的增加,凝胶分数会增大;随着羧甲基壳聚糖的增加,凝胶分数会减少,而抑菌性能会提升;当羧甲基壳聚糖、聚乙烯醇溶液、聚氧化乙烯溶液质量比为1∶8∶4时,凝胶分数达到最大。随着辐射剂量的增加,水凝胶的断裂伸长率先增大后降低,拉伸强度先降低后增大。
推向市场的产品可由水凝胶层、聚氨酯薄膜、保护层组成。与创面接触的水凝胶层,含有聚乙烯醇、聚氧化乙烯、羧甲基壳聚糖等组成的亲水高分子凝胶;半透气的聚氨酯薄膜覆于水凝胶层之上,保护贴覆于水凝胶层之下。水凝胶敷料作为医疗器械产品,为无菌产品,采用电子束辐射方式交联及灭菌;其无皮肤刺激性,无超敏反应,粘附力适宜,使用后无残留,生物相容性良好。同时在凝胶中加入抗菌物质,可以防止伤口感染,在医学临床上有重要的应用价值。
