异体原位心脏移植约14年间心电图及动态心电图特征分析一例
2022-04-27马志玲邵虹李小波杨卫平
马志玲 邵虹 李小波 杨卫平
患者男性,44岁,因扩张型心肌病于2008年1月25日在本院心脏外科行异体原位心脏移植。术后3天ECG 显示加速性交界性心律(图1A),完全性右束支传导阻滞(CRBBB)。超声心动图显示心脏移植术后,左室前壁、侧壁运动欠协调,余无明显异常。术后10天ECG 示:窦性心动过速,可见双P现象(图1B)。

图1 患者植术后3天及10天ECG
2009年1月6日患者因心脏移植术后1年,感胸闷3天主诉入院,ECG 示:CRBBB(图2A),心内膜活检:心肌细胞结构模糊,胞浆内色素沉积,部分间质轻度水肿,少量淋巴细胞浸润。给予抗免疫治疗(吗替麦考酚酯胶囊、他克莫司胶囊、醋酸泼尼松片)30天后,ECG 示:窦性心律,ECG 大致正常(图2B)。心内膜活检:未见异常。随着移植时间的延长,排异反应造成供体血管病变的加重,逐渐出现ST 段的下移,P-R 间期的延长(图2C)。
2013年左前降支(LAD)中段心肌桥收缩时压缩40%,余血管均正常;2014年右冠状动脉(RCA)近端50%狭窄,中端30%狭窄,D1支30%狭窄,左回旋支(LCX)全程30%狭窄,OM2 40%狭窄。2014年11月18日因窦性停搏(最长7.54s),间歇高度、Ⅱ度房室传导阻滞在心脏内科行双腔永久起搏器植入术(图3)。术后5年内起搏器囊袋感染2次,经反复抗感染及清创术无效,行起搏器拔除术。术后多次发生晕厥伴意识丧失,ECG 提示:窦性停搏(图4A),最长13 s。与家属沟通后2019年12月19日植入Micra起搏器,术后6个月程控监测提示参数稳定,心室起搏百分比(VP)1.5%(图4B),现患者健康存活。
讨论 通过本例患者移植后14年ECG 及Holter的观察,符合异体原位心脏移植ECG 图形改变,疾病发展过程中Holter对患者手术策略的选择起到了至关重要的作用。
标准的原位心脏移植术,保留了右房及左房后壁,移植后最显著的变化是双窦房结现象、心脏去神经状态及心脏排斥反应[1]。在患者多次的ECG 中均可显示如图1。患者移植后即刻心律为加速性交界性心律(图1A),可能由于移植后心肌水肿,房室结区抢先占领主导节律,随着水肿的消退,大概10天后,供体窦房结成为主导节律,此时可见双P波现象,受体的自身的P不能下传心室,在ECG 上顺序发生,形成完全性阻滞和完全性心房脱节状态(图1B)。文献报道[1],多数受体心脏右冠状动脉被切除后,随着时间的推迟,受体窦性频率有可能逐渐减慢,甚至消失。本例患者在移植术14年后,受体的自身P波仍存在,可能与自身窦房结动脉供血未中断有关。心脏去神经状态是心脏移植后不再受心脏交感和迷走神经的影响,ECG 上表现为窦性心律加快。本例患者移植后,多年Holter显示患者平均心室率呈逐年增长趋势(2008 年76 次/分;2 009 年80 次/分;2014 年89次/分;2019年94次/分),由于供体不受体神经支配,用β受体阻滞剂对心室率控制疗效甚微。其次,通过观察患者的症状及ECG 的变化可以对心脏排异反应进行初步判断,当发现患者出现心慌、乏力、气短等症状,心率变化,早搏次数增加以及新出现的心律失常、各导联电压的变化时,应及时行心肌内膜活检,明确心脏排异反应的严重程度,及时调整药物剂量。本例患者多次因心慌胸闷之主诉入院,ECG表现为(图2A)心率增快,CRBBB 出现,此时入院心内膜活检显示:心肌细胞结构模糊,胞浆内色素沉积,部分间质轻度水肿,少量淋巴细胞浸润。心肌活体标本:右室心内膜下,心肌纤维萎缩伴退行性变及慢性炎症。此时内毒素测定31.98 ng/ml,正常参考值(0~10 ng/ml);当随着抗排异药物(吗替麦考酚酯胶囊和他克莫司胶囊)、激素(醋酸泼尼松片)剂量的增加,排斥反应的减小CRBBB 消失(图2B);当下一次排异反应加重后CRBBB 又重新出现,且随着移植时间的延长,P-R 间期逐渐延长,下壁导联QRS波电压减小,异常Q波出现(图2C),此时心肌核素灌注显像示:左室心尖部、后侧壁、下后壁局限性心肌血流灌注轻-中度减低,左室间壁心肌室壁运动搏幅减低,与ECG变化相一致。此前已有文献报道[2]:新发的右束支传导阻滞70%存在移植排斥,移植术后出现右束支传导阻滞与移植排斥反应相关。因此,通过ECG 前后对比变化,某种程度上可以减少患者有创性心内膜活检的次数。Holter可以捕捉多种心律失常,弥补ECG时程短,信息量小的特点。本例患者多次ECG 检查均显示正常,但是Holter确捕捉到高度、Ⅱ度房室传导阻滞及长时间窦性停搏(图3 A),随后行双腔永久起搏器植入术(图3B)。移植心脏发生房室传导阻滞多在术后晚期[3],机制尚不明确,小规模单中心研究认为与移植冠状动脉疾病有关[4],心脏移植后5 年约40%~50%的受体经血管造影证实,发生了移植物冠状动脉疾病,表现为血管内膜呈向心性增生且病变弥散,冠状动脉从近端至远端均受累[5]。本例患者在心脏移植后6 年出现高度、Ⅱ度房室传导阻滞。该患者在住院期间做过两次冠状动脉造影,两次造影提示心脏移植冠状动脉病变发展速度非常之快,心脏排斥反应可能是造成血管病变的直接原因。与之前文献报道一致[1]。

图2 患者移植术后1年及10年的典型心电图
本例患者在起搏器植入术后2年就出现了起搏器切口不愈合,经过多次反复清创术、抗感染治疗仍无法控制感染,随后进行了双腔起搏器拔除术。术后1周内患者因反复晕厥就诊,Holter显示多次窦性停搏(图4A),最长停搏13 s。原位心脏移植后患者出现缓慢型心律失常多表现为间歇性传导阻滞或病窦综合征,且再植入有导线心脏电子装置起搏器囊袋感染的发生率较高。Micra起搏器是VVI起搏模式,它可通过微创方式植入心脏内,无导线、无囊袋,感染风险明显降低,因此Micra植入应该是该患者最佳选择方式,术后患者恢复良好(图4B)。经文献查阅目前移植心脏Micra植入国内尚属首例[6]。
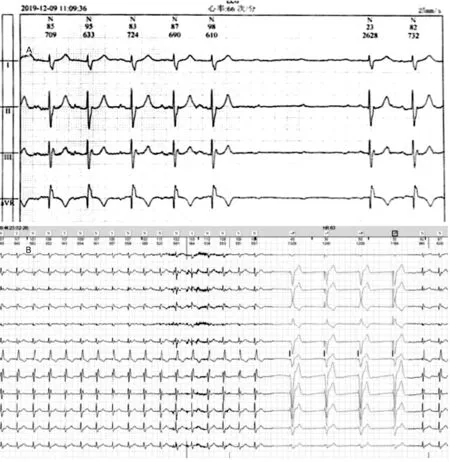
图4 患者2019年起搏器拔除术后及Micra起搏器植入后动态心电图
回顾该患者近14年来的临床资料及ECG、Holter及其他辅助检查资料,不难发现,常规无创心电检查在异体原位心脏移植术后心脏排异反应监测、心律失常及心功能检测中至关重要,临床医生应该掌握这些心电学特征,密切结合患者症状及时对治疗方式作出反应。
