基于证据推理与模型认知的高中化学教学设计*
2022-04-26张延婷杨艳华李艳妮王建坤
孙 昊, 张延婷, 杨艳华, 李艳妮, 王建坤
证据推理与模型认知作为《普通高中化学课程标准(2017年版)》提出的五大核心素养之一, 要求学生基于证据对物质组成、 结构及其变化提出可能的假设, 通过分析推理加以证实或证伪, 建立观点、 结论和证据之间的逻辑关系[1]。 高中二年级学生已有一定的化学基础, 但缺乏整合化学知识的能力, 不能很好地运用已有知识进行推理及分析, 同时缺少对模型的理解, 不能形成完整的知识体系。 教师应考虑学生的学习情况及认知能力, 精心设计教学活动, 培养学生的证据推理与模型认知的能力, 才能解决这些问题。 本文以人教版高中化学选择性必修3 中《第三章 烃的衍生物》 “第二节 醇 酚” 中的乙醇为代表物质, 进行乙醇的教学设计, 乙醇化学性质的知识内容学习进阶过程如图1 所示。 为了帮助学生理解乙醇的物理性质和化学性质, 构建乙醇分子的模型, 分析官能团与乙醇性质的关系, 通过学生现有的认知水平知识进行推理, 结合实验探究来证明乙醇的性质, 达到在实验中培养发展学生的证据推理意识的目的。

图1 乙醇化学性质在教材中呈现的学习进阶过程Fig.1 Advanced learning process of chemical properties of ethanol in teaching material
1 证据推理
“证据推理” 是指在化学教学中, 通过有效的证据事实或数据资料, 对假设进行合理的推理论证[2]。 在进行化学教学时, 教师需要提前设计探究性的问题, 引导学生应用已有的知识作为证据推理的前提, 进而激发学生的想象力和推理能力。
证据推理有利于教师开展实验探究教学, 通过教师进行实验操作, 学生观察实验现象, 同时运用证据推理去发现问题,分析问题, 解决问题。 以乙醇的燃烧为例, 教师根据学生已有的元素守恒观念, 推理乙醇燃烧后的产物必然由作为可燃物(乙醇)中碳元素和氢元素, 以及助燃物(氧气)的氧元素组成,以此为基础进行合理推测, 并通过实验进行探究, 可以初步推断出燃烧产物可能为CO、 CO2和H2O。 在初步结论的基础上,通过实验进行对结果进行检验。 用玻璃片检测有无色透明液体生成, 根据元素观和守恒观, 合理推测此液体为水, 再收集乙醇燃烧后的气体, 通入澄清的石灰水来检测二氧化碳, 以此用实验证据来证明学生的推理是正确的。
2 模型认知
化学课程标准中的“模型认知” 是指化学教育工作者在教学工作中必须具备的一种能力、 思维、 手段, 是在进行一定的教学活动对特定知识点进行的具象化教学[3]。 例如教师在进行乙醇的氧化反应的教学活动时, 乙醇在催化作用下, 氧化生成乙醛, 继续经过催化氧化生成了乙酸, 教师可以利用结构示意图(图2)帮助学生建立化学模型, 帮助学生攻克难点, 使化学知识结构简单化, 有利于培养学生学习的积极性, 同时增强学生的自信心。“模型认知” 在化学教学中起到重要的作用, 有利于提高课堂教学的效率, 推进教学过程的开展。 以乙醇的沸点为例,根据数据可知, 乙醇的沸点要高于丙烷的沸点(乙醇相对分子质量为46、 丙烷相对分子质量44, 两者相对分子质量较为接近), 简单的性质背后隐藏着一个知识难点(氢键), 这时教师可以利用乙烷的分子结构模型和乙醇的分子结构模型, 提醒学生观察两个分子结构模型的区别, 进而发现乙醇存在着分子间氢键(氢键的形成是由于氧原子电负性远远大于氢原子电负性造成的), 所以学生就能理解乙醇的沸点要高于丙烷的沸点。利用模型可以培养学生的观察能力以及理解能力, 模型可以使学生更容易了解微观物质, 同时提升学生对化学微观世界的兴趣。

图2 乙醇氧化过程的两个阶段Fig.2 Two stages of ethanol oxidation

图3 乙醇分子间可形成分子间氢键、 丙烷不能形成分子间氢键Fig.3 Intermolecular hydrogen bonds can be formed in ethanol, but not in propane
3 基于证据推理与模型认知的教学设计
3.1 核心目标
(1)证据推理与模型认知
通过教师展示乙醇分子结构模型, 促使学生初步构建知识框架; 通过教师根据已有证据对学生进行引导, 让学生感受化学的魅力, 发展学生的科学素养。
(2)宏观辨识与微观探析
通过教师引导学生从分子的结构与性质进行联系, 帮助学生形成结构决定性质的观念, 培养学生的科学思维。
(3)科学精神与社会责任
通过教师进行演示实验与教师指导学生进行实验, 激发学生的好奇心, 同时培养学生严谨求实的科学态度。
3.2 教学重点
(1)乙醇的物理性质和化学性质。
(2)乙醇发生取代反应、 消去反应、 氧化反应的化学方程式。
3.3 教学难点
乙醇的消去反应和氧化反应。
3.4 教学方法
实验演示法、 讨论法、 讲授法。
3.5 教学内容
3.5.1 醇的物理性质
(1)情境导入: 疫情期间要注意防范病毒的感染, 外出回归后首先要做的就是用75%的酒精进行消毒, 而酒精也就是今天所学的乙醇俗称, 接下来我们一起学习乙醇的结构以及性质。
设计意图: 以疫情期间的防护措施为基础进行导入, 使学生体会到从生活中走进化学。
(2)乙醇的物理性质: 把准备好的乙醇展示给学生观察,并引导学生从颜色、 状态、 气味来描述乙醇的物理性质。
设计意图: 举例切合实际生活, 加强学生的生活常识。 通过观察乙醇溶液, 既直观的学习乙醇的性质, 又加深学生的理解。
(3)小组讨论: 在烷烃部分学习到烷烃的沸点随碳原子数的增加而升高, 但乙醇的沸点为什么比相对分子质量接近的烷烃或烯烃的沸点高?

图4 乙醇分子的结构模型Fig.4 Structure model of ethanol molecule
设计意图: 学生进行小组讨论, 有利于培养学生团结的精神。 教师以结构模型进行教学, 帮助学生建构乙醇分子的模型认知, 使学生初步形成基本的有机化学概念体系。
3.5.2 乙醇的取代反应
以乙醇与氢溴酸在加热的条件下反应为例, 乙醇分子中的什么基团被谁取代? 与Na 的反应有何不同?

图5 乙醇与氢溴酸发生的取代反应Fig.5 Substitution reaction of ethanol with hydrobromate
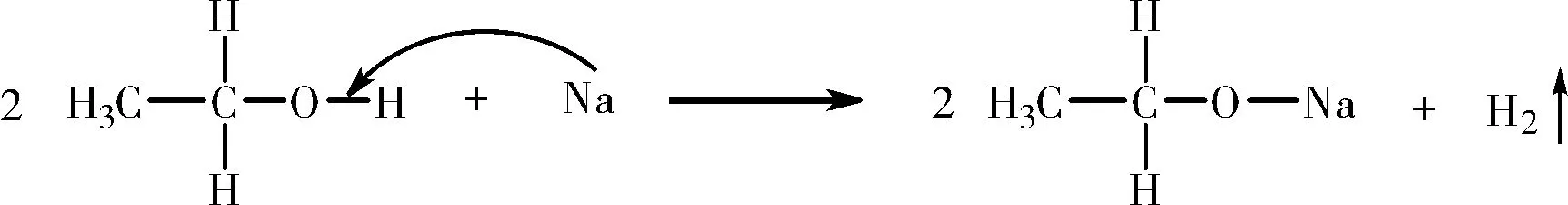
图6 乙醇与钠发生的取代反应Fig.6 Substitution reaction of ethanol with sodium
设计意图: 利用已有知识与新知识之间的联系, 通过引导学生利用证据进行推理, 帮助学生了解乙醇的取代反应过程。
小结: C-O 键和O-H 键都是极性共价键, 且O 的电负性更大, 共用电子对偏向O 原子, 酸中的H+易于O 结合, 削弱了C-O 键, 反应中羟基被卤元素取代, 脱去一分子H2O。 同理, O-H 键中共用电子对也偏向O 原子, 使H 带有部分正电荷, 显示酸性, 可与活泼金属Na 反应, O-H 键断裂, 反应中羟基中的H 被取代, 产生H2。
设计意图: 对乙醇与金属Na 和HBr 发生的取代反应进行总结, 对两种不同的取代类型进行比较, 便于学生从共价键角度理解乙醇的化学性质, 增强证据推理素养。
过渡与拓展: 乙醇分子除了能与氢溴酸发生取代反应, 还能在浓硫酸作催化剂及加热的条件下, 一个乙醇分子脱去碳链上的-OH, 而另一个乙醇分子脱去-OH 上的氢原子, 最后的到的产物是乙醚和水, 这样的反应叫做分子间脱水反应。
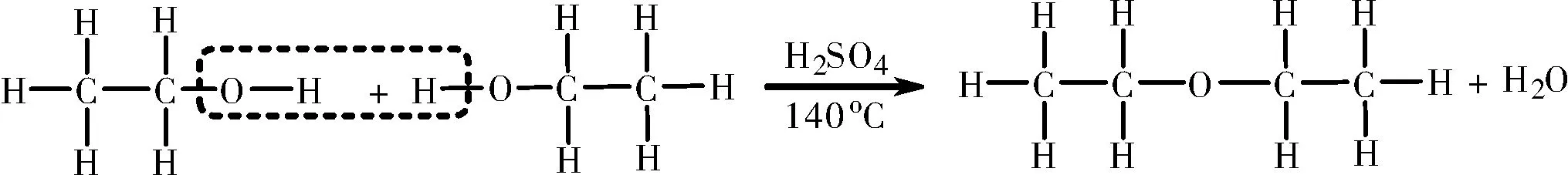
图7 乙醇分子间的脱水反应Fig.7 Dehydration reaction between ethanol molecules
3.5.3 乙醇的消去反应
乙醇发生分子间脱水反应生成乙醚, 若将上面反应的温度迅速升高至170 ℃后, 就可脱水生成乙烯。 在该反应中, 浓硫酸的作用是催化剂和脱水剂。 乙醇在酸性条件下加热, 羟基与酸的氢离子作用生成水离去, 此时与羟基相连的碳原子变成C+, 与它相邻的碳上失去氢质子, 电子转移到C+中和正电荷,形成双键, 从而生成不饱和有机化合物的反应, 叫做消去反应[4]。
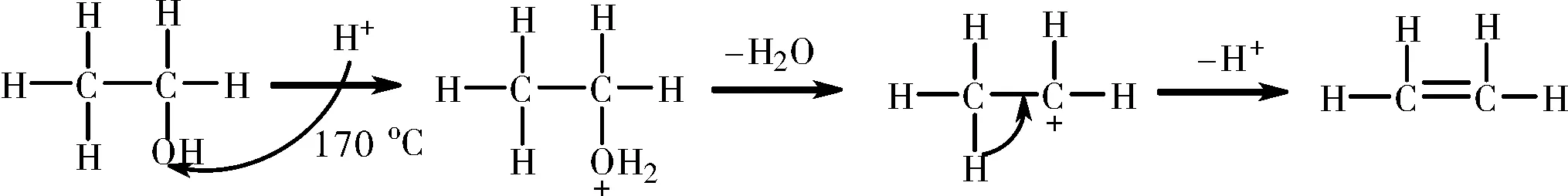
图8 乙醇发生消去反应的机理图Fig.8 Mechanism diagram of ethanol elimination reaction
设计意图: 通过教师的引导, 利用已知证据, 帮助学生学会知识的迁移, 并加强学生的证据推理能力, 同时达成丰富化学知识体系的目的。
小结: 乙醇在浓硫酸及加热的条件下, 不同温度下所发生的反应和得到的产物是不同的。 在140 ℃的条件下发生取代反应, 产物是乙醚和水; 在170 ℃的条件下发生消去反应, 产物是乙烯和水, 二者反应容易混淆, 要学会辨别。
设计意图: 对取代反应和消去反应的内容进行小结, 既巩固了所学知识, 又对新知识进行了区分, 一举两得。
3.5.4 乙醇的氧化反应
乙醇在铜作催化剂的条件下, 能与氧气发生氧化反应, 除了这个方法, 请同学们大胆猜测, 乙醇还能被其他氧化剂氧化吗?
演示实验: 乙醇与酸性K2Cr2O7溶液反应, 可观察到溶液由橙色变为绿色。
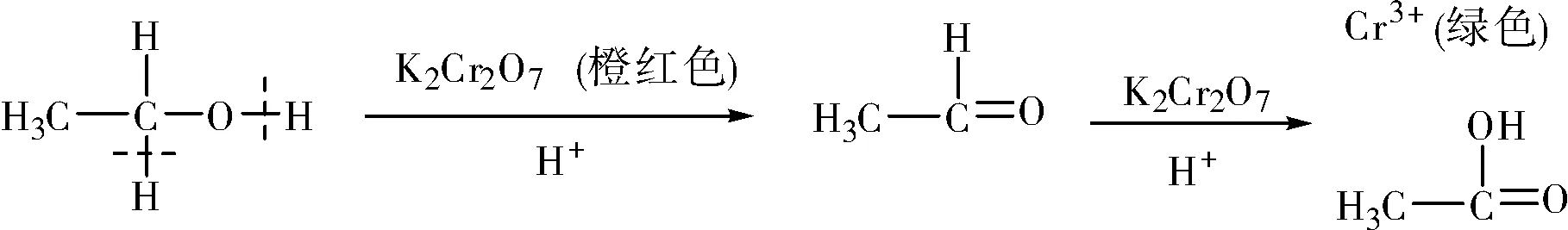
图9 乙醇的催化氧化反应Fig.9 Catalytic oxidation of ethanol
设计意图: 教师通过引导学生描述实验现象, 培养学生的语言表达能力和逻辑思维能力。 由于醇羟基的影响, 使得COH 中与C 相连的H 较为活泼, 容易被氧化或脱氢。
教师讲解: 在反应中, 酸性的K2Cr2O7为氧化剂, 氧化反应过程总颜色变化较为明显, 且不用加热, 根据此原理设计呼吸分析仪, 可用于检测司机是否酒驾[5]。
设计意图: 理论联系实际, 充分理解学以致用, 增加学生对知识点的理解, 增强专业自豪感。
小结: 本章我们学习了乙醇的取代反应、 消去反应和氧化反应。 其中取代反应是由乙醇与氢卤酸在加热的条件下进行反应, 而且乙醇在浓硫酸加热(140 ℃)的条件下发生分子间脱水反应, 生成乙醚; 消去反应是由乙醇在浓硫酸加热(170 ℃)的条件下发生分子内脱水反应, 生成乙烯; 氧化反应是乙醇与酸性重铬酸钾进行反应, 直接氧化成乙酸。

图10 乙醇的化学反应断键模型Fig.10 Chemical reaction bond breaking model of ethanol
设计意图: 将乙醇的所有反应利用模型进行总结, 加深学生的理解, 同时归纳本节课时的所有知识点, 完善学生的知识体系。
4 结 语
在本次的教学设计中, 通过精心设置教学环节, 引导学生对学过的知识点进行回顾, 从而达到加强学生证据推理能力的目的, 形成完整的知识体系。 在学习有机化学的过程中, 需要加强学生对有机化合物分子的认知, 采用模型的形式进行教学, 通过教师讲解模型, 加强学生对模型的认知, 从而提高学生对化学学科的理解能力, 激发学生学习化学的兴趣, 从而达到培养学生发展证据推理和模型认知的目标。
