微波消解-分光光度法测定面食中的铝含量
2022-04-25胡庆兰
胡庆兰
(湖北第二师范学院 化学与生命科学学院,武汉 430205)
1 前言
铝是地壳中含量最丰富的金属元素,自然界中的铝主要源于地质矿化、冶金等而广泛存在于自然界中。铝长期以来作为低毒物质用于抗酸药、食品容器和炊具、食品包装材料、饮水中混凝剂以及食品添加剂[1]。面食作为我国北方大部分地区的主食,铝元素在面食产品中主要来源于泡达粉[2]中,泡达粉在面制食品中主要起疏松膨化作用,尤其是在饼、面包等一些膨化食品中使用广泛。我国也于1994年提出了面制食品中铝的限量卫生标准(≤100mg/kg)[3]。人们在日常生活中摄入一定量的铝,经机体吸收,如果不能及时排出体外,就会残留在人体的组织细胞中,铝的大量摄入会在人体内蓄积而产生慢性毒性。
铝的神经系统毒性:唐焕文等[4]研究表明,人体长期摄入过量的铝,并没有及时地排出体外,可引起大脑顶叶、小脑及海马神经元细胞的数目减少,进而会导致学习记忆功能出现障碍。人体若长期过量摄入铝,而机体又没有及时排出过量的铝元素,会导致人体的平衡失调,认知能力、记忆能力以及逻辑推理能力下降。
铝的骨骼毒性:王晓波[5]通过动物试验表明,铝的摄入浓度与骨蓄积程度之间存在着明显的正相关的关系,过量的铝摄入量会导致人体血磷降低,进而导致骨质脱钙。黄国伟[8]等研究发现铝能直接损害体外培养的人胚成骨细胞的活性,会使细胞变性坏死,从而抑制骨的基质的合成。
铝的生殖毒性:张本忠[6]等探讨铝的发育毒性及机理,通过大鼠胚胎体外培养测量卵黄囊直径、胚胎干重、胚胎体长及头长得出结论,随着铝试剂计量的增加,反映胚胎生长发育和器官分化的各项指标呈现出下降趋势,有一定的剂量与效应关系。当铝试剂的量大于一定时,胚胎的形态分化以及发育情况会受到抑制,同时胚胎畸形的发生率明显变高。
铝的免疫毒性:韦小敏[7]等通过将T、B淋巴细胞进行体外短期培养,探讨铝对人T、B淋巴细胞合成肿瘤坏死因子的影响,试验得出结论铝对人T、B淋巴细胞的生长以及合成分泌肿瘤坏死因子有着直接的抑制作用。
微波消解[8-10]是利用消解液和试样能够吸收微波的能量而被加热,使试样分解。由于微波消解一般采用密闭容器,这样可以加热到较高温度和压力,使样品分解得更完全,同时也可以减少样品和溶剂的用量及易挥发组分的损失。微波消解由于具有快速、准确、省费用、污染少等诸多优点,被广泛应用于植物、土壤、食品等诸多物质的消解。
分光光度法[11]是利用溶液中待测元素与某些显色剂反应生成有色化合物,根据化合物颜色的深浅与溶液中待测元素的含量成正比来测定待测物的浓度,该方法是建立在物质对光的选择性吸收的基础之上的分析方法,符合光的吸收定律:A=kbc(朗伯-比尔定律)。在分光光度法测定铝的含量时,以铬天青S为显色剂来测定铝元素的含量是最常用的一种方法[12-13],铬天青S分光光度法也是目前食品中铝含量测定的国家标准方法。分光光度法由于方法操作简单,灵敏度高,而被广泛使用。
本实验旨在研究测定面食中铝元素的含量,采用微波消解对面食样品进行消解,采用分光光度法测定其中的铝含量,为消费者不盲目食用高铝含量的面食,且为面食中铝含量的测定进一步研究提供了相关实验依据。
2 实验部分
2.1 实验试剂、材料和仪器
铝标准溶液(1000μg/mL,国家有色金属及电子材料分析测试中心)、氨水、浓硝酸、盐酸、对硝基苯酚、硫酸、无水乙醇、乙二胺、抗坏血酸(均为分析纯,国药集团化学试剂有限公司)、聚乙二醇辛基苯醚(TritonX-100)、溴代十六烷基吡啶(CPB)、铬天青S(均为分析纯,上海麦克林生化科技)。
本实验所用水均为超纯水,所用的玻璃仪器均需在使用前用10%硝酸浸泡24h,然后用超纯水冲洗,待其干燥后再使用。在使用微波消解仪时,应该提前将微波消解仪的内罐用10%~20%的硝酸浸泡24h,然后用超纯水清洗,将其晾干,其外壁一定要保持干燥才可将样品装罐再进行消解。
实验样品太阳饼、馒头于湖北第二师范学院楚才源食堂购买。手撕面包在面包店购买。
光束TU-1950型紫外可见分光光度计,TANK BASIC微波消解仪,赶酸器(TK12),QYZH-20A
型超纯水机,ST2100型pH计,FA-2004型电子天平。
2.2 实验方法
2.2.1 标准溶液的配制
100mg/L铝标准中间溶液:准确吸取2.50mL铝标准溶液(1000mg/L)于25mL容量瓶中,用5%硝酸溶液进行定容,至刻度,摇匀,贴上标签。
1.00μg/mL的铝标准使用溶液:准确吸取1.00mL铝标准中间液置于100mL容量瓶中,再用5%硝酸溶液进行定容,至刻度,摇匀,贴上标签。
2.2.2 样品处理
微波消解:准确称取研磨的太阳饼样品0.2000g、面包样品0.2000g、馒头样品0.5000g 于微波消解仪的内罐中,再依次向其中加入10.00mL硝酸,静置10min,然后拧紧消解罐盖子,放于微波消解仪中,按一定的程序(见表1)进行消解,消解完成后,待温度降到60℃时,取出消解罐,然后将其置于赶酸器中,液体接近1~2mL时取出,待其冷却至室温,将消化液倒入烧杯中,用超纯水稍稍润洗消解罐并转移至烧杯中,然后转移至50mL容量瓶中,并用超纯水定容,作为待测液。
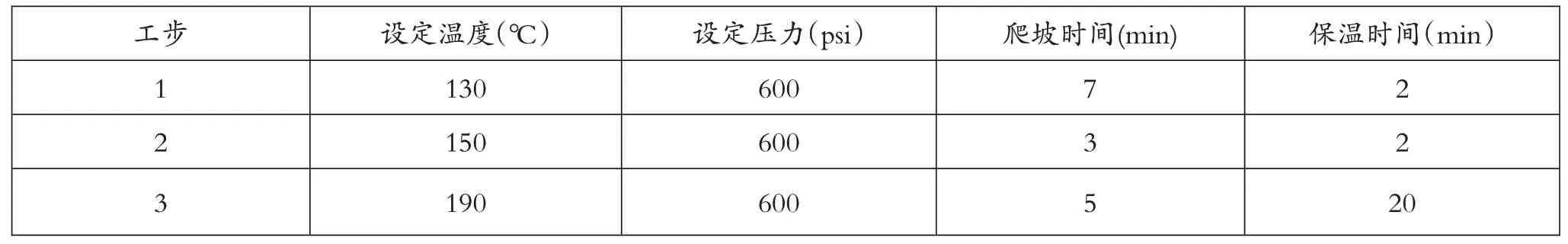
表1 微波消解程序
2.2.3 标准曲线的绘制
取7 只25mL 的比色管,用移液管分别向其中加入0.00mL、0.05mL、1.00mL、2.00mL、3.00mL、4.00mL、5.00mL 1.00μg/mL 铝标准使用溶液,1.00mL 1%硫酸溶液,再分别依次加入超纯水至10mL 刻度线,加入1 滴1g/L对硝基苯酚乙醇溶液,滴加(1+1)氨水溶液至溶液为浅黄色,再加入2.5%硝酸至浅黄色消失,用移液管继续加入1.00mL2.5%硝酸溶液,1.00mL 10g/L 抗坏血酸,2.50mL 1g/L 铬天青S 溶液,再继续滴加1.00mL 3%TritonX-100溶液,3.00mL 3g/LCPB 溶液,加入3.00mL乙二胺-盐酸(pH=6.7~7.0)溶液,用超纯水稀释至刻度,摇匀。静置30min后,用1cm比色皿,以不加铝标液的试剂为参比,测定其各溶液的吸光度,绘制铝标准曲线。
3 结果与讨论
3.1 最佳波长的选择
在编号为1、2 的两只25mL 的比色管中各加入铝标准使用溶液0.00mL、5.00mL,再分别依次加入超纯水至10mL刻度线,加入1滴1g/L对硝基苯酚乙醇溶液,滴加(1+1)氨水溶液至溶液为浅黄色,再滴加2.5%硝酸至浅黄色消失,用移液管量取2.5%硝酸1.00mL 加入比色管中,1.00mL 10g/L 抗坏血酸,3.00mL 1g/L 铬天青S溶液,再继续滴加1.00mL 3%TritonX-100溶液,3.00mL 3g/L CPB溶液,加入3.00mL乙二胺-盐酸(pH=6.7~7.0)溶液,用超纯水稀释至刻度,摇匀。40min 后,用1cm 比色皿,以不加铝标准溶液的空白试剂为参比溶液,在570~650nm之间测吸光度,绘制吸收曲线。
从表2中可以看出,在615nm处,吸光度有最大值,即最佳吸收波长为615nm。

表2 波长与吸光度的关系
3.2 显色剂用量的选择
取7只25mL比色管,分别编号,向其中各依次加入5.00mL铝标准使用溶液、加入超纯水至10mL刻度线、1滴1g/L对硝基苯酚乙醇溶液,继续滴加(1+1)氨水溶液至溶液为浅黄色,滴加2.5%硝酸溶液直至溶液的浅黄色消失,继续加入1.00mL2.5%硝酸溶液,1.00mL 抗坏血酸溶液,再分别加入不同体积的铬天青S(1.00mL、1.50mL、2.00mL、2.50mL、3.00mL、3.50mL、4.00mL)溶液,1.00mL 3%TritonX-100 溶液,3.00mL 3g/LCPB 溶液,加入3.00mL乙二胺-盐酸(pH=6.7~7.0)溶液以超纯水稀释至刻度,摇匀,放置40min后,以超纯水为参比溶液,在选定波长615nm下测定各溶液的吸光度,确定显色剂的最佳用量。
由表3可以看出,不同显色剂用量,其吸光度值不同,显色剂的最佳用量为2.50mL。

表3 显色剂用量与吸光度关系
3.3 抗坏血酸用量的选择
分别给7只25.00mL比色管,分别编号,向其中各依次加入5.00mL铝标准使用溶液、加入超纯水至10mL刻度线、1滴1g/L对硝基苯酚乙醇溶液,继续滴加(1+1)氨水溶液至溶液为浅黄色,滴加2.5%硝酸溶液直至溶液的浅黄色消失,继续加入1.00mL2.5%硝酸溶液,再分别向其中加入0.50mL、1.00mL、1.50mL、2.00mL、2.50mL、3.00mL、3.50mL、4.00mL 的抗坏血酸溶液,加入2.50mL 铬天青S 溶液,1.00mL 3%TritonX-100 溶液,3.00mL 3g/LCPB溶液,加入3.00mL乙二胺-盐酸(pH=6.7~7.0)溶液以超纯水稀释至刻度,摇匀,放置40min后,以超纯水为参比溶液,测定掩蔽剂用量不同时溶液的吸光度,在波长615nm下测定各溶液的吸光度,确定抗坏血酸的最佳用量。
由表4 可以看出,掩蔽剂抗坏血酸的用量为1.00mL 时,吸光度值最大,本实验加入的抗坏血酸用量为1.00mL。

表4 抗坏血酸用量与吸光度关系
3.4 标准曲线的绘制
根据表5 数据,以吸光度为纵坐标,溶液浓度为横坐标,绘制铝标准曲线如图,可知,铝标准溶液在0~0.2μg/mL浓度范围内,标准曲线呈较好的线性关系。

表5 铝元素吸光度值
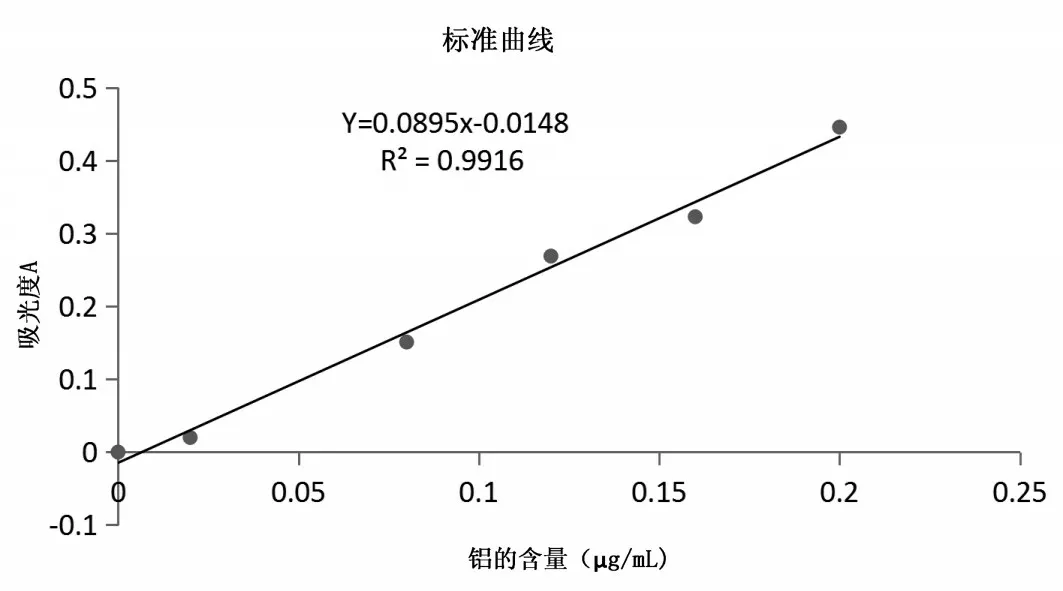
图1 铝标准曲线图
3.5 精密度分析
平行测定五次铝元素的吸光度值,求平均值,计算RSD,以此来表示分析结果的精密度。测定结果如表6:

表6 重现性实验结果
从表中可以看出,溶液中铝元素的RSD为1.00%,说明实验结果较可靠。
3.6 样品中铝的含量
取2只25mL比色管,分别移取0.00mL、1.00mL待测液于比色管中,然后依向25mL比色管中依次加入超纯水至10mL刻度线,加入1滴1g/L对硝基苯酚乙醇溶液,滴加(1+1)氨水溶液至溶液为浅黄色,再滴加2.5%硝酸至浅黄色消失,用移液管继续加入1.00mL 2.5%硝酸溶液,1.00mL 10g/L 抗坏血酸,2.50mL 1g/L 铬天青S溶液,再继续滴加1.00mL 3%TritonX-100溶液,3.00mL 3g/L CPB溶液,加入3.00mL乙二胺-盐酸(pH=6.7~7.0)溶液,以超纯水稀释至刻度,摇匀。静置30min,以不加待测液为参比溶液,在波长615nm下测定样品的吸光度,将其吸光度带入标准曲线从而求得样品中铝的含量。对样品平行测定三次,取平均值。测得其含量值分别见表,从表中数据可以看出,面食样品经过微波消解预处理后,用分光光度法测定太阳饼样品中铝元素的含量为676.3038μg/mg。手撕面包样品中铝元素的含量为83.2417μg/mg;馒头样品中铝元素的含量为29.1976μg/mg。

表8 太阳饼中的铝含量

表9 手撕面包中的铝含量

表10 馒头中的铝含量
3.7 加标回收率实验
为了验证实验的准确性,对三种不同品种的面食样品进行加标回收率实验,铝元素的加标回收率在89.95%~114.75%,结果见表11

表11 面食中铝元素加标回收率
4 结论
本实验用微波消解法将三种不同面食样品进行消解,消解液澄清透明,说明面食样品被消解得很完全。同时采用分光光度法测定三种不同面食样品中铝元素的含量,实验结果表明微波消解—分光光度法测定面食中的铝含量快速、简单,精密度高。实验测得样品太阳饼中铝元素的含量为676.3083μg/mg;手撕面包中铝元素的含量为83.2417μg/mg;馒头中铝元素的含量为29.1976μg/mg;RSD为1.00%,相关系数为0.9916;铝元素的加标回收率为89.95%~114.75%。实验测定的结果表明不同的面食中铝元素的含量不尽相同,其中太阳饼中铝元素的含量最高,手撕面包中铝元素的含量次之,馒头中铝元素的含量最低。
国家标准食品中铝元素的添加量不得超过100μg/mg,而实验中测定太阳饼中的铝含量是国家标准的6~7倍,该样品含铝量偏高,若长期食用,铝摄入量过高,铝在体内没有及时排除,会对人体造成危害。而手撕面包和馒头中铝元素的含量符合国家标准,人们可以放心食用。实验结果提醒人们平时应该多注意面食的食用,自觉提高抵制高铝含量食品的意识,维持人体健康。
