在线净化加速溶剂萃取–气相色谱–质谱法测定土壤中11 种半挥发性有机物
2022-04-25李婧耶曼张利王岚
李婧,耶曼,张利,王岚
(西安西北有色地质研究院有限公司,西安 710054)
我国于2018 年8 月1 日实施了GB 15618—2018 《土壤环境质量 农用地土壤污染风险管控标准》和GB 36600—2018 《土壤环境质量 建设用地土壤污染风险管控标准》,其中农用地主要是耕地﹑园地﹑林地﹑草地等,建设用地主要是建造建筑物﹑构筑物的土地,包括城乡住宅和公共设施用地﹑工矿用地﹑交通水利设施用地﹑旅游用地﹑军事用地等[1–3]。当这两类土壤受到污染后,在农用地上生长的农作物或土壤生态环境会受到不利影响,在建设用地上居住﹑工作的人群会产生慢性中毒或致癌致畸风险。因此进行土壤污染物检测非常有必要。半挥发性有机物(SVOCs)作为最重要的污染物之一,其种类繁多,特性复杂,由于分子量大﹑沸点高,因此在环境中较挥发性有机物更难降解,容易在水﹑土壤﹑空气﹑生物等介质中迁移转化,长期存在于水和土壤中,通过富集而危害人体健康,其环境归宿通常是土壤和沉积物。常见的SVOCs 有苯酚类﹑苯胺类﹑硝基芳香烃类﹑氯代芳香烃类﹑多环芳烃类等[4–6],其来源非常广泛。如酚类化合物主要来源于石油化工﹑塑料制造﹑颜料合成﹑制药﹑造纸等工业污水排放[7];苯胺类化合物来源于制药﹑染料﹑印染﹑橡胶﹑石化等工艺生产过程[8];硝基苯类化合物主要来源于染料合成﹑油漆涂料﹑塑料﹑炸药﹑医药及农药等制造工业[9];多环芳烃类化合物主要来源于煤炭﹑燃油的加工和燃烧,机动车尾气排放等[10]。笔者主要研究GB 36600—2018 《土壤环境质量 建设用地土壤污染风险管控标准》中11 种SVOCs 的基本项目,参考HJ 834—2017 《土壤和沉积物 半挥发性有机物的测定 气相色谱–质谱法》[11],建立一种准确﹑高效的环保型检测方法。
目前土壤中半挥发性有机物的测定由样品提取﹑净化和色谱分析三部分组成。目前前处理方法操作复杂,步骤冗长[12–14]。提取﹑净化过程中,由于样品多次转移,易造成目标物损失,同时,大量溶剂的使用对人体和环境也带来了一定的危害。因此如何尽可能减少样品前处理步骤,同时有效消除杂质对检测的影响,保证目标物不受损失,成为测定半挥发性有机物的关键。笔者采用弗罗里硅土和石墨化碳黑为净化剂,利用快速溶剂萃取仪,将萃取和净化两个过程合并,实现样品的在线净化萃取,去除了净化过程中目标物损失。与传统的离线净化相比,本方法大大简化了样品前处理过程,节省人力消耗,减少了有机溶剂的使用量,降低了对人体和环境的危害,尤其适应于大批量样品的检测。
1 实验部分
1.1 主要仪器与试剂
气相色谱–质谱仪:7890–5977B 型,配自动进样器,美国安捷伦科技有限公司。
全自动高效快速溶剂萃取仪:Flex-HPSE 型,北京莱伯泰科仪器股份有限公司。
平行浓缩仪:Multi Vap-10 型,北京莱伯泰科仪器股份有限公司。
电子天平:SQP 型,感量值为0.1 mg,赛多利斯科学仪器(北京)有限公司。
苯胺:质量浓度为1 000 mg/L,溶剂为甲醇,编号为CDAA–S–650022–AD–1 mL,上海安谱实验科技有限公司。
10 种半挥发性有机物混合标准储备液:包括2-氯苯酚﹑硝基苯﹑萘﹑苯并[a]蒽﹑屈﹑苯并[b]荧蒽﹑苯并[k]荧蒽﹑苯并[a]芘﹑茚并[1,2,3-c,d]芘﹑二苯并[a,h]蒽,质量浓度均为1 000 mg/L,溶剂为二氯甲烷,编号为CDAA–M–690060–KD–1 mL,上海安谱实验科技有限公司。
替代物混合标准储备液:包括2-氟酚﹑苯酚-d6﹑硝基苯-d5﹑2-氟联苯﹑4–4’-三联苯-d14,质量浓度均为1 000 mg/L,溶剂为丙酮–二氯甲烷(体积比为1∶1),标准物质编号为110450–09–1 mL,美国o2 si标准品公司。
内标混合标准储备液:包括萘-d8﹑屈-d12﹑苝-d12,质量浓度均为1 000 mg/L,溶剂为丙酮–二氯甲烷(体积比为1∶1),编号为CDAA–M–629032–XD,上海安谱实验科技有限公司。
二氯甲烷﹑丙酮:均为农残级,上海安谱实验科技有限公司。
硅藻土:75~830 μm,上海安谱实验科技有限公司。
石英砂:优级纯,于马弗炉中400 ℃烘烤4 h,冷却后装入具塞磨口玻璃瓶中密封保存,成都科隆化学品有限公司。
实验用水为超纯水(不含有机物)。
1.2 样品采集与保存
土壤样品按照HJ/T 166 的相关要求采集和保存。样品应于洁净的具塞磨口棕色玻璃瓶中保存。运输过程中应密封﹑避光﹑4 ℃以下冷藏。运至实验室后,若不能及时分析,应于4 ℃以下冷藏﹑避光﹑密封保存,保存时间不超过10 d。
1.3 水分的测定
土壤样品干物质含量测定按照HJ 613–2011《土壤干物质和水分的测定重量法》执行。
1.4 仪器工作条件
1.4.1 快速溶剂萃取仪
萃取温度:100 ℃;压力:10.04 MPa;静态萃取7 min(5 min 预热平衡之后);淋洗体积为40%池体积;氮气吹扫:60 s;循环萃取2 次。
1.4.2 气相色谱条件
色谱柱:HP–5MS–UI 型色谱柱(30 m×0.25 mm,0.25 μm,美国安捷伦科技有限公司);进样口温度:280 ℃;进样方式:无分流进样;进样体积:1.0 μL;程序升温:初始温度为40 ℃,保持2 min,以12 ℃/min 的速率升温至160 ℃,保持5 min,再以10 ℃/min 的速率升温至280 ℃,保持5 min;载气:氦气,流量为1.00 mL/min。
1.4.3 质谱条件
离子源:EI 源;离子源温度:230 ℃;离子化能量:70 eV;接口温度:260 ℃;扫描范围:m/z35~500 Da;溶剂延迟时间9.0 min;11 种SVOCs的质谱参数见表1。

表1 质谱条件
1.5 样品处理
(1)空白样品。选择未受有机物污染的土壤,除去枝叶﹑石子等异物,按四分法粗分,冷冻干燥后研磨,过250 μm(60 目)筛,再经110 ℃烘5 h,制备成空白土壤样品。
(2)待测样品。取适量新鲜样品,放入冷冻干燥机中进行干燥脱水。干燥后的土壤放入研磨机进行研磨,均化处理过250 μm (60 目)筛。称取20 g(精确到0.01 g)样品于烧杯中,加入适量硅藻土混匀,再加入弗罗里硅土粉1 g 和石墨化碳黑粉0.5 g,混合均匀。萃取池体积为34 mL,在萃取池底部铺一层石英砂,再将混合均匀的样品放入萃取池中,用石英砂填满萃取池,加盖,装入快速溶剂萃取仪。以二氯甲烷–丙酮(4+1)混合液为萃取剂,按上述萃取条件进行提取。将萃取液转移至平行浓缩仪中,在水浴温度为30 ℃的条件下浓缩至小于1 mL,加入适量内标物至浓度为5.00 mg/L,用二氯甲烷定容至1.0 mL,混匀,作为样品溶液待测。
1.6 样品测定
按1.4 仪器工作条件进行测定1.5(2)中样品溶液,采用质谱图结合保留时间定性,选择离子定量,计算各目标化合物的含量,并换算其在土壤样品中的含量。
1.7 溶液配制
半挥发性有机物混合标准溶液(含替代物):质量浓度为10 μg/mL,准确移取10 μL 苯胺﹑10μL 10 种半挥发性有机物混合标准储备液和10 μL 替代物混合标准储备液,用二氯甲烷定容至1 mL。
内标混合标准溶液:取10 μL 内标混合标准储备液用二氯甲烷定容至1 mL,萘-d8﹑屈-d12﹑苝-d12质量浓度均为10 μg/mL。
系列混合标准工作液:使用空白土壤作为基底,分别移取半挥发性有机物混合标准溶液(含替代物)5﹑10﹑25﹑50﹑75﹑100﹑125﹑150﹑175﹑200 μL,再各加入内标混合标准溶液50 μL,用二氯甲烷定容至1 mL,配制成0.05﹑0.10﹑0.25﹑0.50﹑0.75﹑1.00﹑1.25﹑1.50﹑1.75﹑2.00 μg/mL 的11 种半挥发性有机物系列混合标准工作溶液。
2 结果与讨论
2.1 色谱图
11 种SVOCs 标准溶液的色谱图如图1 所示。
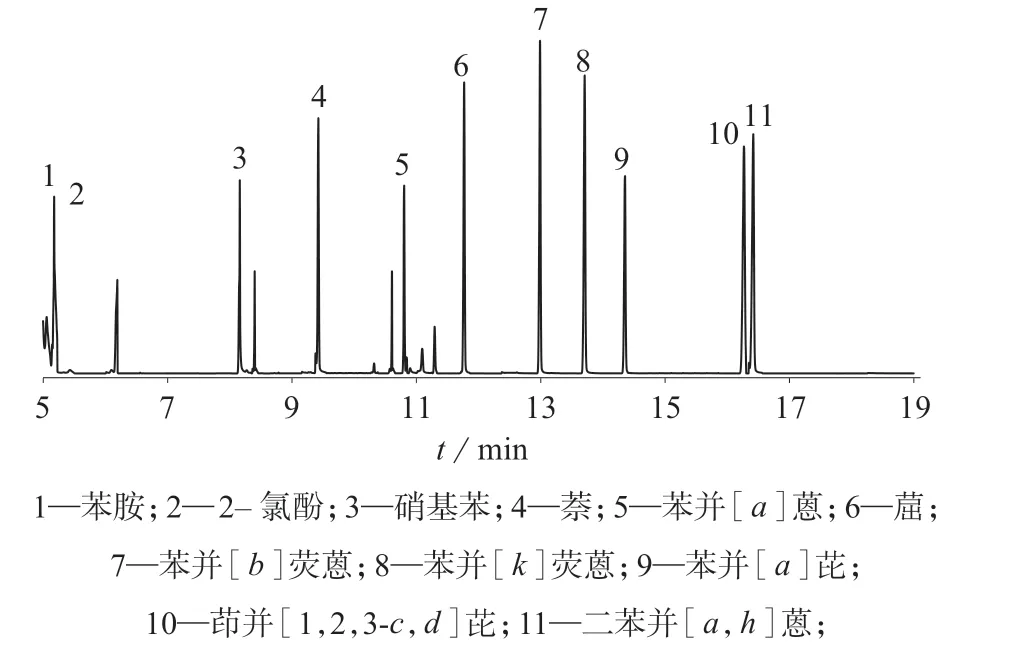
图1 11 种svocs 标准溶液色谱图
2.2 萃取体系的确定
二氯甲烷对非极性到极性范围的化合物均有较高的萃取能力,而且由于其沸点低,萃取后易于浓缩,且密度比水大,分液操作也容易以及不易燃等优点,适用于多组分同时分析,因此笔者也利用其优点,选择其作为前处理萃取剂[13]。同时,由于11 种半挥发性有机物中,萘挥发性较强,采集的土壤样品不能采用风干脱水,只能真空冷冻脱水或者将新鲜土壤样品用无水硫酸钠﹑硅藻土研磨脱水,因此在萃取溶剂中加入能和水互溶的丙酮,溶掉土壤中的水份,可以增大有机萃取溶剂和土壤颗粒的接触面积,
以提高萃取效率。HJ 834—2017 《土壤和沉积物半挥发性有机物的测定 气相色谱–质谱法》标准方法建议离线净化条件下,用二氯甲烷–丙酮(体积比为1∶1)萃取。但是,由于丙酮极性大,能溶解大多数有机物,同时可提取土壤样品中较多的色素物质,多数土壤样品的提取液呈黄色或黄褐色,影响后续测定,所以应减少丙酮的比例。笔者考察了二氯甲烷–丙酮(1∶1)﹑二氯甲烷–丙酮(2∶1)﹑二氯甲烷–丙酮(4∶1)﹑二氯甲烷–丙酮(6∶1)混合液对空白加标样品回收率的影响,测定结果见表2。表2结果表明,以二氯甲烷–丙酮(4∶1)作为提取溶剂时,目标物的回收率最合适。
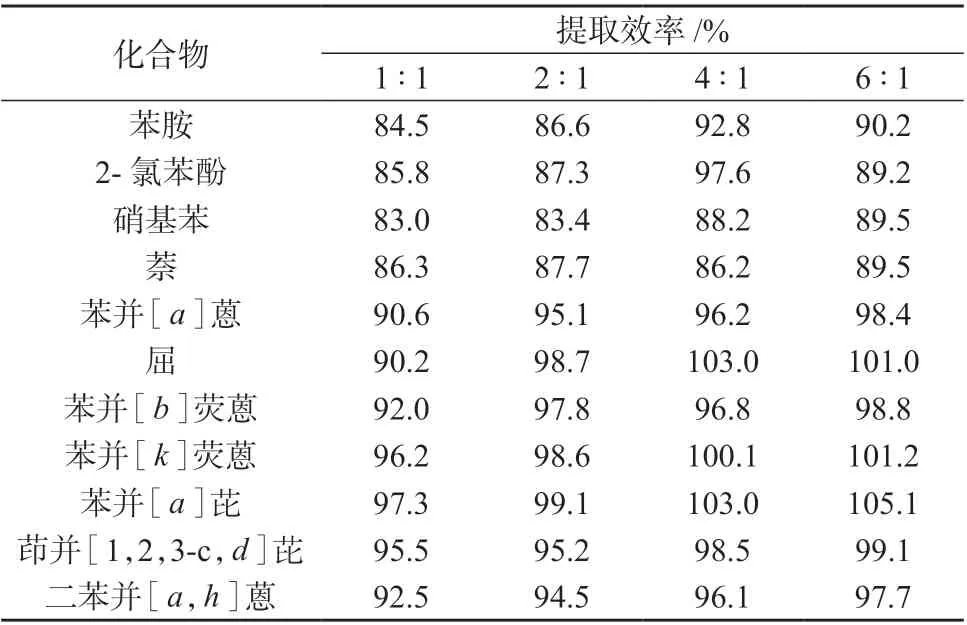
表2 不同二氯甲烷–丙酮比例下的提取效率
2.3 净化条件
由于11 种半挥发性有机物中,萘的挥发性较强,其萃取液的离线净化造成萘的损失较大。因此,实验采用在线净化消除基质干扰。不同净化方式的回收率见表3。
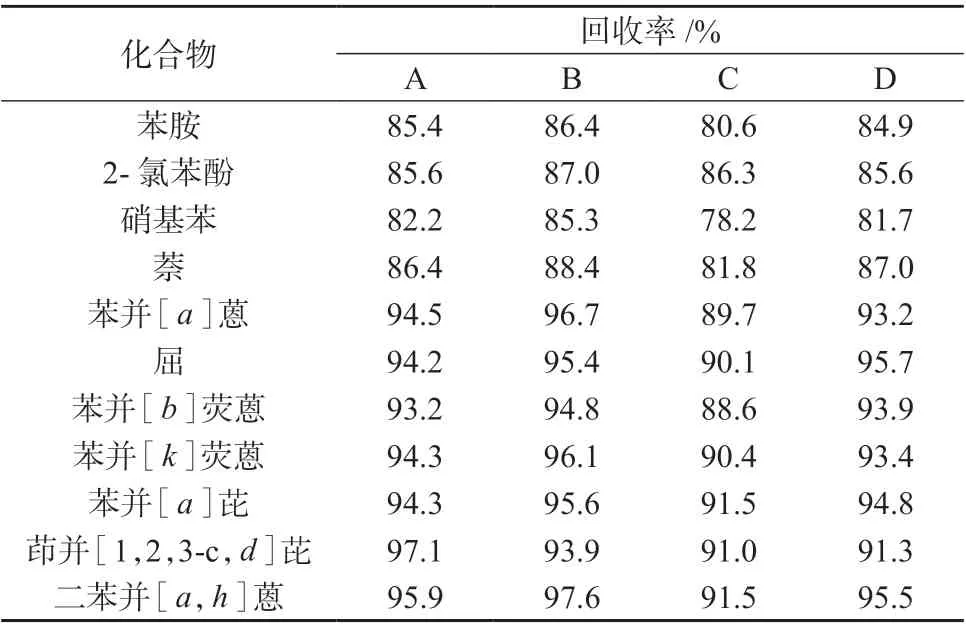
表3 不同净化方式下的回收率
由表3 可知,在线净化时,各化合物的回收率高于离线净化的回收率,这是因为在线净化避免了提取液的多次转移和浓缩。单独采用弗罗里硅土粉或弗罗里硅土柱对提取液净化时,脱色效果较差,背景值较高,对仪器影响较大。以实际土壤样品为基质,进行样品加标试验,并与未净化的样品进行对比,查看净化剂的净化效果。土壤样品经萃取后,未净化的样品明显浑浊,呈较深的褐色;净化后的样品清澈透明。土壤在线净化样品﹑离线净化和未净化样品的色谱图分别如图2﹑图3 和图4 所示。经过净化后的样品杂峰明显减少,净化剂对样品的净化作用明显。因此,选择弗罗里硅土粉–石墨化碳黑粉对化合物进行在线净化提取。
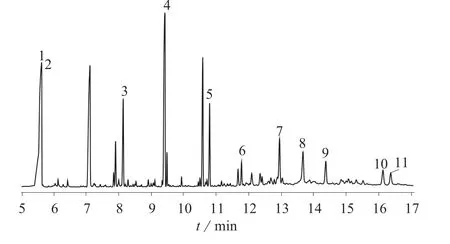
图2 在线净化样品的色谱图
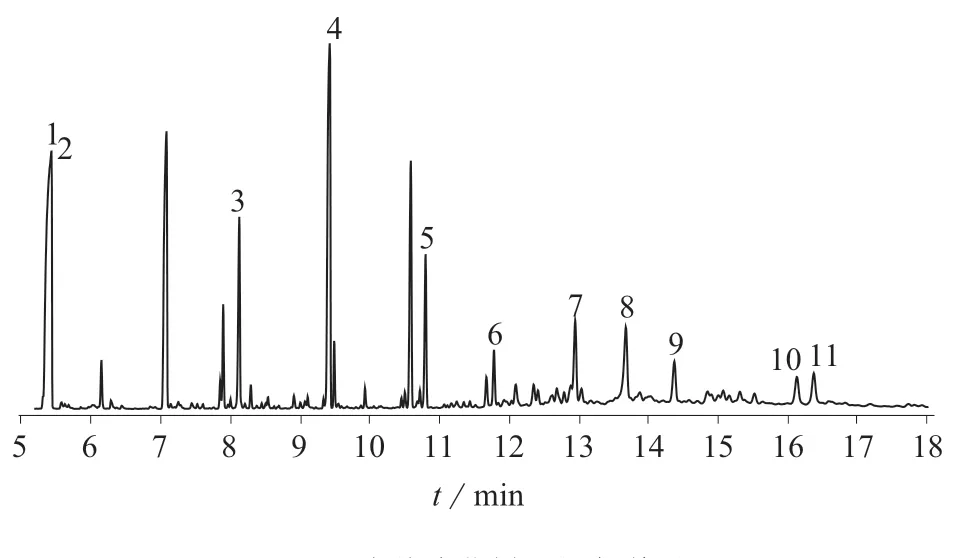
图3 离线净化样品的色谱图

图4 未净化样品的色谱图
2.4 浓缩条件对回收率的影响
半挥发性有机化合物具有一定的挥发性,在浓缩过程中,浓缩时间不易过长,浓缩温度不易过高,否则会降低半挥发性有机物的回收率;且氮气流量要适中,以溶液不形成回旋为宜,流量太大也会造成低沸点半挥发性化合物的挥发损失。因此,利用正交试验设计表的实验条件进行浓缩条件优化实验,考察浓缩过程中温度和氮气流量对回收率的影响。正交试验表见表4,正交试验设计见表5。正交试验结果见表6 ~表8。

表4 实验因素和水平
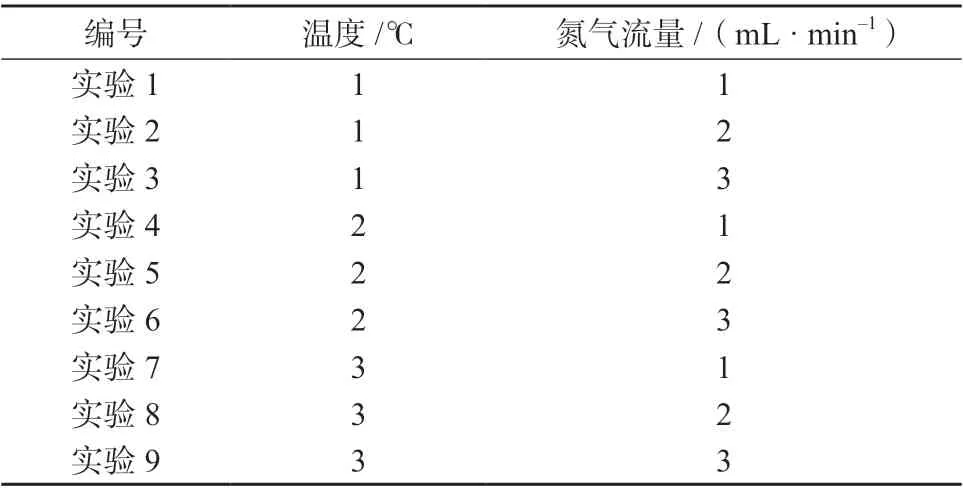
表5 正交试验设计
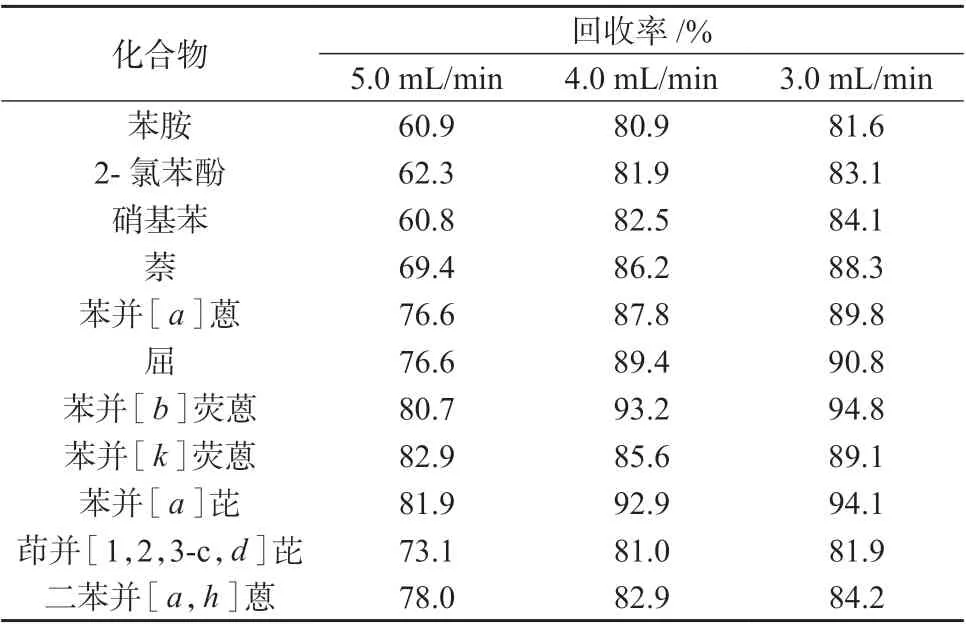
表6 浓缩温度为20℃时不同氮气流量下的回收率
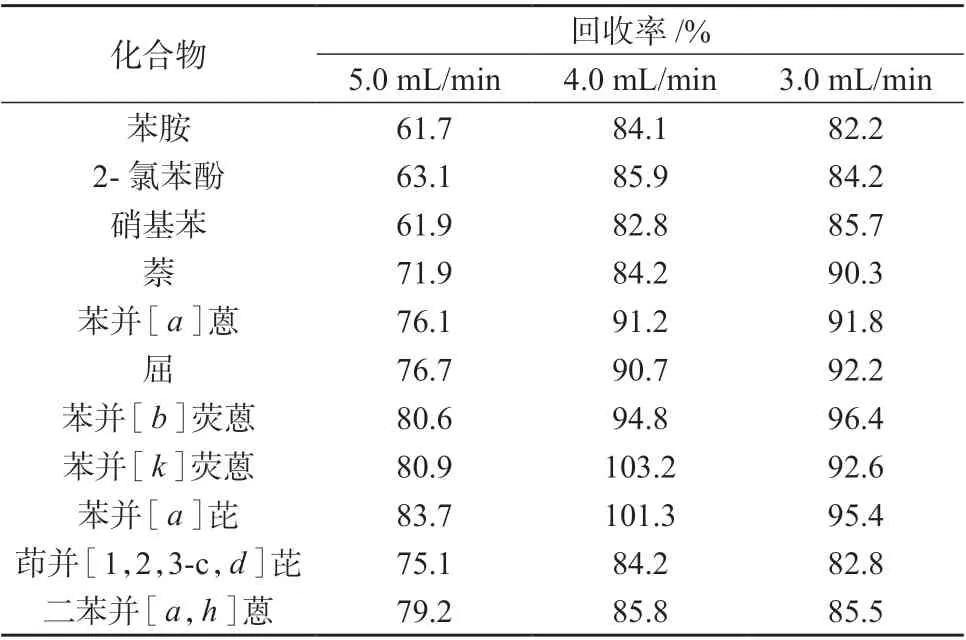
表7 浓缩温度为25℃时不同氮气流量下的回收率
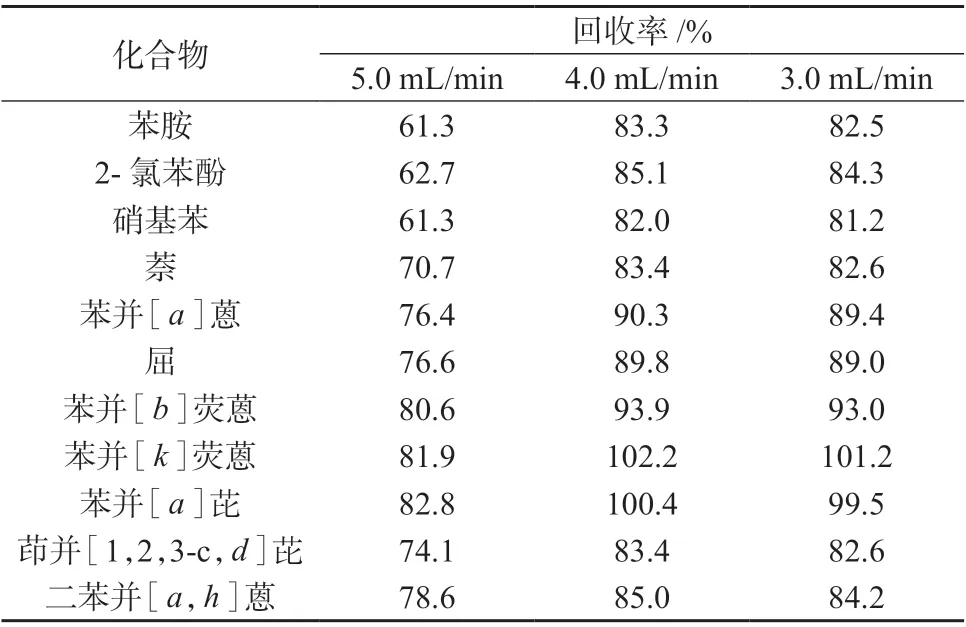
表8 浓缩温度为30℃时不同氮气流量下的回收率
通过正交试验发现,在水温25~30 ℃﹑氮气流量控制在3.0~4.0 mL/min 时,11 种目标化合物的回收率最好,综合考虑浓缩时间和11 种半挥发性有机物的浓缩效果,选择水温为25 ℃﹑氮气流量为4.0 mL/min 作为浓缩条件,另外,由于在避光时,苯胺降解较缓慢,有光存在时,苯胺的降解加速[15],因此在避光环境中进行浓缩。
2.5 线性方程﹑线性范围及检出限
在优化的色谱条件下测定1.7 中的系列混合标准工作溶液,以各物质的质量浓度x(μg/mL)为横坐标,色谱峰面积y为纵坐标进行线性回归,建立工作曲线,采用内标法定量,使用平均相对响应因子计算结果[11]。按照HJ 834—2017 《土壤和沉积物 半挥发性有机物的测定 气相色谱–质谱法》[11]和HJ 168—2020 《环境监测分析方法标准制修订技术导则》[16]对平均响应因子的相对标准偏差﹑检出限等参数进行考察;参考GB 36600-2018 《土壤环境质量建设用地土壤污染风险管控标准》中一类土壤用地筛选限值的1/10 对检出限进行评价,结果见表9,11 种半挥发性有机物的线性范围均为0.05~2.00 μg/mL。

表9 11 种半挥发性有机物线性方程和检出限
由表9 可知,11 种SVOCs 平均响应因子的标准偏差均小于30%,满足HJ 834–2017 《土壤和沉积物半挥发性有机物的测定气相色谱–质谱法》要求,11 种目标物的检出限为0.30~0.65 μg/kg。
2.6 精密度与回收试验
于空白样品中加入0.20 μg/L 半挥发性有机物混合标准溶液,按优化的实验条件萃取浓缩后上机进行检测,平行测定6 份,根据测定结果计算方法的加标回收率及精密度,结果见表10。由表10 可知,样品平均加标回收率为85%~105%,相对标准偏差为4.10%~7.05% (n=6),满足HJ 834—2017 《土壤和沉积物半挥发性有机物的测定 气相色谱–质谱法》要求。

表10 精密度和加标回收试验结果
3 结语
建立了在线净化–气相色谱–质谱法测定土壤中11 种半挥发性有机物的分析方法,该方法满足GB 36600—2018 《土壤环境质量建设用地土壤污染风险管控标准》的要求,11 种半挥发性有机物均在0.05~2.00 μg/L 范围内呈现良好的线性关系,检出限为0.30~0.65 μg/kg。样品平均加标回收率为83.8%~102.7%,与文献报道相比有所提高。可能的原因是采用在线净化萃取,避免了提取液的多次转移和浓缩,降低了目标物的损失,同时,大大缩短了前处理流程,节省了人力消耗,减少了有机溶剂的使用量,降低了对人体和环境的危害,在土壤半挥发性有机物的检测中具有一定的推广意义。
