基于药效筛选与正交试验优化花川保列颗粒提取工艺研究
2022-04-14唐靖雯彭政忠卢礼平张丽艳
唐靖雯 潘 梅 彭政忠 卢礼平 张丽艳
1.贵州威门药业股份有限公司,贵州 贵阳 550018;2.贵州中医药大学药学院,贵州 贵阳 550025
花川保列颗粒是由贵州威门药业股份有限公司研发的一种治疗慢性前列腺炎的纯中药复方制剂,属于国家6类中药新药。本品利用苗药“头花蓼”的优良抗菌抗炎活性特点,结合中医药理论及名老中医多年的临床治疗经验,以头花蓼为君药,配以川芎、粉萆薢、白芷、牛膝等4味药材组方而成,具有清热利湿、活血止痛的功效,用于湿热下注、气血瘀滞所致的淋症。研究根据本品处方的功能主治,结合处方中药物的理化性质,考察水提醇沉物、醇提物的抗菌、抗炎作用优势,确定本品采用醇提制备工艺;并以头花蓼中槲皮素总量为综合评价指标,通过正交试验进一步优选花川保列颗粒的最佳醇提工艺,为该制剂批量生产提供科学依据,为临床上治疗慢性前列腺炎提供一种疗效确切的新药制剂奠定基础。
1 仪器与材料
1.1 仪器 Agilent-1100型高效液相色谱仪(Agilent科技有限公司);AG135型十万分之一电子天平(梅特勒托利多科技有限公司);CH-250型超声波清洗器(北京创新德超声电子研究所);101-5型电热恒温鼓风干燥箱(上海路达实验仪器有限公司);SENCOR®系列旋转蒸发仪(上海申生科技有限公司);予华牌循环水式真空泵(巩义市英峪予华仪器厂)。
1.2 药材 头花蓼药材采自贵州威门药业股份有限公司GAP种植基地,川芎、粉萆薢、白芷、怀牛膝均购于贵州省药材公司,经贵州中医药大学魏升华教授鉴定:头花蓼为蓼科植物头花蓼PolygonumcapitatumBuch.-Ham.ex D.Don的干燥全草或地上部分;川芎为伞形科植物川芎LigusticumchuanxiongHort.的干燥根茎的饮片;粉萆薢为薯蓣科植物粉背薯蓣DioscoreahypoglaucaPalibin的干燥根茎的饮片;白芷本品为伞形科植物白芷Angelicadahurica(Fisch. ex Hoffm.)Benth. et Hook.f.或杭白芷Angelicadahurica(Fisch. ex Hoffm.)Benth. et Hook. f. var.formosana(Boiss.) Shan et Yuan的干燥根的饮片;怀牛膝为苋科植物牛膝AchyranthesbidentataB1. 的干燥根的饮片。头花蓼药材符合地方标准规定,其他药材符合中国药典规定。
1.3 药品与试剂 槲皮素对照品(批号:10081-9905,纯度:96.5%,中国食品药品检定研究院);致炎剂(巴豆油系棕色油状液体,药用级,批号:000309);甲醇、乙腈为色谱纯;水为娃哈哈纯净水;其余试剂均为分析纯。
1.4 实验动物 CV级KM小鼠,雄性,体质量35~40 g,由四川抗菌素工业研究所实验动物中心提供,合格证:川实动管质第99-30号。
2 方法与结果
2.1 基于药效实验的工艺初筛
2.1.1 实验药物制备
2.1.1.1 水提醇沉物的制备 按处方比例称取3日量的药材,加10倍量水提取两次,每次2 h,滤过,合并滤液,滤液浓缩至相对密度为1.1(60 ℃)的清膏,加入95%乙醇,使药液含醇量达70%,静置过夜,滤过,滤液回收乙醇,减压干燥,得浸膏粉。
2.1.1.2 醇提物的制备 按处方比例称取3日量的药材,加10倍70%乙醇提取两次,每次2 h,提取液回收乙醇,减压干燥,得浸膏粉。
2.1.2 抗菌、抗炎作用的评价方法
2.1.2.1 抗菌作用 采用琼脂二倍稀释法测定花川保列颗粒浸膏粉对受试菌株的最低抑菌浓度(MIC)。按原生药含量精密称取花川保列颗粒水提醇沉物、醇提物,加至40 mL融化的琼脂培养基(融化至50 ℃),混匀,从中吸出20 mL至灭菌平皿内,余下的20 mL琼脂中再添加入20 mL无药琼脂混匀,再从中吸出20 mL至下一个平皿内,以此类推,制备含药终浓度为1000,500,250,125……0.03 mg原生药/mL的系列平皿,冷凝后再分别用多点接种仪(DenleyA400)于各平皿表面接种细菌,菌液终浓度为105CFU/mL。置入37 ℃中培养18~24 h,观察结果,以无细菌生长平皿内药物的最低浓度为该菌的最低抑菌浓度(MIC)。链球菌及溶血性链球菌置于35 ℃培养20 h观察结果,淋球菌置于5%CO2环境中培养24~48 h观察结果。
2.1.2.2 抗炎作用 ①剂量设计:根据花川保列颗粒水提醇沉物、醇提物原生药含量初步拟定的人临床剂量为1.125 g生药/kg;此剂量按动物间体表面积推算至小鼠剂量为:水提醇沉提取物为2.17 g/kg,醇提提取物为1.58 g/kg。以此剂量粗略设定为中剂量,故水提醇沉物高中低三剂量组分别为4.34、2.17、1.08 g/kg;醇提物高中低三剂量组分别为3.16、1.58、0.79 g/kg。两种工艺提取物高中低三剂量所含生药量对应相等。氢化可的松剂量20 mg/kg。②样品配置:称取一定量样品后,用0.5%CMC液研磨成混悬液(高剂量组),然后倍半稀释至各剂量组所需浓度。③将90只小鼠随机分9组,10只/组,将配制好的药液按0.5 mL/20 g体重口服给药,给药后60 min,取1%巴豆油30 μL涂沫于小鼠右耳内侧,4 h后将小鼠处死,取二耳,用Φ8 mm打孔器冲下二耳片,精确称重。左右二耳片重量之差为肿胀度(mg),再根据以下公式计算肿胀百分率(%)和肿胀抑制率(%)。


2.1.3 结果
2.1.3.1 对体外抗菌活性的影响 由表1所示,醇提、水提醇沉制备的花川保列颗粒均对临床分离金葡菌、链球菌、溶血性链球菌、大肠埃希菌、阴沟杆菌、铜绿假单孢菌、变形杆菌、痢疾杆菌呈现有抗菌作用,其MIC范围分别在62.5~500 mg原生药/mL、62.5~500 mg原生药/mL;醇提、水提醇沉制备的花川保列颗粒浸膏粉对白色念珠菌的抗菌活性佳,MIC值分别是0.25~125 mg原生药/mL、15.6~1000 mg原生药/mL;醇提、水提醇沉制备的花川保列颗粒浸膏粉对所试淋球菌呈现较强抗菌作用,MIC值分别为7.8~250 mg原生药/mL、31.25~1000 mg原生药/mL。研究表明,醇提工艺略优于水提醇沉工艺。

表1 花川保列颗粒浸膏粉(水提醇沉、醇提)体外抗菌活性比较
2.1.3.2 对小鼠耳肿胀模型抗炎作用的影响 由表2所示,本次抗炎活性比较试验中,两种工艺路线所得的花川保列颗粒浸膏粉均显示一定的抗炎活性,醇提物抗炎活性的量效关系较水提醇沉物明显,肿胀抑制率达到41.3%。
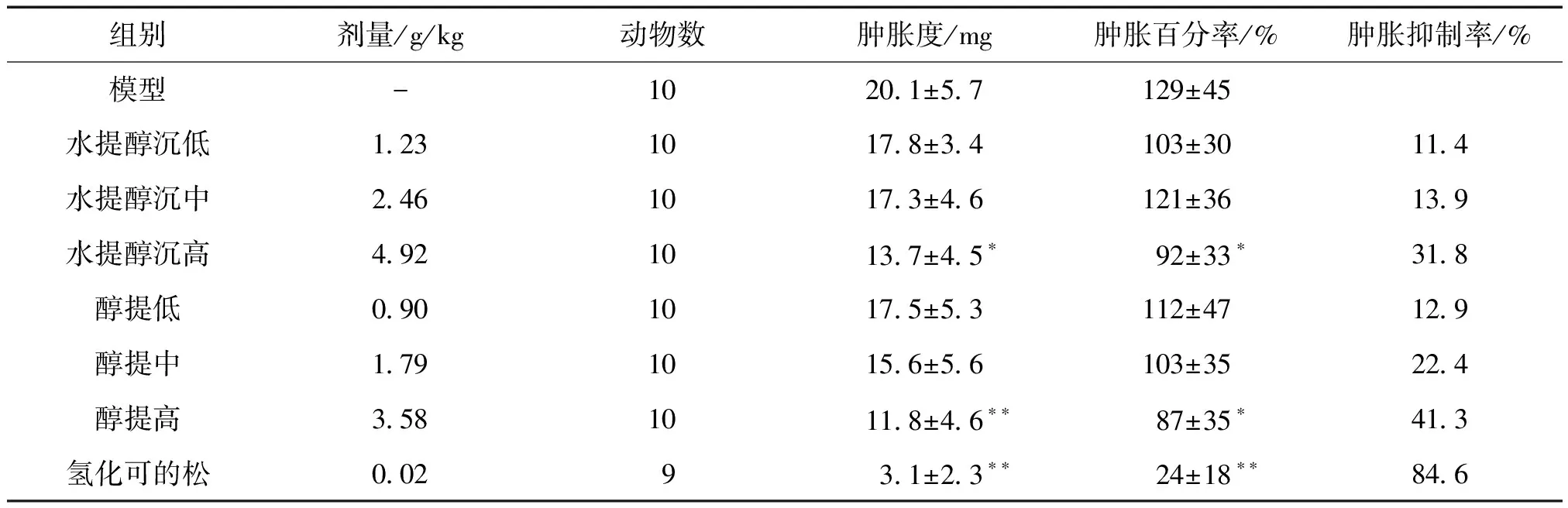
表2 花川保列颗粒浸膏粉(水提醇沉、醇提)抗炎活性比较
基于上述体外抗菌试验及小鼠耳肿胀模型抗炎作用结果,花川保列颗粒的醇提物体外抗菌作用及抗炎作用均优于水提醇沉物,故本研究拟采用醇提工艺,以头花蓼中槲皮素总量为综合评价指标,进一步通过正交试验优选花川保列颗粒的最佳醇提工艺。
2.2 槲皮素的含量测定
2.2.1 色谱条件 色谱柱:Agilent TC-C18(2)(250 mm×4.6 mm,5μm);流动相:甲醇-0.4%磷酸溶液(54∶46,V/V);流速:1 mL/min;检测波长:370 nm;柱温:25 ℃;进样量:10 μL;理论板数按槲皮素峰计算应不低于3000。
2.2.2 对照品溶液的制备 精密称取经五氧化二磷干燥过的槲皮素对照品适量,加甲醇制成每1 mL含25 μg的溶液,即得。
2.2.3 供试品溶液的制备 取醇提浸膏粉约0.5 g,置50 mL具塞锥形瓶中,精密加入甲醇-50%盐酸溶液(4∶1)混合液25 mL,密塞,称定重量,回流1 h,放冷,再称定重量,用提取液补足减失的重量,摇匀,滤过,取续滤液,即得。
2.2.4 阴性样品的制备 精密称取缺头花蓼药材的浸膏粉,按上述供试品溶液的制备方法制备,即得。
2.2.5 专属性试验 分别取对照品溶液、供试品溶液、缺头花蓼的阴性样品溶液各10 μL,按“2.2.1”项下色谱条件测定,结果如图1所示。阴性样品色谱图中,在与槲皮素对照品相同保留时间处未见色谱峰,表明阴性无干扰,方法专属性良好。

A.对照品溶液;B.供试品溶液;C.阴性样品溶液;1.槲皮素图1 花川保列颗粒醇提浸膏粉专属性试验HPLC图
2.2.6 线性关系考察 按“2.2.2”项下对照品溶液的制备方法,加甲醇制成40.19 μg/mL的溶液,分别精密吸取2、4、6、8、10、12 μL注入高效液相色谱仪,以进样量(x,μg)为横坐标,以峰面积(y)为纵坐标,绘制标准曲线,并进行线性回归,得回归方程:y=4016.565x+0.43415,相关系数r=0.9998,槲皮素在0.0804~0.4823 μg范围内线性良好。
2.2.7 精密度试验 按“2.2.2”项下对照品溶液的制备方法,加甲醇制成0.2512 mg/mL溶液,按“2.2.1”项下色谱条件重复进样5次,测定其峰面积,结果RSD为1.44%,表明仪器精密度良好。
2.2.8 稳定性试验 按“2.2.3”项下制备供试品溶液,并按“2.2.1”项下色谱条件,分别在0、1、3、6、9、12、18、24 h注入高效液相色谱仪,结果供试品溶液中槲皮素峰面积在24 h内无明显变化,RSD为1.61%,表明供试品溶液在24 h内具有良好的稳定性。
2.2.9 重复性试验 按“2.2.3”项下制备供试品溶液5份,并按“2.2.1”项下色谱条件测定槲皮素含量,结果RSD为1.50%,表明方法重复性良好。
2.2.10 加样回收率试验 精密称取已知含量的同一醇提浸膏粉(含量1.75 mg/g)约0.25 g,分别加入槲皮素对照品溶液(0.04235 mg/mL)10 mL,按上述“2.2.3”项下供试品溶液制备方法及“2.2.1”项下色谱条件进行测定。结果见表3。
2.3 醇提工艺评价指标 按处方比例分别称取各药材适量,按对应的工艺提取后,合并所有提取液,浓缩、干燥,得浸膏粉。以槲皮素总量为评价指标,对醇提工艺进行评分。
浸膏收率(%)=(干膏粉重/药材总重量)×100%
槲皮素总量(mg)=药材总量×浸膏收率×槲皮素含量

表3 加样回收率试验 (n=6)
2.4 正交试验优选提取工艺
2.4.1 正交试验设计 根据药效实验的工艺筛选,选择以乙醇为溶剂进行提取。以槲皮素总量为考察指标,以乙醇浓度(A)、乙醇用量(B)、提取时间(C)、提取次数(D)为试验因素,每个因素3个水平,用正交表L9(34)进行优选,优选醇提工艺条件。正交试验因素水平见表4。

表4 因素水平表
2.4.2 正交试验及结果 根据“2.4.1”项下设计方案做正交试验,按表4的因素水平和表5试验条件分别经回流提取、滤过、浓缩、干燥等步骤,每一试验重复3次,共得27份浸膏粉,按“2.3”项下方法测定浸膏收率,按上述槲皮素含量测定方法测定槲皮素总量。正交试验结果见表5,方差分析见表6。
根据正交试验结果,以槲皮素含量及浸膏收率为评价指标,A、B、C、D四因素均无显著性影响,直观分析以A1B3C3D3组合较好,结合实际生产,拟选A1B3C2D3。通过对不同提取时间条件进行了比较研究,结果表明,两者提取物中槲皮素总量分别为:6.36 mg和7.06 mg,由此结果分析,采用A1B3C2D3工艺提取的浸膏槲皮素总量高于A1B3C3D3工艺提取的浸膏。因此,花川保列颗粒最佳提取工艺条件为A1B3C2D3,即加10倍量60%乙醇回流1.5 h,共提取3次。

表5 正交试验结果 (n=3)
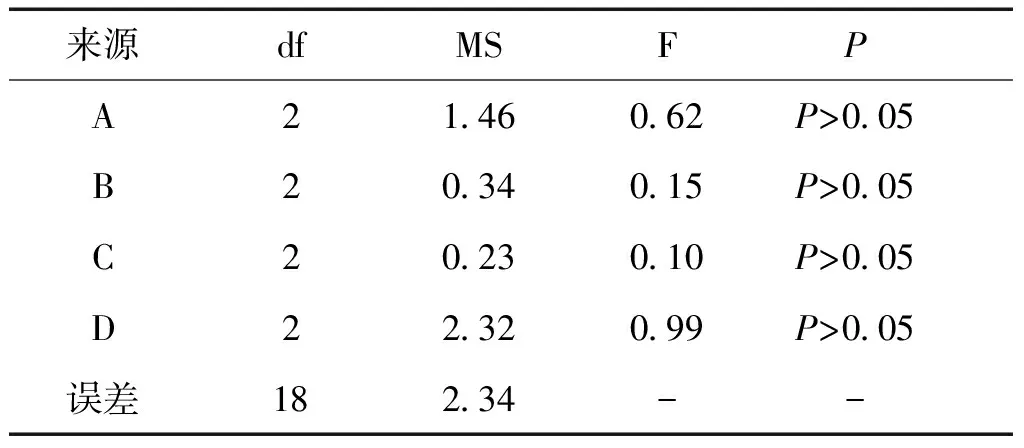
表6 方差分析
2.4.3 验证试验 根据花川保列颗粒处方比例称取各味药材共计3份,采用优选的最佳提取工艺条件进行提取、制备浸膏粉,按“2.3”项下测定浸膏收率;按“2.2.3”项下制备供试品溶液,并按“2.2.1”项下色谱条件测定槲皮素含量,结果见表7。三批样品所得浸膏收率、槲皮素总量RSD值较小,表明该提取工艺稳定可行。

表7 验证试验结果 (n=3)
3 讨论
处方中头花蓼中主要含有芦丁、槲皮素等黄酮类成分,溶于乙醇,具有明显的抗菌、抗炎作用[1];粉萆薢主要成分为薯蓣皂苷,此类成分易溶于热乙醇[2],可抗肿瘤、抗炎止痛、降低血糖、抗骨质疏松、抗肥胖,对心脏、肝脏、肾脏具有保护作用[3];牛膝主要含牛膝皂苷、促蜕皮甾酮、牛膝甾酮、齐墩果酸等[4],齐墩果酸具有抑菌消炎,强心利尿,升高白细胞,增强机体的免疫功能等方面的作用,以醇提为主[5]。通过文献分析可知,以上药材的主要药效成分均能较好地溶于醇溶液,故考虑采用醇提工艺。川芎中有效成分主要为挥发油、阿魏酸、川芎嗪、大黄酚、川芎内酯等,溶于乙醇[6],川芎中川芎嗪、阿魏酸等成分长时间煎煮被大量破坏,高沸点的藁本内酯、金合欢醇等成分经乙醇回流可保留在浓缩液中[7];白芷有效成分为白当归素、欧前胡素和异欧前胡素等[8],其挥发油含量极低,且欧前胡素等香豆素类长时间加热易破坏[9]。本研究通过对3个不同药店购买的川芎、白芷进行了挥发油提取,结果发现:川芎药材几乎提取不出挥发油;白芷挥发油的收率仅为0.10%左右。因此,花川保列颗粒未进行挥发油的提取。
本研究基于药效学与正交试验相结合进行的最佳工艺条件选择,可避免仅以化学成分为评价指标造成的工艺研究的片面性和局限性。本实验是在药效学实验确定的醇提工艺基础上,进一步以君药头花蓼中槲皮素总量为评价指标,采用L9(34)正交试验及方差分析,并结合生产实际确定最佳醇提工艺条件为:10倍量60%乙醇,回流提取3次,每次1.5 h。
