基因分型技术在ABO放散型亚型鉴定中的应用*
2022-04-13张若洋杨东冯晨晨史丽莉李慧薛敏丁文艺陈青
张若洋 杨东 冯晨晨 史丽莉 李慧 薛敏 丁文艺 陈青
ABO血型系统是由卡尔·兰德斯坦纳于1900年首先发现的血型系统,也是目前临床输血和器官移植等医学领域最重要的血型系统[1]。放散型亚型是ABO血型系统的一种亚型,其特点为血清学上一般不被抗-A/B或抗-AB试剂凝集,经吸收放散实验一般可检测出相应的弱A/B抗原。由于血清学鉴定过程会受到试剂、仪器、人员操作熟练度等因素的影响,因此在进行ABO血型定型时容易发生错误。近年来随着分子生物学技术的飞速发展,基因分型技术在ABO放散型亚型鉴定中的作用愈加重要。现将本实验室发现的10例ABO血型系统放散型亚型的血清学及基因分型结果报告如下。
材料与方法
1 研究对象 2017~2020年来自本实验室疑难血型基因检测开放平台正定型为O型,反定型抗-A抗体与抗-B抗体效价之间相差≥2+的10例ABO正反定型不一致样本,均为临床医院送检,样本信息如下表所示(表1)。所有样本经过初检/复核后均发现正反定型不符,因此送至本实验室做进一步检测。
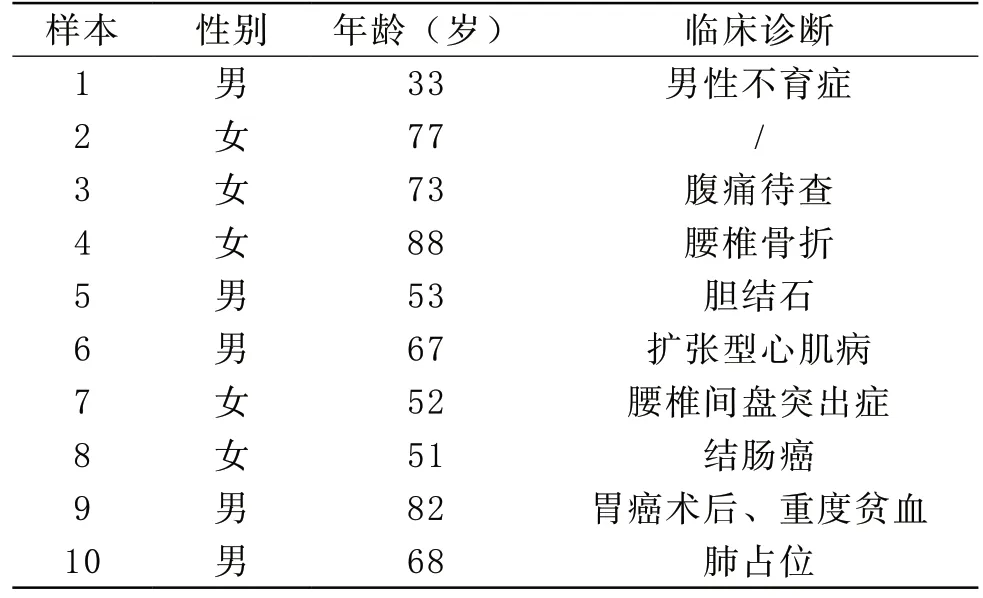
表1 送检样本信息
2 试剂和设备 单克隆抗-A,抗-B血型试剂、ABO反定型标准细胞、抗-H试剂均购自上海血液生物医药有限公司;抗-AB试剂购自美国Immucor公司;少量全血基因组提取试剂盒购自北京原平皓生物技术有限公司;dNTPs购自上海捷瑞生物工程有限公司;MgCl2、10×PCR Buffer、Taq酶购自北京全式金生物技术有限公司;5×TBE缓冲液购自上海生工生物工程股份有限公司;琼脂糖购自美国Sigma公司;GoldView核酸染色剂购自北京艾德莱生物科技有限公司;扩增、测序引物由上海生工生物工程股份有限公司合成;纯化试剂盒购自美国Axygen公司;TA克隆试剂盒购自美国Life Technologies公司;细胞洗涤离心机购自日本Kubota公司;PCR扩增仪购自美国Applied Bio-system公司;凝胶成像分析系统购自美国Alpha Innotech公司。
3 检测方法
3.1 血型血清学实验:根据全国临床检验操作规程[2]进行红细胞ABO血型正反定型、H抗原检测和吸收放散实验。
3.2 DNA提取:根据少量全血基因组提取试剂盒操作说明书抽提DNA。
3.3 PCR扩增及基因测序:PCR扩增ABO基因第1~7外显子、上游CBF/NF-Y增强子区域、启动子、增强子及内含子1的+5.8 kb红细胞特异性调控元件序列,PCR扩增引物、扩增条件及测序引物序列见参考文献[3-4]。PCR扩增结束后,取5 μL PCR产物,经1%琼脂糖凝胶验证PCR产物,与DNA Marker比对鉴定产物的特异性。剩余的PCR扩增产物根据Axygen公司的纯化试剂盒操作说明书进行纯化后委托上海生工生物工程股份有限公司对纯化的扩增产物进行测序。应用Chromas软件阅读测序图谱,使用BioEdit软件对比分析测序结果。
3.4 单倍型克隆测序分析:根据TA克隆试剂盒操作说明书对ABO基因第6、7外显子的扩增片段进行TA克隆,随后挑取数个阳性克隆进行测序分析。
结 果
1 血型血清学结果 血型血清学检测结果显示10例样本正定型均为O型,反定型的抗-A抗体与抗-B抗体之间均存在价差,提示ABO血型正反定型不符(表2)。

表2 血型血清学检测结果
2ABO基因测序结果 对10例样本ABO基因外显子1~7、上游CBF/NF-Y增强子区域、启动子及内含子1的+5.8 kb红细胞特异性调控元件序列进行直接测序及克隆测序后,与ABO*A1.01基因序列进行对比分析,10例样本ABO基因外显子1~5、上游CBF/NF-Y增强子区域、启动子及内含子1的+5.8 kb红细胞特异性调控元件序列未见特异性变异,外显子6~7与ABO*A1.01基因序列对比,结果如下表所示(表3),部分样本特异性变异位点如图所示(图1~3)。

图1 样本1 ABO基因直接测序及克隆测序部分结果
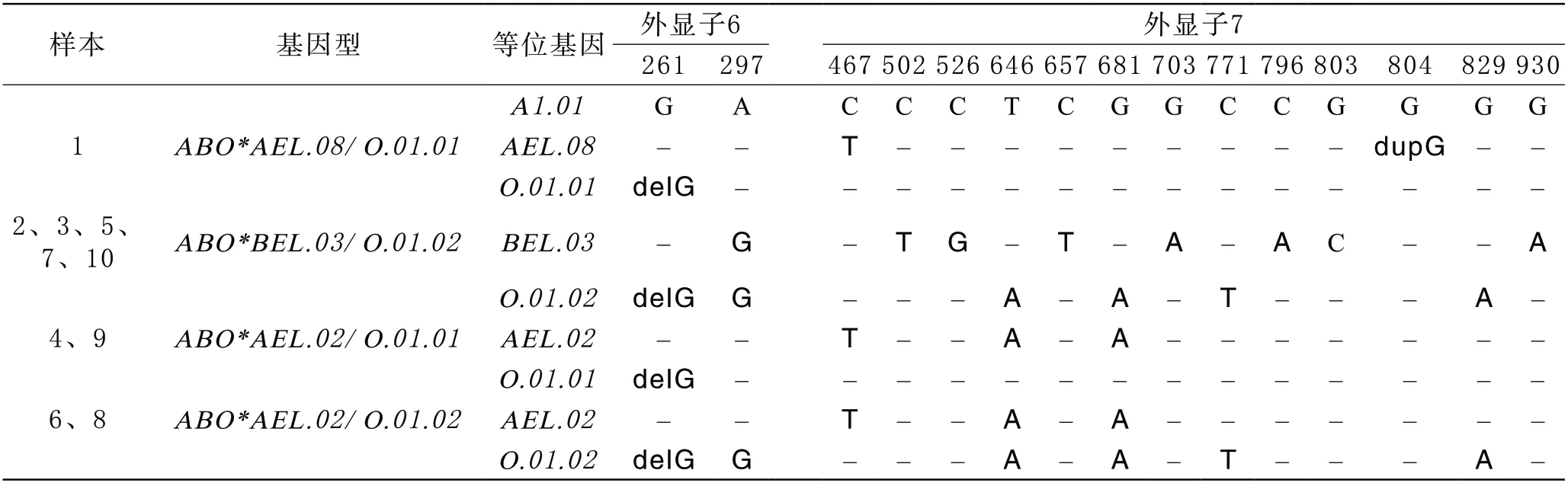
表3 ABO基因外显子6~7测序结果
讨 论
A抗原和B抗原是糖蛋白和糖脂的糖类决定簇,可通过具有免疫显性的末端单糖特性进行区分:A型为N-乙酰氨基半乳糖(GalNAc),B型为半乳糖(Gal)[5]。ABO基因位于9号染色体9q34.1-q34.2上,全长约19~20 kb,包含7个外显子和6个内含子。外显子6、7约占整个编码区的77%,同时编码约91%的糖基转移酶催化区域,因此大部分报道和发现都集中在这2个外显子编码区域[6-7]。ABO*A1.01与ABO*B.01之间存在7个核苷酸差异,分别为c.297A>G、c.526C>G、c.657C>T、c.703G>A、c.796C>A、c.803G>C和c.930G>A,其中有4个为错义突变,导致4个氨基酸替换,分别为p.Arg176Gly、p.Gly235Ser、p.Leu266Met和p.Gly268Ala。ABO*O.01.01与ABO*A1.01相比,在第261位单碱基缺失(c.261delG),导致移码突变,终止密码子提前出现[8]。
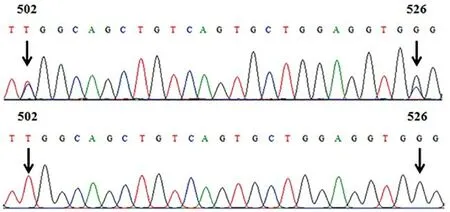
图2 样本2 ABO基因直接测序及克隆测序部分结果
本实验10例样本经过血型血清学试验检测,初步判定为ABO亚型,血清学特点为:正定型为O型,反定型抗-A/抗-B抗体减弱且价差≥2+。经过吸收放散实验,6例样本红细胞表面检出A/B抗原,4例未检出。随后进行ABO基因测序分析,10例样本均为放散型亚型:ABO*AEL.02与ABO*A1.01相比,在c.467C>T、c.646T>A和c.681G>A发生变异,形成两个氨基酸错义突变(p.Pro156Leu和p.Phe216Ile)和一个同义突变。c.467C>T(p.Pro156Leu)在亚洲人中很常见,约为80%~93%,可能并不会影响酶的功能[9]。c.646T>A(p.Phe216Ile)是亚型AEL、AW、B3、BW、BEL和多个O等位基因等的常见变异点,可能会改变糖基转移酶的活性或特异性,从而在某种程度上导致了弱表型的形成[10]。ABO*AEL.08与ABO*A1.01相比,c.467C>T和c.804dupG发生变异,c.804dupG使氨基酸第268位后阅读框架改变,终止密码子位置后移,A等位基因阅读框架延长[11],编码391个氨基酸;其表达产物与A1转移酶相比,不仅随后的86个羧基端氨基酸发生改变,而且比A1转移酶多37个氨基酸,比A2转移酶多16个氨基酸,从而降低了糖基转移酶的活性,导致抗原表达减弱[12];ABO*BEL.03与ABO*B.01相比,在c.502C>T发生变异,导致了p.Arg168Trp的改变。Arg是带长侧链的碱性氨基酸,而Trp是环状结构的疏水性中性氨基酸,二者间的侧链取向有很大差异,可能导致糖基转移酶的构象稳定性或生物学活性发生改变。经进一步的局部结构分析,野生型糖基转移酶p.Arg168的侧链能够与p.Glu138、p.Pro141和p.Met142分别形成多个氢键,使得野生型糖基转移酶构象较为稳定。而p.Arg168Trp突变型糖基转移酶的p.Trp168则能够与p.Gly165形成稳定的氢键,从而减弱了p.Trp168与周围氨基酸之间的相互作用,这可能影响了糖基转移酶的构象稳定性并降低了糖基转移酶的生物学活性[13]。
对于4例经吸收放散实验未检出A抗原的样本,原因分析如下:HOSSEINI-MAAF等[14]认为ABO血型基因第6外显子的3'末端含有重复的Chi序列,可引起等位基因重组。若重组后的等位基因含有c.261delG变异,则该等位基因可能为无功能的O等位基因。同时提出了一个假说,认为骨髓内外体细胞克隆中的基因转换或重组事件可能导致同一个体内产生双细胞群。如果存在不同的O等位基因(例如ABO*O.01.01和ABO*O.02.01),则可能通过重组或基因转换的方式在等位基因之间交换遗传物质,从而产生一个具有功能性的类A等位基因,抑制抗-A抗体的自然产生,这种现象可被称为“自体嵌合”。国内外曾有过类似报道:骆宏等[15-16]发现了若干例表型为O型且吸收放散无法检出A抗原,然而基因型却为A/O型的样本;OLSSON等[17]报道了基因型为ABO*AW.31.01/ABO*O.01.01的个体表现型为O型;CHO等[18]报道了基因型为ABO*AW.10/ABO*O.02.01的个体表现型也为O型。除此之外,氨基酸替换所引起的氢键网格、氨基转移酶稳定性和催化活性的变化,以及在整个DNA复制、转录、翻译和表达过程中可能存在的其他因素的干扰等,都有可能对A抗原的形成造成影响。因此,还需要更多体外实验以对其机制进行深入探讨。

图3 样本4 ABO基因直接测序及克隆测序部分结果
ABO放散型亚型的鉴定相对于常规ABO血型来说较为困难,因此增加H抗原的检测及吸收放散实验很有必要。通过检测H抗原可避免将孟买和类孟买型误判为O型,而吸收放散实验可避免将一些亚型误判为O型[15]。对于基因型相同而表型有差异的情况,一般来说年龄(6个月前的婴儿及老年人)、疾病(白血病等血液疾病或其他恶性疾病)及临床治疗(大量输液等)均有可能导致抗原或抗体的减弱[19],本研究由于样本数量较少及缺失部分临床信息等,有待收集更多样本及进行更多后续实验以进一步探究基因型与表型之间的关系。对于ABO放散型亚型患者的临床输血,应当遵循相容性输注原则,可考虑输注O型洗涤红细胞和AB型血浆及单采血小板;由于ABO放散型亚型的常规血清学鉴定会受到诸多因素的制约,若只通过血清学方法进行鉴定则存在局限性,容易误判为O型,进而影响输注效果甚至威胁患者生命,而采用分子生物学方法进行分析可以使检测结果更为精准可靠[20-21]。本研究将基因分型技术与血型血清学技术相结合,从表型和基因型两个方面对ABO放散型亚型进行血型鉴定,并在对ABO基因第6~7外显子进行常规测序的基础上,增加了对ABO基因第1~5外显子、上游CBF/NF-Y增强子区域、启动子、增强子及内含子1的+5.8 kb红细胞特异性调控元件序列的测序,以便更加精准地进行ABO放散型亚型的鉴定,减少临床输血反应,保障患者用血安全,为输血安全及精准医疗提供科学依据。
利益冲突所有作者均声明不存在利益冲突
